Коллоидный журнал, 2020, T. 82, № 2, стр. 186-194
Синтез и определение характеристик наночастиц серебра в обратных мицеллах неионных поверхностно-активных веществ и в их смешанных мицеллах с АОТ
П. С. Поповецкий *
Институт неорганической химии им. А.В. Николаева СО РАН
630090 Новосибирск, просп. Академика Лаврентьева, 3, Россия
* E-mail: popovetskiy@niic.nsc.ru
Поступила в редакцию 11.10.2019
После доработки 05.11.2019
Принята к публикации 09.11.2019
Аннотация
Получены и охарактеризованы с помощью ряда физико-химических методов стабильные наночастицы серебра в обратных мицеллах известных и доступных неионных поверхностно-активных веществ: сорбитан моноолеата (Span 80) и тетраоксиэтилированных додеканола и п-нонилфенола (Brij 30 и Tergitol NP4 соответственно), – в н-декане. Исследована зависимость стабильности, гидродинамического диаметра и электрокинетического потенциала наночастиц от количества добавляемых воды, хлороформа и анионного поверхностно-активного вещества бис(2-этилгексил)сульфосукцината натрия (АОТ). Показано, что для придания наночастицам достаточной величины электрокинетического потенциала, необходимой для увеличения стабильности и возможности концентрирования методом неводного электрофореза, следует использовать разные способы введения АОТ для разных ПАВ. В случае Brij 30 предпочтительнее введение АОТ после синтеза в качестве “заряжающей добавки”, а в случае Tergitol NP4 – в качестве со-ПАВ на стадии синтеза. При синтезе в мицеллах Span 80 наночастицы обладают значительным электрокинетическим потенциалом даже в отсутствие добавок. Использование АОТ в качестве со-ПАВ приводит в этом случае к уменьшению электрокинетического потенциала наночастиц, а в качестве добавки после синтеза – к его увеличению.
ВВЕДЕНИЕ
Стабильные золи неорганических веществ, в частности металлов, вызывают большой интерес исследователей во всем мире благодаря широким возможностям их использования в электронике, в особенности печатной [1]. Печатный способ получения комплектующих к электронным устройствам видится экспертами одним из наиболее перспективных с точки зрения снижения цены готового продукта [2]. Несмотря на серьезные требования к чернилам для печатной электроники, их рецептур предложено немало [3–6]. Основой таких чернил обычно выступает серебро благодаря рекордной среди металлов электропроводности и значительной химической стойкости [2].
Обычно выделяют два основных подхода к получению наночастиц: “сверху вниз” и “снизу вверх”. В первом случае наночастицы “отделяют” от массива металла, например, методами лазерной абляции, механического измельчения, плазменным испарением и рядом других [7–10]. В обзорных работах [1, 2], посвященных неорганическим наноматериалам в печатной электронике, авторы отмечают, что при таком подходе довольно сложно контролировать распределение получаемых частиц по размеру, что в данном случае принципиально. Другой подход предполагает получение наночастиц из ионных прекурсоров по реакции восстановления или разложения с использованием методов “мокрой химии”. В качестве стабилизаторов наночастиц широко используют полимеры, в особенности полиэлектролиты и поверхностно-активные вещества (ПАВ). Дисперсионной средой для наночастиц может служить как вода, так и органический растворитель. Синтез наночастиц в обратных мицеллах ПАВ позволяет получить очень стабильные наночастицы с узким распределением по размерам [11–13], поэтому он представляется достаточно перспективным способом получения чернил для печатной электроники. Использование органических растворителей негативно сказывается на цене и экологичности чернил, но дает больший простор для варьирования их свойств [14].
Наиболее популярным и детально изученным ПАВ, широко используемым для синтеза наночастиц, является бис(2-этилгексил)сульфосукцинат натрия (Аэрозоль ОТ, АОТ). Наночастицы, стабилизированные анионным АОТ, часто обладают значительным электрокинетическим потенциалом (ζ-потенциалом). По этой причине АОТ также является широко применяемой “заряжающей добавкой” в тех случаях, когда необходимо повысить ζ-потенциал наночастиц [15, 16]. Это не только положительно сказывается на их стабильности, но и позволяет осуществить концентрирование при помощи электрофореза [17–19] со значительными коэффициентами концентрирования и почти количественными степенями извлечения. Использование электрофоретического концентрирования видится наиболее эффективным способом решения главной проблемы микроэмульсионного синтеза – низкого содержания металла в получаемом органозоле.
Однако АОТ имеет ряд недостатков, прежде всего, наличие в его молекулах натрия и серы, от которых довольно сложно избавиться в процессе термической обработки чернил. Снижение концентрации АОТ в чернилах может привести к повышению чистоты полученного после обработки покрытия и улучшению его характеристик, в первую очередь, – проводимости. Одним из возможных способов решения этой проблемы видится частичная или полная замена АОТ на неионные ПАВ (НПАВ) с более низкими температурами начала термического разложения и близкими к количественным потерями массы при термолизе. Однако замена ионного ПАВ на неионное, скорее всего, будет приводить к снижению ζ-потенциала получаемых наночастиц и, как следствие, стабильности.
Целью данной работы являлся синтез и определение характеристик наночастиц серебра в обратных мицеллах широко известных и коммерчески доступных маслорастворимых НПАВ: оценивались гидродинамический диаметр наночастиц и их оптические свойства (форма спектра локализованного поверхностного плазмонного резонанса (ЛППР), положение максимума поглощения, молярный коэффициент экстинкции). Особое влияние уделено ζ-потенциалу получаемых наночастиц: проведено исследование влияния воды, хлороформа и АОТ на величину ζ-потенциала, при этом также контролировались гидродинамический диаметр и стабильность наночастиц. Воду и хлороформ вводили после синтеза, АОТ использовался как в качестве добавки после синтеза, так и в качестве со-ПАВ на стадии синтеза (до 50 мол. %). Для случая АОТ также проведено сопоставление полученных значений ζ-потенциала при различных вариантах его использования для “заряжения” наночастиц.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реактивы и синтез наночастиц
В работе использовали следующие растворители: н-декан (99%) и хлороформ (“х. ч.”, стабилизированный 0.5–0.75% этанола). Исходными веществами для синтеза наночастиц служили нитрат серебра (“х. ч.”), гидразин-гидрат (“х. ч.”). В качестве стабилизаторов использовали распространенные маслорастворимые НПАВ: Span 80 (сорбитан моноолеат, Sigma Aldrich), Brij 30 и Tergitol NP-4 (додеканол и п-нонилфенол со средней степенью оксиэтилирования 4, производства Sigma Aldrich и Dow Chemical соответственно) и АОТ (Sigma Aldrich, содержание основного вещества 97%). Все реактивы дополнительной очистке не подвергали.
Синтез наночастиц осуществляли традиционным микроэмульсионным способом: в две части растворов ПАВ в н-декане с концентрациями 0.1–1 М методом инъекционной солюбилизации вводили 1 об. % реагентов, т.е. нитрата серебра и восстановителя. Нитрат серебра использовали в виде 1 М раствора, а гидразин-гидрат без разбавления (концентрация гидразина около 20 М). После интенсивного перемешивания микроэмульсии с реагентами смешивали и оставляли минимум на 12 ч. В случае синтеза наночастиц в смешанных мицеллах НПАВ + АОТ общая концентрация ПАВ в растворе подбиралась исходя из максимально полученного молярного коэффициента экстинкции после синтеза в отсутствие АОТ. Мольная доля АОТ варьировалась от 10 до 50%. Синтез осуществляли аналогично описанному выше.
Методы исследования
Электронные спектры поглощения органозолей регистрировали на спектрофотометре UV-1700 (Shimadzu, Япония) в кварцевых кюветах с длиной оптического пути 0.2 см. При необходимости органозоли разбавляли исходными растворами ПАВ, чтобы максимальная оптическая плотность не превышала 1.5 оптических единицы.
Эффективный гидродинамический диаметр частиц определяли с помощью спектрометра динамического рассеяния света NanoBrook Omni (Brookhaven Instruments, США) с использованием полимодального анализа, основанного на алгоритме NNLS (Non-Negatively Constrained Least Squares, метод наименьших квадратов с ограничением на неотрицательность). Перед измерением органозоли очищали от пыли 5-кратным циклическим фильтрованием через тефлоновый мембранный фильтр с диаметром пор 0.2 мкм (Sartorius, Германия) непосредственно в измерительную кювету из стекла. Рассеянные частицами фотоны детектировались под углом 90° к источнику излучения – твердотельному лазеру с длиной волны 640 нм и мощностью 35 мВт. Время накопления фотонов в ходе одного измерения составляло 10 с, гидродинамический диаметр определялся как среднее из 20–30 измерений.
Электрокинетический потенциал (ζ-потенциал) наночастиц определяли также при помощи спектрометра NanoBrook Omni методом лазерного электрофореза с опцией фазового анализа рассеянного света (далее по тексту для данного метода будет использована распространенная аббревиатура PALS, от phase analysis light scattering). Измерения проводили в специальной ячейке SRR2 (Brookhaven Instruments), устойчивой к действию органических растворителей, с плоскопараллельными палладиевыми электродами площадью около 45 мм2 и зазором между ними 3.45 мм. Рассеянные частицами фотоны детектировались под углом 15°. Перед измерением органозоли очищали от пыли 10-кратным циклическим фильтрованием, а электроды – непрерывным пропусканием через них растворителя в течение 20 минут с помощью фильтрующей системы BI-SFS (Brookhaven Instruments), скорость потока растворителя составляла 7.8 мл/мин. Измерения скорости движения наночастиц проводили в ручном режиме при напряженности внешнего поля 275–550 В/см (в некоторых случаях и при меньших значениях напряженности), ζ-потенциал определялся как среднее из 10–20 измерений при различных значениях напряженности внешнего поля. Для исследуемых систем зависимость ζ-потенциала от напряженности поля отсутствовала в указанном выше диапазоне. Для расчета ζ-потенциала использовалacь модель Хюккеля–Онзагера [20, 21]. Кроме того, для всех систем предварительно проводили качественное исследование электрокинетических явлений и знака ζ-потенциала методом подвижной границы. Подробно метод описан в работах [18, 19]. Использовались медные электроды площадью около 2 см2, зазор между которыми составлял 1 см. При отсутствии видимого невооруженным глазом электрофоретического движения (формирования границы между рафинатом и органозолем с наночастицами) система в дальнейшем методом PALS не анализировалась.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Гидродинамический диаметр и оптические свойства
Наночастицы в мицеллах неионных ПАВ. В табл. 1 представлены результаты измерения гидродинамического диаметра (dh) наночастиц, полученных в обратных мицеллах неионных ПАВ. Также в табл. 1 указаны интенсивность рассеяния света и характеристики спектров ЛППР.
Таблица 1.
Значения гидродинамического диаметра (dh), интенсивности светорассеяния (I), длины волны максимума поглощения (λmax), молярного коэффициента экстинкции на λmax (εmax) и полной ширины на половине высоты (ПШПВ) пика плазмонного поглощения наночастиц серебра, полученных в обратных мицеллах НПАВ
| СПАВ, моль/л | dh, нм | I, kcps* | εmax × 10–4, л/(моль см) | λmax, нм | ПШПВ, нм | |
|---|---|---|---|---|---|---|
| мода 1 | мода 2 | |||||
| Span 80 | ||||||
| 0.1 | – | 20 | 520 | 0.92 | 414 | 97 |
| 0.25 | 18 | 140 | 500 | 0.87 | 414 | 98 |
| 0.5 | 28 | 140 | 1070 | 1.50 | 413 | 68 |
| 0.75 | – | 92 | 920 | 0.80 | 411 | 67 |
| 1.0 | – | 110 | 620 | 1.29 | 411 | 67 |
| Tergitol NP-4 | ||||||
| 0.1 | 9.8 | – | 295 | – | – | – |
| 0.25 | 8.3 | 140 | 690 | – | – | – |
| 0.5 | 12 | 49 | 3430 | 0.74 | 408 | 57 |
| 0.75 | 6.8 | 76 | 1990 | 0.25 | 409 | 55 |
| 1.0 | 10.4 | 150 | 520 | 0.037 | 411 | 59 |
| Brij 30 | ||||||
| 0.1 | 15 | 120 | 170 | – | – | – |
| 0.25 | – | 32.9 | 177 | 2.10 | 403 | 50 |
| 0.5 | – | 68 | 3920 | 1.60 | 408 | 48 |
| 0.75 | – | 80 | 4800 | 0.73 | 409 | 53 |
| 1.0 | – | 92 | 800 | 0.13 | 409 | 54 |
Исходя из приведенных данных следует отметить, что использование низких концентраций НПАВ (0.1 и 0.25 М в случае Tergitol NP-4 и 0.1 М в случае Brij 30) приводит к резкому снижению стабильности получаемых наночастиц и формированию осадка металлического серебра – полученные при данных концентрациях НПАВ органозоли были бесцветными. При всех исследованных концентрациях Span 80 образующиеся органозоли были ярко окрашены и имели полосу ЛППР, но более широкую, чем в случае оксиэтилированных ПАВ. Вероятно, это связано с более широким распределением получаемых частиц по размеру.
Длина волны максимума ЛППР для всех синтезированных органозолей (за исключением бесцветных) находится в области 400–415 нм, что типично для наночастиц серебра малого размера, гидродинамический диаметр наночастиц во всех случаях не превышал 150 нм. При использовании оксиэтилированных НПАВ наблюдается следующая закономерность: увеличение концентрации в диапазоне 0.5–1 М для Tergitol NP-4 и 0.25–1 М для Brij 30 приводит к увеличению гидродинамического диаметра и снижению стабильности получаемых наночастиц. Также следует отметить, что мода от мицелл ПАВ регистрировалась только в случае Tergitol NP-4, их диаметр составлял около 10 нм, что несколько больше размера безводных мицелл Tergitol NP-4 (6–8 нм в зависимости от концентрации). В остальных случаях моды от мицелл ПАВ не регистрировались по причине низкой интенсивности, обусловленной меньшим размером мицелл Brij 30 и Span 80 по сравнению с мицеллами Tergitol NP-4.
Для дальнейшего исследования были выбраны системы с наиболее высокими значениями молярного коэффициента экстинкции, рассчитанного с учетом всего серебра в системе (5 мМ в пересчете на объем органической фазы) – стабилизированные Brij 30 в концентрации 0.25 М, а Span 80 и Tergitol NP-4 – в концентрации 0.5 М. В случае Span 80 и Tergitol NP-4 данные системы максимально интенсивно рассеивали свет (что ожидаемо), а в случае Brij 30, напротив, рассеяние было минимальным (наблюдалось интенсивное поглощение лазерного излучения наночастицами).
Наночастицы в мицеллах неионных ПАВ с добавками воды, хлороформа и АОТ. При использовании Brij 30 и Span 80 в качестве стабилизаторов полученные органозоли смешивались с 1 М раствором АОТ в любых соотношениях без потери стабильности. В случае Tergitol NP-4 при добавлении АОТ до концентрации 0.05 М и более наблюдалась относительно быстрая потеря стабильности – менее чем за 5 мин гидродинамический диаметр наночастиц увеличивался от 100 до 300 нм, а интенсивность рассеяния света возрастала от 3000 до 7000 kcps.
Органозоль наночастиц, стабилизированных Tergitol NP-4, также проявлял худшую стабильность при введении хлороформа. При добавлении 9 об. % хлороформа и более интенсивность рассеяния света сначала резко уменьшалась до 50 kcps за счет образования агрегатов, интенсивно поглощающих лазерное излучение, а в дальнейшем увеличивалась до 1000 kcps за счет их седиментации. Примечательно, что измеряемый при этом гидродинамический диаметр наночастиц существенно не изменялся. Аналогичные агрегаты наблюдались при добавлении 12 об. % хлороформа к органозолю наночастиц, стабилизированных Brij 30: интенсивность рассеяния света снижалась от 1000 до 70 kcps за счет поглощения лазерного излучения. Седиментации агрегатов и изменения их гидродинамического диаметра за время измерения не наблюдалось. Органозоль наночастиц, стабилизированных Span 80, смешивается с хлороформом в любых соотношениях без потери стабильности.
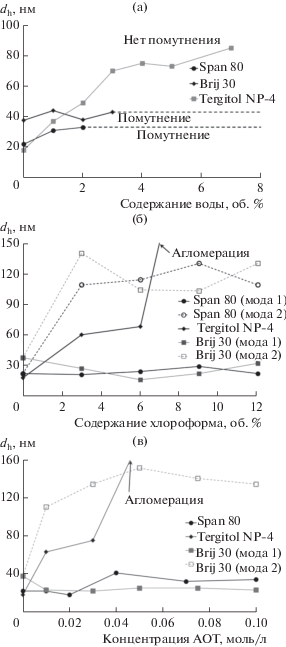
При добавлении воды к органозолю наночастиц, стабилизированных Tergitol NP-4, помутнение наблюдалось только при солюбилизации более 10 об. % H2O. Органозоли наночастиц, стабилизированных Span 80 и Brij 30, мутнели при добавлении уже 3 и 4 об. % воды соответственно. Изменение гидродинамического диаметра наночастиц серебра в данных системах проиллюстрировано на рис. 1.
Рис. 1.
Изменение гидродинамического диаметра наночастиц серебра, полученных в обратных мицеллах НПАВ при введении добавок воды (а), хлороформа (б) и АОТ (в).
Наночастицы в смешанных мицеллах НПАВ + + АОТ. Для синтеза наночастиц серебра в смешанных мицеллах НПАВ + АОТ использовали суммарные концентрации ПАВ, равные 0.25 М, так как основная идея работы заключалась в снижении концентрации АОТ в исследуемых системах. Для случаев Span 80 и Tergitol NP-4 дополнительно использовали системы с суммарной концентрацией ПАВ 0.5 М, для которой получены максимальные значения оптической плотности и интенсивности рассеяния света в отсутствие АОТ. Результаты определения характеристик данных систем представлены в табл. 2.
Таблица 2.
Значения гидродинамического диаметра (dh), интенсивности рассеяния света (I), длины волны максимума поглощения (λmax), молярного коэффициента экстинкции на λmax (εmax) и ПШПВ пика плазмонного поглощения наночастиц серебра, полученных в смешанных обратных мицеллах НПАВ + АОТ
| САОТ, мол. % | dh, нм | I, kcps | εmax × 10–4, л/(моль см) | λmax*, нм | ПШПВ, нм | |
|---|---|---|---|---|---|---|
| мода 1 | мода 2 | |||||
| Span 80 + AOT (0.5 М) | ||||||
| 10 | 6 | 26 | 116 | 1.19 | 409 | 86 |
| 20 | 17 | 110 | 147 | 1.21 | 409 | 90 |
| 30 | 10 | 100 | 157 | 1.30 | 408 | 88 |
| 40 | 30 | 160 | 160 | 1.34 | 407 | 86 |
| 50 | 21 | 160 | 129 | 1.36 | 406 | 88 |
| Tergitol NP-4 + AOT (0.5 М) | ||||||
| 10 | 16 | 60 | 1330 | 1.28 | 408 | 63 |
| 20 | 4 | 72 | 2870 | 0.55 | 407 | 71 |
| 30 | 51 | 370 | 1710 | 0.87 | 407 | 69 |
| 40 | 29 | 210 | 770 | 1.46 | 406 | 70 |
| 50 | 90 | 580 | 450 | 1.52 | 406 | 68 |
| Brij 30 + AOT (0.25 М) | ||||||
| 10 | 8.5 | 88 | 6460 | 1.40 | 412 | 71 |
| 20 | 12 | 91 | 5210 | 1.11 | 413 | 81 |
| 30 | 15 | 112 | 9300 | 0.09 | 416 (650) | 112 |
| 40 | 52 | 320 | 5200 | 0.16 | 422 (640) | 108 |
| 50 | 41 | 230 | 920 | 0.32 | 412 (600) | 101 |
| Span 80 + AOT (0.25 М) | ||||||
| 10 | 15 | 117 | 3480 | 0.91 | 406 | 68 |
| 20 | – | 181 | 4650 | 0.97 | 405 | 80 |
| 30 | 8.9 | 211 | 1270 | 0.92 | 405 | 74 |
| 40 | 12.6 | 180 | 280 | 0.93 | 405 | 83 |
| 50 | 6.2 | 24 | 225 | 0.95 | 406 | 92 |
| Tergitol NP-4 + AOT (0.25 М) | ||||||
| 10 | 12 | 62 | 7170 | 0.98 | 406 | 50 |
| 20 | 13 | 67 | 7100 | 0.91 | 408 | 56 |
| 30 | 34 | 145 | 1300 | 0.48 | 405 (630) | 60 |
| 40 | 18 | 90 | 6160 | 0.59 | 405 (650) | 61 |
| 50 | 22 | 67 | 4700 | 0.86 | 404 | 57 |
В случае Span 80 добавление АОТ не оказывает значительного влияния на характеристики спектров ЛППР при всех исследованных концентрациях: коэффициент экстинкции, длина волны максимума и ширина резонансного пика существенно не изменяются. В остальных случаях при некоторых соотношениях НПАВ/АОТ наблюдается резкое уменьшение коэффициента экстинкции, которое, как правило, сопровождается появлением плеча в длинноволновой области в диапазоне 600–650 нм. Вероятнее всего, это обусловлено особенностями строения смешанных мицелл при данных соотношениях ПАВ. Описанные изменения в спектрах сопровождаются появлением в распределении по размерам моды с гидродинамическим диаметром 100–300 нм в случае смесей Brij 30/AOT, 110–210 нм для смесей Tergitol NP4/АОТ с общей концентрации ПАВ, равной 0.25 М, и 200–600 нм для смесей Tergitol NP4/АОТ с общей концентрации ПАВ, равной 0.5 М. Для смесей Span 80/AOT данные эффекты менее выражены, гидродинамический диаметр этой моды составляет 100–160 нм. Причинами могут быть как агрегирование, так и образование частиц вытянутой формы.
Электрокинетический потенциал
Исходные системы. Для случая наночастиц серебра, стабилизированных оксиэтилированными ПАВ, методом подвижной границы электрофоретическое движение наночастиц ожидаемо не регистрировалось. Для наличия у наночастиц ненулевого электрокинетического потенциала требуется выполнение следующих условий:
1) ненулевой заряд поверхности наночастиц,
2) заряд не должен полностью компенсироваться плотной частью двойного электрического слоя (ДЭС),
3) в системе должны присутствовать свободные носители заряда, формирующие диффузную часть ДЭС.
В обратно-мицеллярных системах носителями заряда могут выступать обратные мицеллы ионных ПАВ, способные за счет межмицеллярного обмена ионами иметь флуктуационный заряд [22], либо некие ионизируемые примеси или добавки, например, более полярного сольватирующего растворителя хлороформа [23]. В системах на основе НПАВ без добавок таких носителей заряда быть не должно. Даже если заряд поверхности наночастицы не равен нулю, то из соображений электронейтральности всей системы он полностью компенсируется плотной частью ДЭС, которую, вероятнее всего, выполняет адсорбционный слой наночастицы.
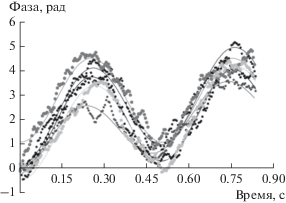
Тем не менее, в случае наночастиц серебра, стабилизированных Span 80, под воздействием электрического поля с напряженностью 200 В/см формировалась размытая граница между бледно-желтым рафинатом, и окрашенным органозолем с наночастицами. Методом PALS в данной системе получены воспроизводимые результаты, указывающие на наличие у наночастиц существенного ζ-потенциала (+16.1 ± 0.2 мВ). На рис. 2 представлены зависимости фазового сдвига рассеянного наночастицами света в процессе их электрофоретического движения. Наблюдается очень хорошее согласие расчетных и экспериментальных данных.
Рис. 2.
Экспериментальные (точки) и расчетные (сплошные линии) зависимости фазы света, рассеянного наночастицами в процессе электрофоретического движения, от времени для 5 параллельных измерений. Данные для наночастиц серебра, стабилизированных Span 80. Напряженность поля – 280 В/см, концентрация серебра – 5 мМ, концентрация Span 80 – 0.5 М, растворитель – н-декан.
Очевидно, что в данной системе присутствуют некие носители заряда, по аналогии с ионными ПАВ, но однозначного объяснения природы этих носителей заряда на данном этапе исследований нет, а изучение причин наличия ненулевого ζ-потенциала у наночастиц, стабилизированных типично неионным ПАВ, не входило в задачи данной работы и будет являться целью отдельного исследования. Наиболее вероятной причиной представляется наличие ионизируемых примесей в коммерческом Span 80.
Электрокинетический потенциал при добавлении воды, хлороформа и АОТ. Для наночастиц серебра, стабилизированных исследуемыми оксиэтилированными ПАВ, различия в характерах зависимости и в полученных величинах ζ-потенциала незначительны, они будут обсуждаться совместно.
Добавки воды (до 5 об. % или до точки помутнения) не оказывали влияния на ζ-потенциал наночастиц, он оставался нулевым. Аналогичная картина наблюдается при использовании этанола. На основании полученных данных можно предположить, что вода и этанол проникают в полярные полости обратных мицелл и не формируют диффузную часть ДЭС.
Добавки хлороформа в количестве более 6 об. % приводили к появлению электрофоретического движения, регистрируемого методом подвижной границы. При наложении электрического поля с напряженностью 200 В/см формировалась четкая граница между бесцветным рафинатом, практически не содержащим наночастиц, и окрашенным органозолем, видимая невооруженным глазом. Наночастицы двигались к катоду, что указывает на их положительный заряд. При попытках измерить величину ζ-потенциала методом PALS воспроизводимых результатов получить не удалось из-за увеличения электропроводности системы, вызванного коагуляцией наночастиц. Таким образом, использование хлороформа для создания диффузной части ДЭС в данном случае не представляется целесообразным, так как приводит к электрокоагуляции.
Добавки АОТ в виде 1 М раствора также приводили к заряжению наночастиц, электрофоретическое движение регистрируется при помощи метода подвижной границы. Увеличение электропроводности системы, вызванное электрокоагуляцией, наблюдалось и в данных системах, но в меньшей степени, что позволяло корректно определить ζ-потенциал с помощью метода PALS, используя более низкую напряженность электрического поля (менее 275 В/см). Значения ζ-потенциала составили около 6 мВ для обоих ПАВ. Зависимость от концентрации АОТ в диапазоне 0.02–0.1 М отсутствовала.
В случае Span 80 добавление 1 об. % воды не оказывало влияния на ζ-потенциал наночастиц серебра, при добавлении 2 об. % воды воспроизводимые данные получить не удалось, а добавление 3 об. % воды и более, как отмечено выше, приводило к помутнению органозоля. Добавление АОТ (концентрация 0.02–0.1 М) или хлороформа (3–15 об. %) увеличивало ζ-потенциал наночастиц до примерно 30 мВ. Зависимость от концентрации АОТ и объема хлороформа в указанном диапазоне отсутствовала.
Таким образом, в случае использования АОТ в качестве “заряжающей добавки” для всех ПАВ удалось получить воспроизводимые результаты измерения ζ-потенциала при помощи метода PALS.
Наночастицы в смешанных мицеллах НПАВ + + АОТ. Прежде всего следует отметить, что для смеси Brij 30 + АОТ воспроизводимые результаты определения ζ-потенциала методом PALS получены не были во всем исследованном диапазоне концентраций, хотя методом подвижной границы электрофоретическое движение наночастиц регистрируется в системах с мольной долей АОТ 30% и выше. Наиболее вероятной причиной видится низкая стабильность полученных наночастиц (их агрегация): пики ЛППР – широкие, с плечом в длинноволновой области, а оптическая плотность органозолей низка. Во всех остальных случаях методом подвижной границы электрофоретическое движение наночастиц регистрируется, а методом PALS получены воспроизводимые значения ζ-потенциала. Зависимости величины ζ-потенциала наночастиц от мольной доли АОТ в смеси ПАВ приведены на рис. 3.
Рис. 3.
Зависимости ζ-потенциала наночастиц, полученных в смешанных мицеллах НПАВ + АОТ, от доли АОТ при общей концентрации ПАВ, равной 0.25 и 0.5 М.
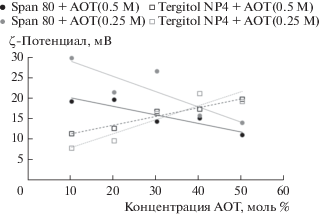
При использовании смеси Tergitol NP4 + АОТ наблюдается ожидаемое линейное увеличение ζ-потенциала наночастиц с ростом мольной доли АОТ за счет дополнительного введения в систему возможных носителей заряда – ионизируемых молекул АОТ. В случае Span 80 ситуация иная: увеличение мольной доли АОТ приводит к уменьшению ζ-потенциала. Скорее всего, это обусловлено способностью Span 80 формировать диффузную часть ДЭС, притом таким образом, чтобы обеспечить более высокие значения ζ-потенциала, чем в случае АОТ.
ЗАКЛЮЧЕНИЕ
В данной работе исследованы наночастицы серебра, стабилизированные неионными ПАВ и их смесями с анионным АОТ. Показано, что АОТ является более предпочтительным “заряжающим агентом”, чем хлороформ, а вода вовсе для этих целей не может использоваться. Однако добавление АОТ приводит к “засорению” системы натрием и серой, от которых сложно в дальнейшем избавиться. Поэтому одной из задач работы было подобрать такой способ, который позволяет получить наночастицы с наибольшим ζ-потенциалом при минимальной концентрации АОТ в системе. Показано, что предпочтительные варианты использования АОТ могут различаться даже для достаточно близких по природе НПАВ. В случае Brij 30 применение АОТ в качестве со-ПАВ на стадии синтеза приводит к снижению стабильности наночастиц, что не позволило получить воспроизводимые данные об их ζ-потенциале. Однако небольшие добавки АОТ после синтеза позволяют получить наночастицы с сравнительно невысоким, но корректно измеряемым ζ-потенциалом. В случае мицелл Tergitol NP4 небольшие добавки АОТ после синтеза приводят к аналогичной ситуации, но при использовании смешанных мицелл Tergitol NP4 + АОТ полученные наночастицы обладают большим ζ-потенциалом. Следует отметить, что при стабилизации смесью Tergitol NP4 + АОТ могут быть получены органозоли с высокой молярной концентрацией металла при помощи метода неводного электрофореза [24]. Оба этих подхода приводят к снижению доли АОТ в системе, благодаря чему можно ожидать увеличения электропроводности получаемых на их основе серебряных покрытий.
Наиболее необычными представляются результаты, полученные для случая Span 80. Стабилизированные данным НПАВ наночастицы обладают сравнительно высоким ζ-потенциалом. Добавление АОТ как со-ПАВ на стадии синтеза приводит к снижению ζ-потенциала наночастиц, а после синтеза, напротив, к его увеличению. Данная система, безусловно, требует дальнейшего детального исследования, прежде всего интерес представляет природа носителей заряда, формирующих диффузную часть ДЭС. Можно ожидать, что в случае Span 80 удастся получить концентрированные органозоли без использования каких-либо “заряжающих добавок”. Такие органозоли будут перспективным вариантом чернил для печатной электроники и позволят получать серебряные покрытия, имеющие более высокие чистоту и проводимость.
Список литературы
Wu W. // Nanoscale. 2017. V. 9. P. 7342.
Kamyshny A., Magdassi S. // Small. 2014. V. 10. P. 3515.
Shin D.-H., Woo S., Yem H., Cha M., Cho S., Kang M., Jeong S., Kim Y., Kang K., Piao Y. // ACS Appl. Mater. Interfaces. 2014. V. 6. P. 3312.
Vassem M., McKerricher G., Shamim A. // ACS Appl. Mater. Interfaces. 2016. V. 8. P. 177.
Jason N.J., Shen W., Cheng W. // ACS Appl. Mater. Interfaces. 2015. V. 7. P. 16760.
Lee K.J., Jun B.H., Kim T.H., Joung J. // Nanotechnology. 2006. V. 17. P. 2424.
Shinde S.R., Banpurkar A.G., Adhi K.P., Limaye A.V., Ogale S.B., Date S.K., Marest G. // Mod. Phys. Lett. B. 1996. V. 10. P. 1517.
Begin-Colin S., Wolf F., Le Caer G. // J. Phys. III. 1997. V. 7. P. 473.
Ananthapadmanabhan P.V., Sreekumar K.P., Venkatramani N., Sinha P.K., Taylor P.R. // J. Alloys Compd. 1996. V. 244. P. 70.
Lu J., Yang H., Yu S., Zou G. // Mater. Chem. Phys. 1996. V. 45. P. 197.
Pileni M.P. // J. Phys. Chem. 1993. V. 97. P. 6961.
Eastoe J., Hollamby M.J., Hudson L. // Adv. Colloid Interface Sci. 2006. V. 128–130. P. 5.
Zhang W., Qiao X., Chen J., Wang H. // J. Colloid Interface Sci. 2006. V. 302. P. 370.
Поповецкий П.С., Шапаренко Н.О., Арымбаева А.Т., Булавченко А.И. // Коллоид. журн. 2016. Т. 78. С. 458.
Sainis S.K., Merrill J.W., Duffresne E.R. // Langmuir. 2008. V. 24. P. 13334.
Sainis S.K., Germain V., Mejean C.O., Duffresne E.R. // Langmuir. 2008. V. 24. P. 1160.
Поповецкий П.С., Булавченко А.И., Манаков А.Ю. // Оптич. журн. 2011. Т. 78. № 7. С. 67.
Bulavchenko A.I., Pletnev D.N. // J. Phys. Chem. C. 2008. V. 112. P. 16365.
Bulavchenko A.I., Popovetskiy P.S. // Langmuir. 2010. V. 26. P. 736.
O’Brien R.W., White L.R. // J. Chem. Soc., Faraday Trans. 2. 1978. V. 74. P. 1607.
Delgado A.V., Gonzalez-Caballero F., Hunter R.J., Koopal L.K., Lyklema J. // J. Colloid Interface Sci. 2007. V. 309. P. 194.
Morrison I.D. // Colloids Surf. A. 2008. V. 71. P. 1.
Поповецкий П.С., Булавченко А.И., Демидова М.Г., Подлипская Т.Ю. // Коллоид. журн. 2015. Т. 77. С. 65.
Popovetskiy P.S., Beketova D.I. // Colloids Surf. A. 2019. V. 568. P. 51.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал


