Коллоидный журнал, 2022, T. 84, № 5, стр. 503-522
Наноразмерные супрамолекулярные системы: от коллоидных пав к амфифильным макроциклам и суперамфифилам
Р. Р. Кашапов 1, *, А. Б. Миргородская 1, Д. М. Кузнецов 1, Ю. С. Разуваева 1, Л. Я. Захарова 1
1 Институт органической и физической химии им. А.Е. Арбузова ФИЦ Казанский
научный центр РАН
420088 Казань, ул. Академика Арбузова, д. 8, Республика Татарстан, Россия
* E-mail: kashapov@iopc.ru
Поступила в редакцию 05.05.2022
После доработки 21.06.2022
Принята к публикации 06.07.2022
- EDN: HKCXGK
- DOI: 10.31857/S0023291222600092
Аннотация
Обзор посвящен самоорганизующимся системам на основе амфифильных соединений различного типа: открытоцепных и макроциклических. Рассмотрены классические коллоидные ПАВ в индивидуальном виде и в присутствии модифицирующих добавок, в том числе электролитов и со-ПАВ. Особое внимание уделено роли структурного фактора; проанализированы случаи наиболее выраженного влияния структуры ПАВ (головной группы, противоиона, перехода к дикатионным ПАВ, наличия каликс[4]аренового ядра) на агрегационные характеристики, морфологическое поведение, функциональную активность. Макроциклические амфифилы представляют собой классические объекты супрамолекулярной химии. В заключительной части обзора проведено сравнение двух типов систем: (1) амфифильных каликсаренов (ковалентная функционализация макроцикла алкильными фрагментами) и (2) бинарных композиций каликсарен–ПАВ (нековалентная модификация макроциклической платформы).
ВВЕДЕНИЕ
Поверхностно-активные вещества (ПАВ) находят широкое и разнообразное применение в промышленности, сельском хозяйстве, фармации, косметике, пищевой промышленности, катализе и др. [1–14]. В основе их практического использования лежит фундаментальное свойство коллоидных ПАВ – способность к самоорганизации в объеме раствора и на поверхностях раздела с образованием агрегатов различного размера и морфологии. Параметры и свойства таких агрегатов, включая величину критической концентрации мицеллообразования (ККМ), числа агрегации, поверхностную активность и др., во многом определяются структурой ПАВ. Поэтому, несмотря на исторически сложившееся приоритетное развитие прикладных исследований с использованием ПАВ, большое внимание уделяется фундаментальным аспектам, установлению закономерностей “структура–свойство”, созданию полуэмпирических и теоретических представлений в области организованных растворов амфифильных соединений [15–20].
Применение ПАВ в области современных нано- и биотехнологий определяет существование достаточно строгих критериев, предъявляемых к дизайну, структурным характеристикам, морфологическим, физико-химическим и биологическим свойствам ПАВ, соответствия требованиям “зеленой химии” и экологической безопасности. К числу приоритетных тенденций можно отнести создание амфифильных соединений, обладающих низким порогом агрегации и отвечающих принципам экономичности, технологичности, биосовместимости, биоразлагаемости, низкой токсичности. В связи с этим большое внимание уделяется исследованиям геминальных (дикатионных) ПАВ, амфифильных соединений, содержащих природные, биоразлагаемые фрагменты и группы, чувствительные к внешним импульсам. C учетом этих тенденций развитие теоретических представлений и полуэмпирических закономерностей в последние годы выполнено на примере перечисленных ПАВ. То же относится к установлению качественных и количественных корреляций “структура–свойство–активность”, которые затрагивают практический потенциал супрамолекулярных систем в области высоких технологий и биомедицины.
1. ВЛИЯНИЕ СТРУКТУРНОГО ФАКТОРА НА АГРЕГАЦИОННЫЕ ХАРАКТЕРИСТИКИ И ФУНКЦИОНАЛЬНУЮ АКТИВНОСТЬ ПАВ И СИСТЕМ НА ИХ ОСНОВЕ
Основным фактором, определяющим агрегационную активность амфифильных соединений в водных средах, является гидрофобный эффект. Надежно установленной закономерностью является зависимость величины ККМ от длины алкильного радикала ПАВ [18, 19], которая выражается линейным графиком в координатах lg(ККМ) – n, где n – число атомов углерода в алкильном заместителе в полярной группе. Наклон этой зависимости для неионных ПАВ составляет примерно 0.5, а для ионных – 0.3 [15, 19], что отражает различный вклад полярных фрагментов (диполь-дипольное взаимодействие в случае неионных ПАВ и электростатическое отталкивание одноименно заряженных головных групп ионных ПАВ) в свободную энергию мицеллообразования. Сочетание структурных элементов в молекуле ПАВ находит свое отражение в величине гидрофильно-липофильного баланса (ГЛБ). Этот показатель, определяемый с помощью различных полуэмпирических моделей, оказывается полезным при анализе закономерностей и различий в процессе агрегации основных типов ПАВ (неионных, анионных, катионных и цвиттер-ионных), которые были достаточно хорошо установлены в классических работах [18, 19]. Значения ГЛБ являются полезными в случае прикладного использования ПАВ в качестве эмульгаторов, моющих или солюбилизирующих агентов, пенообразователей и пр. Основной массив современной литературы в области коллоидной и физической химии направлен на синтез новых ПАВ и исследование специфики проявления структурных характеристик в гомологических рядах с точки зрения изменения агрегационных свойств и функциональной активности (солюбилизационной, антимикробной, каталитической, антикоррозионной, смачивающей и пр.) с целью выявления их практического потенциала.
Более тонкое влияние структуры головной группы наиболее широко исследовано на примере катионных ПАВ, что связано с их высокой практической востребованностью и возможностью синтеза амфифильных молекул, содержащих положительно заряженные, прежде всего ониевые фрагменты, различной химической природы. Как правило, наиболее изученный гомологический ряд триметиламмониевых ПАВ (ТМА-n, где n – количество атомов углерода в алкильном радикале) выступает в качестве ПАВ для сравнения. Следует отметить, что в ряду катионных ПАВ (рис. 1) влияние головной группы на величину основного параметра, определяющего агрегационную активность ПАВ – ККМ, невелико. Ключевым фактором в данном случае является длина алкильного радикала, контролирующего гидрофобный эффект ПАВ [18, 19]. Например, ККМ амфифильных производных диазабициклооктана (DABCO-n) [10], триаллиламмониевых (TAA-n) [21], имидазолиевых (Im-n) [22–24], морфолиниевых (Mph-n) [25], пирролидиниевых (Pyr-n) [26, 27], пиперидиниевых (Pip-n) [28] ПАВ мало отличаются от ТМА-n серии, в частности, ККМ цетилпроизводных ТМА-16 (цетилтриметиламмоний бромид, ЦТАБ), DABCO-16, Im-16, Mph-16, Pyr-16, Pip-16 близки к 1 мМ. Исключение составляет серия трифенилфосфониевых ПАВ (TPP-n) [29]: в этом случае ККМ TPP-16 на порядок ниже и составляет 0.1 мМ (табл. 1).
Таблица 1.
Значения ККМ* и числа агрегации (Nагр)** монокатионных ПАВ различной структуры.
| ПАВ | ККМ, мМ | Nагр (при С, мМ) | Ссылка |
|---|---|---|---|
| ТМА-16 | 0.93 | 6а (7.7 мМ) | [26] |
| Pip-16 | 1.0 | 30а (3 мМ) 24б (3 мМ) |
[28] |
| Pip-16(OH) | 0.90 | 28а (3 мМ) 23б (3 мМ) |
[28] |
| Mph-16 | 1.0 | 89б (5 мМ) | [25], [30] |
| Pyr-16 | 0.86 | 59а (7.7 мМ) | [26] |
| Pyr-16(OH) | 0.42 | 42б (3 мМ) | [27] |
| Im-16 | 0.90 | 64а (4 мМ) | [22], [23] |
| Im-14(OH) | 2.0 | 44а (5 мM) | [31] |
| Im-16(OH) | 0.60 | 142а (5 мM) | [31] |
| Im-18(OH) | 0.20 | 150а (5 мM) | [31] |
| MPI-16 | 0.35 | [32] | |
| TAA-12 | 1.0; 10 | 55а (5 мМ) | [21] |
| TAA-14 | 3.0 | 18а (5 мМ) | [21] |
| TAA-16 | 1.1 | 24а (5 мМ) | [21] |
| DABCO-16 | 1.0 | 72в | [10] |
| TPP-12 | 2.0 | 1а (7 мМ) | [29] |
| TPP-14 | 0.33 | 6а (5 мМ) | [29] |
| TPP-16 | 0.10 | 7а (1 мМ) | [29] |
| CB-4-14 | 1.0 | 62б (3 мМ) 69б (5 мМ) |
[33] |
| CB-4-16 | 0.24 | 32б (0.72 мМ) 35б (1.2 мМ) |
[33] |
| CB-4-18 | 0.09 | 20б (0.27 мМ) 23б (0.35 мМ) |
[33] |
| CB-2-16 | 0.70 | 29б (2.1 мМ) 34б (3.5 мМ) |
[33] |
| CB-6-16 | 0.07 | [34] | |
| CB-8-16 | 0.049 | [35] | |
| CB-12-16 | 0.04 | [35] | |
| CB-Pyr-14(Et) | 2.0 | 32а (5 мM) | [36] |
| CB-Pyr-16(Et) | 0.50 | 33а (5 мM) | [36] |
| CB-Pyr-18(Et) | 0.10 | 27а (5 мM) | [36] |
| CB-Im-14(Et) | 1.3 | 16а (5 мM) | [37] |
| CB-Im-16(Et) | 0.30 | 40а (5 мM) | [37] |
| CB-Im-18(Et) | 0.10 | 38а (5 мM) | [37] |
| CB-Im-14(Bu) | 0.50 | 24а (5 мM) | [38] |
| CB-Im-16(Bu) | 0.15 | 29а (5 мM) | [38] |
Функционализация головных групп фрагментами, способными к специфическим взаимодействиям, может приводить к снижению ККМ. При введении гидроксиалкильных заместителей в головную группу ЦТАБ наблюдается уменьшение значения ККМ в ряду заместителей: гидроксиэтил (0.75 мМ) > дигидроксиэтил > (0.65 мМ) > гидроксипропил (0.50 мМ) [39]. В ряду имидазолиевых [31] и морфолиниевых [25] ПАВ также наблюдается снижение ККМ для гидроксиэтилированных производных до 0.7 мМ, а для пирролидиниевого ПАВ Pyr-16(ОН) – до 0.42 мМ [27]. В случае пиперидиниевых ПАВ агрегационная активность незначительно изменяется при введении гидроксиэтильных и гидроксильных фрагментов [28].
Несмотря на то, что природа головной группы мало влияет на величину ККМ при равном вкладе гидрофобного эффекта, определяемого длиной алкильного радикала, полярный фрагмент может существенно контролировать размер и морфологию агрегатов, а также специфику проявления функциональной активности систем. Например, в ряду имидазолиевых ПАВ как для незамещенных, так и гидроксиэтилированных производных, наблюдается увеличение размера агрегатов: от небольших ≤ 4–6 нм до крупных частиц ∼100 нм в случае высших гомологов. Данные динамического рассеяния света и ТЭМ позволяют сделать предположение о формировании червеобразных агрегатов [22, 31]. В то же время для гомологической серии пирролидиниевых ПАВ размеры агрегатов соответствуют присутствию сферических мицелл и не зависят от длины алкильного радикала [27, 40].
В работе [32] показано, что функционализация имидазолиевых ПАВ метоксифенильным фрагментом (MPI-n; рис. 1) приводит к существенному снижению ККМ, например, в случае цетильного производного – до 0.35 мМ (тензиометрия). Вероятно, кроме дополнительных межмолекулярных взаимодействий с участием введенного ароматического заместителя таких, как стэкинг-эффект, агрегационная активность может контролироваться также геометрическим фактором в связи с изменением параметра упаковки. Влияние геометрического фактора подтверждается изменением морфологии агрегатов в данном гомологическом ряду: наблюдается переход от крупных агрегатов везикулярного типа в случае децильного производного к небольшим сферическим мицеллам.
Систематические исследования агрегационных свойств, размеров и морфологии были проведены при последовательной функционализации катионных ПАВ аммониевого ряда карбаматными группами при варьировании длины алкильного заместителя как у заряженного азота, так и в карбаматном фрагменте (CB-m-n) (рис. 1) [33–35]. Например, значение ККМ снижается в ряду CB-2-16 > CB-4-16 > CB-6-16 > CB-8-16 от 0.7 до 0.05 мМ (тензиометрия) (табл. 1). Увеличение длины алкильного радикала в карбаматном фрагменте от этильного до додецильного сопровождается морфологическим переходом мицелла–везикула, причем в системах CB-8-16 и CB-10-16 наблюдается бимодальное распределение агрегатов по размеру: сосуществование небольших сферических агрегатов и крупных везикулярных частиц около 100 нм.
Введение карбаматного фрагмента в имидазолевые (CB-Im-m-n) [37, 38] и пирролидиниевые (CB-Pyr-m-n) [36] ПАВ (рис. 1) оказывает аналогичный эффект, вызывая снижение ККМ по сравнению с нефункционализированными аналогами. Удлинение алкильного радикала также традиционно сопровождается уменьшением ККМ. Например, для цетильных производных имидазолиевых ПАВ величина ККМ снижается от 0.9 (Im-16) до 0.3 и 0.15 мМ для CB-Im-16 с этильным и бутильным радикалами в карбаматной группе, соответственно (табл. 1). Для пирролидиниевых карбамат-содержащих ПАВ значения ККМ очень близко совпадают с имидазолиевыми аналогами [36].
В случае ионных ПАВ большую роль играет природа противоиона в составе ПАВ, а также добавки внешних электролитов [41–45]. Механизм влияния (так называемый солевой эффект) связан с компенсацией поверхностного заряда мицелл и с увеличением степени связывания противоионов, что было продемонстрировано как для катионных, в том числе геминальных ПАВ [43, 44], так и для анионных ПАВ [45]. Снижение поверхностного заряда приводит к уменьшению ККМ ПАВ, росту размера мицелл, чисел агрегации и сопровождается мицеллярным переходом сфера–цилиндр. При дальнейшем возрастании концентрации противоионов может наблюдаться формирование длинных червеобразных мицелл, образование сетки зацеплений и появление вязкоэластичных свойств. Влияние противоионов и добавок электролитов принято описывать в рамках рядов Хофмейстера (лиотропных серий). В случае катионных ПАВ гидрофильные неорганические противоионы с высокой плотностью заряда обладают высоким сродством к воде и более низкой степенью связывания с мицеллами. Так для галогенид-ионов сродство к мицеллам снижается в ряду: I > Br > Cl > F. Органические электролиты проявляют гораздо более значительный солевой эффект: снижение ККМ и структурные изменения в растворах ПАВ наблюдаются при более низких концентрациях органических противоионов [46–49]. Например, при переходе от бромид- (ЦТАБ; ККМ ∼1 мМ) к тозилат-аналогу (ЦТАТ) значение ККМ снижается до 0.22 мМ [50]. Вместе с тем, для более сложных амфифильных соединений, содержащих природные фрагменты, например, пиримидин-содержащие болаамфифилы [50] и дитерпеноидные производные [51, 52], эти закономерности не соблюдаются. Значение ККМ тозилат-производного болаамфифила практически в два раза ниже, чем для бромид-аналога, однако, степень связывания тозилат-ионов ниже, чем в случае ЦТАТ. Кроме того, в этом случае не происходит типичного роста размеров агрегатов и морфологических перестроек с увеличением концентрации ПАВ. Дитерпеноидные амфифилы с бромид- и тозилат-противоионами характеризуются одинаковыми значениями ККМ. Во всем концентрационном интервале молекулы тозилат-производного в растворе образуют сферические мицеллы, тогда как в случае бромид-производного наблюдаются морфологические переходы мицелла–везикула–мицелла [51, 52].
На примере катионного ПАВ 4-аза-1-алкил-1-азониабицикло[2.2.2]октана (DABCO-n, где n – число атомов углерода в алкильном радикале) [10] исследовано влияние органических электролитов на свойства растворов ПАВ [46–49]. Показано, что солевой эффект увеличивается в ряду бензоат- < тозилат- < салицилат натрия (рис. 2а). Например, в присутствии 0.5 мМ перечисленных электролитов значение ККМ DABCO-16 снижается от 1 до 0.4; 0.14; 0.08 мМ, соответственно [46–49]. Увеличение концентрации солей сопровождается значительным снижением электрокинетического потенциала и возрастанием вязкости раствора (рис. 2б). Реологические свойства систем в значительной степени зависят от природы противоиона; в случае салицилата натрия небольшие добавки электролита инициируют переход к вязкоупругим гелеподобным системам.
Рис. 2.
(а) Зависимость величины ККМ солевых растворов DABCO-16 от логарифма концентрации соли (СS). (б) Зависимость вязкости водных растворов DABCO-16 от концентрации соли; 25 мМ DABCO-16, 35°C. На вставке: зависимость вязкости системы 25 мМ DABCO-16 – 40 мМ тозилата натрия от скорости сдвига.
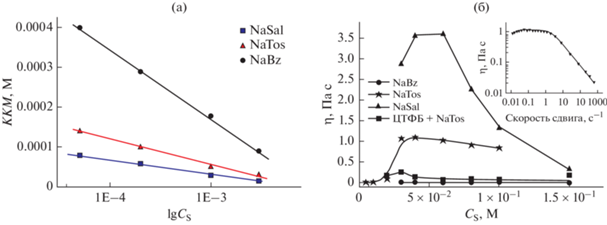
Установлено, что природа головной группы ПАВ оказывает существенное влияние на проявление солевого эффекта. В частности, значимое снижение ККМ ЦТАБ (до 0.4 мМ) происходит при добавке 10 мМ салицилата натрия, а для DABCO-16 и Mph-16 снижение ККМ до 0.08 мМ наблюдается уже в присутствии 0.5 мМ этой соли. Солевой эффект более заметно проявляется для высших гомологов, например, в тех же условиях ККМ Mph-14 снижается от 4.1 до 0.55 мМ. Реологические свойства растворов также зависят от структуры головной группы; вязкость увеличивается в ряду: ЦТАБ < Mph-16 < DABCO-16, причем концентрация электролитов, индуцирующая вязкоупругое поведение, в этом ряду снижается.
Гораздо более существенный эффект, связанный с изменением агрегационных свойств и функциональной активности, наблюдается при переходе от монокатионных ПАВ к их дикатионным аналогам [2, 4, 5, 53–58]. Наблюдаемое в этом случае снижение ККМ является тривиальным следствием увеличения гидрофобности и хорошо отражено в ранних публикациях на примере классической серии m–s–m, где m – число углеродных атомов в алкильных радикалах у головных групп ПАВ, а s – число углеродных атомов в спейсерном фрагменте [53–56]. Дополнительным специфическим фактором, контролирующим свойства геминальных ПАВ, является длина и природа спейсера, которая оказывает существенное влияние как на ККМ, так и морфологию формируемых агрегатов. Для m–s–m серии максимальные значения ККМ наблюдаются при s = 4 – 6; при этом числа агрегации снижаются с увеличением длины спейсера. Как правило, в этом случае образуются сферические мицеллы, а для s = 2 отмечен морфологический переход сфера–цилиндр. Для гидроксиэтилированных производных значения ККМ ниже по сравнению с нефункционализированными геминальными аналогами [59, 60]. Природа головной группы и структура спейсера во многом определяют функциональную активность систем. Для морфолиниевых ПАВ показано значительное усиление солюбилизационных свойств при переходе от монокатионных соединений к геминальным аналогам [61]. Для имидазолиевых геминальных ПАВ выявлена высокая антимикробная активность, в том числе к резистентным штаммам, которая контролируется длиной алкильных радикалов и мало зависит от структуры спейсера [62, 63]. Гидроксиэтилированные геминальные ПАВ также продемонстрировали высокий потенциал в качестве переносчиков ДНК [59, 60], для которых эффективность трансфекции была сопоставима с коммерческими препаратами. Показано, что активность гидроксиэтилированных ПАВ была выше, чем в случае незамещенных гомологов и контролировалась длиной спейсера. Максимальная эффективность трансфекции установлена для геминального ПАВ при s = 12.
Таким образом, ковалентная функционализация амфифильных молекул позволяет в широком диапазоне варьировать их геометрию, значение ГЛБ, и, как следствие, регулировать функциональную активность организованных растворов. На примере систем ПАВ–электролит показано, что нековалентная модификация также является эффективным приемом, позволяющим значительно изменять морфологию, поверхностные свойства и практические характеристики мицеллярных растворов. Широкие возможности в этом плане открывает использование смешанных систем на основе ПАВ различного типа [64, 65]. Этот аспект рассмотрен в следующем разделе.
2. СМЕШАННЫЕ МИЦЕЛЛЯРНЫЕ СИСТЕМЫ
2.1. Бинарные системы катионное-неионное ПАВ
Как отмечено выше, катионные ПАВ находят широкое практическое применение в качестве мицеллярных катализаторов, ингибиторов коррозии, солюбилизаторов, систем доставки лекарственных и диагностических средств, антимикробных агентов [12, 14, 66, 67]. Возможность их использования в биотехнологиях, фармакологии и медицине выдвигает задачи поиска новых нетоксичных ПАВ или создание эффективных систем на их основе, действующих в мягких условиях, обладающих большой солюбилизационной емкостью и способностью преодолевать биологические барьеры. Первый путь, способный обеспечить решение таких задач, предполагает синтез новых катионных ПАВ, обладающих пониженной токсичностью или проявляющих свои свойства в низком концентрационном интервале. Этот подход был рассмотрен выше на примере перехода от классических триалкиламмониевых ПАВ к их функционализированным аналогам или же при замене монокатионных ПАВ их дикатионными (геминальными) аналогами. Альтернативный путь – создание смешанных систем путем сочетания низкотоксичных неионных ПАВ (Твин 20, Твин 80, Тритон Х-100, Тилоксапол, амфифильные блок-сополимеры и др.) [68–71], широко применяемых в качестве солюбилизаторов при получении лекарственных составов и формировании систем доставки, с эффективными ионными ПАВ. Этот путь позволит снизить токсичность и концентрационный порог агрегации системы, не ухудшая ее функциональной, в частности, солюбилизационной активности.
Свойства растворов смесей ПАВ, такие как мицеллообразование, адсорбция и снижение поверхностного натяжения на границе раствор/воздух, пенообразование, солюбилизационное действие зависит от характера межмолекулярных взаимодействий между компонентами системы. Для оценки и описания таких систем используется теория регулярных растворов, предложенная в работах Д. Рубина и М. Розена [72, 73], актуальность которой не пропала и в настоящее время, о чем можно судить по ряду обзорных публикаций, вышедших за последние два года [74–76] и значительному числу оригинальных статей [77, 78]. В смешанных системах гидрофильные фрагменты неионного ПАВ могут встраиваться между заряженными головными группами ионного ПАВ за счет ион-дипольных взаимодействий, снижая таким образом электростатическое отталкивание между ними, уменьшая плотность заряда и электрический потенциал на поверхности мицелл. В случае эффективного взаимодействия между молекулами ПАВ может возникнуть синергетический эффект и отрицательное отклонение от модели идеального смешивания. В противоположном случае наблюдается антагонистический эффект и положительное отклонение, если преобладают силы межмолекулярного отталкивания (рис. 3).
Рис. 3.
Схематическое изображение мицеллообразования в смешанных системах (а) и проявление синергетического эффекта в системе СВ-2,2-16 Твин 80 (б).
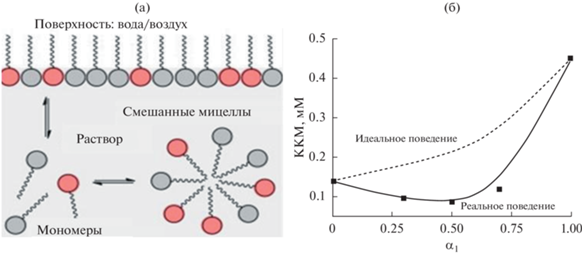
Для идеальных растворов используется простой подход, позволяющий оценить значения ККМ для идеальной системы (C*) по уравнению (3) [79]:
(1)
$\frac{1}{{C{\kern 1pt} *}} = \frac{{{{\alpha }_{1}}}}{{{{C}_{1}}}} + \frac{{{{\alpha }_{2}}}}{{{{C}_{2}}}},$В рамках теории регулярных растворов [73, 74] для учета неидеальности смешанной системы в уравнение (1) вводят коэффициенты активности компонентов ПАВ1 и ПАВ2 (f1 и f2) и параметр взаимодействия между ними в смешанных мицеллах (β):
где x1 – мольная доля ПАВ1 в смешанных агрегатах, которая может быть рассчитана путем решения методом итераций уравнения (4):(4)
$\frac{{x_{1}^{2}\ln \left( {\frac{{{{a}_{1}}C{\kern 1pt} *}}{{{{x}_{1}}{{C}_{1}}}}} \right)}}{{{{{(1 - {{x}_{1}})}}^{2}}\ln \left( {\frac{{(1 - {{a}_{1}})C{\kern 1pt} *}}{{(1 - {{x}_{1}}){{C}_{2}}}}} \right)}} = 1.$Уравнение (5) позволяет рассчитать параметр межмолекулярного взаимодействия β, который учитывает степень отклонения системы от идеального поведения. Величина β < 0 предполагает наличие сил притяжения между разнотипными молекулами ПАВ в агрегатах, тогда как значение β > 0 указывает на преобладание сил отталкивания между ними.
(5)
$\beta = \frac{{\ln \left( {\frac{{{{a}_{1}}C{\kern 1pt} *}}{{{{x}_{1}}{{C}_{1}}}}} \right)}}{{{{{(1 - {{x}_{1}})}}^{2}}}}.$Солюбилизационное действие смешанных систем является одним из важнейших практически значимых проявлений синергизма функциональных свойств. Часто для изучения процессов солюбилизации в качестве удобных и информативных спектральных зондов привлекают разнообразные гидрофобные красители. В таких исследованиях с одной стороны решают фундаментальные проблемы, характеризуя термодинамику взаимодействий компонентов в системе, с другой стороны обращаются к практическим задачам, позволяющим оптимизировать условия применения растворов ПАВ в текстильной промышленности, в природоохранных мероприятиях по удалению красителей из сточных вод и т.д. Среди публикаций последних лет следует выделить серию работ группы А. Ремана и М. Усмана [80–84], где исследованы свойства ряда прямых (Direct Brown 2, Direct Red 13, Direct Red 28, Direct Black 2) и реактивных (Reactive Red 195, Reactive Blue 221) красителей в смешанных системах, содержащих ЦТАБ или цетилпиридиний хлорид в качестве катионной компоненты, и Тритон Х-100 или Твин 20 как неионную составляющую. В них методами спектрофотометрии и кондуктометрии изучено влияние красителя на ККМ индивидуальных и смешанных систем, исследованы области локализации красителя в мицеллах различного состава, определены константы связывания и коэффициенты распределения красителя, а также свободная энергия Гиббса соответствующих процессов. Аналогичный подход применяли в работах [85, 86] при исследовании солюбилизации реактивных красителей Black 5, Yellow 145, Blue-250 и Red-198 в системах ЦТАБ–Тритон Х-100. Авторы показали, что в растворах ЦТАБ эти анионные красители образуют ионную пару с молекулами ПАВ и значительно увеличивают значения ККМ. Добавление неионного ПАВ Тритон Х-100 приводит к усилению гидрофобности агрегата в целом, обеспечивает более глубокое проникновение красителя в мицеллу и приводит к снижению ККМ. Кроме того, авторы отмечали, что смешанные системы имеют расширенный рабочий температурный диапазон и делают систему менее чувствительной к присутствию в растворах различных солей.
Солюбилизацию, как свойство смешанных мицеллярных систем, в которых проявляется синергизм действия катионного и неионного ПАВ, часто используют при доставке лекарственных средств. В работе [87] детально исследовали систему Тритон Х-100–ЦТАБ, определяя калориметрическим методом ККМ и термодинамические параметры, а также солюбилизационное действие в отношении модельного лекарственного соединения (бензойной кислоты). Установлено, что наилучшее действие проявила эквимолярная смесь этих ПАВ. Авторы утверждают, что применяемая ими методология исследования смешанных мицелл может лечь в основу успешного дизайна наноразмерных носителей для труднорастворимых лекарств.
Мицеллы катионных ПАВ серии ТМА-n и неионных (Тилоксапол, Твин 80, Твин 20) были использованы для солюбилизации левофлоксацина [88]. В ходе работы определены константы связывания и термодинамические параметры системы. Показано, что солюбилизация увеличивается по мере роста содержания катионного ПАВ и наилучшие показатели определены для ЦТАБ. Методом кругового дихроизма с использованием структурных и транспортных белков авторами выявлена высокая биосовместимость левофлоксацина, иммобилизованного в смешанных мицеллах.
В работе [89] исследовали солюбилизацию кверцетина в смешанных системах на основе додецилимидазолиевых, пиперидиниевых, пирролидиниевых катионных ПАВ и плюроника F108. Методом дифференциальной импульсной вольтамперометрии было установлено, что кверцетин локализуется в ядре смешанных мицелл, что, как показано на тестах in vitro, обеспечивает его замедленное высвобождение по сравнению со свободным лекарством. На клеточных линиях карциномы молочной железы MDA-MB 231 было продемонстрировано высокое противоопухолевое действие смешанных систем. Отмечено, что свойства исследуемых композиций могут настраиваться за счет изменения строения головной группы катионного ПАВ. Также изменение растворимости кверцетина в зависимости от соотношения компонентов изучали в бинарных системах, состоящих из гидроксипиперидиниевых ПАВ и Твин 80 [90].
Смешанные системы на основе катионных ПАВ, содержащих один или два гидрофобных радикала у четвертичного атома азота, и неионных ПАВ (Бридж 96, Тилоксапол и Tвин 80) были использованы для улучшения растворимости противотуберкулезного препарата рифампицин [91]. Параллельно методами тензиометрии и ТЭМ была показана возможность существования в этих системах агрегатов различного типа – мицелл и везикул. Установлено, что наиболее благоприятным местом локализации рифамицина является гидрофобная область смешанных мицелл, которые не только увеличивают его растворимость, но и повышают стабильность, предохраняя от гидролиза и окисления.
Детальный анализ термодинамических параметров, связанных с распределением четырех антибиотиков тетрациклинового ряда в смешанных мицеллярных системах ЦТАБ–Тритон Х-100 позволил выявить и количественно охарактеризовать механизм солюбилизации лекарств [92]. Авторами сделано заключение, что вариации констант связывания антибиотиков обусловлены наличием различных типов полярных групп в основной кольцевой структуре тетрациклина: наличие дополнительной группы –ОН (в доксициклине и окситетрациклине) способствует их более эффективному распределению в мицеллярных структурах.
Синергизм солюбилизационного действия смешанных систем, сформированных на основе биоразлагаемых карбаматсодержащих ПАВ с неионными амфифилами (Твин 20, Твин 80, Тритон Х-100), по отношению к нестероидным противовоспалительным препаратам (индометацин, мелоксикам) отмечен в работах [93, 94]. Высокое солюбилизационное действие смешанных мицеллярных систем лежит в основе их успешного использования в качестве реакционной среды и проявления мицеллярного каталитического эффекта. Наиболее широко исследовано протекание в таких системах процессов окисления и нуклеофильного замещения. Так в работе [95] была изучена кинетика окисления толуола в смешанных мицеллах 1-тетрадецил-3-метилимидазол-1-иума с неионным ПАВ октилфенолом. В условиях варьирования соотношения ПАВ в растворе определен молярный коэффициент солюбилизации и коэффициент распределения толуола. Авторами подобрана максимально эффективная система, позволяющая проводить селективное окисление субстрата с использованием перекиси водорода в качестве “зеленого” реагента.
Исследование окисления ванилиновой кислоты коллоидным MnO2 в кислой среде, протекающего в индивидуальных растворах ЦТАБ и Tвин 20, а также в их смеси, показало увеличение скорости процесса при переходе из воды в мицеллярные растворы [96]. Авторы сопоставляли данные кондуктометрических исследований и каталитические профили для смешанных систем и в обоих случаях показали отрицательное отклонение от идеальности при синергетическом взаимодействии ПАВ.
Интересен пример исследования кинетики окисления лимонена гидропероксидами в присутствии ЦТАБ, протекающего в хлорбензоле [97]. Показано образование смешанных мицелл катионных ПАВ с неионными амфифильными реагентами, в частности с трет-бутилгидропероксидом, что влечет за собой ускоренный распад гидропероксида на радикалы и существенным образом влияет на скорость и механизм окисления.
Среди работ, посвященных исследованию процессов нуклеофильного замещения в сложных эфирах, можно выделить работы по исследованию щелочного гидролиза эфиров карбоновых кислот и кислот тетракоординированного фосфора [98–103]. Кинетические данные для этих процессов интерпретируются с точки зрения псевдофазной модели мицеллярного катализа. В этом случае предпочтение отдается катионным ПАВ: скорость реакции увеличивается по мере роста гидрофобности и плотности заряда мицеллы. Использование смешанных систем позволяет планомерно снижать поверхностный потенциал и управлять скоростью процесса. Дополнительным инструментом настройки может служить варьирование ГЛБ неионного ПАВ. Так скорость гидролиза этил-п-нитрофенилхлорметилфосфоната в системе ЦТАБ–Бридж 97 падает по мере увеличения доли неионного ПАВ. В индивидуальных растворах Бридж 97 скорость реакции оказывается практически такой же, как в растворах в отсутствие ЦТАБ [98]. При проведении этого же процесса в системе ЦТАБ–Бридж 35 в условиях изменения соотношения компонентов можно наблюдать переход от ускорения до глубокого ингибирования и даже прекращения реакции при высокой концентрации неионного ПАВ [99]. Это связано с различным характером локализации реагентов в мицелле, который в случае Бридж 35 приводит к разобщению субстрата и гидроксид-иона.
Еще один способ регулирования каталитического действия смешанных систем реализуется в случае, если используемое катионное ПАВ содержит фрагменты, способные к депротонизации. Образующийся при этом амфифильный нуклеофил вступает во взаимодействие со сложным эфиром и вносит дополнительный, порой значительный, вклад в наблюдаемую скорость его расщепления. Добавление неионного ПАВ влияет на кислотно-основные равновесия в системе, как правило уменьшая долю анионной (нуклеофильной) формы катионного ПАВ, изменяя при этом не только скорость, но и механизм процесса. Такая ситуация описана для растворов гидроксипиперидиниевых ПАВ [101], а также пиперидиниевых и имидазолиевых ПАВ, функционализированных оксимным фрагментом [102], в сочетании с Твин 80, в реакциях расщепления эфиров кислот фосфора.
Аналогичные примеры синергизма в бинарных композициях характерны и для другого типа нуклеофильного замещения – аминолиза, например, реакции пиперидина и фенилсалицилата в растворах ЦТАБ и моногексадецилового эфира полиэтиленгликоля [104]. В работах [105–107] исследованы процессы аминолиза эфиров карбоновых кислот, протекающие в растворах катионных ПАВ в присутствии жирных аминов, которые выполняют роль неионного ПАВ. Образующиеся смешанные мицеллы позволяют достигать высоких ускорений реакции. Показано, что процесс аминолиза п-нитрофенилкаприната в присутствии дециламина протекает в 70 раз быстрее, чем в присутствии этиламина. Таким образом использование бинарных растворов катионного и неионного ПАВ в качестве реакционной среды открывает широкие перспективы для направленного влияния на скорость и механизм протекающих в них процессов.
2.2. Катанионные системы
В настоящее время смешанные системы на основе катионных и анионных ПАВ вызывают все больший интерес [108–110]. Это связано с тем, что между компонентами системы возникает эффект сильного синергизма, обусловленного электростатическим взаимодействием между противоположно заряженными головными группами молекул ПАВ, что проявляется в их большей поверхностной активности, более низкой ККМ и улучшенных реологических свойствах по сравнению с исходными ПАВ [111]. Основными факторами, ответственными за снижение ККМ в смешанных системах, являются увеличение энтропии за счет смешивания ПАВ и уменьшение свободной энергии мицеллообразования из-за снижения плотности поверхностного заряда, вызванного эффективной ассоциацией противоположно заряженных амфифилов [110]. Смеси катионных и анионных ПАВ обычно называют катанионными системами. Впервые этот термин был использован П. Йокела с соавторами в 1987 году [112]. Особый интерес к этим системам возник после сообщения о спонтанном образовании везикул в катанионных смесях [113].
Обычно катанионные системы не стабильны в эквимолярных концентрациях, поэтому катанионные агрегаты образуются при избытке либо положительного, либо отрицательного заряда. Наиболее широко изучена катанионная система на основе додецилсульфата натрия (ДСН), ЦТАБ и цетилтриметиламмоний хлорида [114–117]. Показано снижение порога агрегации, улучшение межфазных характеристик, разнообразие морфологии агрегатов, исследована солюбилизация лекарственных веществ [114], а также пролонгированное высвобождение субстратов [118].
Для катанионных смесей характерно мультифазное поведение и равновесное распределение самособирающихся структур в объеме раствора, включая сферические, палочковидные или червеобразные смешанные мицеллы [119–122]. Показано, что инициировать различные морфологические перестройки можно при изменении концентрации ПАВ и температуры [123], воздействии УФ-облучения [124] или включении каких-либо добавок [125, 126]. Способность катанионных систем образовывать везикулы широко используется для инкапсулирования лекарственных веществ [127–129] и субстратов различной природы, например, полициклических ароматических углеводородов [130] или растительных белков, в частности зеина [131]. В работе [128] показано, что катанионные агрегаты, в которых роль катионной составляющей выполняет производное хлорамбуцила, применяющееся в качестве химиотерапевтического средства, могут использоваться для безопасной и эффективной доставки лекарств для лечения рака. Липосомальные катанионные комплексы также могут быть использованы для доставки терапевтических агентов в ткани/органы с высоким локальным рН [129]. Свойства катанионных везикул, где катионной составляющей является ПАВ на основе аргинина, а анионной – соли жирных кислот, изучены в работе [126]. Авторы утверждают, что путем изменения соотношения катионное/анионное ПАВ можно модулировать антимикробную и гемолитическую активность целевого амфифила. Показано, что включение холестерина в катанионные смеси повышает стабильность этих коллоидных систем и значительно снижает их цитотоксичность, не влияя на их антимикробную активность. Везикулы бензил-н-гексадецилдиметиламмоний 1,4-бис-2-этилгексилсульфосукцината обладают высокой стабильностью при различных температурах и значениях pH, что делает их эффективными носителями различных лекарств, таких как инсулин [132]. В работе [133] катанионные везикулы на основе ДСН и морфолиния, функционализированного сложным эфиром, использовали в качестве матрицы для получения наносфер кремнезема, пригодных для инкапсулирования диклофенака натрия.
В настоящее время значительный интерес вызывают биосовместимые ПАВ. Включение фосфолипидов в качестве одного из ПАВ придает большую биосовместимость наноконтейнерам и обеспечивает низкую токсичность систем [108, 134, 135]. В ряде работ [136–141] получены смешанные системы на основе катионных ПАВ и отрицательно заряженных липидов. Показано, что модифицированные липосомальные формулировки обладали низкой токсичностью, способностью инкапсулировать лекарственные вещества различной природы (гидрофильные и гидрофобные), а также преодолевать биологические барьеры (гематоэнцефалический барьер, митохондриальную и клеточную мембраны, модель кожи). Кроме того, для данных систем наблюдалось пролонгированное высвобождение субстратов, а также хорошая коллоидная стабильность частиц, которая обеспечивалась высоким положительным зарядом везикул.
Таким образом, катанионные системы обладают значительным потенциалом для успешного применения в области доставки лекарств. Эти системы могут вести себя как носители, инкапсулируя лекарственные вещества, и могут использоваться для их пролонгированного высвобождения. Кроме того, лекарственные вещества могут выступать в качестве одного из компонентов катанионной смеси, что при формировании бислойной мембраны приводит к увеличению загрузки лекарственного вещества.
3. СУПРАМОЛЕКУЛЯРНЫЕ СИСТЕМЫ НА ОСНОВЕ МАКРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
3.1. Амфифильные макроциклы
Среди всего многообразия амфифильных молекул особый интерес вызывают амфифильные макроциклы, прежде всего каликсарены. Низкая токсичность, биосовместимость, а также способность каликсаренов к комплексообразованию с широким спектром органических и неорганических веществ закладывают прочную основу для их практического применения в биомедицине в качестве наноконтейнеров для доставки лекарств. Данные макроциклы имеют гидрофобную полость с регулируемым размером и конформацией, а верхний и нижний ободы каликсаренов могут быть функционализированы разнообразными заместителями, придающими рецепторные, стимул-чувствительные и таргетные свойства. Лекарственные препараты могут локализоваться в “чашах” каликсаренов за счет образования комплексов “гость-хозяин” [142–144], солюбилизироваться в гидрофобную область агрегатов [144, 145] и инкапсулироваться в водном ядре везикулярных частиц [146].
Амфифильные каликс[4]арены имеют гидрофильный головной фрагмент, образованный ионными группами на одном ободе, чаще всего на более широком верхнем, и гидрофобную часть, образованную н-алкильными заместителями на противоположном ободе (рис. 4). Из-за разной ширины верхнего и нижнего ободов каликс [4]арен представляет собой тетрамерную конусообразную молекулу, что является предпосылкой для мицеллярной агрегации [147, 148]. Немодифицированные каликсарены и каликсарены, имеющие метильные фрагменты на нижнем ободе, не образуют агрегатов, а сульфонатные каликсарены с н-бутильными и более длинными “цепями” самоорганизуются в мицеллы. Причем порог агрегации амфифильных макроциклов значительно ниже, чем у аналогичных по химическому строению классических ПАВ. Например, значения ККМ додецилбензолсульфоната натрия и его геминального производного составляют 3.2 и 0.52 мМ [149] соответственно, в то время как значение ККМ додецильного сульфокаликс[4]арена равно 0.02 мМ [150]. Молекулы ПАВ в составе сформированных ими мицелл имеют меньшую степень свободы, чем в объеме воды, поэтому энтропия амфифилов в процессе их агрегации значительно уменьшается. Предорганизованная структура каликсарена приводит к гораздо меньшим потерям энтропии в процессе формирования агрегатов, чем в случае соответствующего ему мономера, что и обусловливает более низкое значение ККМ по сравнению с ПАВ [151].
Аналогично поведению геминальных ПАВ [152], значение ККМ амфифильных каликсаренов зависит не от общего числа метиленовых звеньев, а от числа звеньев в одной алкильной группе [153]. Интересно провести соотнесение зависимостей ККМ от числа углеродных атомов алкильных “цепей” амфифильных ПАВ и макроциклов. Если полулогарифмическая зависимость ККМ от длины алкильных заместителей виологенового каликс[4]резорцина (ВР-n) (рис. 1) пересекает ось ординат в области отрицательных значений (рис. 5) [154, 155], то для виологенового ПАВ (В-n) данная точка пересечения с осью ординат обычно положительная [79, 157–159] и отражает неблагоприятное влияние переноса гидрофильной группы из водной среды в мицеллярную псевдофазу на процесс мицеллообразования. Отрицательная точка пересечения с осью ординат в случае макроциклов говорит о том, что влияние ионных групп на процесс агрегации компенсируется тем, что ароматические “кольца” и метиленовые “мостики” каликсареновой платформы также способствуют образованию агрегатов из-за кооперативных нековалентных взаимодействий.
Рис. 5.
Зависимость логарифма значений ККА водных растворов ВР-n и B-n от длины алкильных заместителей в их структуре.

Помимо очевидного влияния длины алкильных фрагментов в составе амфифильных каликсаренов на процессы их самоорганизации в водной среде, агрегационное поведение данных макроциклов также зависит от числа ароматических звеньев. При этом обнаружена немонотонная корреляция между тенденцией изменения значений ККМ и числом мономерных единиц в структуре макроцикла. С увеличением числа ароматических единиц в составе каликсаренов их агрегация усиливается из-за возрастания гидрофобности [160, 161]. Однако в ряде других работ показано снижение агрегации с увеличением числа звеньев в структуре макроцикла [155, 162]. В этом случае увеличение значений ККМ обусловлено необходимостью предварительного изменения конформации гекса- и ок-томерного аналогов на коническую, подходящую для образования сферических агрегатов, что требует дополнительных затрат энергии [153, 155].
Агрегаты, формируемые каликсаренами, отличаются большим разнообразием по сравнению с агрегатами сходных по строению ПАВ. Например, молекулы ДСН образуют сферические мицеллы со средним радиусом 2.1 нм, соответствующий ему амфифильный сульфонатокаликс[4]арен формирует мицеллы со средним радиусом 6.9 нм [150], а гексамерное производное образует агрегаты различного размера с радиусом от 70 нм до 195 нм в зависимости от концентрации [163]. В связи этим заранее предсказать морфологию агрегатов на основе каликсаренов достаточно сложно из-за их уникальной структуры, что объясняется конформационной лабильностью, а также множественными внутри- и межмолекулярными взаимодействиями.
Амфифильные макроциклы отличаются от ПАВ не только агрегационными свойствами, но и особой биологической активностью. Стоит отметить пониженную гемо- и цитотоксичность виологеновых макроциклов по отношению к нормальным клеткам по сравнению с виологеновыми ПАВ [154]. Учитывая наличие виологеновых и алкильных групп в структуре макроциклов в четырехкратном избытке по сравнению с ПАВ, можно говорить об удивительном эффекте предорганизации функциональных групп на каликсареновой платформе, позволяющем благоприятно изменить биологические свойства с точки зрения снижения токсичности систем.
3.2. Супраамфифилы макроцикл–ПАВ
Неамфифильные макроциклы обладают способностью влиять на агрегатные свойства некоторых ПАВ благодаря формированию комплексов “гость–хозяин”. Добавление такого типа макроцикла к ПАВ приводит к образованию супрамолекулярного амфифила (супраамфифила) за счет нековалентных взаимодействий (электростатических, гидрофобных, ван-дер-ваальсовых, водородных связей и т.д.) [164]. Динамическая и обратимая природа нековалентных взаимодействий может придать сформированной супрамолекулярной системе чувствительность к внешним факторам, что создает предпосылки использования подобных супрамолекулярных ансамблей в качестве интеллектуальных наноматериалов.
Совместная агрегация с участием макроцикла и ПАВ обычно начинается при определенной концентрации ПАВ аналогично формированию полимер-коллоидных систем, и такую концентрацию принято называть критической концентрацией агрегации (ККА), которая ниже значения ККМ свободного ПАВ [165]. В некоторой степени эти системы подобны катанионным мицеллярным ансамблям, рассмотренным в предыдущем разделе. Мультизаряженный макроцикл может эффективно снижать потенциальную энергию электростатического отталкивания головных групп ПАВ, в результате чего происходит совместная агрегация в более компактные наночастицы при более низкой концентрации, чем ККМ индивидуального ПАВ. В присутствии сульфонатного каликс[6]арена порог агрегации октил-, додецил- и октадецилтриметиламмониевого ПАВ снижается в 12, 70 и 15 раз, соответственно [166]. На примере додецилтриметиламмония бромида показано, что концентрация макроцикла слабо влияет на значение ККА при совместной агрегации [167]. Благодаря сульфонатному каликс[4]арену значение ККА виологенового ПАВ с додецильной группой снижается практически в 1000 раз [168].
Коллоидные свойства как ПАВ, так и каликсаренов могут модулироваться путем образования супраамфифилов, что приводит к появлению специфических адсорбционных и спектральных свойств. В работе [169] показано ускоренное снижение поверхностного натяжения ЦТАБ в присутствии сульфонатных каликсаренов. Интересно, что в индивидуальном состоянии данные ПАВ и макроциклы не флуоресцируют, а формирование супраамфифилов при стехиометрическом соотношении компонентов вызвало появление флуоресцентного сигнала. Кроме этого, в данной работе отмечается способность супраамфифилов связывать белки и влиять на их активность.
Супраамфифилы подобно мицеллярным агрегатам на основе индивидуальных ПАВ способны увеличивать растворимость липофильных лекарств в воде. Супраамфифил на основе сульфонатного каликс[5]арена и бола-ПАВ более чем в 1000 раз увеличивает водную растворимость противоопухолевого препарата тамоксифена [170]. В зависимости от длины молекулы бола-ПАВ возможно образование не только смешанных везикул на основе супраамфифилов, но и капсул. Совершенно очевидно, что формирование супраамфифилов позволяет объединять структурные и физические свойства исходных компонентов в единой супрамолекулярной системе, уникальные свойства которой могут быть положены в основу разработки перспективных полифункциональных наноматериалов.
ЗАКЛЮЧЕНИЕ
Таким образом, рассмотрены два класса амфифильных соединений: классические коллоидные ПАВ и макроциклические аналоги на основе каликсаренов. Проанализировано влияние структурного фактора (природа полярного фрагмента, геометрия молекул, гидрофобность соединений) на проявление агрегационных свойств и функциональной активности. Показано, что двумя альтернативными подходами к дизайну новых супрамолекулярных систем является ковалентная функционализация амфифильных молекул и нековалентная модификация, связанная с формированием смешанных систем. Индивидуальная и совместная агрегация ПАВ служит универсальной стратегией получения функциональных наноплатформ, рациональный дизайн которых является одной из центральных проблем коллоидной и супрамолекулярной химии. Направленный синтез амфифильных соединений позволяет создавать новые строительные блоки, сочетающие в себе преимущества классических ПАВ и молекул более сложной геометрии, использование которых в создании супрамолекулярных систем может придать им уникальные свойства и улучшить эксплуатационные характеристики. Срез современной литературы свидетельствует о широком интересе к фундаментальным аспектам [171, 172] и возрастающем практическом потенциале супрамолекулярных систем, позволяющем оперативно реагировать на вызовы, связанные с решением биомедицинских [173, 174] и экологических [175] проблем.
Список литературы
Buettner C.S., Cognigni A., Schröder C. et al. Surface-active ionic liquids: a review // Journal of Molecular Liquids. 2022. V. 347. P. 118160.
Ahmady A.R., Hosseinzadeh P., Solouk A. et al. Cationic gemini surfactant properties, its potential as a promising bioapplication candidate, and strategies for improving its biocompatibility: a review // Advances in Colloid and Interface Science. 2022. V. 299. P. 102581.
Захарова Л.Я., Коновалов А.И. Супрамолекулярные системы на основе катионных поверхностно-активных веществ и дифильных макроциклов // Коллоидный журнал. 2012. Т. 74. № 2. С. 209.
Brycki B., Szulc A. Gemini surfactants as corrosion inhibitors. A review // Journal of Molecular Liquids. 2021. V. 344. P. 117686.
Naqvi A.Z., Din K., Panda M. Mixed micellization: improved physicochemical behavior of different amphiphiles in presence of gemini surfactants // Journal of Molecular Liquids. 2021. V. 343. P. 116876.
Petkova B., Tcholakova S., Chenkova M. et al. Foamability of aqueous solutions: role of surfactant type and concentration // Advances in Colloid and Interface Science. 2020. V. 276. P. 102084.
Mustan F., Politova-Brinkova N., Vinarov Z. et al. Interplay between bulk aggregates, surface properties and foam stability of nonionic surfactants // Advances in Colloid and Interface Science. 2022. V. 302. P. 102618.
Дементьева О.В. Мезопористые частицы-контейнеры из кремнезема: новые подходы и новые возможности // Коллоидный журнал. 2020. Т. 82. № 5. С. 523.
Jesus C.F., Alves A.A.S., Fiuza S.M. et al. Mini-review: synthetic methods for the production of cationic sugar-based surfactants // Journal of Molecular Liquids. 2022. V. 342. P. 117389.
Zakharova L.Y., Pashirova T.N., Doktorovova S. et al. Cationic surfactants: self-assembly, structure-activity correlation and their biological applications // International Journal of Molecular Sciences. 2019. V. 20. № 22. P. 5534.
Zakharova L.Y., Mirgorodskaya A.B., Zhiltsova E.P. et al. // Molecular Encapsulation: Organic Reactions in Constrained Systems. Ed. by Brinker U.H. and Mieusset J.L. Chichester: Wiley, 2011. P. 15.
Kashapov R., Gaynanova G., Gabdrakhmanov D. et al. Self-assembly of amphiphilic compounds as a versatile tool for construction of nanoscale drug carriers // International Journal of Molecular Sciences. 2020. V. 21. № 18. P. 6961.
Антипин И.С., Алфимов М.В., Арсланов В.В. и др. Функциональные супрамолекулярные системы: дизайн и области применения // Успехи химии. 2021. Т. 90. № 8. С. 895.
Gaynanova G., Vasileva L., Kashapov R. et al. Self-assembling drug formulations with tunable permeability and biodegradability // Molecules. 2021. V. 26. № 22. P. 6786.
Русанов А.И. Мицеллообразование в растворах поверхностноактивных веществ. Санкт-Петербург: Химия, 1992.
Tanford C. The Hydrophobic Effect: Formation of Micelles and Biological Membranes, 2nd ed. New York: Wiley, 1980.
Israelachvili J.N., Mitchell D.J., Ninham B.W. Theory of self-assembly of hydrocarbon amphiphiles into micelles and bilayers // Journal of the Chemical Society, Faraday Transactions 2. 1976. V. 72. P. 1525.
Шинода К., Накагава Т., Тамамуси Б. и др. Коллоидные поверхностно-активные вещества / Под ред. Таубмана А.Б., Маркиной З.Н. Москва: Мир, 1966.
Jonsson B., Lindman B., Holmberg K. Surfactants and Polymers in Aqueous Solutions. Chichester: Wiley, 2002.
Русанов А.И. К термодинамике солюбилизации // Коллоидный журнал. 2021. Т. 83. № 1. С. 98. [Rusa-nov A.I. On the Thermodynamics of Solubilization // Colloid Journal. 2021. V. 83. № 1. P. 127.]
Kuznetsov D.M., Kuznetsova D.A., Gabdrakhmanov D.R. et al. Triallyl ammonium amphiphiles: self-assembly and complexation with bovine serum albumin // Surface Innovations. 2022. V. 10. № 4–5. P. 298.
Samarkina D.A., Gabdrakhmanov D.R., Lukashenko S.S. et al. Cationic amphiphiles bearing imidazole fragment: from aggregation properties to potential in biotechnologies // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2017. V. 529. P. 990.
Dong B., Zhao X., Zheng L. et al. Aggregation behavior of long-chain imidazolium ionic liquids in aqueous solution: micellization and characterization of micelle microenvironment // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2008. V. 317. № 1–3. P. 666.
Samarkina D.A., Gabdrakhmanov D.R., Lukashenko S.S. et al. Aggregation capacity and complexation properties of a system based on an imidazole-containing amphiphile and bovine serum albumin // Russian Journal of General Chemistry. 2017. V. 87. № 12. P. 2826.
Mirgorodskaya A.B., Lukashenko S.S., Yatskevich E.I. et al. Aggregation behavior, anticorrosion effect, and antimicrobial activity of alkylmethylmorpholinium bromides // Protection of Metals and Physical Chemistry of Surfaces. 2014. V. 50. № 4. P. 538.
Zhao M., Zheng L. Micelle formation by N-alkyl-N-methylpyrrolidinium bromide in aqueous solution // Physical Chemistry Chemical Physics. 2011. V. 13. № 4. P. 1332.
Васильева Э.А., Лукашенко С.С., Волошина А.Д. и др. Синтез и свойства гомологической серии катионных ПАВ с пирролидиниевой головной группой, содержащей гидроксиэтильный фрагмент // Известия Академии наук. Серия химическая. 2018. Т. 7. 1280.
Kushnazarova R.A., Mirgorodskaya A.B., Kuznetsov D.M. et al. Modulation of aggregation behavior, antimicrobial properties and catalytic activity of piperidinium surfactants by modifying their head group with a polar fragment // Journal of Molecular Liquids. 2021. V. 336. P. 116318.
Gaynanova G.A., Vagapova G.I., Valeeva F.G. et al. A novel supramolecular catalytic system based on amphiphilic triphenylphosphonium bromide for the hydrolysis of phosphorus acid esters // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2016. V. 489. P. 95.
Mirgorodskaya A.B., Yackevich E.I., Gabdrakhmanov D.R. et al. Self-organization and lipoplex formation of cationic surfactants with morpholinium head group // Journal of Molecular Liquids. 2016. V. 220. P. 992.
Kuznetsova D.A., Gabdrakhmanov D.R., Lukashenko S.S. et al. Supramolecular systems based on cationic imidazole-containing amphiphiles bearing hydroxyethyl fragment: aggregation properties and functional activity // Journal of Molecular Liquids. 2019. V. 289. P. 111058.
Kuznetsova D.A., Kuznetsov D.M., Amerhanova S.K. et al. Cationic imidazolium amphiphiles bearing a methoxyphenyl fragment: synthesis, self-assembly behavior, and antimicrobial activity // Langmuir. 2022. V. 38. № 16. P. 4921.
Mirgorodskaya A.B., Kushnazarova R.A., Lukashenko S.S. et al. Carbamate-bearing surfactants: micellization, solubilization, and biological activity // Journal of Molecular Liquids. 2018. V. 269. P. 203.
Mirgorodskaya A.B., Kushnazarova R.A., Kuznetsov D.M. et al. Aggregation Behavior and Catalytic Action of Carbamate-Bearing Surfactants in Aqueous Solutions // Kinetics and Catalysis. 2022. V. 63. № 3. P. 261.
Kushnazarova R.A., Mirgorodskaya A.B., Lukashenko S.S. et al. Novel cationic surfactants with cleavable carbamate fragment: tunable morphological behavior, solubilization of hydrophobic drugs and cellular uptake study // Journal of Molecular Liquids. 2020. V. 318. P. 113894.
Kuznetsova D.A., Kuznetsov D.M., Vasileva L.A. et al. Pyrrolidinium surfactants with a biodegradable carbamate fragment : self-assembling and biomedical application // Journal of Molecular Liquids. 2021. V. 340. P. 117229.
Kuznetsova D.A., Gabdrakhmanov D.R., Ahtamyanova L.R. et al. Novel self-assembling systems based on imidazolium amphiphiles with cleavable urethane fragment for construction of soft nanocontainers for biomedicine application // Journal of Molecular Liquids. 2020. V. 298. P. 111961.
Kuznetsova D.A., Gabdrakhmanov D.R., Kuznetsov D.M. et al. Biocompatible supramolecular systems based on novel cationic imidazolium- and urethane-containing amphiphiles: self-assembly and antimicrobial properties // Journal of Molecular Liquids. 2020. V. 319. 114094.
Mirgorodskaya A.B., Yackevich E.I., Syakaev V.V. et al. Micellization and catalytic properties of cationic surfactants with head groups functionalized with a hydroxyalkyl fragment // Journal of Chemical & Engineering Data. 2012. V. 57. № 11. P. 3153.
Васильева Л.А., Кузнецова Д.А., Валеева Ф.Г. и др. Мицеллярные наноконтейнеры на основе катионных ПАВ с пирролидиниевой головной группой для повышения биодоступности лекарственных средств // Известия Академии наук. Серия химическая. 2021. Т. 7. С. 1341. [Vasileva L.A., Kuznetsova D.A., Valeeva F.G. et al. Micellar nanocontainers based on cationic surfactants with a pyrrolidinium head group for increasing drug bioavailability // Russian Chemical Bulletin. 2021. V. 70. № 7. P. 1341.]
Yusof N.S.M., Khan M.N. Quantitative correlation between counterion-affinity to cationic micelles and counterion-induced micellar growth // Advances in Colloid and Interface Science. 2013. V. 193–194. P. 12.
Kang B., Tang H., Zhao Z. et al. Hofmeister series: insights of ion specificity from amphiphilic assembly and interface property // ACS Omega. 2020. V. 5. № 12. P. 6229.
Saha A., Mal A., Ghosh S. An elaborate investigation on the transition of rod-like micelle of cetyltrimethylammonium p-toluenesulfonate in presence of different additives // Journal of Molecular Liquids. 2020. V. 309. P. 113084.
Ding H., Jiang Y., Wang Y. et al. Distributions of counterions on adsorption and aggregation behavior of gemini quaternary ammonium salt // Journal of Molecular Liquids. 2021. V. 342. P. 117495.
Jakubowska A. Interactions of divalent metal cations with headgroups of monomers, dimers, and trimers of anionic surfactant // Journal of Molecular Liquids. 2021. V. 336. P. 116331.
Валеева Ф.Г., Куряшов Д.А., Захаров С.В. и др. Супрамолекулярная система бромид 4-аза-1-гексадецил-1-азониабицикло[2.2.2]октана—салицилат натрия. Агрегационные и реологические свойства // Известия Академии наук. Серия химическая. 2013. Т. 4. С. 989.
Васильева Э.А., Захаров С.В., Куряшов Д.А. и др. Супрамолекулярные системы на основе катионных поверхностно-активных веществ: влияние гидротропных солей и противоположно заряженных полиэлектролитов // Известия Академии наук. Серия химическая. 2015. Т. 8. С. 1901.
Гайнанова Г.А., Валеева Ф.Г., Кушназарова Р.А. и др. Влияние гидротропных соединений на самоорганизацию и солюбилизационные свойства катионных ПАВ // Журнал физической химии. 2018. Т. 92. № 7. С. 1158.
Миргородская А.Б., Валеева Ф.Г., Захаров С.В. и др. Агрегационное поведение морфолиниевых ПАВ в присутствии органических электролитов // Известия Академии наук. Серия химическая. 2018. Т. 2. С. 291.
Zakharova L., Syakaev V., Voronin M. et al. New self-assembling systems based on bola-type pyrimidinic surfactants // Journal of Colloid and Interface Science. 2010. V. 342. № 1. P. 119.
Voronin M.A., Gabdrakhmanov D.R., Khaibullin R.N. et al. Novel biomimetic systems based on amphiphilic compounds with a diterpenoid fragment: role of counterions in self-assembly // Journal of Colloid and Interface Science. 2013. V. 405. P. 125.
Gabdrakhmanov D.R., Voronin M.A., Zakharova L.Y. et al. Supramolecular design of biocompatible nanocontainers based on amphiphilic derivatives of a natural compound isosteviol // Physical Chemistry Chemical Physics. 2013. V. 15. № 39. P. 16725.
Menger F.M., Littau C.A. Gemini surfactants: a new class of self-assembling molecules // Journal of the American Chemical Society. 1993. V. 115. № 22. P. 10083.
Menger F.M., Keiper J.S. Gemini surfactants // Angewandte Chemie International Edition. 2000. V. 39. P. 1906.
Zana R. Dimeric (gemini) surfactants: effect of the spacer group on the association behavior in aqueous solution // Journal of Colloid and Interface Science. 2002. V. 248. № 2. P. 203.
Hait S.K., Moulik S.P. Gemini surfactants: a distinct class of self-assembling molecules // Current Science. 2002. V. 82. P. 1101.
Hassan M., Al-Hazmi S.M., Alhagri I.A. et al. Micellar catalysis of chemical reactions by mixed surfactant systems and gemini surfactants // Asian Journal of Chemistry. 2021. V. 33. № 7. P. 1471.
Хилько С.Л., Котенко А.А., Гребенюк С.А. и др. Тензиометрические и реологические свойства функционализированных имидазолиевых ПАВ на границе раздела жидкость–газ // Коллоидный журнал. 2019. Т. 81. № 3. С. 344.
Zakharova L., Gabdrakhmanov D., Ibragimova A. et al. Structural, biocomplexation and gene delivery properties of hydroxyethylated gemini surfactants with varied spacer length // Colloids and Surfaces B: Biointerfaces. 2016. V. 140. P. 269.
Gabdrakhmanov D.R., Vasilieva E.A., Voronin M.A. et al. Soft nanocontainers based on hydroxyethylated geminis: role of spacer in self-assembling, solubilization, and complexation with oligonucleotide // The Journal of Physical Chemistry C. 2020. V. 124. № 3. P. 2178.
Mirgorodskaya A.B., Zakharova L.Y., Khairutdinova E.I. et al. Supramolecular systems based on gemini surfactants for enhancing solubility of spectral probes and drugs in aqueous solution // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2016. V. 510. P. 33.
Voloshina A.D., Gumerova S.K., Sapunova A.S. et al. The structure–activity correlation in the family of dicationic imidazolium surfactants: antimicrobial properties and cytotoxic effect // Biochimica et Biophysica Acta – General Subjects. 2020. V. 1864. № 12. P. 129728.
Amerkhanova S.K., Voloshina A.D., Mirgorodskaya A.B. et al. Antimicrobial properties and cytotoxic effect of imidazolium geminis with tunable hydrophobicity // International Journal of Molecular Sciences. 2021. V. 22. № 23. P. 13148.
Смирнова Н.А. Фазовое поведение и формы самоорганизации растворов смесей поверхностно-активных веществ // Успехи химии. 2005. Т. 74. № 2. С. 138.
Bose A.L., Bhattacharjee D., Goswami D. Mixed micelles and bicontinuous microemulsions: promising media for enzymatic reactions // Colloids and Surfaces B: Biointerfaces. 2022. V. 209. P. 112193.
Bures F. Quaternary ammonium compounds: simple in structure, complex in application // Topics in Current Chemistry. 2019. V. 377. P. 14.
Sar P., Ghosh A., Scarso A. et al. Surfactant for better tomorrow: applied aspect of surfactant aggregates from laboratory to industry // Research on Chemical Intermediates. 2019. V. 45. P. 6021.
Bodratti A.M., Alexandridis P. Formulation of poloxamers for drug delivery // Journal of Functional Biomaterial. 2018. V. 9. № 1. P. 11.
Bhardwaj P., Tripathi P., Gupta R. et al. Niosomes: a review on niosomal research in the last decade // Journal of Drug Delivery Science and Technology. 2020. V. 56 (A). P. 101581.
Solomonov A.V., Marfin Y.S., Rumyantsev E.V. et al. Self-assembled micellar clusters based on Triton-X-family surfactants for enhanced solubilization, encapsulation, proteins permeability control, and anticancer drug delivery // Materials Science and Engineering: C. 2019. V. 99. P. 794.
Yadav K.S., Rajpurohit R., Sharma S. Glaucoma: current treatment and impact of advanced drug delivery systems // Life Sciences. 2019. V. 221. P. 362.
Rosen M.J., Hua X.Y. Surface concentrations and molecular interactions in binary mixtures of surfactants // Journal of Colloid and Interface Science. 1982. V. 86. P. 164.
Rubingh D.N. // Solution Chemistry of Surfactants. Ed. by Mittal K.L. N.Y.: Plenum Press, 1979. V. 1. P. 337.
Moulik S.P., Rakshit A.K., Naskar B.J. Evaluation of non-ambiguous critical micelle concentration of surfactants in relation to solution behaviors of pure and mixed surfactant systems: a physicochemical documentary and analysis // Journal of Surfactants and Detergents. 2021. V. 24. P. 535.
Naqvi A.Z., Kabir-ud-Din, Panda M. Mixed micellization: improved physicochemical behavior of different amphiphiles in presence of gemini surfactants // Journal of Molecular Liquids. 2021. V. 343. P. 116876.
Kumar H., Kaur G. Scrutinizing self-assembly, surface activity and aggregation behavior of mixtures of imidazolium based ionic liquids and surfactants: a comprehensive review // Frontiers in Chemistry. 2021. V. 9. P. 667941.
Farahani R.K., Bagheri A. The interaction of the surface active ionic liquid with nonionic surfactants (Triton X-100 and Triton X-405) in aqueous solution by using tensiometry method // Journal of Molecular Liquids. 2022. V. 345. P. 118260.
Zhou Y., Zhang X., Yang X. et al. Synergism and phase behavior of alcohol polyoxyethylene ether acetate and cationic surfactant-mixed systems // Journal of Surfactants and Detergents. 2020. V. 23. P. 145.
Clint J.H. Micellization of mixed nonionic surface active agents // Journal of the Chemical Society, Faraday Transactions. 1975. V. 1. № 71. P. 1327.
Rehman A., Usman M., Bokhari T.H. et al. The application of cationic-nonionic mixed micellar media for enhanced solubilization of Direct Brown 2 dye // Journal of Molecular Liquids. 2020. V. 301. P. 112408.
Rehman A., Usman M., Bokhari T.H. et al. Effects of nonionic surfactant (TX-100) on solubilizing power of cationic surfactants (CTAB and CPC) for Direct Red 13 // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2020. V. 586. P. 124241.
Rehman A., Nisa M. U., Usman M. et al. Application of cationic-nonionic surfactant based nanostructured dye carriers: mixed micellar solubilization // Journal of Molecular Liquids. 2021. V. 326. P. 115345.
Irshad S., Sultana H., Usman M. et al. Solubilization of direct dyes in single and mixed surfactant system: a comparative study // Journal of Molecular Liquids. 2021. V. 321. P. 114201.
Younis S., Usman M., ul Haq A. et al. Solubilization of reactive dyes by mixed micellar system: synergistic effect of nonionic surfactant on solubilizing power of cationic surfactant // Chemical Physics Letters. 2020. V. 738. P. 136890.
Noor S., Taj M. B. Mixed-micellar approach for enhanced dye entrapment: a spectroscopic study // Journal of Molecular Liquids. 2021. V. 338. P. 116701.
Noor S., Taj M.B., Iram S.M. Comparative solubilization of reactive dyes in single and mixed surfactants // Journal of Dispersion Science and Technology. 2021. Ahead-of-print. P. 1.
Juhász Á., Seres L., Varga N. et al. Detailed calorimetric analysis of mixed micelle formation from aqueous binary surfactants for design of nanoscale drug carriers // Nanomaterials. 2021. V. 11. P. 3288.
Saraf A., Sharma S., Sachar S. Evaluation of surfactants as solubilizing medium for levofloxacin // Journal of Molecular Liquids. 2020. V. 319. P. 114060.
Singla P., Singh O., Chabba S. et al. Pluronic-SAILs (surface active ionic liquids) mixed micelles as efficient hydrophobic quercetin drug carriers // Journal of Molecular Liquids. 2018. V. 249. P. 294.
Миргородская А.Б., Кушназарова Р.А., Лукашенко С.С. и др. Смешанные мицеллярные растворы гексадецилпиперидиниевых ПАВ и твин 80: агрегационное поведение и солюбилизационные свойства // Журнал физической химии. 2020. Т. 94. № 9. С. 1385.
Kumar A., Kansal S.K., Ibhadon A.O. et al. Mixed surfactant (altering chain length and head group) aggregates as an effective carrier for tuberculosis drug // Chemistry and Physics of Lipids. 2018. V. 215. P. 11.
Tinku S.Ch. A thermodynamic approach to understand the partitioning of tetracycline family antibiotics in individual and mixed micellar systems // The Journal of Chemical Thermodynamics. 2022. V. 165. P. 106664.
Mirgorodskaya A.B., Kushnazarova R.A., Lukashenko S.S. et al. Aggregation behavior and solubilization properties of mixed micellar solutions and microemulsions based on nonionic and carbamate-bearing cationic surfactants // Journal of Molecular Liquids. 2019. V. 292. P. 111407.
Миргородская А.Б., Кушназарова Р.А., Щербаков А.Ю. и др. Смешанные системы на основе катионного ПАВ с бутилкарбаматным фрагментом и неионного ПАВ твин 80: агрегационное поведение и солюбилизационные свойства // Известия Академии наук. Серия химическая. 2018. Т. 11. С. 1992.
Deore T.S., Sadgar A.L., Jayaram R.V. Mixed micelles of surface active ionic liquid (SAIL) – octylphenol ethoxylate: a novel reaction medium for selective oxidation of toluene to benzaldehyde // Journal of Surfactants and Detergents. 2021. V. 24. № 1. P. 185.
Hassan M., Dahadha A., Al-Dhoun M. et al. Kinetics of oxidation of vanillic acid by colloidal MnO2: correlation of micellar catalysis to the micellar properties of surfactants and mixed surfactants // Reaction Kinetics, Mechanisms and Catalysis. 2021. V. 133. P. 933.
Касаикина О.Т., Потапова Н.В., Круговов Д.А. и др. Катализ радикальных реакций в смешанных мицеллах поверхностно-активных веществ с гидропероксидами // Кинетика и катализ. 2017. Т. 58. № 5. С. 567.
Zakharova L., Valeeva F., Zakharov A. et al. Micellization and catalytic activity of the cetyltrimethylammonium bromide–Brij 97–water mixed micellar system // Journal of Colloid and Interface Science. 2003. V. 263. P. 597.
Захарова Л.Я., Валеева Ф.Г., Ибрагимова А.Р. и др. Факторы, определяющие каталитическую активность смешанной мицеллярной системы цетилтриметиламмонийбромид-бридж-35 в реакции гидролиза эфира фосфоновой кислоты // Кинетика и катализ. 2012. Т. 53. № 3. С. 358.
Миргородская А.Б., Яцкевич Е.И., Захарова Л.Я. и др. Смешанные мицеллярные системы геминальное поверхностно-активное вещество-неионный полимер // Коллоидный журнал. 2012. Т. 74. № 1. С. 96.
Миргородская А.Б., Валеева Ф.Г., Кушназарова Р.А. и др. Каталитический эффект мицеллярных систем на основе гидроксипиперидиниевых поверхностно активных веществ в процессах гидролиза п-нитрофенилфосфоната // Кинетика и катализ. 2020. Т. 61. № 6. С. 819.
Kapitanov I.V., Mirgorodskaya A.B., Valeeva F.G. et al. Physicochemical properties and esterolytic reactivity of oxime functionalized surfactants in pH-responsive mixed micellar system // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2017. V. 524. P. 143.
Muff J., MacKinnon L., Durant N.D. et al. Solubility and reactivity of surfactant-enhanced alkaline hydrolysis of organophosphorus pesticide DNAPL // Environmental Science and Pollution Research. 2020. V. 27. P. 3428.
Fagge I.I., Khalid Kh., Noh M.A.M. et al. Study of cationic and nonionic mixed micelles with NaBr and 3,5-Cl2C6H3CO2Na by use of probe nucleophilic reaction of piperidine with ionized phenyl salicylate // Journal of Oleo Science. 2018. V. 67. № 1. P. 55.
Миргородская А.Б., Кудрявцева Л.А., Вылегжанина Н.Н. и др. Смешанные мицеллярные системы геминальных алкиламмонийных ПАВ и длинноцепных аминов // Известия Академии наук. Серия химическая. 2010. № 4. С. 774.
Миргородская А.Б., Кудрявцева Л.Я., Иванов Б.Е. Влияние мицеллообразования n-дециламина на его основность и реакционую способность при взаимодействии с эфирами карбоновых кислот // Известия Академии наук. Серия химическая. 1996. № 2. С. 366.
García-Río L., Leis J.R., López-Fontán J.L. et al. Mixed micelles of alkylamines and cetyltrimethylammonium chloride // Journal of Colloid and Interface Science. 2005. V. 289. № 2. P. 521.
Dhawan V.V., Nagarsenker M.S. Catanionic systems in nanotherapeutics – biophysical aspects and novel trends in drug delivery applications // Journal of Controlled Release. 2017. V. 266. P. 331.
Tomašić V., Mihelj T. The review on properties of solid catanionic surfactants: main applications and perspectives of new catanionic surfactants and compounds with catanionic assisted synthesis // Journal of Dispersion Science and Technology. 2017. V. 38. № 4. P. 515.
Ghosh S., Ray A., Pramanik, N. Self-assembly of surfactants: an overview on general aspects of amphiphiles // Biophysical chemistry. 2020. V. 265. P. 106429.
Ghosh S., Ray A., Pramanik N. et al. Can a catanionic surfactant mixture act as a drug delivery vehicle? // Comptes Rendus Chimie. 2016. V. 19. № 8. P. 951.
Jokela P., Joensson B., Khan A. Phase equilibria of catanionic surfactant−water systems // The Journal of Physical Chemistry. 1987. V. 91. № 12. P. 3291.
Kaler E., Murthy A., Rodriguez B. et al. Spontaneous vesicle formation in aqueous mixtures of single-tailed surfactants // Science. 1989. V. 245. № 4924. P. 1371.
Russo Krauss I., Imperatore R., De Santis A. et al. Structure and dynamics of cetyltrimethylammonium chloride-sodium dodecylsulfate (CTAC-SDS) catanionic vesicles: high-value nano-vehicles from low-cost surfactants // Journal of Colloid and Interface Science. 2017. V. 501. P. 112.
Rajkhowa S., Mahiuddin S., Ismail K. An assessment of the aggregation and adsorption behavior of the sodium dodecylsulfate–cetyltrimethylammonium bromide mixed surfactant system in aqueous medium // Journal of Solution Chemistry. 2016. V. 46. № 1. P. 11.
Garcia M.T., Ribosa I., Gonzalez J.J. et al. Catanionic mixtures of surface-active ionic liquids and N-lauroyl sarcosinate: surface adsorption, aggregation behavior and microbial toxicity // Journal of Molecular Liquids. 2020. V. 318. P. 114040.
Ju H., Jiang Y., Geng T. et al. A green and easy synthesis method of catanionic surfactant ammonium benzenesulfonate and its surface properties and aggregation behaviors // Journal of Molecular Liquids. 2018. V. 264. P. 306.
Bibi I., Kousar T., Shah S.W.H. et al. Pseudo zwitterionic microvesicles for sustained urea release // Journal of the Serbian Chemical Society. 2020. V. 85. № 4. P. 493.
Zhai Z., Yan X., Xu J. et al. Phase behavior and aggregation in a catanionic system dominated by an anionic surfactant containing a large rigid group // Chemistry – A European Journal. 2018. V. 24. № 36. P. 9033.
Zhang J., Wang Y., Xu G. et al. Formation and rheological behavior of wormlike micelles in a catanionic system of fluoroacetic acid and tetradecyldimethylaminoxide // Soft Matter. 2017. V. 13. № 3. P. 670.
Wang P., Tan J., Pei S. et al. Dual effects of cationic surfactant on the wormlike micelle formation of catanionic surfactants mixtures: an experiment and simulation study // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2017. V. 529. P. 95.
Di Gregorio M.C., Severoni E., Travaglini L. et al. Bile acid derivative-based catanionic mixtures: versatile tools for superficial charge modulation of supramolecular lamellae and nanotubes // Physical Chemistry Chemical Physics. 2018. V. 20. № 28. P. 18957.
Lone M.S., Afzal S., Chat O.A. et al. Temperature- and composition-induced multiarchitectural transitions in the catanionic system of a conventional surfactant and a surface-active ionic liquid // ACS Omega. 2021. V. 6. № 18. P. 11974.
Liu T., Lei Q., Dong J. et al. Light-responsive vesicles based on azobenzene containing imidazolium surfactants and sodium oleate // Colloid and Polymer Science. 2019. V. 297. № 11–12. P. 1489.
Havlíková M., Szabová J., Jugl A. et al. Study of cholesterol’s effect on the properties of catanionic vesicular systems: comparison of light-scattering results with ultrasonic and fluorescence spectroscopy // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2020. V. 607. P. 125526.
Pinazo A., Pons R., Marqués A. et al. Biocompatible catanionic vesicles from arginine-based surfactants: a new strategy to tune the antimicrobial activity and cytotoxicity of vesicular systems // Pharmaceutics. 2020. V. 12. № 9. P. 857.
Rajput S.M., Mondal K., Kuddushi M. et al. Formation of hydrotropic drug/gemini surfactant based catanionic vesicles as efficient nano drug delivery vehicles // Colloid and Interface Science Communications. 2020. V. 37. P. 100273.
Jiang Y., Hu X., Zhang J. et al. Chlorambucil prodrug-participating catanionic aggregates for sustained drug release and improved antitumour activity // Journal of Molecular Liquids. 2019. V. 274. P. 556.
Reddy S.T., Sivaramakrishna D., Swamy M.J. Physicochemical characterization of lauryl glycinate-dodecyl sulfate equimolar complex: a base-triggerable catanionic liposomal system // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2017. V. 516. P. 139.
Yadav S.K., Parikh K., Kumar S. Mixed micelle formation of cationic gemini surfactant with anionic bile salt: a PAH solubilization study // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2017. V. 522. P. 105.
Chen Y., Ji X., Han Y. et al. Self-assembly of oleyl bis(2-hydroxyethyl)methyl ammonium bromide with sodium dodecyl sulfate and their interactions with zein // Langmuir. 2016. V. 32. № 32. P. 8212.
Stagnoli S., Sosa Alderete L., Luna M.A. et al. Catanionic nanocarriers as a potential vehicle for insulin delivery // Colloids and Surfaces B: Biointerfaces. 2020. V. 188. P. 110759.
Rajput S.M., Kuddushi M., Shah A. et al. Functionalized surfactant based catanionic vesicles as the soft template for the synthesis of hollow silica nanospheres as new age drug carrier // Surfaces and Interfaces. 2020. V. 20. P. 100596.
Chen Y., Qiao F., Fan Y. et al. Interactions of cationic/anionic mixed surfactant aggregates with phospholipid vesicles and their skin penetration ability // Langmuir. 2017. V. 33. № 11. P. 2760.
Ohshima H. Encyclopedia of Biocolloid and Biointerface Science. V. 2. First Edition. New Jersey: John Wiley & Sons, Inc. Published, 2016.
Mirgorodskaya A.B., Kuznetsova D.A., Kushnazarova R.A. et al. Soft nanocarriers for new poorly soluble conjugate of pteridine and benzimidazole: synthesis and cytotoxic activity against tumor cells // Journal of Molecular Liquids. 2020. V. 317. P. 114007.
Kuznetsova D.A., Gaynanova G.A., Vasileva L.A. et al. Mitochondria-targeted cationic liposomes modified with alkyltriphenylphosphonium bromides loaded with hydrophilic drugs: preparation, cytotoxicity and colocalization assay // Journal of Materials Chemistry B. 2019. V. 7. P. 7351.
Kuznetsova D.A., Gabdrakhmanov D.R., Lukashenko S.S. et al. Novel hybrid liposomal formulations based on imidazolium-containing amphiphiles for drug encapsulation // Colloids and Surfaces B: Biointerfaces. 2019. V. 178. P. 352.
Kuznetsova D.A., Vasileva L.A., Gaynanova G.A. et al. Comparative study of cationic liposomes modified with triphenylphosphonium and imidazolium surfactants for mitochondrial delivery // Journal of Molecular Liquids. 2021. V. 330. P. 115703.
Kuznetsova D.A., Vasileva L.A., Gaynanova G.A. et al. Cationic liposomes mediated transdermal delivery of meloxicam and ketoprofen: optimization of the composition, in vitro and in vivo assessment of efficiency // International Journal of Pharmaceutics. 2021. V. 605. P. 120803.
Pavlov R.V., Gaynanova G.A., Kuznetsova D.A. et al. Biomedical potentialities of cationic geminis as modulating agents of liposome in drug delivery across biological barriers and cellular uptake // International Journal of Pharmaceutics. 2020. V. 587. P. 119640.
Hu X., Gao J., Chen F. et al. A host-guest drug delivery nanosystem for supramolecular chemotherapy // Journal of Controlled Release. 2020. V. 324. P. 124.
Dai X., Zhou X., Liao C. et al. A nanodrug to combat cisplatin-resistance by protecting cisplatin with p-sulfonatocalix[4]arene and regulating glutathione S-transferases with loaded 5-fluorouracil // Chemical Communications. 2019. V. 55. P. 7199.
Li M., Mao L., Chen M. et al. Characterization of an amphiphilic phosphonated calixarene carrier loaded with carboplatin and paclitaxel: a preliminary study to treat colon cancer in vitro and in vivo // Frontiers in Bioengineering and Biotechnology. 2019. V. 7. P. 238.
Granata G., Paterniti I., Geraci C. et al. Potential eye drop based on a calix[4]arene nanoassembly for curcumin delivery: enhanced drug solubility, stability, and anti-inflammatory effect // Molecular Pharmaceutics. 2017. V. 14. № 5. P. 1610.
Kashapov R.R., Razuvayeva Y.S., Ziganshina A.Y. et al. Design of N-methyl- D-glucamine-based resorcin[4]arene nanoparticles for enhanced apoptosis effects // Molecular Pharmaceutics. 2020. V. 17. № 1. P. 40.
Kellermann M., Bauer W., Hirsch A. et al. The first account of a structurally persistent micelle // Angewandte Chemie International Edition. 2004. V. 43. № 22. P. 2959.
Israelachvili J.N. // Intermolecular and Surface Forces. 3-rd ed. Waltham: Academic Press, 2011.
Neupane D., Park J.W. Binding of dialkylated disulfonated diphenyl oxide surfactant onto alumina in the aqueous phase // Chemosphere. 1999. V. 38. № 1. P. 1.
Wang K.P., Chen Y., Liu Y. A polycation-induced secondary assembly of amphiphilic calixarene and its multi-stimuli responsive gelation behavior // Chemical Communications. 2015. V. 51. P. 1647.
Steed J. W., Turner D.R., Wallace K.J. // Core concepts in supramolecular chemistry and nanochemistry. 1-st ed. Chichester: Wiley, 2007.
Zana R., Benrraou M., Rueff R. Alkanediyl-α,ω-bis(dimethylalkylammonium bromide) surfactants. 1. Effect of the spacer chain length on the critical micelle concentration and micelle ionization degree // Langmuir. 1991. V. 7. № 6. P. 1072.
Basilio N., Garcia-Río L., Martín-Pastor M. Calixarene-based surfactants: evidence of structural reorganization upon micellization // Langmuir. 2012. V. 28. № 5. P. 2404.
Kashapov R., Razuvayeva Y., Ziganshina A. et al. Effect of preorganization and amphiphilicity of calix[4]arene platform on functional properties of viologen derivatives // Journal of Molecular Liquids. 2022. V. 345. P. 117801.
Basilio N., Garcia-Rio L. Calixarene-based surfactants: conformational-dependent solvation shells for the alkyl chains // ChemPhysChem. 2012. V. 13. № 9. P. 2368.
Wang J., Liu D., Guo X. et al. Ammonium and imidazolium-based amphiphilic tetramethoxy resorcinarenes: adsorption, micellization, and protein binding // Journal of Molecular Liquids. 2020. V. 313. P. 113587.
Valeeva F.G., Karimova T.R., Pavlov R.V. et al. Introduction of isothiuronium surfactant series: Synthesis, structure-dependent aggregation overview and biological activity // Journal of Molecular Liquids. 2021. V. 324. P. 114721.
Pashirova T.N., Burilova E.A., Lukashenko S.S. et al. Nontoxic antimicrobial micellar systems based on mono- and dicationic Dabco-surfactants and furazolidone: Structure-solubilization properties relationships // Journal of Molecular Liquids. 2019. V. 296. P. 112062.
Krieg M., Pileni M.P., Braun A. et al. Micelle formation and surface activity of functional redox relays: viologens substituted by a long alkyl chain // Journal of Colloid and Interface Science. 1981. V. 83. P. 209.
Shinkai S., Arimura T., Araki K. et al. Syntheses and aggregation properties of new water-soluble calixarenes // Journal of the Chemical Society, Perkin Transactions 1. 1989. V. 11. P. 2039.
Zhao Z.M., Wang Y., Han J. et al. Preparation and characterization of amphiphilic calixarene nanoparticles as delivery carriers for paclitaxel // Chemical and Pharmaceutical Bulletin. 2015. V. 63. № 3. P. 180.
Xu Z., Peng S., Wang Y. et al. Broad-spectrum tunable photoluminescent nanomaterials constructed from a modular light-harvesting platform based on macrocyclic amphiphiles // Advanced Materials. 2016. V. 28. № 35. P. 7666.
Ryzhkina I.S., Kiseleva Y.V., Murtazina L.I. et al. Disperse systems based on a dodecyl derivative of p-sulfonatocalix[6]arene: Self-organization and physicochemical properties in a wide range of concentrations and temperatures // Macroheterocycles. 2017. V. 10. № 2. P. 190.
Ouyang G., Liu M. Self-assembly of chiral supra-amphiphiles // Materials Chemistry Frontiers. 2020. V. 4. № 1. P. 155.
Szutkowski K., Kołodziejska Z., Pietralik Z. et al. Clear distinction between CAC and CMC revealed by high-resolution NMR diffusometry for a series of bis-imidazolium gemini surfactants in aqueous solutions // RSC Advances. 2018. V. 8. № 67. P. 38470.
Basilio N., García-Río L. Sulfonated calix[6]arene host-guest complexes induce surfactant self-assembly // Chemistry – A European Journal. 2009. V. 15. № 37. P. 9315.
Basilio N., Gõmez B., Garcia-Rio L. et al. Using calixarenes to model polyelectrolyte surfactant nucleation sites // Chemistry – A European Journal. 2013. V. 19. № 14. P. 4570.
Wang K., Guo D., Wang X. et al. Multistimuli responsive supramolecular vesicles based on the recognition of p-sulfonatocalixarene and its controllable release of doxorubicin // ACS Nano. 2011. V. 5. № 4. P. 2880.
Zhu J., Chen L., Guo X. Distinctive spectroscopic properties and adsorption behaviors of p-sulfonatocalixarene-cetyltrimethylammonium bromide supra-amphiphilic systems // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2020. V. 601. P. 125029.
Pisagatti I., Barbera L., Gattuso G. et al. Tuning the aggregation of an amphiphilic anionic calix[5]arene by selective host–guest interactions with bola-type dications // New Journal of Chemistry. 2019. V. 43. P. 7628.
Kelleppan V.T., King J.P., Butler C.S.G. et al. Heads or tails? The synthesis, self-assembly, properties and uses of betaine and betaine-like surfactants // Advances in Colloid and Interface Science. 2021. V. 297. P. 102528.
La Mesa C., Risuleo G. Surface activity and efficiency of cat-anionic surfactant mixtures // Frontiers in Chemistry. 2021. V. 9. P. 790873.
Wu Y., Li X., Gan Y. et al. Nanoparticle-mediated surfactant therapy in patients with severe COVID-19: a perspective // Journal of Materials Chemistry B. 2021. V. 9. № 35. P. 6988.
Razuvayeva Y., Kashapov R., Zakharova L. Calixarene-based pure and mixed assemblies for biomedical applications // Supramolecular Chemistry. 2020. V. 32. № 3. P. 176.
Kim J.H., Anwer H., Kim Y.S. et al. Decontamination of radioactive cesium-contaminated soil/concrete with washing and washing supernatant– critical review // Chemosphere. 2021. V. 280. P. 130419.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал




