Коллоидный журнал, 2023, T. 85, № 5, стр. 629-640
Микроэмульсии лецитина как носители лекарственных веществ
Н. М. Мурашова *
Российский химико-технологический университет имени Д.И. Менделеева
125047 Москва, Миусская пл., 9, Россия
* E-mail: namur_home@mail.ru
Поступила в редакцию 29.06.2023
После доработки 29.07.2023
Принята к публикации 03.08.2023
- EDN: DMFLDC
- DOI: 10.31857/S0023291223600517
Аннотация
В работе описаны примеры микроэмульсий на основе широко известного биосовместимого поверхностно-активного вещества (ПАВ) лецитина и возможности их применения в качестве носителей лекарственных веществ. Основной проблемой при разработке микроэмульсий лецитина является поиск подходящих соПАВ. Для получения микроэмульсий лецитина в качестве соПАВ лучше всего подходят молекулы с короткой алкильной цепью (4–5 атомов С) и относительно большой полярной “головой”, например короткоцепочечные алифатические спирты, кислоты и амины; при этом требуются высокие концентрации соПАВ (массовое соотношение соПАВ : лецитин обычно составляет 1 : 1). Чаще всего для получения микроэмульсий лецитина в различных природных и синтетических маслах в качестве соПАВ используют этанол, н-пропанол или н-бутанол. Чтобы заменить токсичные спирты на менее токсичные компоненты, в микроэмульсии лецитина можно ввести другие известные ПАВ, такие как Brij 96V (полиэтиленгликольолеат), Tween 80 (полиоксиэтилен-20-сорбитанмоноолеат), Tween 20 (полиоксиэтилен-20-сорбитанмонолаурат), Тритон Х-100 (трет-октилфениловый эфир полиэтиленгликоля) или олеиновую кислоту. Описаны композиции на основе микроэмульсий лецитина для местной анестезии, для доставки витаминов, с противовоспалительным, противогрибковым, противораковым и ранозаживляющим действием. Рассмотренные примеры показывают перспективность исследования и разработки микроэмульсий лецитина как носителей лекарственных веществ.
ВВЕДЕНИЕ
Перспективными носителями лекарственных веществ являются лиофильные коллоидные системы, образованные молекулами поверхностно-активных веществ (ПАВ), такие как микроэмульсии (МЭ). Для них характерно самопроизвольное образование при смешивании нужных компонентов в заданных условиях; теоретически, при неизменном составе и условиях, МЭ способны существовать бесконечно долго. Следствием термодинамической устойчивости МЭ являются их преимущества с точки зрения фармацевтической технологии – зависимость свойств МЭ только от их состава, а не от условий смешивания компонентов, простота методов получения, высокая воспроизводимость свойств, длительные сроки хранения.
В качестве достоинств МЭ как носителей лекарственных веществ можно указать возможность включения в их состав биологически активных веществ с различными физико-химическими свойствами. Для МЭ, имеющих капли размером в единицы и десятки нанометров, характерна высокая удельная поверхность на границе “масло-вода”, что приводит к более высокой скорости диффузии биологически-активных веществ из капель МЭ по сравнению с обычными эмульсиями. Внутренний объем капель МЭ существенно больше, чем у мицелл, что обеспечивает их более высокую солюбилизационную емкость. Таким образом, в МЭ сочетается ряд достоинств эмульсионных и мицеллярных систем. Чаще всего МЭ предлагаются для нанесения на кожу (для местного действия и для трансдермального введения лекарственных веществ) и на слизистые оболочки носа и глаз, известны примеры МЭ для перорального введения. В последние годы опубликован ряд обзорных работ, посвященных применению МЭ, образованных различными синтетическими и природными ПАВ, для адресной доставки лекарственных веществ [1–6].
Основной недостаток МЭ – наличие ПАВ и соПАВ в высоких концентрациях. МЭ, предназначенные для фармацевтики, должны содержать нетоксичные биосовместимые компоненты. В качестве нетоксичного ПАВ для получения МЭ перспективно использовать лецитин, который является основным липидным компонентом клеточных мембран.
Нужно отметить, что в биохимии слово “лецитин” часто является синонимом sn-3-фосфатидилхолина (или L-α-фосфатидилхолина). В пищевой промышленности термин “лецитин” часто используют для обозначения смеси фосфолипидов с преобладанием фосфатидилхолина. В основном лецитин и другие фосфолипиды применяют в качестве эмульгаторов в пищевой и косметической промышленности, фармацевтике, а также как пищевые и биологически активные добавки. В США лецитин относится к категории пищевых добавок GRAS (Generally recognized as safe – общепризнанных как безопасных) и не имеет максимальной суточной дозы [7].
В отсутствии соПАВ, в трехкомпонентных системах, содержащих лецитин, масло и воду, в области высоких концентраций лецитина существуют жидкокристаллические мезофазы [8–11], а при более низких его концентрациях – обратные мицеллы различной формы: сферические, как в системе лецитин–бензол–вода [11, 12], либо цилиндрические, которые в алифатических углеводородах могут формировать структуру лецитиновых органогелей [11, 13, 14]. Полагают, что лецитин – это излишне липофильный ПАВ, неспособный образовывать на межфазной границе гибкий монослой с нулевой спонтанной кривизной, который необходим для формирования сбалансированной (т.е. способной включать сравнимые количества воды и масла) МЭ. Поэтому для получения МЭ необходимо введение соПАВ, которое повысит гибкость монослоя и изменит его спонтанную кривизну [15]. Для разработки МЭ лецитина, предназначенных для медицины или косметики, необходимо подбирать одно или несколько биосовместимых соПАВ и применять биосовместимые масла, что, с учетом склонности лецитина к формированию жидкокристаллических фаз, является сложной, нетривиальной задачей и требует значительных усилий для ее решения.
В работе рассмотрены известные МЭ лецитина в различных четырех- и многокомпонентных системах и примеры их применения в качестве носителей лекарственных веществ.
МИКРОЭМУЛЬСИИ ЛЕЦИТИНА В РАЗЛИЧНЫХ СИСТЕМАХ
Микроэмульсии в четырехкомпонентных системах лецитин–соПАВ–масло–вода
Первой статьей, посвященной микроэмульсиям лецитина, считают работу Shinoda с соавт., опубликованную в 1991 году [16], в которой описана МЭ в системе соевый лецитин–гексадекан–н-пропанол–вода при концентрации пропанола в воде 10–15 мас. %. При низкой концентрации лецитина, равной 1 мас. %, микроэмульсионная фаза существует в равновесии c водной и органической фазами (система типа Винзор III), а при содержании лецитина выше 2.3 мас. % образуется только микроэмульсионная фаза (система типа Винзор IV). При уменьшении концентрации н-пропанола происходит постепенное изменение структуры МЭ от прямой к бинепрерывной и обратной [16].
Aboofazeli с соавт. в 1993–1994 годах опубликовали ряд статей по исследованию МЭ лецитина в четырехкомпонентных системах лецитин–соПАВ–органический растворитель–вода [17–20]. Было показано, что для систем лецитин–спирт–изопропилмиристат–вода тип использованного лецитина – соевый или яичный, практически не влияет на размер и форму области существования МЭ. Авторами были использованы такие спирты, как н-пропанол, н-бутанол, н-пентанол, изопропанол, изобутанол, втор-бутанол, трет-бутанол [17]. Для систем лецитин–короткоцепочечные спирты–изопропилмиристат–вода, содержащих лецитин с различной концентрацией основного вещества (92 и 68–72 мас. % фосфатидилхолина), было установлено, что везде образуется обратная МЭ. Вид фазовых диаграмм был сходным, но при концентрациях масла ниже 50 мас. % наблюдалось существенное различие в ширине области существования МЭ [18].
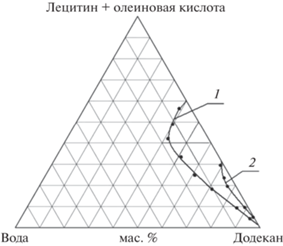
На фазовых диаграммах систем лецитин–изопропилмиристат–соПАВ–вода были показаны области существования МЭ при соотношении ПАВ : соПАВ = 1 : 1 [19], в качестве соПАВ были рассмотрены алифатические кислоты – н-гексановая и н-пентановая; амины и диолы различного строения – 2-аминопентан, 3-аминопентан, втор-бутиламин и трет-бутиламин, 1,2-гександиол, 1,2-пентандиол, 1,2-бутандиол; моногексиловый, монопентиловый и монобутиловый эфиры диэтиленгликоля; алифатические спирты с различным количеством углеродных атомов и расположением OH-группы – н-бутанол, втор-бутанол, трет-бутанол, н-пентанол, 2-пентанол и 3-пентанол, а также н-гексанол. Области существования сбалансированной МЭ, способной включать примерно одинаковые количества масла и воды, были показаны для втор- и трет-бутиламина, 2- и 3-аминопентана и для 1,2-пентандиола. Для других рассмотренных соПАВ показаны области существования только обратных МЭ. Можно полагать, что для формирования МЭ лецитина в изопропилмиристате лучше всего подходят соПАВ с короткой алкильной цепью и относительно большой полярной “головой”. На рис. 1 представлены примеры областей существования МЭ в системах лецитин–изопропилмиристат–соПАВ–вода при массовом соотношении лецитин : соПАВ, равном 1 : 1; при использовании в качестве соПАВ 2-аминопентана и 3-аминопентана образуется сбалансированная МЭ (диаграмма 1), а при использовании н-пентановой и н-гексановой кислоты – обратная МЭ с относительно узкой областью существования (диаграмма 2) [19].
Рис. 1.
Примеры областей существования сбалансированной (1) и обратной (2) МЭ лецитина в системах лецитин–изопропилмиристат–соПАВ–вода при массовом соотношении лецитин : соПАВ, равном 1 : 1. СоПАВ: 1 – 2-аминопентан (пунктир) и 3-аминопентан (точки); 2 – н-пентановая кислота (пунктир) и н-гексановая кислота (точки) [19].

Области существования обратных МЭ были показаны для систем лецитин–масло–н-пропанол или н-бутанол–вода, содержащих ряд масел со снижающейся полярностью: октановая и олеиновая кислоты, этилоктаноат, этилолеат, Migliol 812 (синтетические триглицериды), соевое масло. МЭ с наиболее широкой областью существования наблюдались в системах, содержащих этилоктаноат и этилолеат, в присутствии как бутанола, так и пропанола при различных их соотношениях с лецитином, а также в системе, содержащей соевое масло, при массовом соотношении лецитин : пропанол, равном 1 : 1 [20].
На примере синтетических лецитинов с углеводородными “хвостами” одинаковой длины С8–С16 и н-алканов С8–С16 были выявлены следующие закономерности: для получения МЭ на основе короткоцепочечных лецитинов лучше подходит н-бутанол, требуемое для получения МЭ количество бутанола возрастает с уменьшением числа атомов С в молекулах лецитина; для получения МЭ на основе длинноцепочечных лецитинов в системах с короткоцепочечными алканами в качестве соПАВ лучше подходит н-пропанол; при этом для МЭ в одинаковых растворителях нужное количество спирта увеличивается с ростом числа углеродных атомов в молекулах лецитина. Увеличение количества атомов С в молекуле алкана действует аналогично укорочению цепей в молекуле лецитина: приводит к уменьшению количества пропанола и к увеличению количества бутанола, необходимого для образования МЭ. Получается, что для формирования МЭ на основе соевого лецитина, содержащего длинные углеводородные “хвосты”, в алканах с длинной цепью лучше всего подходит н-бутанол, а в алканах с короткой цепью –пропанол [21]. Формирование МЭ в системах с циклогексаном и синтетическими короткоцепочечными лецитинами также изучено в работе [22].
Были описаны обратные МЭ в системах, содержащих лецитин, н-пропанол или н-бутанол, изооктан и воду. Для системы с пропанолом был продемонстрирован переход от МЭ с изолированными каплями к перколированной обратной МЭ при мольном соотношении воды и лецитина W > 30 [23]. Методом микрокалориметрии было исследовано образование МЭ при титровании водой раствора лецитина в смеси н-бутанола и изооктана; показано взаимодействие воды с молекулами лецитина и бутанола, что приводит к образованию обратных мицелл или капель обратной МЭ [24].
Таким образом, можно отметить, что формированию МЭ лецитина лучше всего способствует использование в качестве соПАВ молекул с короткой алкильной цепью (4–5 атомов С) и относительно большой полярной “головой”, которые должны эффективно встроиться в монослой молекул лецитина и повысить его гибкость; при этом требуется высокая концентрация соПАВ (массовое соотношение лецитин : соПАВ обычно состав-ляет 1 : 1). Эффективность соПАВ зависит от длины цепей в молекуле лецитина и углеводородного растворителя, а также от полярности масла. Чаще всего для получения МЭ лецитина в различных растворителях в качестве соПАВ использовали н-пропанол и н-бутанол.
Микроэмульсии лецитина в четырехкомпонентных системах с биосовместимыми маслами
Кроме упомянутого выше изопропилмиристата [17], в качестве компонентов МЭ лецитина были рассмотрены другие природные и синтетические масла. Например, в работе [25] для создания МЭ лецитина было предложено использовать лимонен – вещество из класса терпенов, обладающее приятным запахом и используемое в парфюмерии и косметике. Была показана широкая область существования МЭ типа “вода в масле” для соПАВ н-пропанола и узкая область существования обратной МЭ (не более 10 мас. % воды) для соПАВ 1,2-пропандиола; исследование проводили при массовом соотношении лецитин : спирт, равном 1 : 1, и T = 30°С. С помощью спектроскопии электронного парамагнитного резонанса было установлено, что в случае н-пропанола монослой ПАВ обладает большей гибкостью, чем в случае 1,2-пропандиола; этим фактом авторы объясняют большую ширину области существования МЭ при применении в качестве соПАВ н-пропанола [25].
Для создания МЭ лецитина были успешно использованы синтетические масла, применяемые в косметических композициях, такие как MCT (смесь триацилглицеридов C8–C10) и Peceol (смесь моно-, ди- и триглицеридов жирных кислот, в основном олеиновой). Для систем соевый лецитин–масло MCT–соПАВ–вода были показаны области существования МЭ и фазовые равновесия с участием прямых, обратных и бинепрерывных МЭ и лиотропных жидких кристаллов. В качестве соПАВ были рассмотрены алифатические спирты н-пропанол, н-бутанол, трет-бутанол и н-пентанол. Структура МЭ зависела от использованного соПАВ: например, для МЭ с содержанием 20 мас. % спирта, 25–30 мас. % лецитина и равных количеств масла и воды в присутствии н-пропанола наблюдалось образование прямой МЭ, н-пентанола – обратной, н-бутанола – бинепрерывной или обратной [26]. Было исследовано образование МЭ в системе, содержащей соевый лецитин, этанол, масло Peceol и воду при варьировании соотношения лецитин : этанол. Наилучшее для получения МЭ массовое соотношение лецитин : этанол составило 60 : 40, при нем достигалась максимальная площадь области существования обратной МЭ [27]. Этанол как биосовместимое соПАВ предлагался также для получения МЭ в изопропилмиристате – была показана область существования обратных МЭ при массовом соотношении лецитин : этанол, равном 1 : 2, 1 : 1, 2 : 1 и 3 : 1 [28].
Известны МЭ лецитина в природных растительных маслах, которые являются смесью триацилглицеридов, содержащих в основном остатки жирных кислот с 16 и 18 атомами углерода. Определена область существования МЭ в системе с рапсовым маслом, соевым лецитином (с содержанием фосфатидилхолина 63.6 мас. %), н-пропанолом и водой. МЭ существует при высоком содержании лецитина и спирта, при этом соотношение лецитин : пропанол (мас.) составляло: 67 : 33, 60 : 40, 50 : 50, 40 : 60. [29]. В аналогичной системе с подсолнечным маслом определена область существования МЭ при соотношении лецитин : пропанол (мас.), равном 2 : 1. МЭ также образуется при высоких концентрациях лецитина и пропанола [30]. Была определена область существования МЭ в системе лецитин (63.6 мас. % фосфатидилхолина)–оливковое масло–н-пропиловый спирт–вода [31] и в системе лецитин–соевое масло–н-пропиловый спирт–вода при массовом соотношении лецитин : пропанол, равном 1 : 1 [32].
Таким образом, показана возможность получения МЭ лецитина в природных маслах, таких как рапсовое, подсолнечное, оливковое и соевое, а также в синтетических биосовместимых растворителях, применяемых в косметике, таких как изопропилмиристат, MCT (смесь триацилглицеридов C8–C10) и Peceol (смесь моно-, ди- и триглицеридов жирных кислот, в основном олеиновой). Но в качестве соПАВ при этом в основном использовались короткоцепочечные алифатические спирты н-пропанол или этанол в высоких концентрациях (как правило, при массовом соотношении лецитин : спирт, равном 1 : 1), что имеет ограничения подходит для медицинского применения.
Для разработки МЭ лецитина, пригодных для применения в фармацевтике и пищевой промышленности, недостаточно только подобрать биосовместимые масла, необходимо еще решить более сложную задачу: заменить токсичные соПАВ (короткоцепочечные спирты, амины, диолы, кислоты) на нетоксичные. Для решения этой задачи многие авторы пошли путем усложнения состава разрабатываемых МЭ, вводя дополнительные биосовместимые ПАВ.
Микроэмульсии в четырех- и пятикомпонентных системах, содержащих лецитин и другие ПАВ
Для применения в фармацевтике были предложены МЭ, содержащие, кроме лецитина, еще одно биосовместимое ПАВ и алифатические спирты с короткой цепью, такие как этанол, н-пропанол и н‑бутанол. Например, показана область существования сбалансированной МЭ в системе лецитин–лизолецитин–н-бутанол–изопропилмири-стат–вода при соотношениях (мас.) лизолецитин : лецитин 0.7 : 1; 1.4 : 1 и 2.1 : 1, при этом массовое соотношение (лецитин + лизолецитин) : бутанол составляло 1 : 1. МЭ с более узкой областью существования получались при использовании в качестве соПАВ н-пропанола или этанола и при изменении массового соотношения (лецитин + лизолецитин) : спирт с 1 : 1 на 2 : 1 [32]. Были получены МЭ и определены их области существования в системах лецитин–синтетические н-алканолфосфохолины С6–С12–этанол, н-пропанол или н-бутанол–изопропилмиристат–вода [33]. МЭ с относительно узкой областью существования образуются также в системах, содержащих лецитин, децилгликозид или каприл-каприлилгликозид, изопропилмиристат, этанол и воду [34].
Описаны МЭ, содержащие лецитин и еще одно известное ПАВ, и не содержащие спирты. Было исследовано образование МЭ в системах лецитин–Brij 96V (полиэтиленгликольолеат)–изопропилмиристат–вода [35] и лецитин–Tween 80 (полиоксиэтилен-20-сорбитанмоноолеат)–изопропилмиристат–вода [36]. В системе лецитин + Tween 20 (полиоксиэтилен-20-сорбитанмонолаурат) в соотношении 1 : 1 (мас.) – Captex 200 (пропиленгликоль дикаприлат/дикапрат) – вода наблюдалось формирование как обратной, так и прямой МЭ [37]. Образование прямой МЭ наблюдалось также в системах соевый лецитин–Tween 80–этилолеат или соевое масло–вода, массовое соотношение лецитин : Tween 80 составляло 0.3 [38], но поскольку в рассмотренных системах количество лецитина меньше, чем Tween 80, т.е. это уже МЭ Tween 80, а не лецитина.
Описаны МЭ в пятикомпонентных системах, содержащих лецитин, другие биосовместимые ПАВ и не содержащих спирты. Например, показаны равновесия микроэмульсионной фазы с водной и органической фазами (равновесия типа Винзор I, II и III) и существование МЭ как одной фазы (Винзор IV) в системах лецитин–смесь рамнолипида и софоролипида (ПАВ микробного происхождения)–масло–вода; в качестве масел использовали декан, гексадекан, лимонен и изопропилмиристат [39]. Изучена область существования МЭ в системе лецитин–Тритон Х-100 (трет-октилфениловый эфир полиэтиленгликоля)–изопропилмиристат–бутиллактат–вода при соотношени (мас.) лецитин : Тритон Х-100 : бутилактат = 1 : 1 : 4 [40]. Отметим, что в описанных системах доля лецитина в смеси ПАВ и соПАВ составляла не более 25 мас. %, то есть лецитин не являлся основным ПАВ, образующим МЭ.
Acosta с соавт. [41–43] предложил заменить традиционные соПАВ в составе МЭ лецитина комбинацией липофильного и гидрофильного линкеров – молекул–“связок”, которые располагаются вблизи границы “масло–вода” со стороны органической и водной фаз соответственно. Молекулы линкеров можно рассматривать как “ассиметричные ПАВ”, которые “связывают” межфазную границу (монослой ПАВ) с водной или органической фазой; при этом в отсутствие лецитина (основного ПАВ) введение комбинации липофильного и гидрофильного линкеров не приводит к формированию МЭ. Таким образом, для создания МЭ лецитина вместо токсичных спиртов можно использовать сочетание биосовместимых ПАВ-линкеров. Этот подход был успешно применен для получения сбалансированной МЭ в системе, содержащей лецитин, липофильный линкер Span 80 (сорбитанмоноолеат), гидрофильный линкер смесь каприловой кислоты и каприлата натрия, изопропилмиристат и воду [41, 42]. Образование МЭ показано также в системе лецитин–липофильный линкер глицеролмоноолеат–гидрофильный линкер полиглицерол каприлат–этилкаприлат–модельное содержимое тонкого кишечника [43].
Таким образом, был предложен ряд составов МЭ лецитина, где в качестве соПАВ в основном рассматривались короткоцепочечные алифатические спирты – н-пропанол, н-бутанол, этанол. Попытки отказаться от использования спиртов приводили к усложнению состава МЭ: предлагалось введение еще одного или двух ПАВ в количествах, сопоставимых с содержанием лецитина, или комбинации гидрофильного и липофильного линкеров. При таком подходе количество лецитина в смеси ПАВ и соПАВ становится значительно меньше 50 мас. %, т.е. лецитин перестает быть основным ПАВ, образующим МЭ. Поэтому необходим поиск других биосовместимых соПАВ, которые будут присутствовать в системе в относительно небольших количествах и при этом способствовать образованию МЭ лецитина.
Для создания МЭ лецитина, предназначенных для медицинского применения, было предложено использовать в качестве соПАВ олеиновую кислоту [44, 45]. Наличие относительно небольшой полярной “головы” (карбоксильной группы) и изогнутого углеводородного “хвоста” (олеиновая кислота – это цис-изомер) дает олеиновой кислоте возможность повышать гибкость монослоя ПАВ на границе “масло–вода” и изменять спонтанную кривизну монослоя в сторону отрицательных значений, что должно способствовать формированию обратной МЭ.
Было показано [44, 45], что в системе лецитин–олеиновая кислота–додекан–вода при соотношении молярных концентраций олеиновой кислоты и лецитина Сол/Слец > 0.6 наблюдается образование обратной МЭ, имеющей размер капель в несколько нанометров. Область существования МЭ в указанной системе при Сол/Слец = 0.8 и, для сравнения, лецитиновых органогелей при Сол/Слец = 0.1 приведена на рис. 2. Область существования МЭ относительно узкая, максимальное содержание воды не превышает 16.8 мас. %. Удельная электропроводность образцов МЭ была от 0.1 до 1.1 мкСм/см при значениях W, равных 28–32, что характерно для обратных МЭ. При содержании лецитина в органической фазе 10 мас. %, Сол/Слец = 0.8 и W = 5 гидродинамический диаметр капель МЭ составлял 6.5 ± 0.1 нм [45].
Рис. 2.
Области существования в системе лецитин–олеиновая кислота - додекан–вода: 1 – МЭ при Сол/Слец = 0.8; 2 – органогеля при Сол/Слец = 0.1. Т = 25°С. Лецитин Lipoid S100 (96.3 мас. % основного вещества) [44].
Обратные МЭ в системах с олеиновой кислотой можно получать на основе коммерческих образцов соевого лецитина, в том числе фосфолипидных концентратов. Была предложена композиция для трансдермальной доставки биологически активных веществ в форме МЭ лецитина [45, 46], содержащая (мас. %): лецитин (фосфолипидный концентрат с содержанием фосфолипидов 97 мас. %, в том числе фосфатидилхолина 22 мас. %) – 14.3–23.3; вазелиновое масло – 29.6–34.7; олеиновая кислота – 5.0–7.1; жирное растительное масло, например масло авокадо – 29.6–34.7; эфирное масло, например масло чайного дерева – 1.4–5.7; вода – остальное. Мольное отношение олеиновой кислоты и лецитина составляло 0.6–0.8, что соответствует величине соотношения соПАВ : лецитин (мас.) от 0.22 до 0.29. Таким образом, МЭ можно получить при относительно низком содержании соПАВ. Поскольку в разработанных обратных МЭ количество масляной фазы существенно выше, чем водной, такие МЭ могут включать маслорастворимые биологически активные вещества в концентрациях единицы процентов, а водорастворимые – в концентрациях в десятые доли процента (табл. 1).
Таблица 1.
Включение масло- и водорастворимых биологически активных веществ в МЭ, содержащую, мас. %: лецитин (фосфолипидный концентрат с содержанием фосфолипидов 97 мас. %) – 19.1; олеиновая кислота – 6.7; масло авокадо – 32.6; вазелиновое масло – 32.6; эфирное масло чайного дерева – 4.2; вода – 4.8 [46]
| Вещество | α-Токоферола ацетат | Глюкоза | Аскорбиновая кислота |
|---|---|---|---|
| Сmax в МЭ, мас. % | 9.9 | 0.50 | 0.21 |
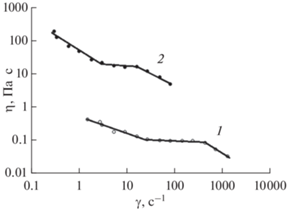
Вязкость МЭ обычно невысокая, по порядку величин она сопоставима с вязкостью дисперсионной среды. Относительно низкие значения вязкости позволяют создавать на основе МЭ композиции, которые можно вводить с помощью шприца, например подкожно. В качестве примера на рис. 3 приведена зависимость вязкости от скорости сдвига для обратной МЭ, содержащей 19.1 мас. % лецитина (линия 1) в сравнении с такой же зависимостью для ламеллярных жидких кристаллов, содержащих 70.0 мас. % лецитина (линия 2). Рассмотренные носители имеют аналогичный качественный состав, они включают лецитин, смесь масел и воду, но отличаются, главным образом, концентрацией лецитина и наличием в МЭ соПАВ олеиновой кислоты. Хорошо заметна разница в величинах вязкости образцов: для МЭ она примерно на два порядка ниже и при высоких скоростях сдвига сопоставима с вязкостью вазелинового и растительных масел (десятые доли Па с) [46].
Рис. 3.
Зависимость динамической вязкости (η) от скорости сдвига (γ') для образцов МЭ (1) и жидких кристаллов (2). Состав МЭ, мас. %: лецитин - 19.1; вазелиновое масло - 32.6; масло авокадо – 32.6; олеиновая кислота – 6.7; эфирное масло чайного дерева – 4.2; вода – 4.8. Состав жидких кристаллов, мас. %: лецитин – 70.0; масло авокадо – 10.0; эфирное масло чайного дерева – 5.0; вода – 15.0. T = 25°С [46].
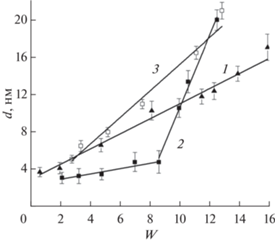
На модельной системе с красителем Родамином С показано, что скорость переноса водорастворимых веществ через диализную мембрану из обратной МЭ лецитина в физиологический раствор была 14.3 × 10–3 г/(м2 ч), что примерно в 2.5 раза выше, чем из ламеллярных жидких кристаллов в системе лецитин–растительное масло–эфирное масло–вода. Более высокая скорость высвобождения веществ из МЭ по сравнению с жидкокристаллическим носителем объясняется существенно большей вязкостью жидких кристаллов. За 7 ч диализа из МЭ выделилось 3.6% Родамина С, что позволяет разрабатывать на ее основе медицинские и косметические средства с замедленным высвобождением биологически активных веществ [46]. В состав органической фазы МЭ лецитина можно вводить растительные масла, обладающие собственной биологической активностью, например масло из тропического растения гака (Momordica cochinchinensis) и эфирное масло куркумы (Curcuma longa). Показано, что в МЭ можно ввести не менее 6.5 мас. % воды при концентрации лецитина в органической фазе 20 мас. %, массовом соотношении вазелинового масла и масла гака 1 : 1 и при мольном соотношении олеиновой кислоты и лецитина от 0.2 до 0.8. Гидродинамический диаметр капель предложенных обратных МЭ составлял от 3 до 21 нм в зависимости от содержания воды и лецитина. Наблюдалась линейная зависимость гидродинамического диаметра от параметра W, характерная для обратных МЭ: наклон линий менялся при варьировании соотношения лецитина с олеиновой кислотой и эфирным маслом (рис. 4) [47].
Рис. 4.
Зависимость гидродинамического диаметра капель микроэмульсий от W. Состав органической фазы МЭ, мас. %: 1 – лецитин – 20.0, олеиновая кислота – 4.5, вазелиновое масло – 35.5, масло гака – 35.5, эфирное масло куркумы – 4.5; 2 – лецитин – 10.0, олеиновая кислота – 2.25, вазелиновое масло – 41.62, масло гака – 41.63, эфирное масло куркумы – 4.5; 3 – лецитин – 10.0, олеиновая кислота – 2.25, вазелиновое масло – 42.75, масло гака – 42.75, эфирное масло куркумы – 2.25; T = 25°С [47].
МИКРОЭМУЛЬСИИ ЛЕЦИТИНА КАК НОСИТЕЛИ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ
МЭ лецитина можно использовать для транс-дермальной доставки лекарственных веществ, а также при разработке препаратов для местного применения, которые могут наноситься на кожу или слизистые оболочки.
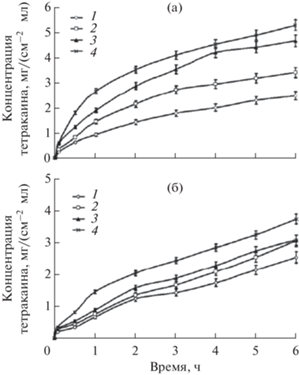
Для трансдермальной доставки тетракаина, используемого для местной анестезии, были предложены МЭ различных типов в системе лецитин–изопропилмиристат–н-пропанол–вода; тип МЭ определялся массовым соотношением лецитин : пропанол [48, 49]. В экспериментах с использованием диффузионной ячейки Франца было показано, что повышение концентрации воды как в прямой, так и в обратной МЭ приводит к возрастанию скорости транспорта тетракаина через образцы кожи мышей (рис. 5); значения скоростей переноса были в интервале от 7.66 до 18.28 мг/(см2 ч). Тип МЭ влияет на скорость переноса лекарственного вещества: на рис. 5. представлены данные по кинетике переноса тетракаина через кожу при использовании прямой (рис. 5а) и обратной (рис. 5б) МЭ. При одинаковом содержании воды скорость переноса была выше для прямой МЭ, но эта разница не очень значительная [48].
Рис. 5.
Кинетика переноса тетракаина через кожу мышей в фосфатный буферный раствор (pH 7.4) из прямой (a) и обратной (б) МЭ в системе лецитин–н-пропанол–изопропилмиристат–водный раствор тетракаина. Соотношение лецитин : н-пропанол (мас. %): a – 0.5 : 1; б – 1.5 : 1. Содержание воды в МЭ, мас. %: 1 – 20; 2 – 32; 3 – 42; 4 – 49. T = 37°С [48].
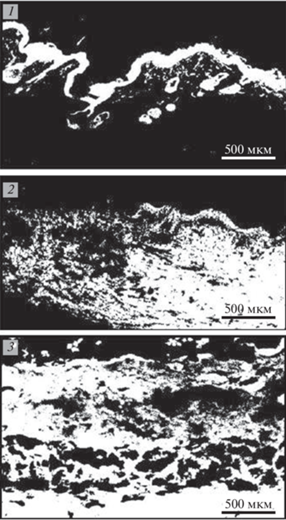
С помощью конфокальной лазерной сканирующей микроскопии было продемонстрировано [48], что при времени эксперимента 0.5–2 ч водорастворимый флуоресцентный краситель постепенно проникал в эпидермис и верхние слои дермы при нанесении на кожу как прямой, так и обратной МЭ, в то время как при нанесении раствора в пропаноле за 6 ч флуоресцеин-5-изотиоцианат проникал только в верхний слой эпидермиса. На рис. 6 представлены примеры микрофотографий срезов кожи мышей при проникновении красителя из раствора, прямой и обратной МЭ. В качестве основного механизма увеличения проницаемости кожи при нанесении на нее МЭ считают увеличение промежутков между клетками, образующими роговой слой эпидермиса, за счет взаимодействия лецитина с межклеточными липидами, и формирование при этом каналов, по которым идет проникновение компонентов МЭ в кожу. В переносе веществ могут также участвовать волосяные фолликулы и потовые железы [48]. Аналогичные результаты были показаны при проникновении липофильного флуоресцентного красителя Нильского красного: при времени эксперимента 1 ч краситель практически не проникал в кожу свиней из раствора в изопропилмиристате, но проникал на глубину 300 мкм при использовании обратной МЭ лецитина [41].
Рис. 6.
Проникновение флуоресцентного красителя в кожу мышей (сканирующая лазерная конфокальная микроскопия) после обработки: 1 – 6 ч 0.5 мМ раствором флуоресцеин-5-изотиоцианата (контроль); 2 – 2 ч обратной МЭ в системе лецитин–изопропилмиристат–н-МЭ–водный 0.5 мМ раствор флуоресцеин-5-изотиоцианата; 3 – 2 ч прямой МЭ в той же системе. Белый цвет – фруоресценция красителя [48].
В экспериментах in vivo было показано [49], что при использовании как прямой, так и обратной МЭ лецитина в качестве носителя местного анестетика тетракаина анальгезирующий эффект проявлялся при концентрации тетракаина в МЭ от 2.7 до 12 мг/мл. Максимальный анальгезирующий эффект был обнаружен спустя 10–15 мин после нанесения МЭ, затем его величина снижалась, но даже через 3 ч эффект обезболивания еще присутствовал. Для МЭ обоих типов эффект анальгезии увеличивался с ростом концентрации тетракаина и при повышении содержания воды в МЭ [49], что согласуется с результатами экспериментов по кинетике переноса тетракаина через кожу [48].
Было продемонстрировано, что нанесение на кожу как прямой, так и обратной МЭ в системе лецитин–н-пропанол–изопропилмиристат–водный раствор тетракаина не приводило к раздражению кожи и не вызывало окислительного стресса [49]. Низкий уровень раздражающего действия на кожу был показан также для МЭ в системах лецитин–н-бутанол–масло Migliol 812 N (синтетические триглицериды)–вода [50] и лецитин–спирт (этанол или изопропанол)–масло Capryol 90 (пропиленгликоль монокаприлат)–вода [51].
Было разработано ранозаживляющее средство на основе обратных МЭ, содержащих лецитин, олеиновую кислоту, вазелиновое масло, масло авокадо, эфирное масло чайного дерева и воду, активным компонентом являлся белково-пептидный экстракт из органов иммунной системы свиней. Оценка эффективности ранозаживления проводилась на модели плоскостных ран мышей. Показано, что прочность рубца через восемь дней после нанесения раны при лечении МЭ, не содержащей активный компонент, была 197 ± 15% (по сравнению с контролем, принятым за 100%), а при лечении такой же МЭ, содержащей водный белково-пептидный экстракт, составляла 282 ± 12% [52].
Таким образом, на нескольких примерах была продемонстрирована безопасность и эффективность МЭ лецитина, которые могут использоваться для местного применения (например, для обезболивания и ранозаживления) и для трансдермальной доставки лекарственных веществ. Известные из литературы варианты составов МЭ лецитина и возможностей их применения как носителей лекарственных веществ приведены в табл. 2.
Таблица 2.
Примеры составов МЭ лецитина, предложенных в качестве носителей лекарственных веществ
| Состав микроэмульсии | Лекарственное вещество | Применение композиции | Ссылка |
|---|---|---|---|
| Лецитин–н-пропанол–изопропилмиристат–вода | Тетракаин гидрохлорид | Трансдермально, для местной анестезии |
48, 49 |
| Лецитин–Span 80 (сорбитанмоноолеат)–каприлат натрия/каприловая кислота–изопропилмиристат − вода | Лидокаин | Трансдермально, для местной анестезии |
41, 53 |
| Лецитин–н-бутанол–масло Migliol 812 N (синтетические триглицериды)–вода | Кетопрофен | Трансдермально, противовоспалительное | 50 |
| Лецитин–спирт (этанол или изопропанол)–масло Capryol 90 (пропиленгликоль монокаприлат)–вода | Такролимус | Местно (на кожу) для лечения кожных заболеваний | 51 |
| Лецитин–этанол–изопропилмиристат–вода | Троксерутин | Перорально, витамин | 28 |
| Лецитин–Tween 80–соевое масло–вода | Куркумин | Перорально, противораковое | 38 |
| Лецитин–Tween 80–изопропилмиристат–вода, Лецитин–Brij 96V–изопропилмиристат–вода |
Амфотерицин В | Внутривенно, противогрибковое | 35, 54 |
| Лецитин–Tween 20–Captex (пропиленгликоль дикаприлат/дикапрат)–вода | Амфотерицин В | Противогрибковое | 37 |
| Лецитин–олеиновая кислота–вазелиновое масло–масло авокадо–эфирное масло чайного дерева–вода | Белково-пептидный экстракт из органов иммунной системы свиней | Ранозаживляющее | 52 |
Кроме применения в фармацевтике, МЭ лецитина было предложено использовать в смежных областях, например в пищевой промышленности для солюбилизации фермента липазы [25], для экстрагирования лютеина из лепестков календулы [30] и извлечения ликопена из томатной пасты [31].
ЗАКЛЮЧЕНИЕ
Лецитин является широко известным биосовместимым ПАВ, МЭ на его основе могут служить носителями лекарственных веществ.
Было показано, что формированию МЭ лецитина лучше всего способствует использование в качестве соПАВ молекул с короткой алкильной цепью (4–5 атомов С) и относительно большой полярной “головой”, таких как короткоцепочечные алифатические спирты, кислоты и амины; при этом требуется высокая концентрация соПАВ (массовое соотношение соПАВ : лецитин составляет обычно 1 : 1). Чаще всего для получения МЭ лецитина в различных растворителях в качестве соПАВ применяют этанол, н-пропанол и н-бутанол; с точки зрения биосовместимости этанол выглядит предпочтительнее. Показана возможность получения МЭ лецитина в природных маслах, таких как рапсовое, подсолнечное, оливковое и соевое, а также в синтетических биосовместимых маслах, например изопропилмиристат, MCT (смесь триацилглицеридов C8–C10) и Peceol (смесь моно-, ди- и триглицеридов жирных кислот, в основном олеиновой). Чтобы заменить токсичные спирты на менее токсичные компоненты, в МЭ лецитина вводили другие известные ПАВ, такие как Brij 96V (полиэтилен-гликольолеат), Tween 80 (полиоксиэтилен-20-сорбитанмоноолеат), Tween 20 (полиоксиэтилен-20-сорбитанмонолаурат), Тритон Х-100 (трет-октилфениловый эфир полиэтиленгликоля) и др.
Для создания МЭ лецитина, пригодных для фармацевтики, было предложено использовать олеиновую кислоту как нетоксичное биосовместимое соПАВ. Обратные МЭ в системах с олеиновой кислотой можно получать на основе коммерческих образцов соевого лецитина, в состав МЭ можно вводить растительные масла, обладающие собственной биологической активностью, например, масло авокадо, масло из тропического растения гака, эфирные масла чайного дерева и куркумы. Недостатком МЭ лецитина с олеиновой кислотой является относительно узкая область их существования.
В данной работе приведены примеры, показывающие безопасность и эффективность МЭ на основе лецитина, предложенных для трансдермальной доставки биологически активных веществ. Описаны композиции на основе МЭ лецитина для местной анестезии, для доставки витаминов, с противовоспалительным, противогрибковым, противораковым и ранозаживляющим действием.
Несмотря на очевидные преимущества лецитина как ПАВ для получения МЭ, необходима работа по подбору других компонентов. “Идеальная” МЭ лецитина должна иметь широкую, желательно симметричную область существования (т.е. быть сбалансированной) и содержать нетоксичные и биосовместимые другие компоненты: ПАВ, соПАВ и масла, предпочтительно недорогие и разрешенные для медицинского применения или используемые в пищевых продуктах. Возможные поиски новых составов МЭ лецитина могут пойти как по пути усложнения системы и добавления шестого, седьмого и т.д. компонента, так и по пути введения в качестве соПАВ новых веществ, которые ранее для таких целей не рассматривались. Задача создания “идеальной” МЭ лецитина еще не решена, и это стимулирует дальнейшие поиски.
Список литературы
Lawrence M.J., Rees G.D. Microemulsion-based media as novel drug delivery systems // Advanced Drug Delivery Reviews. 2012. V. 64. Supplement. P. 175–193. https://doi.org/10.1016/j.addr.2012.09.018
Fanun M. Microemulsions as delivery systems // Current Opinion in Colloid and Interface Science. 2012. V. 17. № 5. P. 306–313. https://doi.org/10.1016/j.cocis.2012.06.001
Callender S.P., Mathews J.A., Kobernyk K., Wettig S.D. Microemulsion utility in pharmaceuticals: Implications for multi-drug delivery // International Journal of Pharmaceutics. 2017. V. 526. № 1–2. P. 425–442. https://doi.org/10.1016/j.ijpharm.2017.05.005
Shukla T., Upmanyu N., Agrawal M. et al. Biomedical applications of microemulsion through dermal and transdermal route // Biomedicine & Pharmacotherapy. 2018. V. 108. P. 1477–1494. https://doi.org/10.1016/j.biopha.2018.10.021
Alves L.P., da Silva Oliveira K., da Paixao Santos J.A. et al. A review on developments and prospects of anti-inflammatory in microemulsions // Journal of Drug Delivery Science and Technology. 2020. V. 60. P. 102008. https://doi.org/10.1016/j.jddst.2020.102008
Szumała P., Macierzanka A. Topical delivery of pharmaceutical and cosmetic macromolecules using microemulsion systems // International Journal of Pharmaceutics. 2022. V. 615. P. 121488. https://doi.org/10.1016/j.ijpharm.2022.12148
van Nieuwenhuyzen W. Production and Utilization of Natural Phospholipids // Ahmad M.U., Xu X. (Editors) Polar lipids. Biology, Chemistry and Technology. Urbana, Illinois, USA: AOCS Press. 2015. P. 245–276. https://doi.org/10.1016/B978-1-63067-044-3.50013-3
Sjolund M., Rilfors L., Lindblom G. Reversed hexagonal phase formation in lecithin−alkane−water systems with different acyl chain unsaturation and alkane length // Biochemistry. 1989. V. 28. № 3. P. 1323–1329. https://doi.org/10.1021/bi00429a057
Angelico R., Ceglie A., Olsson U., Palazzo G. Phase diagram and phase properties of the system lecithin−water−cyclohexane // Langmuir. 2000. V. 16. № 5. P. 2124–2132. https://doi.org/10.1021/la9909190
Angelico R., Ceglie A., Colafemmina G. et al. Phase behavior of the lecithin/water/isooctane and lecithin/water/decane systems // Langmuir. 2004. V. 20. № 3. P. 619–631. https://doi.org/10.1021/la035603d
Щипунов Ю.А. Самоорганизующиеся структуры лецитина // Успехи химии. 1997. Т. 66. № 4. С. 328–352.
Kumar V.V., Kumar C., Raghunathan P. Studies on lecithin reverse micelles: Optical birefringence, viscosity, light scattering, electrical conductivity and electron microscopy // Journal of Colloid and Inteface Science. 1984. V. 99. № 2. P. 315–323.
Scartazzini R., Luisi P.L. Organogels from lecithins // Journal of Physical Chemistry. 1988. V. 92. № 3. P. 829–833. https://doi.org/10.1021/j100314a047
Мурашова Н.М., Юртов Е.В. Лецитиновые органогели как перспективные функциональные наноматериалы // Российские нанотехнологии. 2015. Т. 10. № 7–8. С. 5–14.
Shinoda K., Carlsson A., Lindman B. On the importance of hydroxyl groups in the polar head-group of nonionic surfactants and membrane lipids // Advances in Colloid and Interface Science. 1996. V. 64. P. 253–271. https://doi.org/10.1016/0001-8686(95)00287-1
Shinoda K., Araki M., Sadaghiani A. et al. Lecithin-based microemulsions: Phase behavior and microstructure // Journal of Physical Chemistry. 1991. V. 95. № 2. P. 989–993. https://doi.org/10.1021/j100155a091
Aboofazeli R., Lawrence M.J. Investigations into the formation and characterization of phospholipid microemulsions. I. Pseudo-ternary phase diagrams of systems containing water−lecithin−alcohol−isopropyl myristate // International Journal of Pharmaceutics. 1993. V. 93. № 1–3. P. 161–175. https://doi.org/10.1016/0378-5173(93)90174-E
Aboofazeli R., Lawrence M.J. Investigations into the formation and characterization of phospholipid microemulsions. II. Pseudo-ternary phase diagrams of systems containing water−lecithin−isopropyl myristate and alcohol: Influence of purity of lecithin // International Journal of Pharmaceutics. 1994. V. 106. № 1. P. 51–61. https://doi.org/10.1016/0378-5173(94)90275-5
Aboofazeli R., Lawrence C.B., Wicks S.R., Lawrence M.J. Investigations into the formation and characterization of phospholipid microemulsions. III. Pseudo-ternary phase diagrams of systems containing water-lecithin-isopropyl myristate and either an alkanoic acid, amine, alkanediol, polyethylene glycol alkyl ester or alcohol as cosurfactant // International Journal of Pharmaceutics. 1994. V. 111. № 1. P. 63–72. https://doi.org/10.1016/0378-5173(94)90402-2
Aboofazeli R., Patel N., Thomas M., Lawrence M.J. Investigations into the formation and characterization of phospholipid microemulsions. IV. Pseudo-ternary phase diagrams of systems containing water-lecithin-alcohol and oil: The influence of oil // International Journal of Pharmaceutics. 1995. V. 125. № 1. P. 107–116. https://doi.org/10.1016/0378-5173(95)00125-3
Kahlweit M., Busse G., Faulhaber B. Preparing microemulsions with lecithins // Langmuir. 1995. V. 11. № 5. P. 1576–1583. https://doi.org/10.1021/la00005a027
Schurtenberger P., Peng Q., Leser M.E., Luizi P.-L. Structure and phase behavior of lecithin-based microemulsions: A study of the chain-length dependence // Journal of Colloid and Interface Science. 1993. V. 156. № 1. P. 43–51. https://doi.org/10.1006/jcis.1993.1078
Avramiotis S., Bekiari V., Lianos P., Xenakis A. Structural and dynamic properties of lecithin–alcohol based w/o microemulsions: A luminescence quenching study // Journal of Colloid and Interface Science. 1997. V. 194. № 2. P. 326–331. https://doi.org/10.1006/jcis.1997.5135
Reis M.F.T., Bonomo R.C.F., de Souza A.O. et al. Calorimetric studies of microemulsion systems with lecithin, isooctane and butanol // Food Research International. 2012. V. 49. № 2. P. 672–676. https://doi.org/10.1016/j.foodres.2012.08.014
Papadimitrou V., Pispas S., Syriou S. et al. Biocompatble microemulsions based on limonene: Formulation, structure and application // Langmuir. 2008. V. 24. № 7. P. 3380–3386. https://doi.org/10.1021/la703682c
Leser M.E., van Evert W.C., Agterof W.G.M. Phase behaviour of lecithin–alcohol–triacylglycerol mixtures // Colloids and Surfaces A. Physicochemical and Engineering Aspects. 1996. V. 116. № 3. P. 293–308. https://doi.org/10.1016/0927-7757(96)03628-X
Mouri A., Diat O., Lerner D.A. et al. Water solubilization capacity of pharmaceutical microemulsions based on Peceol, lecithin and ethanol // International Journal of Pharmaceutics. 2014. V. 475. № 1–2. P. 324–334. https://doi.org/10.1016/j.ijpharm.2014.07.018
Xu M., Yu Q., Zhao Q. et al. Development and in vitro-in vivo evaluation of water-in-oil microemulsion formulation for the oral delivery of troxerutin // Drug Development and Industrial Pharmacy. 2016. V. 42. № 2. P. 280–287. https://doi.org/10.3109/03639045.2015.1047849
Abbasi S., Radi M. Food grade microemulsion systems: Canola oil/lecithin:n-propanol/ water // Food Chemistry. 2016. V. 194. P. 972– 979. https://doi.org/10.1016/j.foodchem.2015.08.078
Jalali-Jivan M., Abbasi S. Novel approach for lutein extraction: Food grade microemulsion containing soy lecithin and sunflower oil // Innovative Food Science and Emerging Technologies. 2020. V. 66. P. 102505. https://doi.org/10.1016/j.ifset.2020.102505
Amiri-Rigi A., Abbasi S. Extraction of lycopene using a lecithin-based olive oil microemulsion // Food Chemistry. 2019. V. 272. P. 568–573. https://doi.org/10.1016/j.foodchem.2018.08.080
Trotta M., Cavalli R., Ugazio E., Gasco M.R. Phase behaviour of microemulsion systems containing lecithin and lysolecithin as surfactants // International Journal of Pharmaceutics. 1996. V. 143. № 1. P. 67–73. https://doi.org/10.1016/S0378-5173(96)04688-1
Trotta M., Pattarino F., Grosa G. Formation of lecithin-based microemulsions containing n-alkanol phosphocholines // International Journal of Pharmaceutics. 1998. V. 174. № 1–2. P. 253–259. https://doi.org/10.1016/S0378-5173(98)00273-7
Graf A., Ablinger E., Peters S. et al. Microemulsions containing lecithin and sugar-based surfactants: Nanoparticle templates for delivery of proteins and peptides // International Journal of Pharmaceutics. 2008. V. 350. № 1–2. P. 351–360. https://doi.org/10.1016/j.ijpharm.2007.08.053
Brime B., Moreno M.A., Frutos G. et al. Amphotericin B in oil−water lecithin-based microemulsions: Formulations and toxicity evaluation // Journal of Pharmaceutical Sciences. 2002. V. 91. № 4. P. 1178–1185. https://doi.org/10.1002/jps.10065
Moreno M.A., Ballesteros M.P., Frutos P. Lecithin-based oil-in-water microemulsions for parenteral use; pseudoternary phase diagrams, characterization and toxicity studies // Journal of Pharmaceutical Sciences. 2003. V. 92. № 7. P. 1428–1437. https://doi.org/10.1002/jps.10412
Pestana K.C., Formariz T.P., Franzini C.M. et al. Oil-in-water lecithin-based microemulsions as a potential delivery system for amphotericin B // Colloids and Surfaces B: Biointerfaces. 2008. V. 66. № 2. P. 253–259. https://doi.org/10.1016/j.colsurfb.2008.06.016
Lin C.-C., Lin H.-Y., Chi M.-H. et al. Preparation of curcumin microemulsions with food-grade soybean oil/lecithin and their cytotoxicity on the HepG2 cell line // Food Chemistry. 2014. V. 154. P. 282–290. https://doi.org/10.1016/j.foodchem.2014.01.012
Nguyen T.T.L., Edelen A., Neighbors B., Sabatini D.A. Biocompatible lecithin-based microemulsions with rhamnolipid and sophorolipid biosurfactants: Formulation and potential applications // Journal of Colloid and Interface Science. 2010. V. 348. № 2. P. 498–504. https://doi.org/10.1016/j.jcis.2010.04.053
Das A., Mitra R.K. Formulation and characterization of a biocompatible microemulsion composed of mixed surfactants: lecithin and Triton X-100 // Colloid and Polymer Science. 2014. V. 292. № 3. P. 635–644. https://doi.org/10.1007/s00396-013-3110-y
Yuan J.S., Acosta E.J. Extended release of lidocaine from linker-based lecithin microemulsions // International Journal of Pharmaceutics. 2009. V. 368. № 1–2. P. 63–71. https://doi.org/10.1016/j.ijpharm.2008.09.063
Acosta E., Chung O., Xuan X.Y. Lecithin-linker microemulsions in transdermal delivery // Journal of Drug Delivery Science and Technology. 2011. V. 21. № 1. P. 77–87. https://doi.org/10.1016/S1773-2247(11)50007-3
Nouraei M., Acosta E.J. Predicting solubilisation features of ternary phase diagrams of fully dilutable lecithin linker microemulsions // Journal of Colloid and Interface Science. 2017. V. 495. P. 178–190. https://doi.org/10.1016/j.jcis.2017.01.114
Murashova N.M., Prokopova L.A., Trofimova E.S., Yurtov E.V. Effects of oleic acid and phospholipids on the formation of lecithin organogel and microemulsion // Journal of Surfactants and Detergents. 2018. V. 21. № 5. P. 635–645. https://doi.org/10.1002/jsde.12170
Мурашова Н.М. Самоорганизующиеся структуры ди-(2-этилгексил)фосфата натрия и лецитина в системах “вода–масло–ПАВ” и функциональные наноматериалы на их основе. Диссертация на соискание ученой степени доктора химических наук. М.: РХТУ им. Д.И. Менделеева, 2022. 380 с.
Мурашова Н.М., Трофимова Е.С., Костюченко М.Ю. и др. Микроэмульсии и лиотропные жидкие кристаллы лецитина как системы для трансдермальной доставки лекарственных веществ // Российские нанотехнологии. 2019. Т. 14. № 1–2. С. 69–75.
Мурашова Н.М., Нгуен Х.Т. Микроэмульсии лецитина с маслом гака и эфирным маслом куркумы // Коллоидный журнал. 2023. Т. 85. № 2. С. 191–199.
Changez M., Varshney M., Chander J., Dinda A.M. Effect of the composition of lecithin/n-propanol/isopropyl myristate/water microemulsions on barrier properties of mice skin for transdermal permeation of tetracaine hydrochloride: In vitro // Colloids and Surfaces B: Biointerfaces. 2006. V. 50. № 1. P. 18–25. https://doi.org/10.1016/j.colsurfb.2006.03.018
Changez M., Chander J., Dinda A.M. Transdermal permeation of tetracaine hydrochloride by lecithin microemulsion: In vivo // Colloids and Surfaces B: Biointerfaces. 2006. V. 48. № 1. P. 58–66. https://doi.org/10.1016/j.colsurfb.2006.01.007
Paolino D., Ventura C.A., Nistico S. et al. Lecithin microemulsions for the topical administration of ketoprofen: Percutaneous adsorption through human skin and in vivo human skin tolerability // International Journal of Pharmaceutics. 2002. V. 244. № 1–2. P. 21–31. https://doi.org/10.1016/s0378-5173(02)00295-8
Savic V., Todosijevic M., Ilic T. et al. Tacrolimus loaded biocompatible lecithin-based microemulsions with improved skin penetration: Structure characterization and in vitro/in vivo performances // International Journal of Pharmaceutics. 2017. V. 529. № 1–2. P. 491–505. https://doi.org/10.1016/j.ijpharm.2017.07.036
Basov A., Fedulova L., Vasilevskaya E. et al. Sus scrofa immune tissues as a new source of bioactive substances for skin wound healing // Saudi Journal of Biological Sciences. 2021. V. 28. № 3. P. 1826–1834. https://doi.org/10.1016/j.sjbs.2020.12.028
Yuan J.S., Ansari M., Samaan M., Acosta E.M. Linker-based lecithin microemulsions for transdermal delivery of lidocaine // International Journal of Pharmaceutics. 2008. V. 349. № 1– 2. P. 130–143. https://doi.org/10.1016/j.ijpharm.2007.07.047
Brime B., Molero G., Frutos P., Frutos G. Comparative therapeutic efficacy of a novel lyophilized ampho-tericin B lecithin-based oil–water microemulsion and deoxycholate-amphotericin B in immunocompetent and neutropenic mice infected with Candida albicans // European Journal of Pharmaceutical Sciences. 2004. V. 22. № 5. P. 451–458. https://doi.org/10.1016/j.ejps.2004.04.008
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал


