Координационная химия, 2019, T. 45, № 2, стр. 84-91
Синтез и характеристика координационных соединений малонатов 3d-металлов с фенилацетилгидразидом. Кристаллическая структура [Cu(L)2][Cu(Mal)2] ⋅ 4.5H2O (L = фенилацетилгидразид, Mal2– = анион малоновой кислоты)
В. С. Сергиенко 1, 2, *, Т. В. Кокшарова 3, М. Д. Суражская 1, Т. В. Мандзий 3
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН, Москва, Россия
2 Всероссийский институт научной и технической информации РАН, Москва, Россия
3 Одесский национальный университет им. И.И. Мечникова, Украина
* E-mail: sergienko@igic.ras.ru
Поступила в редакцию 22.05.2018
После доработки 15.06.2018
Принята к публикации 13.06.2018
Аннотация
Синтезированы три комплекса [M(L3)](Mal) фенилaцетилгидразид малонатов кобальта(II) (I), никеля(II) (II), цинка(II) (III), а также [Cu(L)2][Cu(Mal)2] ⋅ 4.5H2O(IV). Полученные соединения охарактеризованы методами химического анализа, спектроскопии ИК, диффузного отражения и термогравиметрии. Проведен РСА соединения IV, где L – фенилацетилгидразид, Mal2– – анион малоновой кислоты (CIF file CCDC № 1844502).
Малонат-анион (дианион малоновой кислоты) по своему поведению отличается от других дикарбоксилатных лигандов. Авторы [1] обнаружили, что с ионами 3d-металлов он может проявлять различные способы координации: бидентатный, бидентатный + монодентатный, бидентатный + бис(монодентатный), бидентатный + бис(монодентатный) + μ-оксо. В последнем случае в дополнение к бидентатной и бис(монодентатной) координации один из атомов кислорода действует как μ-оксомостик между двумя металлическими центрами. Ранее мы синтезировали и структурно охарактеризовали [Co(R)(Mal)(H2O)2]H2O [2] (R = бензгидразид, малонат-анион входит в состав внутрикомплексного соединения с образованием хелатного шестичленного цикла [2]) и [Ni(Z)2][Ni(Mal)2 (H2O)2]2 ⋅ 3.51H2O (Z = тиосемикарбазид, малонат-ион также образует шестичленные циклы, однако в составе комплексного аниона [3]). Для фенилацетгидразида описано мало комплексов; мы определили структуру гидратированных комплексов никеля состава 1 : 3 на основе бензоата [4] и 5-сульфосалицилата [5].
В настоящей статье описаны синтез, спектры ИК и диффузного отражения, термогравиграммы комплексов малонатов с фенилацетилгидразидом [M(L)3]Mal (M = Co (I), Ni (II), Zn (III); L = фенилацетил гидразид, Mal2– = анион малоновой кислоты), [Cu(L)2][Cu(Mal)2] ⋅ 4.5H2O (IV). Методом РСА определена кристаллическая и молекулярная структура IV.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез комплексов I–IV. 4.5 г фенилацетгидразида (0.03 моль) растворяли в 50 мл метанола, прибавляли 0.01 моль сухого измельченного малоната соответствующего металла и перемешивали до полного растворения. Смесь оставляли на неделю для самопроизвольного испарения растворителя. Выпавший осадок отделяли, промывали смесью воды с метанолом (1 : 1) и сушили на воздухе до постоянной массы. В случае меди(II) выпавшие кристаллы оказались пригодными для РСА.
Исходные малонаты получали взаимодействием малоната натрия с нитратом соответствующего 3d-металла.
| Найдено, %: | С 53.05; | H 5.03; | N13.46; | Co 9.79. |
| Для C27H32N6O7Co (I) | ||||
| вычислено, %: | С 53.02; | H 5.24; | N 13.75; | Co 9.66. |
| Найдено, %: | С 53.01; | H 5.37; | N13.43; | Ni 9.63. |
| Для C27H32N6O7Ni (II) | ||||
| вычислено, %: | С 53.02; | H 5.24; | N 13.75; | Ni 9.66. |
| Найдено, %: | С 52.30; | H 5.50; | N13.77; | Zn 10.95. |
| Для C27H32N6O7Zn (III) | ||||
| вычислено, %: | С 52.51; | H 5.19; | N 13.61; | Zn 10.53. |
| Найдено, %: | С 37.05; | H 4.37; | N7.46; | Cu 17.79. |
| Для C22H33N4O14.5Cu2 (IV) | ||||
| вычислено, %: | С 37.03; | H 4.63; | N 7.85; | Cu 17.95. |
Элементный анализ на металл проводили методом атомно-эмиссионной спектрометрии с индуктивно связанной плазмой на приборе Perkin-Elmer Optima 8000, на углерод, водород и азот – с помощью CHN анализатора.
ИК-спектры снимали на приборе Perkin-Elmer Spectrum BX II FT-IR System, образцы готовили в виде таблеток с KBr. Спектры диффузного отражения (СДО) регистрировали на спектрофотометре Lambda-9 (Perkin-Elmer), стандарт – MgO (βMgO = 100%).
Термогравиграммы снимали на дериватографе системы Paulik–Paulik–Erdey на воздухе, скорость нагрева 10 град/мин.
РСА IV. Структура расшифрована прямым методом и уточнена методом наименьших квадратов в полноматричном анизотропном приближении для всех неводородных атомов. Позиции всех атомов водорода (включая атомы Н молекул воды) рассчитаны геометричеcки и включены в уточнение по модели “наездника”. Кристаллографические данные и характеристики эксперимента для кристаллов IV приведены в табл. 1, основные межатомные расстояния и валентные углы – в табл. 2, геометрические параметры водородных связей – в табл. 3.
Таблица 1.
Кристаллографические характеристики, данные эксперимента и уточнения структуры соединения IV
| Параметр | Значение |
|---|---|
| М | 712.60 |
| Температура, К | 293(2) |
| Сингония; пр. гр. | Триклинная; P1 |
| Параметры ячейки: | |
| a, Å | 7.904(2) |
| b, Å | 10.191(3) |
| c, Å | 11.143(3) |
| α, град | 110.12(2) |
| β, град | 97.254(10) |
| γ, град | 111.98(2) |
| V, Å3 | 747.3(4) |
| Z; ρ(выч.), г/см3 | 1; 1.584 |
| F(000) | 367 |
| µ, мм–1 | 2.414 |
| Размер кристалла, мм | 0.18 × 0.08 × 0.03 |
| Дифрактометр | Enraf-Nonius CAD4 |
| Тип сканирования | ω |
| Излучение; λ, Å | CuKα; 1.5418 |
| θmin–θmax, град | 4.42– 62.47 |
| Интервалы индексов | –9 ≤ h ≤ 9, –11 ≤ k ≤ 11, –20 ≤ l ≤ 20 |
| Число отражений: | |
| Измеренных/независимых | 3380/1880 |
| Rint | 0.0231 |
| Комплектность по θ, % | 79.3 |
| Учет поглощения | ψ-scan |
| Tmin, Tmax | 0.6705, 0.9311 |
| Метод уточнения | Полноматричный МНК по F 2 |
| Число уточняемых параметров | 203 |
| GOOF (F 2) | 1.03 |
| Rhkl (I > 2σ(I)) | R1 = 0.0552, wR2 = 0.1471 |
| Rhkl (по всем отражениям) | R1 = 0.0654, wR2 = 0.1576 |
| Δmax/Δminе/Å3 | 1.286/–0.590 |
Таблица 2.
Основные длины связей (Å) и валентные углы (град) в структуре IV
| Связь | d, Å | Связь | d, Å |
|---|---|---|---|
| Cu(1)–O(1) | 1.912(4) | N(2)–N(1) | 1.422(6) |
| Cu(1)–O(2) | 1.887(4) | N(2)–C(4) | 1.310(8) |
| O(1)–C(1) | 1.275(7) | C(4)–C(5) | 1.509(8) |
| O(2)–C(2) | 1.272(7) | C(5)–C(6) | 1.518(8) |
| O(3)–C(2) | 1.239(7) | C(6)–C(7) | 1.375(9) |
| O(4)–C(1) | 1.234(7) | C(7)–C(8) | 1.374(10) |
| C(1)–C(3) | 1.484(8) | C(8)–C(9) | 1.334(11) |
| C(2)–C(3) | 1.492(8) | C(9)–C(10) | 1.374(12) |
| Cu(2)–O(5) | 1.958(4) | C(6)–C(11) | 1.366(9) |
| Cu(2)–N(1) | 1.983(5) | C(11)–C(10) | 1.378(11) |
| O(5)–C(4) | 1.255(7) | ||
| Угол | ω, град | Угол | ω, град |
| O(2)Cu(1)O(1) | 93.76(16) | N(2)N(1)Cu(2) | 105.9(3) |
| C(1)O(1)Cu(1) | 128.4(4) | O(5)C(4)N(2) | 121.4(6) |
| C(2)O(2)Cu(1) | 129.7(3) | O(5)C(4)C(5) | 120.6(6) |
| O(4)C(1)O(1) | 122.0(5) | N(2)C(4)C(5) | 118.0(6) |
| O(4)C(1)C(3) | 116.1(5) | C(4)–C(5)–C(6) | 111.4(5) |
| O(1)C(1)C(3) | 121.8(5) | C(11)C(6)C(7) | 119.2(6) |
| O(3)C(2)O(2) | 121.6(5) | C(11)C(6)C(5) | 120.2(6) |
| O(3)C(2)C(3) | 117.8(5) | C(7)C(6)C(5) | 120.5(6) |
| O(2)C(2)C(3) | 120.6(5) | C(6)C(11)C(10) | 119.0(8) |
| C(1)C(3)C(2) | 123.4(5) | C(6)C(7)C(8) | 120.5(7) |
| O(5)Cu(2)N(1) | 83.79(18) | C(9)C(8)C(7) | 120.7(8) |
| C(4)O(5)Cu(2) | 111.2(4) | C(8)C(9)C(10) | 119.2(7) |
| C(4)N(2)N(1) | 117.7(5) | C(9)C(10)C(11) | 121.2(8) |
Таблица 3.
Геометрические параметры водородных связей в соединении IV*
| D–H···A | Расстояние, Å | Угол DHA, град | ||
|---|---|---|---|---|
| D–H | H···A | D···A | ||
| N(1)–H(1B)···O(8) | 0.90 | 2.12 | 2.80(2) | 132 |
| N(1)–H(1A)···O(2) | 0.90 | 2.08 | 2.862(6) | 144 |
| N(2)–H(2A)···O(6) | 0.86 | 1.84 | 2.688(8) | 169 |
| O(7)–H(71)···O(8)#1 | 0.85 | 1.55 | 2.40(2) | 179 |
| N(1)–(1A)···O(1)#2 | 0.90 | 2.53 | 3.311(6) | 146 |
| O(6)–H(6)···O(4)#2 | 0.86 | 1.90 | 2.761(7) | 179 |
| N(1)–H(1B)···O(7)#3 | 0.90 | 2.20 | 3.056(8) | 160 |
| O(6)–H(61)···O(7)#4 | 0.85 | 2.02 | 2.866(9) | 179 |
| O(7)–H(7)···O(3)#5 | 0.85 | 1.86 | 2.712(7) | 179 |
Координаты атомов и другие параметры структуры IV депонированы в Кембриджском банке структурных данных (КБСД № 1844502; deposit@ ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk/ data_request/cif).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
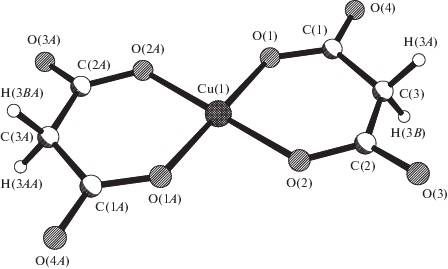
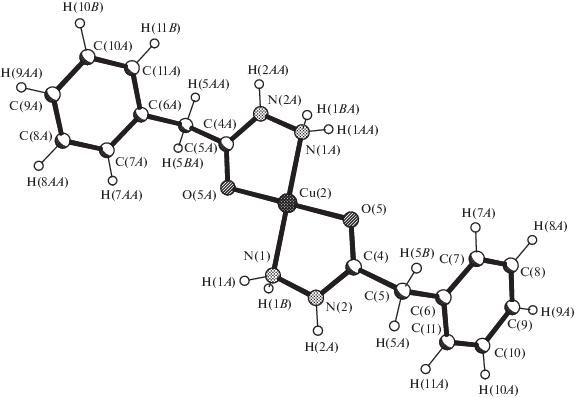
Из результатов химического анализа следует, что соотношение металл : фенилацетил гидразид составляет 1 : 1 для Cu(II) в комплексе IV и 1 : 3 для Co(II), Ni(II), Zn(II) в соединениях I–III. По данным РСА, структурные единицы соединения IV – комплексные катионы [Cu(1)(L2)]2+ (рис. 1), комплексные анионы [Cu(2)(Mal)2]2– (рис. 2) и кристаллизационные молекулы воды. Оба центросимметричных комплексных иона имеют искаженную квадратную координацию: атом Cu(1) катиона – четырьмя атомами кислорода двух билентатно-хелатных малонат-ионов (средн. Сu(1)–О 1.900(4) ± 0.013 Å, атом Cu(2) аниона – двумя атомами кислорода и двумя атомами азота двух бидентатно-хелатных молекул фенилацетил-гидразида (Cu(2)–O(5) 1.958(4), Cu(2)–N(1) 1.983(5) Å, хелатный угол O(5)Сu(2)N(1) 83.8(2)°). При координации с атомами меди ионoв Mal2– и молекул L замыкаются по два эквивалентных металлоцикла – шестичленные Сu(1)OC3O (А) и пятичленные Сu(2)N2CO (Б) соответственно. Хелатный цикл А практически плоский (±0.004–0.014 Å), металлоцикл Б несколько гофрирован (±0.027–0.065 Å, среднее отклонение атомов от усредненной плоскости 0.040 Å).
В КБСД (6, версия 5.38, ноябрь, 2017) нет результатов о строении комплексных ионов [Cu(L)2]2+ и [Cu(Mal)2]2–, но есть сведения о кристаллической структуре четырех соединений, содержащих дианион диаквадималонат меди(II), [Cu(Mal)2(H2O)2]2– (Ан) и одного нейтрального комплекса с монопротонированными однозарядными малонат-ионами HMal– – все c вытянутой вследствие эффекта Яна–Теллера тетрагонально-бипирамидальной координацией атома металла. Известны три оригинальных варианта структуры [Cu(H2O)6] · Ан (V) [7–9], результаты РСА при двух температурах – 120 и 294 К – комплекса [Cu(HMal)2(H2O)2] (VI) [10]. Кроме того, в КБСД есть данные о кристаллической структуре трех соединений более сложного состава с общей формулой {Cu(H2O)n(μ-Mal)2{Cu(H2O)4}2]2+[Cu(Mal)2 (H2O)2]2– · [{Cu(H2O)2(Mal)(μ-Mal)}{Cu(H2O)4}], содержащих, кроме трехъядерных комплексных анионов и моноядерного анионного комплекса, нейтральные биядерные молекулы. Для соединений с n = 2 (определена структура двух моноклинных модификаций: пр. гр. С2/с, Z = 8 (VII) [11] и пр. гр. Р21/c, Z = (VIII) [12]). Для комплекса с n = = 1 (IX) [13] центральный атом меди в трехъядерном комплексном катионе имеет удлиненную тетрагонально-пирамидальную координацию, а для аналогичного атома Cu в структуре VII, VIII – вытянутую тетрагонально-бипирамидальную.
Связи Cu–O(Mal) в комплексе [Cu(Mal)2]2– исследованной нами структуре IV в среднем заметно короче, чем в комплексных анионах структуры V–IX (соответственно 1.900 и 1.936–1.994 Å). Интервалы длин аксиальных связей Cu–O(H2O)акс и хелатных углов О(Mal)CuO(Mal) в структуре V–IX составляют соответственно 2.409–2.480 Å и 91.0°–93.5°. Угол О(Mal)CuO(Mal) в структуре IV составляет 93.8(2)°.
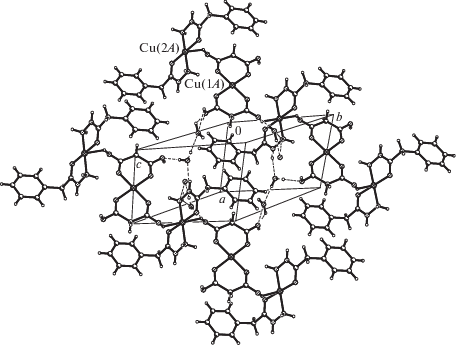
На рис. 3 показана упаковка структурных единиц в кристалле IV. Комплексные катионы и анионы, а также кристаллизационные молекулы воды соединены разветвленной сеткой водородных связей (ВС) – акцепторных (с участием атомов азота лиганда L и молекул воды) и донорных (при участии атомов кислорода лигандов Mal2–, L и молекул Н2О). Отметим весьма прочную ВС О(7)–Н(71)···О(8) между молекулами воды (Н···О 1.55, О···О 2.40 Å, угол ОНО 180°).
Сравнение ИК-спектров фенилацетгидразида и синтезированных комплексов с малонатами 3d-металлов (табл. 4), проведенное с учетом литературных данных [14–17], показывает, что частота поглощения ν(C=O) увеличивается. Обычно при координации через атом кислорода происходит ее понижение [18–24]. Необычное поведение ν(C=O) для полученных нами комплексов связано с тем, что эта полоса в спектре исходного фенилацетгидразида понижена из-за присутствия внутри- и межмолекулярных ВС. Еще в 1956 г. Йенсен [15] подтвердил наличие у фенилацетилгидразида ВС и в твердом состоянии, и даже в концентрированных растворах в хлороформе. Он установил, что при отсутствии ВС поглощение ν(C=О) должно проявляться около 1710 см–1. Таким образом, можно утверждать, что в результате комплексообразования частота ν(C=О) понижается, но, очевидно, величина сдвига, вызванного комплексообразованием, уступает величине ее понижения, обусловленного ВС. Повышение ν(C=O) в результате комплексообразования составляет 13–15 см–1 для комплексов I–III состава 1 : 3 и 25 см–1 для IV. Еще одно отличие в спектре последнего – отсутствие полос νas(C–H), δ(NH2) и ν(С–С) ароматического кольца, которые в спектрах комплексов I–III наблюдаются, соответственно, практически при одинаковых частотах. Полосы δ(СH2) в спектрах комплексов I–III (1 : 3) почти совпадают с соответствующей полосой в спектре органической молекулы L, а для комплекса меди IV частота этой полосы понижается. В ИК-спектрах всех четырех синтезированных нами комплексов для валентных колебаний ν(NH) исчезает дублет, что соответствует участию азота в координации и разрушению ВС. Уменьшается число полос и в области 1100–1200 см–1, где также проявляются полосы связей с участием азота, при этом положение полос почти одинаково для всех комплексов I–IV. Для дублета в области 1000–1100 см–1, в который также вносят вклад связи с участием азота, уменьшение разности частот между двумя полосами, примерно одно и то же для всех комплексов I–IV. Для комплекса меди IV частота δ(СNН) + δ(CСС) чуть выше, а δ(СCN) + (δ(NСО) чуть ниже, чем для I–III.
Таблица 4.
Отнесение полос поглощения (см–1) в ИК-спектрах фенилацетгидразида и его комплексов с малонатами 3d-металлов
| Отнесение | L | [Co(L)3]Mal | [Ni(L)3]Mal | [Zn(L)3]Mal | [Cu(L)2][Cu(Mal)2] · 4.5H2O |
|---|---|---|---|---|---|
| ν(NH), ν(NH2) | 3294, 3200 | 3221 | 3214 | 3224 | 3205 |
| νas(C–H) (CH2) | 3030 | 3062, 3031 | 3062, 3030 | 3062, 3031 | |
| νs(C–H) (CH2) | 2917 | 2951 | 2896 | ||
| ν(C=O) | 1644 | 1659 | 1657 | 1659 | 1669 |
| δ(NH2) | 1607 | 1609 | 1610 | ||
| ν(С–С)аром. кольца | 1529 | 1545 | 1543 | 1542 | |
| δ(СH2) | 1455 | 1454 | 1454 | 1454 | 1433 |
| ω(NH2) | 1352, 1265 | 1358 | 1360, 1277 | 1354, 1277 | 1369, 1275 |
| ν(CN) + ν(N–N) + + τ(NH2) + δ(CСН) | 1205, 1156, 1137 | 1195, 1165 | 1196, 1171 | 1190, 1162 | 1195, 1163 |
| νпульс.кольца + ρ(NH2) + + τ(NH2) | 1074, 1007 | 1060, 1032 | 1062, 1033 | 1064, 1033 | 1063, 1033 |
| ρ(CСН) + δ(CСН) | 773 | 780 | 784 | ||
| δ(СNН) + δ(CСС) | 705, 623 | 696 | 696 | 696 | 702 |
| δ(СCN) + δ(NСО) | 539 | 542 | 547 | 530 |
Таким образом, изменения полос в ИК-спектрах согласуются с данными РСА для IV об участии кислорода и азота в образовании хелатного цикла в комплексных катионах.
Ранее при сопоставлении данных ИК-спектроскопии и РСА [25–27] мы показали, что величина ΔΔν(COO–) – разность Δν(COO–) между смешанолигандным комплексом и исходным карбоксилатом металла (где Δν(COO–) = νas(COO–) – νs(COO–)) – может характеризовать тип связывания карбоксилат-ионов в координационных соединениях. Большие величины ΔΔν(COO–) характерны для монодентатной координации карбоксилата, гораздо меньшие – при бидентатной координации и для внешнесферных анионов. Для полученных соединений I–III состава 1 : 3 величина ΔΔν(COO–) сравнительно невелика, что соответствует внешнесферному характеру малонат-ионов, а для IV она отрицательна, поскольку уже в исходном малонате меди присутствует идентичный комплексный анион (табл. 5).
Таблица 5.
Полосы поглощения (см–1) карбоксилат-ионов в ИК-спектрах малонатов 3d-металлов и их комплексов с фенилацетгидразидом
| Соединение | νas(COO–) | νs(COO–) | Δν(COO–) | ΔΔν(COO–) |
|---|---|---|---|---|
| Co(Mal) · 2H2O | 1567 | 1374 | 193 | |
| [Co(L)3]Mal | 1594 | 1358 | 236 | 43 |
| Ni(Mal) · 2H2O | 1567 | 1380 | 187 | |
| [Ni(L)3]Mal | 1595 | 1360 | 235 | 48 |
| Zn(Mal) · 2H2O | 1566 | 1378 | 188 | |
| [Zn(L)3]Mal | 1596 | 1354 | 242 | 54 |
| Na2[Cu(Mal)2] · 2H2O | 1592 | 1366 | 226 | |
| [Cu(L)2][Cu(Mal)2] · 4.5H2O | 1584 | 1369 | 215 | –11 |
Данные СДО (табл. 6) для комплексов I и II согласуются с их октаэдрическим строением. Широкая полоса с максимумом при 15 400 см–1 в спектре IV характерна для квадратных комплексов меди(II) [28].
Таблица 6.
Спектры диффузного отражения комплексов фенилацетгидразида с малонатами 3d-металлов
| Соединение | ν, см–1 | Отнесение |
|---|---|---|
| [Co(L)3]Mal | 19 850 | 4T1g(F) → 4T1g(P) |
| 8750 | 4T1g(F) → 4T2g | |
| [Ni(L)3]Mal | 16 300 | 3A2g → 3T1g |
| 9600 | 3A2g → 3T2g | |
| [Cu(L)2][Cu(Mal)2] · 4.5H2O | 15 400 ш |
Термогравиграммы (табл. 7) соединений I–III состава 1 : 3 довольно похожи: сначала наблюдается эндоэффект с небольшой потерей массы при 120–140°С, затем экзоэффект при ~200°С с потерей массы несколько больше 20% и экзоэффект при ~400°С, на который приходится более половины всей потери массы. Очевидно, эндоэффекты соответствуют деструкции комплексов, экзоэффекты – выгоранию органической части. Для комплекса IV эффектов на термогравиграмме больше, что, вероятно, связано с более сложным строением (две координационные сферы). В зависимости от комплексообразователя термостабильность падает в ряду: Ni2+ > Co2+ ≈ Zn2+ > Cu2+.
Таблица 7.
Данные термогравиметрии для комплексов фенилацетгидразида с малонатами 3d-металлов
| Соединение | Эндоэффект | Экзоэффект | Общая убыль массы, % |
||
|---|---|---|---|---|---|
| T, °C* | Δm, % | T, °C* | Δm, % | ||
| [Co(L)3]Mal | 120–140(130) | 4.4 | 190–260(240) | 22.2 | 78.8 |
| 400–570(540) | 42.8 | ||||
| [Ni(L)3]Mal | 140–160(150) | 3.5 | 210–260(230) | 3.5 | 80.0 |
| 260–270(265) | 28.2 | ||||
| 400–530(500) | 40.5 | ||||
| [Zn(L)3]Mal | 120–140(130) | 2.4 | 190–250(220) | 20.4 | 78.8 |
| 330–360(350) | 4.9 | ||||
| 420–570(560) | 42.3 | ||||
| [Cu(L)2][Cu(Mal)2] · 4.5H2O | 110–140(130) | 12.3 | 200–270(250) | 5.4 | 73.8 |
| 140–200(190) | 35.7 | 330–400(360) | 11.3 | ||
| 400–510(450) | 7.4 | ||||
Список литературы
Rodrıguez-Martın Y., Hernandez-Molina M., Delgado F.S. et al. // CrystEngComm. 2002. V. 4. № 87. P. 522.
Анцышкина А.С., Кокшарова Т.В., Садиков Г.Г. и др. // Журн. неорган. химии. 2016. Т. 61. № 4. С. 455. (An-tsyshkina A.S., Koksharova T.V., Sadikov G.G. et al. // Russ. J. Inorg. Chem. 2016. V. 61. № 4. P. 434).
Анцышкина А.С., Садиков Г.Г., Кокшарова Т.В. и др. // Журн. неорган. химии. 2014. Т. 59. № 2. С. 176. (An-tsyshkina A.S., Sadikov G.G., Koksharova T.V. et al. // Russ. J. Inorg. Chem. 2014. V. 59. № 2. P. 50).
Кокшарова Т.В., Сергиенко В.С., Суражская М.Д. и др. // Журн. неорган. химии. 2017. Т. 62. № 12. С. 1576. (Koksharova T.V., Sergienko V. S., Surazhskaya M.D. et al. // Russ. J. Inorg. Chem. 2017. V. 62. № 12. P. 1568).
Koksharova T.V., Sergienko V.S., Surazhskaya M.D. et al. // Russ. J. Coord. Chem. 2018. V. 44. № 11. P. 678. doi 10.1134/S1070328418110040
Allen F.H. // Acta Crystallogr. B. 20012. V. 58. P. 380.
Димитрова Г.И., Аблов А.В., Киосе Г.А. и др. // Докл. АН CCCP. 1974. Т. 216. № 5. С. 1055.
Филиппова И.Г. // Коорд. химия. 2000. Т. 26. № 4. С. 295.
Rodrigues-Marin Y., Sanchiz J., Ruiz-Perez C. et al. // CrystEngComm. 2002. V. 4. P. 631.
Lenstra A.T.H., Kataeva O.N. // Acta Crystallogr. B. 2001. V. 57. P. 497.
Филиппова И.Г., Кравцов В.Х., Гданец М. // Коорд. химия. 2000. Т. 26. № 11. С. 860.
Naumov P., Ristova M., Soptrajanov B. et al. // Croat. Chem. Acta. 2002. V. 75. № 3. P. 701.
Ruiz-Perez C., Sanchiz J., Hernandez Molina M. et al. // Inorg. Chem. 2000. V. 39. P. 1363.
Odunola O.A., Adeoye I.O., Woods J.A.O. // Synth. React. Inorg. Metal-Org. Chem. 2002. V. 32. № 4. P. 801.
Jensen J.B. // Acta Chem. Scand. 1956. V. 10. № 4. P. 667.
Гордон А., Форд Р. Спутник химика. М.: Мир, 1976. 541 с.
Ul Ain Q., Ashiq U., Ara J.R. et al. // Arab. J. Chem. 2017. V. 1. № 4. P. 488.
Odunola O.A., Adeoye I.O., Woods J.A.O. et al. // Synth. React. Inorg Metal-Org. Chem. 2003. V. 33. № 2. P. 205.
Issa R.M., El-Shazly M.F., Iskander M.F. // Z. Anorg. Allg. Chem. 1967. V. 354. № 1–2. P. 90.
Zidan A.S.A. // Synth. React. Inorg. Metal-Org. Chem. 2004. V. 34. №. 4. P. 743.
Гогоришвили П.В., Каркарашвили М.В., Каландаришвили Д.З. // Журн. неорган. химии. 1969. Т. 14. № 6. С. 1516.
Dutta A.A., Chaudhuri N.R. // J. Inorg. Nucl. Chem. 1971. V. 33. № 1. P. 189.
Narang K.K., Singh M. // Synth. React. Inorg. Metal-Org. Chem. 1985. V. 15. № 6. P. 821.
Narang K.K., Pandey J.P., Singh K.P. et al. // Synth. React. Inorg. Metal-Org. Chem. 1990. V. 20. № 10. P. 1301.
Кокшарова Т.В., Садиков Г.Г., Анцышкина А.С. и др. // Журн. неорган. химии. 2006. Т. 51. № 6. С. 966. (Koksharova T.V., Sadikov G.G., Antsyshkina A.S. et al. // Russ. J. Inorg. Chem. 2006. V. 51. № 6. P. 895).
Анцышкина А.С., Кокшарова Т.В., Садиков Г.Г. и др. // Журн. неорган. химии. 2006. Т. 51. № 6. С. 972. (An-tsyshkina A.S., Koksharova T.V., Sadikov G.G. et al. // Russ. J. Inorg. Chem. 2006. V. 51. № 6. P. 901).
Анцышкина А.С., Садиков Г.Г., Кокшарова Т.В. и др. // Журн. неорган. химии. 2006. Т. 51. № 10. С. 1671. (Antsyshkina A.S., Sadikov G.G., Koksharova T.V. et al. // Russ. J. Inorg. Chem. 2006. V. 51. № 10. P. 1571).
Ливер Э. Электронная спектроскопия неорганических соединений. Т. 2. М.: Мир, 1987.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия