Координационная химия, 2019, T. 45, № 5, стр. 259-269
Синтез и магнитные свойства бис-о-семихиноновых комплексов цинка с бидентатными n-донорными лигандами
А. В. Пискунов 1, *, А. В. Малеева 1, А. С. Богомяков 2, Г. К. Фукин 1
1 Институт металлоорганической химии им. Г.А. Разуваева РАН
Нижний Новгород, Россия
2 Международный томографический центр СО РАН
Новосибирск, Россия
* E-mail: pial@iomc.ras.ru
Поступила в редакцию 26.06.2018
После доработки 08.11.2018
Принята к публикации 03.12.2018
Аннотация
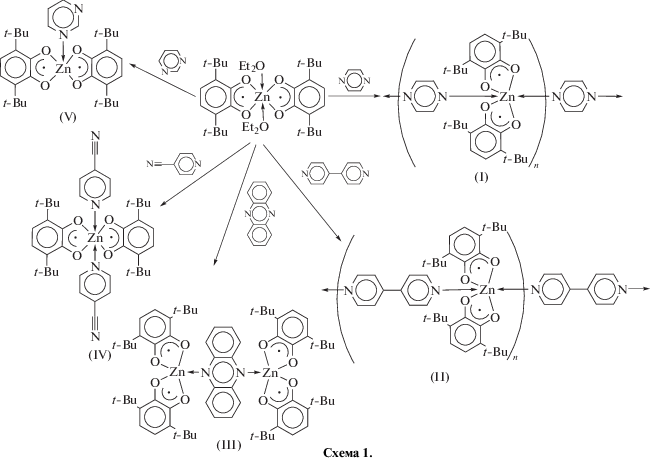
По реакции бис(3,6-ди-трет-бутил-о-бензосемихинолято)цинка (SQ2Zn) с бидентатными N-донорными лигандами (L1–5) (пиразин (L1), 4,4'-дипиридил (L2), феназин (L3), 4-цианопиридин (L4), пиримидин (L5)) синтезированы бирадикальные моноядерные SQ2${\text{ZnL}}_{2}^{4}$ и SQ2ZnL5, биядерный SQ2Zn(L3)ZnSQ2 комплексы и координационные полимеры (SQ2ZnL1(2))n. Структура синтезированных соединений установлена методом РСА (СIF files CCDC № 1846558–1846563). Биядерный SQ2Zn(L3)ZnSQ2 и моноядерный SQ2ZnL5 комплексы содержат пятикоординированные атомы металла, в то время как цинк в соединениях на основе лигандов L1,2,4 имеет октаэдрическое окружение с транс-расположенными о-семихинолятными лигандами. Координационные полимеры (SQ2ZnL1(2))n способны деполимеризоваться при растворении в органических растворителях. Согласно данным измерений температурной зависимости магнитной восприимчивости, в кристаллах полученных соединений реализуется антиферромагнитный обмен между неспаренными электронами органических анион-радикалов.
Исследования молекулярного и электронного строения комплексов металлов с редокс-активными лигандами обособились в весьма многообещающее и интенсивно развивающееся направление современной координационной и элементоорганической химии. Среди многообразия важных химических и физико-химических свойств соединений данного типа необходимо выделить один важный аспект, а именно их магнитную активность и возможность управлять ею в широких пределах, варьируя природу комплексообразующих металлов и парамагнитных лигандов. Данное обстоятельство позволяет рассматривать комплексы металлов с редокс-активными лигандами как потенциальные строительные блоки для получения магнитных материалов [1–3]. При этом необходимо отметить, что формирование прочного металлоорганического координационного полимера [4] максимально полно отвечает требованиям функциональных материалов. Первые удачные попытки получения координационных полимеров, содержащих парамагнитные о-семихиноновые лиганды, осуществлены на примере кобальта [5] и марганца [6], в которых фрагменты (диоксолен)2M были связаны пиразином в полимерные цепи. Позднее были синтезированы различные конструкции, где бис-о-семихиноляты металла связаны в полимерные цепи посредством разнообразных дипиридильных линкеров. Получены соединения меди [7], редокс-изомерные производные кобальта [8–13], а также каталитически активные комплексы марганца [14, 15]. В ходе исследования возможностей механохимического синтеза бис-о-семихинолятов металлов получен первый полимерный бис-о-бензосемихинолят цинка [16].
В рамках представленной работы мы предприняли попытку получения координационных полимеров на основе бирадикального фрагмента бис(3,6-ди-трет-бутил-о-бензосемихинолято)цинка и некоторых бидентатных N-донорных лигандов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе все операции по синтезу комплексов цинка проводили в анаэробных условиях. Использованные в работе растворители очищали и обезвоживали согласно рекомендациям [17]. Применяли коммерческие реактивы: пиразин (L1), 4,4'-дипиридил (L2), феназин (L3), 4-цианопиридин (L4), пиримидин (L5). Исходный комплекс цинка SQ2Zn(Et2O)2 (SQ2Zn = бис(3,6-ди-трет-бутил-о-бензосемихинолято)цинка) синтезировали по известной методике [18].
Синтез комплексов I–IV. К раствору комплекса цинка SQ2Zn(Et2O)2 (0.5 ммоль) в 15 мл толуола приливали необходимое количество нейтрального N-донорного лиганда в 10 мл того же растворителя. Полученную реакционную смесь нагревали на водяной бане в течение 30 мин, поле чего жидкую фазу удаляли при пониженном давлении. Остаток темно-синего цвета перекристаллизовали из подходящего растворителя.
Комплекс SQ2ZnL1 (I): а) m(L1) = 0.04 г. Кристаллы SQ2ZnL1 · C7H8 (Iа), пригодные для РСА, получали медленным охлаждением толуольного раствора. Выход 0.27 г (79%).
ИК-спектр (ваз. масло; ν, см–1): 451 с, 501 с, 553 ср, 655 с, 674 с, 702 сл, 798 сл, 804 ср, 829 с, 930 сл, 957 с, 1027 сл, 1044 ср, 1053 с, 1073 сл, 1107 сл, 1129 ср, 1153 ср, 1180 ср, 1202 ср, 1234 сл, 1276 с, 1344 с, 1363 ср, 1386 сл, 1419 с, 1456 сл, 1504 сл, 1551 сл, 1568 сл, 1614 сл.
б) m(L1) = 0.04 г. Кристаллы SQ2ZnL1 · C6H14 (Iб), пригодные для РСА, получали из смеси CH2Cl2–гексан (1 : 1). Выход 0.23 г (68%).
ИК-спектр (ваз. масло; ν, см–1): 451 с, 501 с, 553 ср, 655 с, 674 с, 702 сл, 798 сл, 804 ср, 829 с, 930 сл, 957 с, 1027 сл, 1044 ср, 1053 с, 1073 сл, 1107 сл, 1129 ср, 1153 ср, 1180 ср, 1202 ср, 1234 сл, 1276 с, 1344 с, 1363 ср, 1386 сл, 1419 с, 1456 сл, 1504 сл, 1551 сл, 1568 сл, 1614 сл.
Комплекс SQ2ZnL2 (II): a) m(L2) = 0.079 г. Кристаллы II · 3C7H8, пригодные для РСА, получали медленным охлаждением толуольного раствора. Выход 0.38 г (82%).
ИК-спектр (ваз. масло; ν, см–1): 462 сл; 499 ср; 528 сл; 625 с; 651 с; 665 ср; 677 сл; 697 сл; 810 с; 821 с; 831 сл; 852 сл; 926 сл; 948 с; 974 сл; 988 сл; 1005 сл; 1024 сл; 1041 сл; 1062 ср; 1111 сл; 1126 сл; 1176 ср; 1203 сл; 1216 ср; 1276 ср; 1319 сл; 1342 ср; 1352 ср; 1360 ср; 1405 с; 1438 с,1478 с, 1537 ср; 1601 с.
Комплекс SQ2Zn(L3)ZnSQ2 (III): a) m(L3) = = 0.045 г. Кристаллы III · 4C7H8, пригодные для РСА, получали медленным охлаждением толуольного раствора. Выход 0.28 г (72%).
ИК-спектр (ваз. масло; ν, см–1): 463 сл, 503 ср, 554 ср, 594 ср, 654 с, 661 сл, 675 с, 702 сл, 728 сл, 746 с, 805 сл, 823 сл, 834 сл, 919 сл, 956 с, 965 сл, 1026 сл, 1058 ср, 1129 ср, 1182 сл, 1204 ср, 1237 сл, 1278 сл, 1289 сл, 1311 сл, 1344 ср, 1356 ср, 1386 ср, 1454 с, 1488 с, 1504 с, 1521 сл, 1557 сл, 1610 сл.
Комплекс ${\mathbf{S}}{{{\mathbf{Q}}}_{{\mathbf{2}}}}{\mathbf{ZnL}}_{{\mathbf{2}}}^{{\mathbf{4}}}$ (IV): a) m(L4) = 0.104 г. Кристаллы IV, пригодные для РСА, получали медленным охлаждением толуольного раствора. Выход 0.23 г (65%).
ИК-спектр (ваз. масло; ν, см–1): 463 сл; 503 ср; 537 ср; 563 с; 601 сл; 655 с; 674 ср; 692 сл; 705 сл; 729 ср; 753 сл; 776 сл; 801 сл; 829 с; 866 сл; 926 сл; 955 с; 979 сл; 1016 ср; 1027 ср; 1071 сл; 1092 сл; 1110 ср; 1182 ср; 1200 ср; 1205 ср; 1218 ср; 1276 с; 1318 сл; 1327 сл; 1342 ср; 1351 ср; 1358 ср; 1416 ср; 1553 с; 1605 с; 2242 ср.
Комплекс SQ2ZnL5 (V): a) m(L5) = 0.04 г. Кристаллы V, пригодные для РСА, получали медленным охлаждением толуольного раствора. Выход 0.17 г (58%).
ИК-спектр (ваз. масло; ν, см–1): 462 сл; 499 ср; 553 ср; 598 сл; 636 ср; 655 с; 675 ср; 692 сл; 712 ср; 727 ср; 804 сл; 814 сл; 831 ср; 890 сл; 927 сл; 954 с; 1011 ср; 1026 ср; 1048 сл; 1080 ср; 1167 ср; 1180 ср; 1199 сл; 1205 сл; 1228 сл; 1238 сл; 1279 ср; 1344 ср; 1351 ср; 1364 ср; 1385 с, 1408 с; 1477 с; 1490 с; 1550 сл; 1564 сл; 1589 с.
ИК-спектры регистрировали на ИК Фурье-спектрометре ФСМ-1201 в вазелиновом масле в кюветах из KBr. Спектры ЭПР фиксировали на спектрометре Bruker EMX. В качестве стандарта при определении g-фактора использовали 2,2-дифенил-1-пикрилгидразил (g = 2.0037). Для определения точных параметров спектр ЭПР симулировали с помощью программы WinEPR SimFonia (Bruker).
Магнитную восприимчивость поликристаллических образцов комплексов измеряли при помощи SQUID-магнетометра Quantum Design MPMSXL в интервале температур 2–300 K в магнитном поле 0.5 Т. При расчетах парамагнитной составляющей магнитной восприимчивости (χ) комплексов учитывали аддитивный диамагнитный вклад ионов в соответствии с константами Паскаля. Эффективный магнитный момент в зависимости от температуры вычисляли по формуле:
РСА комплексов проведен на дифрактометрах Smart Apex I (Ia, III) Bruker D8 Quest (Iб, V) и Oxford Xcalibur (II, IV) при 100 K (λ(MoKα) = 0.71073 Å). Структура соединений расшифрована прямыми методами и уточнена МНК по F 2 в полноматричном анизотропном приближении для всех неводородных атомов (SHELXTL) [19]. Поглощение учтено по программам SADABS [20] (Ia, Iб, III и V) и ABSPACK [21] (II, IV). Основные длины связей и валентные углы в молекулах I–V сведены в табл. 1, кристаллографические параметры и детали уточнения структур приведены в табл. 2.
Таблица 1.
Основные длины связей (Å) и валентные углы (град) в комплексах I–V
| Cвязь | Ia | Iб | II | III | IV | V |
|---|---|---|---|---|---|---|
| Zn(1)–O(1) | 2.058(3) | 2.0421(10) | 2.0670(10) | 2.0398(17) | 2.0306(12) | 2.017(6) |
| Zn(1)–O(2) | 2.039(3) | 2.0379(10) | 2.0713(11) | 2.0225(17) | 2.017(6) | |
| Zn(1)–O(3) | 2.052(3) | 2.0826(10) | 2.0140(17) | |||
| Zn(1–O(4) | 2.054(3) | 2.0827(10) | 2.0282(17) | |||
| Zn(1)–N(1) | 2.213(3) | 2.2798(16) | 2.1272(13) | 2.102(2) | 2.243(3) | 2.130(6) |
| Zn(1)–N(2) | 2.189(3) | 2.2109(16) | 2.2635(13) | |||
| O(1)–C(1) | 1.287(5) | 1.2787(17) | 1.2763(18) | 1.283(3) | 1.276(2) | 1.316(7) |
| O(2)–C(2) | 1.279(4) | 1.2819(15) | 1.2797(18) | 1.285(3) | 1.316(7) | |
| O(3)–C(7) | 1.295(4) | 1.2750(18) | ||||
| O(4)–C(8) | 1.283(5) | 1.2841(18) | ||||
| C(1)–C(2) | 1.475(6) | 1.476(2) | 1.488(2) | 1.480(3) | 1.440(2) | 1.480(4) |
| С(1)–С(1А) | 1.472(3) | |||||
| C(1)–C(6) | 1.455(5) | 1.4426(18) | 1.444(2) | 1.436(3) | 1.428(4) | |
| C(2)–C(3) | 1.444(6) | 1.437(2) | 1.440(2) | 1.433(3) | 1.370(2) | 1.425(4) |
| C(3)–C(4) | 1.370(5) | 1.3716(19) | 1.373(2) | 1.367(3) | 1.365(4) | |
| С(3)–С(3А) | 1.422(3) | |||||
| C(4)–C(5) | 1.407(6) | 1.420(2) | 1.421(2) | 1.425(3) | 1.425(4) | |
| C(5)–C(6) | 1.369(6) | 1.362(2) | 1.373(2) | 1.370(3) | 1.364(4) | |
| C(7)–C(8) | 1.460(6) | 1.484(2) | ||||
| C(8)–C(9) | 1.462(6) | 1.440(2) | ||||
| C(9)–C(10) | 1.372(6) | 1.369(2) | ||||
| C(10)–C(11) | 1.403(6) | 1.533(2) | ||||
| C(11)–C(12) | 1.371(6) | 1.424(2) | ||||
| C(7)–C(12) | 1.449(6) | 1.444(2) | ||||
| Угол | Ia | Iб | II | III | IV | V |
| O(1)Zn(1)O(2) | 80.86(11) | 80.80(4) | 79.19(4) | 80.24(7) | 81.3(2) | |
| O(1)Zn(1)O(4) | 97.67(11) | 172.72(4) | 148.49(7) | |||
| O(1)Zn(1)O(1A) | 174.10(6) | 99.50(7) | 140.20(12) | |||
| O(1)Zn(1)O(1B) | 180.00(10) | |||||
| O(1)Zn(1)O(3) | 177.52(13) | 100.70(4) | 89.11(7) | |||
| O(1)Zn(1)O(2A) | 99.12(4) | 90.5(2) | ||||
| O(2)Zn(1)O(4) | 178.02(12) | 99.58(4) | 91.85(7) | |||
| O(2)Zn(1)O(1A) | ||||||
| O(2)Zn(1)O(3) | 100.44(11) | 171.85(4) | 146.22(7) | |||
| O(2)Zn(1)O(2A) | 178.36(6) | 140.15(12) | ||||
| O(1A)Zn(1)O(3) | 80.98(11) | 79.48(4) | ||||
| O(1A)Zn(1)O(2A) | ||||||
| O(1)Zn(1)N(1) | 87.93(13) | 87.05(3) | 92.43(5) | 102.41(7) | 98.59(5) | 95.1(3) |
| O(2)Zn(1)N(1) | 90.61(13) | 89.18(3) | 94.85(5) | 105.99(7) | 107.6(3) | |
| O(4)Zn(1)N(1) | 87.29(12) | 93.66(5) | 109.08(7) | |||
| O(1A)Zn(1)N(1) | 81.41(5) | |||||
| O(2A)Zn(1)N(1) | 89.92(13) | |||||
| O(3)Zn(1)N(1) | 94.47(4) | 107.60(7) | ||||
| O(1)Zn(1)N(2) | 90.61(13) | 92.95(3) | 85.64(4) | |||
| O(2)Zn(1)N(2) | 92.11(13) | 90.82(3) | 87.09(4) | |||
| O(4)Zn(1)N(2) | 89.23(13) | 86.02(4) | ||||
| O(1A)Zn(1)N(2) | ||||||
| O(3)Zn(1)N(2) | 91.46(13) | 85.87(4) | ||||
| O(2A)Zn(1)N(2) | ||||||
| N(1)Zn(1)N(2) | 176.02(14) | 180.0 | 178.06(5) |
Таблица 2.
Кристаллографические данные и параметры рентгеноструктурного анализа соединений I–V
| Параметр | Значение | |||||
|---|---|---|---|---|---|---|
| Ia | Iб | II | III | IV | V | |
| М | 678.19 | 672.23 | 938.55 | 1560.67 | 714.19 | 586.06 |
| Сингония | Тетрагональная | Моноклинная | Триклинная | Триклинная | Тетрагональная | Моноклинная |
| Пр. гр. | P41212 | P21/c | P–1 | P–1 | P42/mnm | P21/n |
| a, Å | 14.342(2) | 28.5467(8) | 11.45372(13) | 11.0257(14) | 10.29120(10) | 10.2662(3) |
| b, Å | 14.342(2) | 7.2684(2) | 12.91641(18) | 12.3052(18) | 10.29120(10) | 10.2695(3) |
| c, Å | 37.188(6) | 19.6044(5) | 19.6170(3) | 17.128(3) | 17.8078(2) | 17.6397(5) |
| α, град | 90 | 90 | 103.3422(12) | 72.662(2) | 90 | 90 |
| β, град | 90 | 110.7250(10) | 99.2711(11) | 73.001(3) | 90 | 90.0260(10) |
| γ, град | 90 | 90 | 103.0182(11) | 79.257(2) | 90 | 90 |
| V, Å3 | 7650(3) | 3804.47(18) | 2680.85(6) | 2108.8(5) | 1886.00 | 1859.73(9) |
| Z | 8 | 4 | 2 | 1 | 2 | 2 |
| ρ, г/см3 | 1.178 | 1.174 | 1.163 | 1.229 | 1.258 | 1.047 |
| µ, мм–1 | 0.681 | 0.684 | 0.504 | 0.626 | 0.695 | 0.691 |
| Размер кристалла, мм | 0.390 × 0.350 × 0.090 | 0.360 × 0.120 × 0.100 | 0.500 × 0.400 × 0.300 | 0.300 × 0.120 × 0.060 | 0.300 × 0.150 × 0.100 | 0.430 × 0.300 × 0.260 |
| θmin–θmax, град | 2.008–26.998 | 2.221–27.999 | 2.996–26.000 | 1.880–29.000 | 3.024–26.976 | 3.044–25.996 |
| Всего отражений | 32 115 | 38 934 | 38 937 | 22 342 | 29 124 | 37 006 |
| Независимых отражений | 8183 | 4554 | 10 479 | 11 053 | 1148 | 3596 |
| Rint | 0.0687 | 0.0273 | 0.0316 | 0.0571 | 0.0365 | 0.0319 |
| Отражений с I > 2σ(I) |
6443 | 4320 | 9381 | 7468 | 1070 | 3255 |
| Число уточняемых параметров | 470 | 249 | 610 | 501 | 101 | 228 |
| R (I > 2σ(I)) | R1 = 0.0517 wR2 = 0.0961 |
R1 = 0.0322 wR2 = 0.0797 |
R1 = 0.0339 wR2 = 0.0806 |
R1 = 0.0591 wR2 = 0.1032 |
R1 = 0.0266 wR2 = 0.0658 |
R1 = 0.0829 wR2 = 0.2270 |
| GOOF (F 2) | 1.025 | 1.066 | 1.037 | 1.023 | 1.076 | 1.066 |
| Δρmax/Δmin, e Å–3 | 0.618/–0.292 | 0.529/–0.595 | 0.477/–0.318 | 0.847/–0.555 | 0.336–0.306 | 1.329–0.975 |
Кристаллографические данные депонированы в Кембриджском банке структурных данных (№ 1846558−1846563); deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для получения серии комплексов была использована стандартная методика лигандного обмена, успешно применявшаяся ранее для дизайна бис-о-семихиноновых комплексов магния [22, 23] и цинка [24–26]. К раствору SQ2Zn с двумя молекулами координированного эфира в толуоле приливали раствор нейтрального лиганда L1, L2, L3, L4, L5 в том же растворителе (схема 1 ). Реакции образования комплексов I, III, IV и V нечувствительны к стехиометрии исходных реагентов. Независимо от соотношения SQ2Zn и нейтрального лиганда L1 (L3, L4 или L5) (2 : 1, 1 : 1, 1 : 2) в кристаллическом состоянии были выделены координационный полимер I, биядерный III и моноядерные комплексы IV и V. Реакция с 4,4'-дипиридилом в соотношении реагентов 1 : 1 позволяет получить представленный на схеме 1 координационный полимер II, при недостатке азотсодержащего лиганда формируется биядерный комплекс, опубликованный ранее [26].
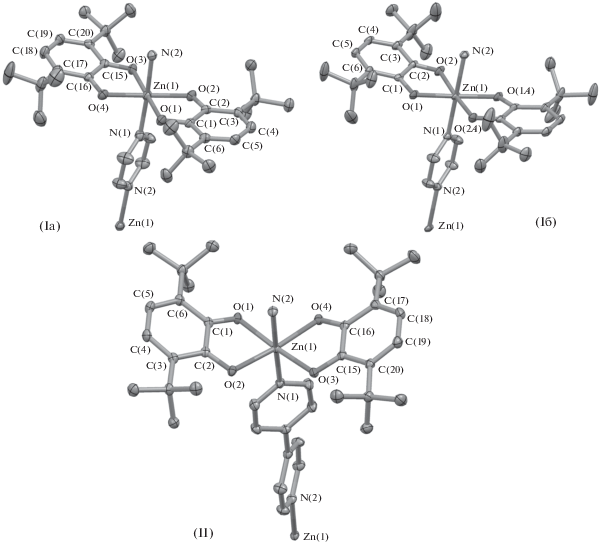
В случае комплекса I получены две полиморфные формы при кристаллизации из различных растворителей. Первый тип кристаллов Ia получен медленным охлаждением раствора в толуоле, второй тип Iб – добавлением гексана к раствору SQ2ZnL1 в хлористом метилене. Кристаллические ячейки комплексов Iа и Iб содержат молекулы сольватных растворителей (толуола и гексана соответственно), по одной на молекулу комплекса. Кристаллы II, пригодные для РСА, удалось получить медленным охлаждением комплекса SQ2ZnL2 в толуоле. Кристаллическая ячейка комплекса II содержит три сольватные молекулы толуола. Комплексы Iа, Ib и II представляют собой координационные полимеры, однако их кристаллическая упаковка критично различается. В кристалле комплекса Ia цепочки координационного полимера (SQ2ZnL)n перпендикулярны друг другу, в кристаллах комплексов Iб и II – только параллельные цепочки. В молекулах комплексов Iа, Iб и II атомы металла имеют искаженное октаэдрическое окружение (рис. 1). Экваториальную плоскость в октаэдре занимают атомы кислорода диоксоленовых лигандов, в аксиальных положениях находятся атомы азота N-донорных лигандов. о-Семихиноновые лиганды в кристаллах I и II несколько выгнуты к одному из азотных мостиковых лигандов. Двугранный угол между плоскостями о-семихиноновых лигандов составляет 9.94°, 15.63° и 42.28° для Ia, Iб и II соответственно. Это приводит к неравноценному связыванию цинка с азотом. Более длинная связь цинка с азотом наблюдается с тем пиразином (дипиридилом), в сторону которого происходит искривление (Zn–N(2) в случае кристаллов Iа (Iб) и Zn–N(1) для комплекса II) (рис. 1). Ароматические кольца дипиридильного лиганда в полимерных цепочкaх II некомпланарны – двугранный угол между их плоскостями составляет 49.79°. Угол N(1)Zn(1)N(2) 176.02° в комплексе Ia, 180° в Ib и 178.06° в комплексе II.
Рис. 1.
Молекулярная структура мономерной единицы координационныx полимерoв Ia, Iб и II. Приведены тепловые эллипсоиды 50%-ной вероятности. Атомы водорода не показаны для ясности.
Мостиковым бидентатным N-донорным лигандом в комплексе III является феназин, вызывающий повышенную стерическую загруженность координационного центра по сравнению с аналогичным ему пиразином. Это приводит к значительно большему углу излома по линии SQ–Zn–SQ – двугранный угол между о-семихиноновыми лигандами увеличивается по сравнению с соединением I и составляет 54.49°. Как результат в молекуле III не реализуется полимерная структура. Соединение представляет собой биядерный комплекс, в котором феназин связывает два пятикоординированных металлических центра (рис. 2). Атомы цинка в III имеют тетрагонально-пирамидальную координацию, при этом атомы кислорода о-семихиноновых лигандов формируют основание пирамиды, а атомы азота феназина находятся в апикальных позициях. В кристаллической ячейке комплекса III содержатся также четыре молекулы сольватного толуола.
Рис. 2.
Молекулярная структура комплексов III, IV, V. Приведены тепловые эллипсоиды 50%-ной вероятности. Атомы водорода не показаны для ясности.
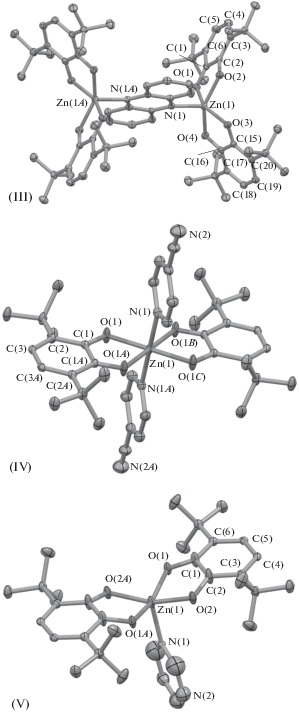
Циано-группы мостикового 4-цианопиридина в комплексе IV не участвуют в координационных связях. Независимо от соотношения исходных реагентов при формировании кристаллической фазы образуется соединение, содержащее две молекулы нейтрального лиганда и шестикоординированный атом металла (рис. 2). Ранее в реакциях бис(3,6-ди-трет-бутил-о-бензосемихинолято)цинка с 4-иминозамещенными пиридинами [26] были получены пятикоординационные производные металла. С другой стороны, результаты комплексообразования SQ2Zn с 4-цианопиридином находятся в соответствии с результатами, полученными в ходе исследований с участием родственных соединений кобальта [27] и марганца [28]. Кристаллическая ячейка IV содержит три сольватных молекулы толуола на молекулу комплекса. 4-Цианопиридин разупорядочен по двум позициям, в результате чего атом цинка лежит на двух взаимно перпендикулярных осях второго порядка. При этом октаэдрический координационный полиэдр, как и в случае соединений I и II, в основании формируется атомами кислорода о-семихиноновых лигандов, а атомы азота донорных лигандов занимают апикальные позиции. При этом связь Zn(1)–N(1) не ортогональна экваториальной плоскости. Атом азота отклоняется от строго вертикальной позиции на 13.37°.
В комплексе V реализуется соотношение SQ2Zn : L5 = 1 : 1. Однако второй атом азота не координирован с атомом металла соседних молекул, что не позволяет сформировать координационный полимер. Ароматические системы о-семихиноновых лигандов параллельны и лежат в одной плоскости (рис. 2). Атом цинка разупорядочен по двум позициям, располагающимся над и под этой плоскостью на расстоянии 0.734 Å. Плоскость хелатного цикла Zn(1)O(1)C(1)C(2)O(2) образует двугранный угол с плоскостью ароматических систем о-семихиноновых лигандов, равный 15.78°. Пиримидиновый фрагмент в молекуле V разупорядочен по четырем позициям.
Расстояния Zn–O и Zn–N в комплексах I–V лежат в интервалах, характерных для данного типа соединений, имеющих пяти- и шестикоординированные атомы металла [16, 18, 24–26]. При этом дистанции металл–кислород и металл–азот закономерно растут при переходе от пятикоординационных III и V к шестикоординационным I, II и IV. Значения длин связей C–O и распределение длин С–С в диолатном лиганде типичны для о‑семихинолятных лигандов и подтверждают его анион-радикальный характер. В ароматическом кольце анион-радикального лиганда наблюдается хиноидное альтернирование связей [29, 30].
Все синтезированные комплексы I–V имеют глубокую синюю окраску, устойчивы к кислороду и влаге воздуха в кристаллическом состоянии, обладают умеренной растворимостью в органических растворителях. Поликристаллические образцы I–V демонстрируют широкий неразрешенный сигнал ЭПР как при комнатной температуре, так и при 77 K c g-фактором 2.002, типичным для органических свободных радикалов. Спектр ЭПР в замороженной матрице толуола для комплексов I–V демонстрируeт суперпозицию нескольких типов сигналов. Для всех соединений наблюдаются хорошо разрешенные синглеты при g = 4, характерные для бирадикальных частиц и относящиеся к запрещенному переходу Δms = 2. При g = 2 (рис. 3) наблюдается суперпозиция синглета, отвечающего за монорадикальную примесь, образующуюся при диссоциации (ассоциации) бис-о-семихинолятов цинка в растворе, и сигнала, характеризующего диполь-дипольное взаимодействие в бирадикальных системах. Для точного определения параметров расщепления в нулевом поле комплексов I–V их спектры ЭПР, записанные при 150 K, промоделированы с использованием программного обеспечения WinEPR Simfonia. Параметры расщепления в нулевом поле спектров ЭПР бирадикальных комплексов I–V приведены в табл. 3. Необходимо отметить, что значение параметров спектров для комплексов I и II близки к наблюдаемым для аналогичных пятикоординационных cоединений [18, 26]. Это, в совокупности с хорошей растворимостью координационных поли-меров, указывает на разрыв более длинной связи Zn–N в полимерной цепочке. О разрыве одной из координационных связей Zn–N свидетельствует и спектр ЭПР для шестикоординационного комплекса IV, для которого наблюдаются сигналы от двух различных бирадикальных частиц. Преобладающий сигнал с параметром |D| = 179 Гс (0.0167 см–1) отвечает исходному шестикоординационному комплексу, а второй (минорный, |D| = 204 Гс (0.0191 см–1)) – продукту диссоциации с отрывом одного из цианопиридильных лигандов с образованием соответствующего пятикоординационного производного.
Рис. 3.
Экспериментальный (1) и симулированный (2) спектры ЭПР комплекса I в замороженной матрице толуола (150 K). Сигнал от примеси монорадикала в экспериментальном спектре обозначен (*). Сигнал, отвечающий запрещенному переходу Δms = 2, приведен во вставке. Параметры симуляции: S = 1, |D| = 199 Гс, |E| = 5 Гс, gX = 2.0023, gY = 2.0010, gZ = 2.0020, ΔHХ = 15 Гс, ΔHY = 12 Гс, ΔHZ = 15 Гс, L/G = 0.2.
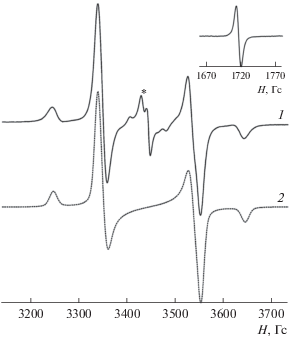
Таблица 3.
Параметры расщепления в нулевом поле спектров ЭПР бирадикальных комплексов I–IV в замороженной матрице толуола при T = 150 K
| Комплекс | |D|, Гс/см–1 | |E|, Гс/см–1 | r, Å* |
|---|---|---|---|
| I | 199/0.0186 | 5/0.0005 | 5.42 |
| II | 200/0.0187 | 6/0.0006 | 5.41 |
| III | 205/0.0191 | 7/0.0006 | 5.37 |
| IV | 204/0.0190 179/0.0167 |
5/0.0005 7/0.0006 |
5.38 5.59 |
| V | 206/0.0192 | 6/0.0006 | 5.36 |
* Расстояние между радикальными центрами, рассчитанное в приближении взаимодействия точечных диполей [37].
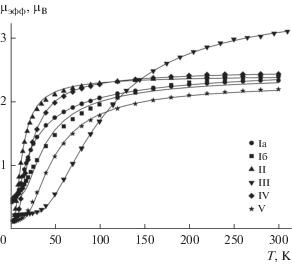
Температурная зависимость эффективного магнитного момента (µэфф) для комплексов I–V представлены на рис. 4. Высокотемпературные значения µэфф для соединений Ia, Iб, II, IV и V (2.40, 2.43, 2.44, 2.45 и 2.20 µB при Т = 300 K соответственно) близки к теоретической чисто спиновой величине 2.45 µB для двух невзаимодействующих SQ лигандов со спинами S = 1/2 при g-факторе, равном 2. Для координационных полимеров расчет проводился на одно мономерное звено. Для биядерного комплекса III значение µэфф (3.11 µB при Т = 300 K) соответствует теоретически чисто спиновой величине 3.46 µB для четырех невзаимодействующих SQ лигандов со спинами S = 1/2 при g-факторе, равном 2 (рис. 4). Значения µэфф для всех соединений плавно уменьшаются с последующим понижением температуры вплоть до 50 K. Ниже 50 K значения µэфф заметно убывают и при 5 K достигают величин, близких к 0 μB. Такое поведение зависимостей µэфф(T) указывает на наличие антиферромагнитных обменных взаимодействий между спинами SQ-лигандов. Оценку параметров обменного взаимодействия в комплексах проводили в рамках модели обменно-связанного димера (H = –2JS1S2). Рассчитанные параметры обменного взаимодействия представлены в табл. 4. Использование модели обменно-связанного димера для фрагментов (SQ)2Zn в координационных полимерах Ia и Iб позволяет лишь оценить параметр обмена, поскольку полученная величина междимерных взаимодействий (примерно –25 см–1) сопоставима по величине с обменом внутри фрагмента {(SQ)2Zn}. Большое значение параметра межкластерных обменных взаимодействий указывает на наличие сопоставимых по величине обменных взаимодействий как во фрагментах {(SQ)2Zn}, так и между ними. Однако на данный момент подходящих аналитических выражений для таких моделей обменно-связанных цепочек нет.
Таблица 4.
Оптимальные значения g-фактора, параметров обменного взаимодействия J, zJ' и примеси мономера p для комплексов I–V по данным магнетохимических исследований
| Комплекс | g | J, см–1 | zJ', см–1 | p, % |
|---|---|---|---|---|
| Ia | 2.07 | –17.5 | –24.1 | 3.6 |
| Ib | 2.0 (фикс.) | –32.5 | –10 | 5 |
| II | 1.98 | –12.3 | 0 | 0 |
| III | 2.09 | –94.6 | 0 | 0.5 |
| IV | 2.04 | –20.3 | 0 | 0.3 |
| V | 1.90 | –45.0 | 0 | 0.4 |
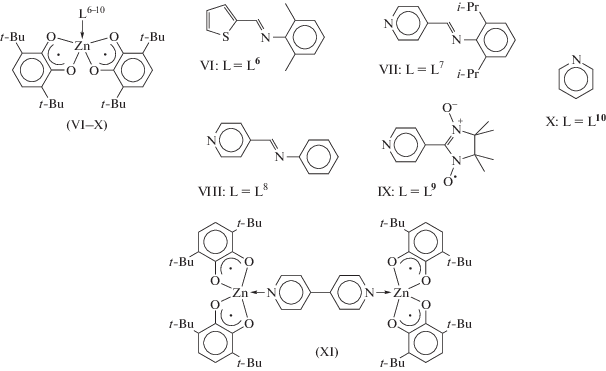
При переходе от опубликованных ранее шестикоординационных бис-о-семихиноновых комплексов цинка с цис-расположением радикальных лигандов [25] к их ближайшим аналогам c транс-расположением диолатных фрагментов (комплексы I, II, IV) меняется знак обменного взаимодействия с ферромагнитного на антиферромагнитный, и энергия обмена растет по абсолютному значению. Кроме того, росту энергии обмена также способствует искажение октаэдрического координационного окружения (комплекс IV) в сторону тетрагонально-бипирамидального при удлинении одной из связей Zn–N (соединения I и II). В [26] прямой магнитный обмен между радикальными лигандами был предложен в качестве основного определяющего магнитное поведение пятикоординационных бис-о-семихинолятов цинка. При этом была обнаружена зависимость величины энергии обмена от расстояния между центрами делокализации спиновой плотности в органических лигандах. Данные, полученные в ходе настоящей работы, хорошо коррелируют с результатами, полученными ранее для аналогичных бирадикальных соединений цинка VI–IX [18, 26] (схема 2 ).
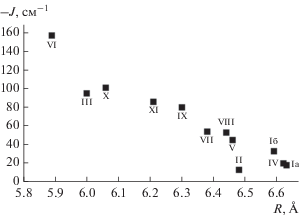
На рис. 5 представлена зависимость –J = f(R), где R – расстояние между радикалами, определенное как дистанция между центроидами, построенными по атомам C(1–6), O(1), O(2) и С(15–20), O(3), O(4). Результаты, полученные для комплексов I–V в ходе настоящего исследования, объединены с результатами [26] для соединений VI–IX. Cоответствие представленных результатов позволяет предположить, что в случае соединений I–V также преобладает канал прямого магнитного обмена. Важно отметить, что для родственных бирадикальных комплексов трехвалентных элементов (Al, Ga, In), содержащих в качестве апикального заместителя не нейтральный дононорный лиганд, а валентно-связанный диамагнитный анион, превалирует канал косвенного обмена [31–36]. Последний связан с перекрыванием магнитных орбиталей органических лигандов с σ*-связью M–X (M = Ga, Al; X = анионный апикальный заместитель) [31, 32] или с включением неподеленных электронных пар гетероатомов Х в формирование частично заполненных орбиталей [35].
Рис. 5.
Зависимость энергии антиферромагнитного обмена от расстояния между радикальными центрами в бирадикальных комплексах I–XI.
Таким образом, в ходе проведенного исследования синтезированы новые моно-, биядерные и полимерные бис-о-семихиноновые комплексы цинка, содержащие различные мостиковые бидентатные N-донорные лиганды. Молекулярное строение полученных комплексов установлено методом РСА. Обнаружено, что координационный полимер с пиразиновым мостиком образует две полиморфные кристаллические модификации, отличающиеся взаимным расположением полимерных цепей. Все исследованные соединения характеризуются антиферромагнитным взаимодействием между неспаренными электронами органических парамагнитных лигандов
Схема 2 .
Физико-химические исследования соединений выполнены с использованием оборудования аналитического центра ИМХ РАН.
Работа выполнена при финансовой поддержке Российского научного фонда (грант № 14-13-01296).
Список литературы
Ovcharenko V.I., Sagdeev R.Z. // Russ. Chem. Rev. 1999. V. 68. P. 345.
Koivisto B.D., Hicks R.G. // Coord. Chem. Rev. 2005. V. 249. P. 2612.
Ratera I., Veciana J. // Chem. Soc. Rev. 2012. V. 41. P. 303.
D’Alessandro D.M. // Chem. Commun. 2016. V. 52. P. 8957.
Jung O.-S., Pierpont C.G. // J. Am. Chem. Soc. 1994. V. 116. P. 2229.
Attia A.S., Pierpont C.G. // Inorg. Chem. 1997. V. 36. P. 6184.
Abakumov G.A., Lobanov A.V., Cherkasov V.K. et al. // Dokl. Akad. Nauk SSSR. 1985. V. 285. P. 906.
Chen X.-Y., Wei R.-J., Zheng L.-S., Tao J. // Inorg. Chem. 2014. V. 53. P. 13212.
Chen L., Wei R., Tao J. et al. // Sci. China Chem. 2012. V. 55. P. 1037.
Imaz I., Maspoch D., Rodriguez-Blanco C. et al. // Angew. Chem., Int. Ed. 2008. V. 47. P. 1857.
Drath O., Gable R.W., Poneti G. et al. // Cryst. Growth Des. 2017. V. 17. P. 3156.
Drath O., Gable R.W., Moubaraki B. et al. // Inorg. Chem. 2016. V. 55. P. 4141.
Cheng W.-Q., Li G.-L., Zhang R. et al. // J. Mol. Struct. 2015. V. 1087. P. 68.
Goswami S., Panja A., Butcher R.J. et al. // Inorg. Chim. Acta. 2011. V. 370. P. 311.
Shaikh N., Goswami S., Panja A. et al. // Inorg. Chem. 2005. V. 44. P. 9714.
Glavinovic M., Qi F., Katsenis A.D. et al. // Chem. Sci. 2016. V. 7. P. 707.
Гордон А., Форд Р. Спутник химика. М.: Мир, 1976. 543 с.
Пискунов А.В., Малеева А.В., Абакумов Г.А. и др. // Коорд. химия. 2011. Т. 37. С. 243 (Piskunov A.V., Maleeva A.V., Abakumov G.A. et al. // Russ. J. Coord. Chem. 2011. V. 37. P. 243. doi 10.1134/S1070328411030092).
Sheldrick G.M. SHELXTL. Version 6.12. Structure Determination Software Suite. Madison (WI, USA): Bruker AXS, 2000.
Sheldrick G.M. SADABS. Version 2.01. Bruker/Siemens Area Detector Absorption Correction Program. Madison (WI, USA): Bruker AXS, 1998.
Agilent Technologies. CrysAlis Pro. Yarnton (England): Agilent Technologies Ltd., 2011.
Пискунов А.В, Ладо А.В., Абакумов Г.А. и др. // Изв. АН. Сер. хим. 2007. С. 92 (Piskunov A.V., Lado A.V., Abakumov G.A. et al. // Russ. Chem. Bull. 2007. V. 56. P. 97. doi 10.1007/s11172-007-0016-1).
Пискунов А.В., Малеева А.В., Богомяков А.С., Фукин Г.К. // Изв. АН. Сер. хим. 2017. С. 1618 (Piskunov A.V., Maleeva A.V., Bogomyakov A.S., Fukin G.K. // Russ. Chem. Bull. 2017. V. 66. P. 1618. doi 10.1007/s11172-017-1933-2).
Ilyakina E.V., Poddel’sky A.I., Piskunov A.V. et al. // New J. Chem. 2012. V. 36. P. 1944.
Piskunov A.V., Maleeva A.V., Bogomyakov A.S. et al. // Polyhedron. 2015. V. 102. P. 715.
Piskunov A.V., Maleeva A.V., Fukin G.K. et al. // Inorg. Chim. Acta. 2017. V. 455. P. 213.
Schmidt R.D., Shultz D.A., Martin J.D., Boyle P.D. // J. Am. Chem. Soc. 2010. V. 132. P. 6261.
Jana N.Ch., Brandao P., Panja P. // J. Inorg. Biochem. 2016. V. 159. P. 96.
Poddels’ky A.I., Cherkasov V.K., Abakumov G.A. // Coord. Chem. Rev. 2009. V. 253. P. 291.
Brown S.N. // Inorg. Chem. 2012. V. 51. P. 1251.
Myers T.W., Holmes A.L., Berben L.A. // Inorg. Chem. 2012. V. 51. P. 8997.
Cates C.D., Myers T.W., Berben L.A. // Inorg. Chem. 2012. V. 51. P. 11891.
Piskunov A.V., Mescheryakova I.N., Bogomyakov A.S. et al. // Inorg. Chem. Commun. 2009. V. 12. P. 1067.
Piskunov A.V., Meshcheryakova I.N., Ershova I.V. et al. // RSC Adv. 2014. V. 4. P. 42494.
Piskunov A.V., Ershova I.V., Bogomyakov A.S. et al. // Inorg. Chem. 2015. V. 54. P. 6090.
Piskunov A.V., Ershova I.V., Bogomyakov A.S. et al. // Inorg. Chem. Commun. 2016. V. 66. P. 94.
Керрингтон А., Мак-Лечлан Э. Магнитный резонанс и его применение в химии. М.: Мир, 1970. С. 156.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия