Координационная химия, 2019, T. 45, № 5, стр. 306-310
Полиядерные глицингидроксиматные металламакроциклические комплексы Cu(II)–Gd(III): галохромные свойства
Г. Ю. Жигулин 1, *, Г. С. Забродина 1, М. А. Каткова 1, С. Ю. Кетков 1
1 Институт металлоорганической химии им. Г.А. Разуваева РАН
Нижний Новгород, Россия
* E-mail: gzhigulin@gmail.com
Поступила в редакцию 06.07.2018
После доработки 24.10.2018
Принята к публикации 03.12.2018
Аннотация
Методом электронной спектроскопии показано, что видимый спектр поглощения полиядерного металламакроциклического Cu(II)–Gd(III) комплекса чувствителен к рН. Так, интенсивность пика поглощения при 577 нм падает в 5 раз при уменьшении рН от 6.8 до 3.3, а затем возвращается к исходному уровню при увеличении рН вплоть до 12.4. На основе DFT расчетов и анализа топологических характеристик электронной плотности предложено объяснение изменений спектра в результате протонирования атома азота глицингидроксиматного лиганда.
Полиядерные металламакроциклические соединения, впервые описанные американской исследовательской группой под руководством Pecoraro в 1989 г. – уникальный класс супрамолекулярных соединений, структурно напоминающих краун-эфиры [1–3]. Объекты наших исследований – водорастворимые d–f-полиядерные 15-MC-5 металлaкрауны на основе α-аминогидроксамовых кислот [4]. α-Аминогидроксамовые кислоты (NH2–CHR–CO–NH–OH), известные широким спектром биологической активности, являются эффективными хелатирующими лигандами N,N- и O,O-типа. Отличительная особенность хелатных комплексов на основе гидроксамовых кислот – многообразие получаемых структур в зависимости от R-заместителя и природы металла, которые можно использовать для создания моделей ряда природных ферментов [5, 6]. Следует отметить, что одним из самых простых внешних раздражений, вызывающих “вкл–вы-кл–вкл” действия ферментов является изменение pH среды [7]. Явление галохромизма связано с обратимым изменением спектра поглощения в зависимости от pH. Однако большинство исследований галохромных соединений основано на органических молекулах и гораздо меньше внимания уделяется комплексам металлов [8]. Среди комплексов переходных металлов соединения меди(II) считаются наиболее перспективными для создания химически чувствительных pH материалов [9]. Ранее мы разработали оригинальный синтетический подход к водорастворимым гетероядерным 15-MC-5 комплексам меди(II) и лантанида(III) на основе глицингидроксамовой кислоты [10–14]. Комплексы Cu(II) и Gd(III) представляют отдельный интерес для их использования в качестве контрастирующих агентов для высокопольной МРТ [15, 16]. В продолжение этих работ с целью исследования поведения полиядерного металламакроцикла при различных значениях pH, на примере глицингидроксиматного комплекса Cu(II)-Gd(III) исследованы галохромные свойства 15-MC-5 соединений, связанные с протонированием атома азота аминогидроксиматного лиганда.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали коммерчески доступные (фирмы Aldrich) моногидрат ацетата меди, гексагидрат хлорида гадолиния и глицингидроксамовую кислоту.
Синтез Gd(H2O)4[15-MCCu(II)Glyha-5](Cl)3 ∙ 10H2O (I). К раствору 0.2 г (1 ммоль) Cu(OAc)2 ∙ H2O и 0.08 г (0.2 ммоль) GdCl3 ∙ 6H2O в 25 мл бидистиллированной воды при интенсивном перемешивании добавляли 0.09 г (1 ммоль) глицингидроксамовой кислоты. Через 40 мин раствор приобретал насыщенный сине-фиолетовый цвет. Смесь выдерживали 24 ч при 20°C и отфильтровывали. Темно-синие игольчатые кристаллы получали медленным испарением водного фильтрата при 40°C и дважды перекристаллизовывали из воды. Выход 0.21 г (84%).
| Найдено, %: | С 9.41; | H 3.83; | N 11.03; | Gd 12.29. |
| Для C10H48Cl3Cu5GdN10O24 | ||||
| вычислено, %: | С 9.43; | H 3.80; | N 11.00; | Gd 12.34. |
ИК-спектр (ν, см–1): 3220 сл, 1642 ср, 1594 с, 1439 ср, 1403 ср, 1308 ср, 1177 сл, 1147 сл, 1135 сл, 1074 с, 1035 с, 933 сл, 602 сл, 545 сл, 488 ср. УФ (293 K, H2O): λ = 575 нм.
ИК-спектры регистрировали на ИК-Фурье спектрометре ФСМ 1201. Образцы готовили по стандартной методике в вазелиновом масле. ЭСП получали на спектрометре Perkin Elmer Lambda 25. Элементный анализ выполняли с использованием C,H,N-анализатора Euro EA 3000.
Методика расчетов. DFT исследование медьсодержащих модельных фрагментов 15-MC-5 реализовали при помощи программного пакета Gaussian09 [17]. Оптимизацию геометрии выполняли с использованием гибридного XC функционала B3LYP [18–20] и двойного ζ-базиса DGDZVP [21, 22] в приближении поляризованного континуума PCM [23] для учета растворителя воды. Энергетические минимумы структур, полученных в ходе оптимизации, подтверждали анализом гармонических колебаний, среди которых не обнаружено мод с мнимыми частотами. Трехъядерные комплексы меди(II) с общими зарядами +2 и +3 смоделированы как высокоспиновые системы с мультиплетностью 4. Карты деформационной электронной плотности получали с использованием программы Multiwfn 3.3.9 [24] путем вычитания из молекулярной электронной плотности комплексов плотности сферически симметричных атомов. Анализ в рамках квантовой теории атомов в молекулах (QTAIM) [25, 26] выполняли по программе AIMAll [27].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
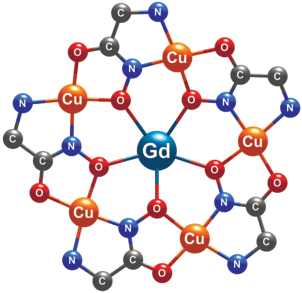
Водорастворимый комплекс Gd(H2O)4[15-MCCu(II)Glyha-5](Cl)3 (I) синтезировали на воздухе при комнатной температуре из глицингидроксамовой кислоты, ацетата меди(II) и хлорида Gd(III). Особенность строения комплекса I определяется наличием плоского металламакроцикла, состоящего из пяти ионов Cu2+, пяти глицингидроксиматных лигандов и центрального иона Gd3+, координационно связанного с пятью атомами кислорода металламакроцикла [15] (рис. 1). Помимо атомов кислорода лигандов гадолиний содержит в координационной сфере четыре молекулы воды.
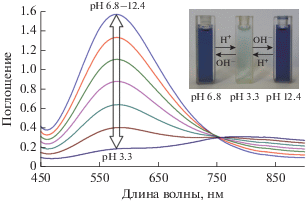
Такая металлaмакроциклическая структура медного “крауна” формирует характерный ЭСП с полосой при 577 нм (ε = 420 М–1 см–1), соответствующей d–d-переходам Cu(II). Было обнаружено, что комплекс I проявляет галохромные свойства. Так, интенсивность пика поглощения при 577 нм под действием кислоты падает в 5 раз при уменьшении pH от 6.8 до 3.3, а затем восстанавливается при добавлении основания с увеличением pH вплоть до 12.4 (рис. 2).
Наблюдаемое pH-индуцированное изменение интенсивности сигнала можно объяснить обратимым изменением хромофорной структуры в результате протонирования и депротонирования гидроксиматных лигандов металлaмакроциклического кольца. Известно, что оксиамидные фрагменты могут существовать в разнообразных изомерных и таутомерных формах, что позволяет называть их “химическими хамелеонами” [28]. Наши квантово-химические расчеты в рамках теории функционала плотности на уровне B3LYP/DGDZVP показывают, что протонирование иминового атома азота N(1) в модельном фрагменте A металламакроцикла приводит к увеличению деформационной электронной плотности (ДЭП) вдоль связи Cu–N(1) в окрестности атома азота (рис. 3). Интересно, что при этом заряд на атоме азота становится менее отрицательным (его величина, рассчитанная в рамках QTAIM, изменяется от –0.68 до –0.59 е). При протонировании расстояние Cu–N(1) увеличивается от 1.961 до 2.231 Å; остальные координационные связи меди изменяются незначительно (табл. 1).
Рис. 3.
Оптимизированные структуры модельных фрагментов A (а) и B (б) комплекса I и соответствующие карты положительной деформационной электронной плотности (0.01–0.13 ат. ед., шаг 0.01 ат. ед.) в плоскостях CuN(1)N(2) (в, г).
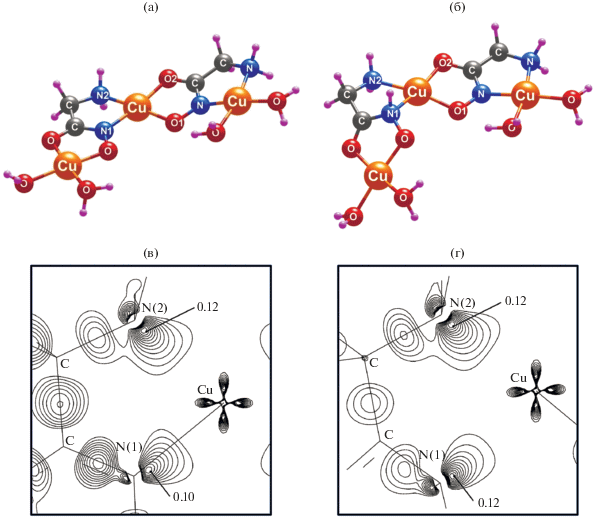
Таблица 1.
Межатомные расстояния (Å) комплекса I по данным РСА [15] и модельных фрагментов A, B по данным DFT
| Связь | d, Å | ||
|---|---|---|---|
| I | A* | B* | |
| Cu–Nimine | 1.905(3)–1.929(3) | 1.961 | 2.231 |
| Cu–Namine | 2.005(4)–2.023(3) | 2.056 | 2.040 |
| Cu–Ooxime | 1.928(3)–1.944(3) | 1.965 | 1.921 |
| Cu–Ocarbonyl | 1.946(3)–1.957(3) | 1.990 | 1.993 |
Исследования, проведенные в рамках QTAIM предсказывают существенное понижение значений электронной плотности ρ(r) и лапласиана ∇2ρ(r) в критической точке (3, –1) связи Cu–N(1): от 0.0981 до 0.0535 ат. ед. и от 0.3038 до 0.1700 ат. ед. соответственно (табл. 2). На примере комплексов Cu(II) в [29] обнаружено аналогичное уменьшение значений ρ(r) и ∇2ρ(r) в критической точке (3, –1) при удлинении координационной связи, которое сопровождается увеличением максимума положительной ДЭП в окрестности донорного атома. Отношение модуля плотности потенциальной энергии |V(r)| к плотности кинетической энергии G(r) позволяет классифицировать тип межатомных контактов: |V(r)|/G(r) < 1 указывает на взаимодействие замкнутых оболочек, в том числе ионное, а |V(r)|/G(r) > 2 характерно для ковалентных связей [30, 31]. Расчетные значения |V(r)|/G(r) в критических точках координационных связей меди с глицингидроксиматными лигандами лежат в интервале от 1 до 2 (табл. 2), что соответствует промежуточному типу взаимодействий. Отметим, что уменьшение величины |V(r)|/G(r) связи Cu–N(1) от 1.3978 до 1.2780 при протонировании (A → B) не приводит к изменению ее характера, хотя свидетельствует об увеличении вклада ионных взаимодействий. Ранее было показано, что значение плотности потенциальной энергии в критической точке (3, –1) коррелирует с энергией координационной связи [32, 33]. Поэтому уменьшение величины |V(r)| от 0.1764 до 0.0754 (табл. 2), можно рассматривать как признак значительного ослабления связи Cu–N(1) при протонировании.
Таблица 2.
Топологические параметры электронной плотности (ат. ед.) в критических точках (3, –1) координационных связей центрального атома меди модельных фрагментов A и B
| Атомы | ρ(r) | ∇2ρ(r) | V(r) | G(r) | |V(r)|/G(r) |
|---|---|---|---|---|---|
| A | |||||
| Cu–N(1) | 0.0981 | 0.3038 | –0.1764 | 0.1262 | 1.3978 |
| Cu–N(2) | 0.0821 | 0.2278 | –0.1361 | 0.0965 | 1.4104 |
| Cu–O(1) | 0.0892 | 0.3333 | –0.1692 | 0.1262 | 1.3407 |
| Cu–O(2) | 0.0830 | 0.3203 | –0.1569 | 0.1185 | 1.3241 |
| B | |||||
| Cu–N(1) | 0.0535 | 0.1700 | –0.0754 | 0.0590 | 1.2780 |
| Cu–N(2) | 0.0840 | 0.2472 | –0.1434 | 0.1026 | 1.3977 |
| Cu–O(1) | 0.0992 | 0.3757 | –0.1929 | 0.1434 | 1.3452 |
| Cu–O(2) | 0.0840 | 0.3099 | –0.1567 | 0.1171 | 1.3382 |
Анализ молекулярных орбиталей модельных комплексов А и B показал, что присоединение протона к атому азота приводит к уменьшению энергетической щели между β-ВЗМО и β-НСМО от 1.91 до 1.53 эВ. Разность между энергиями β‑НСМО и β-ВЗМО фрагмента A, содержащими вклад d-орбиталей меди, хорошо согласуется с наблюдаемым положением максимума полосы поглощения в ЭСП комплекса I, которое соответствует энергии 2.15 эВ. Расчетное уменьшение щели β-ВЗМО – β-НСМО при протонировании A отвечает сдвигу электронного перехода в область 800 нм. Действительно, при уменьшении pH увеличивается интенсивность поглощения в длинноволновой области спектра (рис. 2). Таким образом, расчеты подтверждают объяснение изменения окраски раствора комплекса I протонированием атома азота гидроксиматного лиганда.
Работа выполнена с использованием научного оборудования Центра коллективного пользования “Аналитический центр ИМХ РАН”.
Исследования электронной плотности и спектральных свойств комплексов проведены в рамках проекта Российского научного фонда (№ 18-13-00356). Г.Ю. Жигулин благодарит за финансовую поддержку Российский фонд фундаментальных исследований (проект № 18-33-01252 мол_а).
Список литературы
Mezei G., Zaleski C.M., Pecoraro V.L. // Chem. Rev. 2007. V. 107. P. 4933.
Tegoni M., Remelli M. // Coord. Chem. Rev. 2012. V. 256. P. 289.
Bodwin J.J., Cutland A.D., Malkani R.G. et al. // Coord. Chem. Rev. 2001. V. 216–217. P. 489.
Каткова М.А. // Коорд. химия. 2018. Т. 44. С. 135 (Kаtkova M.A. // Russ. J. Coord. Chem. 2018. V. 44. P. 284. doi 10.1134/S107032841804005X).
Sigel H., Martin R.B. // Chem. Rev. 1982. V. 82. P. 385.
Ford P. // Chem. Sci. 2016. V. 7. P. 2964.
Guha S., Liu J., Baltazar G. et al. // Adv. Exp. Med. Bi-ol. 2014. V. 801. P. 105.
Solomon E.I., Heppner D.E., Johnston E.M. et al. // Chem. Rev. 2014. V. 114. P. 3659.
Golchoubian H., Moayyedi G., Rezaee E. et al. // Polyhedron. 2015. V. 96. P. 71.
Katkova M.A., Zabrodina G.S., Muravyeva M.S. et al. // Inorg. Chem. Commun. 2015. V. 52. P. 31.
Katkova M.A., Zabrodina G.S., Muravyeva M.S. et al. // Eur. J. Inorg. Chem. 2015. V. 2015. P. 5202.
Kremlev K.V., Samsonov M.A., Zabrodina G.S. et al. // Polyhedron. 2016. V. 114. P. 96.
Makarov S.G., Zabrodina G.S., Cherkasov A.V. et al. // Macroheterocycles. 2016. V. 9. P. 263.
Katkova M.A., Zabrodina G.S., Kremlev K.V. et al. // Thin Solid Films. 2017. V. 628. P. 112.
Muravyeva M.S., Zabrodina G.S., Samsonov M.A. et al. // Polyhedron. 2016. V. 114. P. 165.
Katkova M.A., Zabrodina G.S., Baranov E.V. et al. // Appl. Organomet. Chem. 2018. V. 32. e4389. doi https://doi.org/10.1002/aoc.4389
Frisch M.J., Trucks G.W., Schlegel H.B. et al. Gaussian 09, Revision B.01. Wallingford (CT, USA): Gaussian, Inc., 2010.
Becke A.D. // J. Chem. Phys. 1993. V. 98. P. 5648.
Lee C., Yang W., Parr R.G. // Phys. Rev. B: Condens. Matter. 1988. V. 37. P. 785.
Stephens P.J., Devlin F.J., Chabalowski C.F. et al. // J. Phys. Chem. 1994. V. 98. P. 11623.
Godbout N., Salahub D.R., Andzelm J. et al. // Can. J. Chem. 1992. V. 70. P. 560.
Sosa C., Andzelm J., Elkin B.C. et al. // J. Phys. Chem. 1992. V. 96. P. 6630.
Tomasi J., Mennucci B., Cammi R. // Chem. Rev. 2005. V. 105. P. 2999.
Lu T., Chen F. // J. Comput. Chem. 2012. V. 33. P. 580.
Bader R.F.W. Atoms in Molecules: A Quantum Theory. Oxford: Oxford Univ. Press, 1990. 456 p.
Cortes-Guzman F., Bader R.F.W. // Coord. Chem. Rev. 2005. V. 249. P. 633.
Keith T.A. AIMAll. Version 10.05.04. Overland Park: TK Gristmill Software, 2010. URL: http://aim.tkgristmill.com.
Mikhaleva A.I., Zaitsev A.B., Trofimov B.A. // Russ. Chem. Rev. 2006. V. 75. P. 797.
Dos Santos L.H.R., Lanza A., Barton A.M. et al. // J. Am. Chem. Soc. 2016. V. 138. P. 2280.
Espinosa E., Alkorta I., Elguero J. et al. // J. Chem. Phys. 2002. V. 117. P. 5529.
Gibbs G.V., Cox D.F., Crawford T.D. et al. // J. Chem. Phys. 2006. V. 124. P. 084704.
Borissova A.O., Korlyukov A.A., Antipin M.Yu., Lyssenko K.A. // J. Phys. Chem. A. 2008. V. 112. P. 11519.
Puntus L.N., Lyssenko K.A., Antipin M.Yu., Bünzli J.-C.G. // Inorg. Chem. 2008. V. 47. P. 11095.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия