Координационная химия, 2019, T. 45, № 6, стр. 378-384
Особенности строения мономерных октаэдрических монооксокомплексов d2-рения(V) с атомами кислорода тридентатно-хелатных (О,P,О и O,P,N) лигандов
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
2 Всероссийский институт научной и технической информации РАН
Москва, Россия
* E-mail: sergienko@igic.ras.ru
Поступила в редакцию 16.07.2018
После доработки 12.09.2018
Принята к публикации 18.10.2018
Аннотация
Рассмотрены особенности строения восьми моноядерных октаэдрических монооксокомплексов d2-Re(V) с тридентатно-хелатными (О,Р,О и O,P,N) лигандами [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)$$\left( {{\text{L}}_{{{\text{б и }}}}^{n}} \right)$], [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)$Cl2], [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)$Cl(PPh3)]. Показано, что связи Re–O${{\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)}_{{т р а н с }}}$ cоизмеримы по длине (или несколько короче) со связями Re–O${{\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)}_{{ц и с }}}$ или Re–O(СТ), что свидетельствует о наличии в структуре псевдо-диоксогрупп ReO2 c повышенной кратоностью обеих расположенных в транс-положениях друг к другу связей Re–O. В структуре двух соединений связи Re–O${{\left( {{\text{L}}_{{{\text{б и }}}}^{2}} \right)}_{{т р а н с }}}$ в среднем на 0.094 Å длиннее, чем Re–O(СТ) и на 0.189 Å длиннее, чем Re–O${{\left( {{\text{HL}}_{{{\text{б и }}}}^{3}} \right)}_{{ц и с }}}$ в соответствии со структурным проявлением транс-влияния кратносвязанного оксолиганда.
Строение мономерных октаэдрических комплексов (МОК) d 0-, d 2-металлов V–VII групп (Nb, V, Mo, W, Re, Tc) с кратносвязанными лигандами О(оксо) подробно описано в [1–7]. Для d 2-Re(V) методом РСА определена кристаллическая структура более 500 соединений – см. Кембриджский банк структурных данных (КБСД, вeрсия 5.38, ноябрь 2017 г. [8]. Большинство из этих комплексов – МОК ReOоксоО(Lig)транс – с атомами кислорода моно- и полидентатных лигандов в транс-позициях к оксолигандам. Ранее мы опубликовали ряд обобщающих статей по МОК d 2‑Re(V) c лигандами – атомами галогенидов, азота, серы и водорода, кислорода монодентатных ацидолигандов [гидроксо, алкоксо (метоксо-, этоксо-, пропоксо-), ОRn– (n = 1, 2; R = Ph, Cy, C6H4OH, C6H4OMe, P(O)(OMe)2, C(O)(CF3), OCMe(CF3)2, BF3), OERn– (n = 1, 2; Е = Si, B, S; R = Me3, F3, О2CF3)], бидентатно-хелатных (О,О), (O,S), (O,C), (О,Р), (O,N) однозарядных лигандов, тридентатно-хелатных (О,N,O) [9], (О,О,О) [10], (O,S,O и S,O,S) [11] одно- и двузарядных лигандов, а также нейтральных кислородсодержащих лигандов молекул воды, фосфин- и арсиноксидных OER3 (E = P, As; R3 = Ph3, PhEt2), молекул OR' [ДМФ, R''OH (R'' = Me, Et, Pr), L (ON4C6 · C6H10, O–(C6H3MeCH2NH+Et2)), O–(NH+C5H4)] в транс-позициях к кратносвязанным лигандам О(оксо). Ранее мы опубликовали обзорные статьи по особенностям строения МОК d 0-Re(VII) [12] и d 0-, d 2-технеция(V, VII) [13].
Структурное проявление транс-влияния кратносвязанного лиганда O(оксо) (СПТВ) – удлинение противолежащей связи Re–Lтранс – характеризуется параметром ∆ (разность длин одноименных связей {[Re–Lтранс] – [Re–Lцис]}). Если в структуре нет лигандов одного сорта и в транс-, и в цис-позициях к О(оксо), мы используемем параметр {[Re–Lтранс] – [Re–L(СТ)]}, где СТ – среднестатистическая стандартная длина связи Re(V) с атомом лиганда того же сорта, что и Lтранc. В качестве параметра Re–O(СТ) мы приняли (как и в [4]) значение 2.04 Å.
В настоящей статье обсуждается строение мономерных октаэдрических монооксокомплексов [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)$$\left( {{\text{L}}_{{{\text{б и }}}}^{n}} \right)$], [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)$Cl2], содержащих тридентатно-хелатный (О,Р,О или O,P,N), а также бидентатно-хелатный или два монодентатных лигандa.
Основные длины связей в восьми структурно исследованных соединениях указанного выше типа приведены в табл. 1.
Таблица 1.
Основные геометрические параметры (Å) в мономерных октаэдрических комплексах с тридентатно-хелатными (О,Р,О и O,P,N) лигандами*
| Комплекс | Re=O | Re–Lцис | Re–Отранс | Δ, (Δ) | Литeрaтура |
|---|---|---|---|---|---|
| [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{1}}}} \right)$Cl(PPh3)] CH3Cl2 (I) | 1.670(3) | 2.019(3) O$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{1}}}} \right)$ | 2.047(3) | 0.028 | [14] |
| 2.4833(12) P$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{1}}}} \right)$ | O$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{1}}}} \right)$ | ||||
| 2.4240(12) P(PPh3) | |||||
| 2.3759(12) Cl | |||||
| [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{2}}}} \right)$$\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{1}}}} \right)$] (II) | 1.692(3) | 2.050(3) O$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{2}}}} \right)$ | 2.026(3) | –0.024 | [15] |
| 1.994(2) O$\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{1}}}} \right)$ | O$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{2}}}} \right)$ | ||||
| 2.391(1) P$\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{2}}}} \right)$ | |||||
| 2.428(1) P$\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{1}}}} \right)$ | |||||
| [ReO$\left( {{\text{HL}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$Cl2] (III) | 1.680(7) | 2.224(8) N$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$ | 1.943(7) | (–0.097) | [16] |
| 2.414(2) P$\left( {{\text{HL}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$ | O$\left( {{\text{HL}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$ | ||||
| 2.453(3) Cl(транс к Р) | |||||
| 2.353(3) Cl(транс к N) | |||||
| [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$Cl2] (IV) | 1.695(9) | 2.111(11) N$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$ | 1.953(9) | (–0.087) | [16] |
| 2.433(4) P$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$ | O$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$ | ||||
| 2.438(4) Cl(транс к Р) | |||||
| 2.376(4) Cl(транс к N) | |||||
| [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$Cl2] · · 0.25CH2Cl2 (V) | 1.702(12) ± 0.009 | 2.123(15) ± 0.014 N $\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$ | 1.966(12) ± 0.005 | (–0.080) | [17] |
| 2.447(6) ± 0.005 P$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$ | O$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)$ | ||||
| 2.438(6) ± 0.007 Cl(транс к Р) | |||||
| 2.396(6) ± 0.007 Cl(транс к N) | |||||
| [ReO$\left( {{\text{HL}}_{{{\text{т р и }}}}^{{\text{4}}}} \right)$Cl2] · · MeOH (VI) | 1.679(4) | 2.195(4) N $\left( {{\text{HL}}_{{{\text{т р и }}}}^{{\text{4}}}} \right)$ | 1.976(3) | (–0.064) | [18] |
| 2.414(1) P$\left( {{\text{HL}}_{{{\text{т р и }}}}^{{\text{4}}}} \right)$ | O$\left( {{\text{HL}}_{{{\text{т р и }}}}^{{\text{4}}}} \right)$ | ||||
| 2.429(1) Cl(транс к Р) | |||||
| 2.344(1) Cl(транс к N) | |||||
| [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{5}}}} \right)$$\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{2}}}} \right)$] · · MeOH (VII) | 1.6680(4) | 1.951(4) O$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{5}}}} \right)$ | 2.100(4) | (0.060) 0.149 |
[19] |
| 2.025(5) N$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{5}}}} \right)$ | O$\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{2}}}} \right)$ | ||||
| 2.471(2) P$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{5}}}} \right)$ | |||||
| 2.459 P$\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{2}}}} \right)$ | |||||
| [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{5}}}} \right)$$\left( {{\text{HL}}_{{{\text{б и }}}}^{{\text{3}}}} \right)$]Cl (VIII) | 1.667 ± 0.004 | 1.939 ± 0.003 O$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{5}}}} \right)$ | 2.168(3) ± 0.003 | (0.128) 0.229 |
[19] |
| 2.012 ± 0.017 N$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{5}}}} \right)$ | O$\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{2}}}} \right)$ | ||||
| 2.465 ± 0.017 P$\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{5}}}} \right)$ | |||||
| 2.455 ± 0.004 P$\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{3}}}} \right)$ |
* ${{\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{1}}}} \right)}^{{{\text{2}}--}}}$ = P(C6H4O)2C6H5OSiMe3; ${{\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{2}}}} \right)}^{{{\text{2}}--}}}$ = (OC6H4)2PPh; ${{\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{3}}}} \right)}^{ - }}$ = OC6H4CH=NH(CH2)3PPh3; ${{\left( {{\text{HL}}_{{{\text{т р и }}}}^{{\text{4}}}} \right)}^{ - }}$ = = Ph2PC6H4CH2NHC6H4O; ${{\left( {{\text{L}}_{{{\text{т р и }}}}^{{\text{5}}}} \right)}^{{{\text{2}}--}}}$ = OСH2NС(=O)С6H4PPh2; ${{\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{1}}}} \right)}^{--}}$ = OC6H4PPh2; ${{\left( {{\text{L}}_{{{\text{б и }}}}^{{\text{2}}}} \right)}^{--}}$ = OC(=O)C6H4PPh2; ${\text{HL}}_{{{\text{б и }}}}^{{\text{3}}}$ = = OC{NH(CH2)2OH}C6H4PPh2.
СТРОЕНИЕ КОМПЛЕКСОВ С ТРИДЕНТАТНО-ХЕЛАТНЫМ (О,Р,O) ЛИГАНДОМ
В каждом из двух рассматриваемых в данной главе комплексов все три атома двухзарядных тридентатно-хелатных (О,P,O) лигандов ${\text{L}}_{{{\text{т р и }}}}^{m}$ (m = = 1, 2) расположены на общей грани октаэдра атома Re (fac-изомер). Транс-позицию к кратносвязанному оксолиганду в обеих структурах занимает один из двух алкоксиатомов кислорода лиганда ${\text{L}}_{{{\text{т р и }}}}^{m}.$ При координации с атомом рения лигандов ${\text{L}}_{{{\text{т р и }}}}^{m}$ замыкаются два сочлененных по связи Re–P аналогичных пятичленных металлоцикла ReOC2P.
Строение комплекса [ReO$\left( {L_{{т р и }}^{1}} \right)$Cl(PPh3)] · · CH3Cl2 (I). В кристаллической структуре I [14] (рис. 1) в тридентатном бис(хелатном) ((2-триметилсилилокси)фенил)бис(2-фенолято)фосфиновом лиганде P(C6H4O)2(C6H4OSiMe3$\left( {{\text{L}}_{{{\text{т р и }}}}^{1}} \right)$ группа Me3SiOC6H4 концевая. Связь Re–O2$\left( {{\text{L}}_{{{\text{т р и }}}}^{1}} \right)$ в транс-позиции к О1(оксо) 2.047 Å на 0.028 Å длиннее, чем Re–O3${{\left( {{\text{L}}_{{{\text{т р и }}}}^{1}} \right)}_{{ц и с }}}$ 2.019 Å. Из двух связей Re–P одна – с атомом Р(1) лиганда ${\text{L}}_{{{\text{т р и }}}}^{1}$ (2.4833 Å) – заметно длиннее, чем Re–P2(PPh3) (2.4240 Å).
Рис. 1.
Строение комплексов: [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{1}} \right)$Сl(PPh3)] (I); [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{2}} \right)$$\left( {{\text{L}}_{{{\text{б и }}}}^{1}} \right)$] (II).
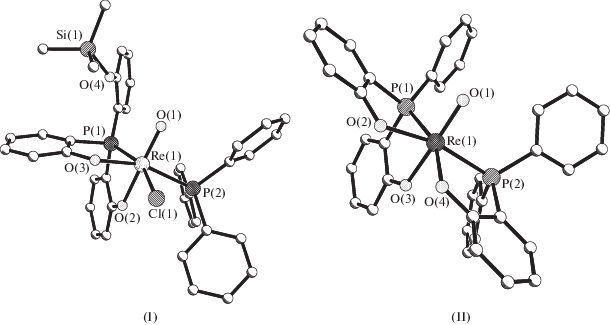
Строение комплекса [ReO$\left( {L_{{т р и }}^{2}} \right)$$\left( {L_{{б и }}^{1}} \right)$] (II) с бидентатно-хелатным (О,P) лигандом $L_{{б и }}^{1}{\mathbf{.}}$ В кристаллической структуре II [15] (рис. 1) тридентатно-хелатный бис(о-гидроксифенил)фенилфосфиновый лиганд (OC6H4)2PPh ${{\left( {{\text{L}}{{{_{{{\text{т р и }}}}^{2}}}^{{}}}} \right)}^{{2 - }}}$ замыкает два пятичленных металлоцикла ReOC2P, а однозарядный бидентатно-хелатный (О,Р) (о-гидроксифенил)дифенилфосфиновый лиганд ОС6Н4PPh2$\left( {{\text{L}}_{{{\text{б и }}}}^{1}} \right)$ – один аналогичный хелатный цикл. Отметим, что в комплексе II, в отличие от I, связь Re–O3${{\left( {{\text{L}}_{{{\text{т р и }}}}^{2}} \right)}_{{т р а н с }}}$ 2.026 Å не длиннее, а несколько короче (на 0.024 Å), чем Re–O2${{\left( {{\text{L}}_{{{\text{т р и }}}}^{2}} \right)}_{{ц и с }}}$ (2.050 Å), а также связь Re–P1$\left( {{\text{L}}_{{{\text{т р и }}}}^{2}} \right)$ 2.391 Å заметно короче (на 0.092 Å), чем аналогичная связь в I, и на 0.037 Å короче связи Р2$\left( {{\text{L}}_{{{\text{б и }}}}^{2}} \right)$ в данном соединении II (2.428 Å). В комплексе II атом рения, как обычно, смещен из экваториальной плоскости атомов O2P2 к оксолиганду: параметр ΔRe равен 0.273 Å.
СТРОЕНИЕ КОМПЛЕКСОВ С ТРИДЕНТАТНО-ХЕЛАТНЫМ (О,Р,N) ЛИГАНДОМ
Известна кристаллическая структура шести моноядерных октэдрических комплексов, содержащих тридентатный бис(хелатный) лиганд (O,P,N).
В каждом из этих соединений все три атома однозарядных тридентатно-хелатных (О,P,N) лигандов ${\text{L}}_{{{\text{т р и }}}}^{m}$ (m = 3–5) расположены на общей грани октаэдра атома Re (fac-изомер). Транс-позицию к кратносвязанному оксолиганду во всех шести структурах занимает фенольный атом кислорода лиганда ${\text{L}}_{{{\text{т р и }}}}^{m}.$ При координации с атомом рения лигандов ${\text{L}}_{{{\text{т р и }}}}^{m}$ замыкаются два сочлененных по связи Re–N хелатных цикла, один из которых всегда шестичленный RePC3N, а второй различается дентатностью (подробнее см. далее).
Строение комплексов [ReO$\left( {L_{{т р и }}^{m}} \right)$Cl2)] (m = 3, 4). Определена структура четырех соединений, содержащих однозарядные тридентатные бис(хелатные) лиганды (O,P,N). Во всех комплексах хлоро-лиганды расположены в цис-позициях друг к другу. Комплексные молекулы в трех из них – [ReOCl2$\left( {{\text{HL}}_{{{\text{т р и }}}}^{3}} \right)$] (III) [16], [ReOCl2$\left( {{\text{L}}_{{{\text{т р и }}}}^{3}} \right)$] (IV) [16] (рис. 2) и [ReOCl2$\left( {{\text{L}}_{{{\text{т р и }}}}^{3}} \right)$] 0.25CH2Cl2 (V) [17] – имеют близкое строение. В комплексе III атом азота лиганда (2-дифенилфосфинопропиламинометил)фенолято ОС6Н4-2-CH2NH–(CH2)3PPh2$\left( {{\text{HL}}_{{{\text{т р и }}}}^{3}} \right)$– протонирован и sp3-гибридизован, в отличие от sp2-гибридизованного атома N лиганда 2-дифенилфосфинопропилиминометил)фенолято ОС6Н4-2-CH=N–(CH2)3PPh2$\left( {{\text{L}}_{{{\text{т р и }}}}^{3}} \right)$ в структуре IV, V c двойной связью N=C(1). Длины связей в октаэдрах ReO2NPCl2 в трех структурах близки по длине, за одним исключением: связи Re–N$\left( {{\text{L}}_{{{\text{т р и }}}}^{3}} \right)$ в IV, V 2.111, 2.123 ± 0.014 Å (в структуре V – две независимые молекулы) заметно короче, чем 2.224 Å в III. Естественно, что двойная связь N=C(1) в IV, V 1.35(2) 1.305(20) ± 0.005 Å cущественно короче одинарной в III (1.504(14) Å), а углы ReNC1 в IV, V 127.5(11)°, 126.9(13)° ± 2.1° больше, чем в III (111.8(6)°). При координации с атомом Re лиганды ${\text{L}}_{{{\text{т р и }}}}^{3},$ ${\text{HL}}_{{{\text{т р и }}}}^{3}$ формируют два шестичленных металлоцикла: RePC3N и ReOC3N. Отметим, что во всех трех структурах две независимые связи Re–Cl различаются по длине: Re–Cl(1), транс к Р, длиннее, чем Re–Cl(2), транс к N (соответственно 2.438–2.454 и 2.353–2.396 Å), очевидно, из-за более сильного транс-влияния атома фосфора. Авторы [17] явно ошибочно приписывают разницу длины двух связей Re–Cl транс-эффекту более прочной связи Re–N.
Рис. 2.
Строение комплексов: [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{3}} \right)$Cl2] (IV); [ReO$\left( {{\text{HL}}_{{{\text{т р и }}}}^{4}} \right)$Cl2] (VI); [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{5}} \right)$$\left( {{\text{HL}}_{{{\text{б и }}}}^{3}} \right)$]+ (VIII).
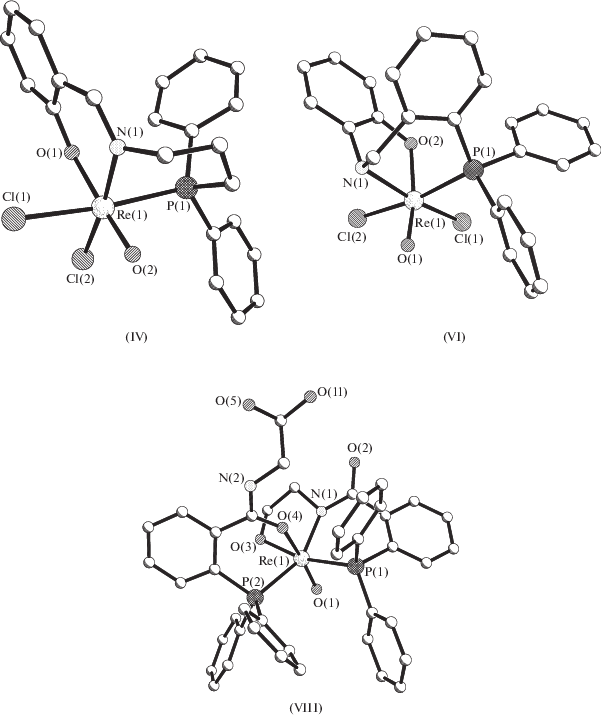
В кристaллической структуре [ReOCl2$\left( {{\text{HL}}_{{{\text{т р и }}}}^{4}} \right)$] (VI) [18] (рис. 2) лиганд 2-((2-дифенилфосфино)бензиламино)фенолято Ph2PC6H4-2-CH2NHC6H4O– (HL4), координируясь с атомом рения, замыкает два металлоцикла (сопряженных по связи Re–N) – шестичленный RePC3N и пятичленный ReOC2N.
Строение комплексов [ReO$\left( {L_{{т р и }}^{5}} \right)$$\left( {L_{{б и }}^{n}} \right)$] с бидентатно-хелатными лигандами (О,Р). Определена кристаллическая структура двух соединений [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{5}} \right)$$\left( {{\text{L}}_{{{\text{б и }}}}^{n}} \right)$] [19], содержащих двухзарядный 2-(дифенилфосфинил)-N-(2-оксоэтил)бензамидный лиганд O(CH2)2NC(=O)C6H4PPh2$\left( {{\text{L}}_{{{\text{т р и }}}}^{5}} \right).$ Соединения различаются бидентатно-хелатными (О,Р) лигандами – однозарядный 2-(дифенилфосфанил)бензоато OC(=O)C6H4PPh2$\left( {{\text{L}}_{{{\text{б и }}}}^{n}} \right)$ в структуре нейтрального комплекса с метанольным сольватом [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{5}} \right)$$\left( {{\text{L}}_{{{\text{б и }}}}^{n}} \right)$] · MeOH (VII) и нейтральный 2-(2-(дифенилфосфанил)-N-(2-гидроксиэтил)бензамид OC{NH(CH2)2CO2}C6H4PPh2$\left( {{\text{HL}}_{{{\text{б и }}}}^{3}} \right)$ в катионном однозарядном комплексе c противоионом хлором [ReO$\left( {{\text{L}}_{{{\text{т р и }}}}^{5}} \right)$$\left( {{\text{HL}}_{{{\text{б и }}}}^{3}} \right)$]Cl (VIII) (рис. 2). В обеих структурах комплексы имеют сходное строение. Лиганд ${\text{L}}_{{{\text{т р и }}}}^{5},$ имеющий в VII, VIII меридианальную (mer) геометрию, при координации с атомом Re замыкает сочлененные по связи Re–N шести- и пятичленный металлоциклы RePC3N (A) и ReOC2N (Б). Бидентатно-хелатные лиганды ${\text{L}}_{{{\text{б и }}}}^{n}$ в структуре VII, VIII образуют с атомами металла пятичленные хелатные циклы ReOC3P (В). Структура VIII, содержащая две кристаллографические молекулы, определена с невысокой точностью, и ее геометрические параметры в [19] не обсуждаются. В структуке VII шестичленный металлоцикл А существенно неплоский; максимальное отклонение от средней плоскости (Δср) составляет 0.223 Å. Пятичленный хелатный цикл Б имеет конформацию N-конверта с отклонением атома азота от средней плоскости ReOC2 (±0.022 Å) на 0.179 Å. Так же, как и А, металлоциклы В в обоих комплексах структуры VIII существенно неплоские (Δср 0.341 Å). В транс-позициях к оксолигандам в структуре VII, VIII, в отличие от структуры комплекса II, находятся атомы кислорода бидентатно-хелатных ${\text{L}}_{{{\text{б и }}}}^{n}$ (а не тридентатно-хелатного ${\text{L}}_{{{\text{т р и }}}}^{2},$ как в II). При этом связи Re–O$\left( {{\text{L}}_{{{\text{б и }}}}^{n}} \right)$ в VII, VIII (2.100, 2.168 Å) cущественно длиннее, чем Re–O$\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)$ в I–VI (1.943–2.047 Å) (подробнее см. далее).
ОСОБЕННОСТИ СТРОЕНИЯ МОНОМЕРНЫХ ОКТАЭДРИЧЕСКИХ МОНООКСОКОМПЛЕКСОВ РЕНИЯ(V) C ТРИДЕНТАТНО-ХЕЛАТНЫМИ ЛИГАНДАМИ (О,Р,О И O,Р,N)
В табл. 2 приведены средние значения основных геометрических параметров в структуре I–VIII.
Таблица 2.
Основные геометрические параметры (Å) мономерных октаэдричеcких монооксокомплексов d2‑Re(V) с тридентатнo-хелатными (О,P,О и N,P,O) лигандами
| Параметр | Значение, Å* |
|---|---|
| Re–O(оксо) | 1.667–1.702 {8} (1.682 ± 0.020) |
| Re–O${{\left( {{\text{L}}_{{{\text{б и }}}}^{n}} \right)}_{{т р а н с }}}$ | 2.100, 2.168 {2} (2.134 ± 0.034) |
| Re–O${{\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)}_{{т р а н с }}}$ | 1.943–2.047 {6} (2.003 ± 0.060) |
| Re–O${{\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)}_{{ц и с }}}$ | 1.939–2.050 {4} (1.990 ± 0.060) |
| Δ{Re–O$\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)$} | 0.028, –0.024 {2} (0.002 ± 0.026) |
| (Δ){Re–O$\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)$} | –0.097…–0.064 {4} (–0.082 ± 0.018) |
| (Δ){Re–O$\left( {{\text{L}}_{{{\text{б и }}}}^{n}} \right)$} | 0.149, 0.229 {2} (0.189 ± 0.040) |
| Re–N${{\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)}_{{ц и с }}}$ | 2.001–2.224 {6} (2.115 ± 0.109) |
| Re–Cl(транс к Р) | 2.424–2.454 {5} (2.437 ± 0.014) |
| Re–Cl(транс к N) | 2.344–2.396 {4} (2.368 ± 0.028) |
| Δ{Re–Сl(транс к P–транс к N)} | 0.042–0.101 {4} (0.072 ± 0.030) |
| Re–P$\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)$ | 2.391–2.483 {8} (2.440 ± 0.049) |
| Re–P$\left( {{\text{L}}_{{{\text{б и }}}}^{n}} \right)$ | 2.428–2.459 {3} (2.442 ± 0.017) |
| Re–P(Ph3) | 2.424 {1} |
Оcтановимся на двух особенностях стереохимии октаэдрических монооксокомплексов металлов V–VII групп (в том числе рения).
1. Выбор транс-партнера (при наличии конкурирующих лигандов) определяется “принципом самосогласованности” [2]: в транс-положении к кратносвязанному лиганду О(оксо) по преиму-ществу располагается наименее поляризуемый нейтральный σ-донорный лиганд (атом), связь с которым легче ослабить, а не отрицательно заряженный (ацидо) лиганд (атом).
2. Связи Re–L, транс к О(оксо), удлиняются из-за СПТВ кратносвязанного оксолиганда.
Первое правило не реализуется во всех восьми обсуждаемых в данном обзоре комплексах: в соединениях I–VIII в транс-позициях к О(оксо) расположены ацидоатомы кислорода лигандов Lтри, Lби. При этом связи Re–O${{\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)}_{{т р а н с }}}$ 1.943–2.047 Å в шести из восьми рассмотренных комплексов I–VI соизмеримы по длине со связями Re–O${{\left( {{\text{L}}_{{{\text{т р и }}}}^{m}} \right)}_{{ц и с }}}$ в I, II, VII, VIII: 1.939–2.050 Å [а не длиннее, как Re–O${{\left( {{\text{L}}_{{{\text{б и }}}}^{n}} \right)}_{{т р а н с }}}$ в VII, VIII (на 0.149, 0.229 Å) и в большинстве монооксооктаэдрических комплексов d2-Re(V) вследствие СПТВ]. Этот факт, казалось бы, противоречит “принципу самосогласованности” [2]. Однако на самом деле расстояния Re–O(Lтри) в транс-позициях к оксолигандам в соединениях I–VI можно рассматривать как имеющие повышенную кратность, так как они заметно меньше по длинe Re–O(СТ) 2.04 Å [4]. B данном случае можно говорить о псевдодиоксокомплексах, содержащих два лиганда О(оксо) и О(L)транс повышенной кратности. Напомним, что в диоксокомплексах d2-металлов V–VII групп два кратносвязанных лиганда всегда располагаются в транс-позициях друг к другу.
Отметим, что в комплексах III–VI два типа связей рений–хлор – в транс-позициях к атомам фосфора и азота лигандов ${\text{L}}_{{{\text{т р и }}}}^{m}$ – существенно различаются по длине. Первые из них (Re–Cl(1) 2.424–2.454 Å, средн. 2.437 Å) заметно (в среднем на 0.069 Å) длиннее вторых (Re–Cl(2) 2.344–2.396 Å, средн. 2.368 Å).
Список литературы
Порай-Кошиц М.А., Гилинская Э.А. Кристаллохимия. М.: ВИНИТИ. Итоги науки и техники, 1966. С. 126.
Порай-Кошиц М.А., Атовмян Л.О. // Коорд. химия. 1975. Т. 1. С. 1271.
Griffith F., Wicing C. // J. Chem. Soc. A. 1968. P. 379.
Порай-Кошиц М.А. // Изв. Югосл. кристаллогр. центра. 1974. Т. 9. С. 19.
Порай-Кошиц М.А., Атовмян Л.О. Кристаллохимия координационных соединений молибдена. М.: Наука, 1974. 231 с.
Shustorovich E.M., Porai-Koshits M.A., Buslaev Yu.A. // Coord. Chem. Rev. 1975. V. 17. P. 1.
Порай-Кошиц М.А., Сергиенко В.С. // Успехи химии. 1990. Т. 59. С. 86.
Allen F.H. // Acta Crystallogr. B. 2002. V. 58. P. 380.
Sergienko V.S. // Russ. J. Inorg. Chem. 2018. V. 63. № 14. P. 1757.
Сергиенко В.С. // Журн. неорган. химии. 2019. V. 64.
Сергиенко В.С., Чураков А.В. // Журн. неорган. химии. 2019. V. 64. № 3. С. 260.
Сергиенко В.С., Чураков А.В. // Кристаллография. 2014. Т. 59. № 3. С. 341 (Sergienko V.S., Churakov A.V. // Сrystallogr. Rep. 2014. V. 59. № 3. Р. 300. doi 10.1134/S1063774514030171).
Сергиенко В.С., Чураков А.В. // Кристаллография. 2013. Т. 58. № 1. С. 3 (Sergienko V.S., Churakov A.V. // Сrystallogr. Rep. 2013. V. 58. № 1. Р5. doi 10.1134/ S1063774513010112).
Cavell R.G., Hilts R.W., Luo H., McDonald R. // Inorg. Chem. 1999. V. 38. P. 897.
Lao H., Setyawati I., Rettig S.J., Orvig C. // Inorg. Chem. 1995. V. 34. P. 2287.
Banbery H.J., Hussain W., Hamor T.A. et al. // Polyhedron. 1991. V. 10. P. 243.
Banbery H.J., Hussain W., Hamor T.A. et al. // Dalton Trans. 1990. P. 657.
Barandov A., Abram U. // Polyhedron. 2009. V. 28. P. 1355.
Correia J.D., Domingos A., Paulo A., Santos I. // Dalton Trans. 2000. P. 2477.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия


