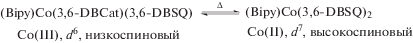Координационная химия, 2019, T. 45, № 9, стр. 546-552
Гетероспиновые комплексы кобальта, никеля и меди – производные 4-TEMPO-окси-3,6-ди-трет-бутил-о-бензохинона
Н. О. Дружков 1, Е. Н. Николаевская 2, А. В. Черкасова 1, К. А. Кожанов 1, *, М. П. Бубнов 1, А. В. Черкасов 1, А. С. Богомяков 3, В. К. Черкасов 1, **
1 Институт металлоорганической химии им. Г.А. Разуваева РАН
Нижний Новгород, Россия
2 Институт органической химии им. Н.Д. Зелинского РАН
Москва, Россия
3 Международный томографический центр СО РАН
Новосибирск, Россия
* E-mail: kostik@iomc.ras.ru
** E-mail: cherkasov@iomc.ras.ru
Поступила в редакцию 05.12.2018
После доработки 25.03.2019
Принята к публикации 04.04.2019
Аннотация
Синтезирован ряд гетероспиновых бис-о-семихиноновых комплексов кобальта, никеля и меди, производных 4-TEMPO-окси-3,6-ди-трет-бутил-о-бензохинона: (DMSO)Cu(4-TEMPO-O-3,6-DBSQ)2 (I), (THF)2Ni(4-TEMPO-O-3,6-DBSQ)2 (II), (Py)2Ni(4-TEMPO-O-3,6-DBSQ)2 (III) и (Py)2Ni(4-TEMPO-O-3,6-DBSQ)2 (IV) (4-TEMPO-O-3,6-DBQ = 4-(3,6-ди-трет-бутил-1,2-диоксоциклогекса-3,5-диен-4-илокси)-2,2,6,6-тетраметилпиперидин-1-оксил 4-окси-2,2',6,6'-тетраметилпиперидин-1-оксил). Все комплексы охарактеризованы элементным анализом, ИК-спектроскопией, магнетохимией, ЭПР. Строение комплекса I установлено методом РСА (CIF file CCDC № 1882878). Координационный полиэдр атома меди в молекулярной структуре бис-о-семихинонового комплекса Сu(II) с диметилсульфоксидом – искаженная тетрагональная пирамида, в экваториальной плоскости которой расположены о-семихиноновые лиганды, в апикальном положении находится молекула ДМСО. Магнитные свойства комплексов I–IV согласуются с их составом и строением. В случае комплексов меди I и никеля II, III их магнитное поведение определяется балансом двух вкладов: ферромагнитного обменного взаимодействия металл–лиганд и антиферромагнитного лиганд–лиганд. Температурная зависимость магнитного момента комплекса кобальта IV отражает свойственное такого рода комплексам редокс-изомерное превращение, сопряженное со спиновым переходом. Участия нитроксильных радикальных центров в межмолекулярной координации не обнаружено.
Особый интерес в качестве строительных блоков при построении молекулярных магнетиков представляют бирадикальные гетероспиновые лиганды, содержащие два различных по природе магнитных центра, каждый из которых способен связываться с металлом [1–10]. Недавно мы синтезировали новый стерически экранированный о-бензохинон, содержащий 2,2,6,6-тетраметилпиперидиноксильную функциональную группу и показали, что его одноэлектронное восстановление является эффективным методом генерации неизвестных ранее гетероспиновых бирадикалов, содержащих одновременно нитроксильный и о‑семихиноновый радикальные центры [11]. Исходя из известной способности нитроксильных радикалов выступать в качестве лигандов в координационных соединениях [12–15], мы в настоящей работе синтезировали ряд гетероспиновых бис-о-семихиноновых комплексов кобальта, никеля и меди – производных 4-TEMPO-окси-3,6-ди-трет-бутил-о-бензохинона с целью выяснения возможного участия нитроксильного центра в образовании межмолекулярных координационных связей.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все синтетические процедуры проводили в вакуумированных ампулах в отсутствие следов кислорода воздуха и воды. Растворители очищали по стандартным методикам [16]. Реагенты и растворители приобретали из коммерческих источников (Aldrich, Fluka, Stream). о-Хинон, замещенный фрагментом TEMPO-O-, получали по методике [11].
Синтез (DMSO)Cu(4-TEMPO-O-3,6-DBSQ)2 · · 3DMSO (I). В вакуумированную ампулу помещали свежеочищенную металлическую медь (проволока), к которой затем добавляли раствор 4-TEMPO-O-3,6-DBQ (0.06 г, 1.54 × 10–4 моль) в 10 мл ДМСО. Ампулу оставляли на 2 мес. при комнатной температуре. В результате реакции выделяли продукт в виде слоистых игл зеленого цвета. Соединение в кристаллическом виде устойчиво на воздухе, хорошо растворимо в органических растворителях (за исключением предельных углеводородов), растворы чувствительны к действию кислорода воздуха. Выход I 0.07 г (75%).
| Найдено, %: | C 56.60; | H 8.03; | Cu 5.05; | S 10.87. |
| Для C54H96N2O12S4Cu | ||||
| вычислено, %: | C 56.05; | H 8.36; | Cu 5.49; | S 11.08. |
ИК-спектр (ν, см–1): 1576 ср, 1458 о. с, 1359 с, 1331 с, 1288 ср, 1238 ср, 1186 с, 1091 с, 1060 ср, 1022 с, 982 сл, 951 ср, 935 сл, 914 сл, 897 ср, 843 ср, 814 сл, 794 сл, 754 сл, 721 сл, 707 сл, 692 сл, 665 сл, 634 сл, 605 сл, 588 сл, 567 сл, 516 сл, 497 сл.
Синтез(THF)2Ni(4-TEMPO-O-3,6-DBSQ)2 (II). К замороженному раствору 0.35 г (0.9 ммоль) 4‑TEMPO-O-3,6-DBQ в 30 мл ТHF конденсировали 0.077 г (0.45 ммоль) карбонила никеля. При размораживании реакционной смеси до комнатной температуры наблюдали выделение СО и изменение цвета раствора на коричнево-зеленый. После окончания выделения газа (~2 ч) реакционную смесь концентрировали до 7–8 мл и высаживали продукт 50 мл гексана. Выход II в виде зеленого мелкокристаллического порошка 0.33 г (75%).
| Найдено, %: | C 66.07; | H 9.13; | N 2.63; | Ni 5.68. |
| Для C54H88N2O10Ni | ||||
| вычислено, %: | C 65.91; | H 9.01; | N 2.85; | Ni 5.96. |
ИК-спектр (ν, см–1): 1576 ср, 1489 с, 1458 о. с, 1452 о. с, 1363 ср, 1356 ср, 1327 с, 1242 ср, 1230 ср, 1196 ср, 1184 с, 1090 с, 1051 сл, 1026 сл, 1006 сл, 983 сл, 916 ср, 897 ср, 839 сл, 815 сл, 794 сл, 750 сл, 721 сл, 698 сл, 680 сл, 659 сл, 603 сл, 555 сл, 515 сл, 490 сл.
Синтез(Py)2Ni(4-TEMPO-O-3,6-DBSQ)2 (III). В вакуумированной ампуле растворяли 0.3 г (0.3 ммоль) комплекса Ni(4-TEMPO-O-3,6-DBSQ)2 ∙ 2THF (SQ = семихиноновый лиганд) в 5 мл пиридина. Из полученного раствора продукт высаживали медленным прибавлением 50 мл гексана. Выход комплекса III в виде темно-зеленого мелкокристаллического порошка 0.27 г (89%).
| Найдено, %: | C 67.18; | H 8.45; | N 5.84; | Ni 5.60. |
| Для C56H82N4O8Ni | ||||
| вычислено, %: | C 67.40; | H 8.28; | N 5.61; | Ni 5.88. |
ИК-спектр (ν, см–1): 1601 сл, 1576 сл, 1485 с, 1456 о. с, 1363 ср, 1323 ср, 1228 ср, 1217 ср, 1182 ср, 1082 ср, 1139 сл, 1024 сл, 1006 сл, 985 сл, 966 сл, 931 сл, 912 сл, 895 сл, 760 сл, 721 сл, 700 ср.
Синтез (Bipy)Co(4-TEMPO-O-3,6-DBSQ)2 (IV). В вакуумированной ампуле растворяли 0.5 г (1.28 ммоль) 4-TEMPO-O-3,6-DBQ, 0.11 г (0.32 ммоль) октакарбонилдикобальта и 0.1 г (0.64 ммоль) 2,2'-бипиридила (Bipy) в 40 мл THF. В течение 4 ч наблюдали медленное выделение СО и изменение цвета раствора на серо-коричневый. После окончания выделения газа удаляли растворитель, сухой остаток растворяли в 50 мл толуола при нагревании, затем из полученного раствора при охлаждении до –18°С выделили 0.48 г (75%) темно-коричневого мелкокристаллического порошка комплекса IV.
| Найдено, %: | C 67.78; | H 8.23; | N 5.33; | Со 5.71. |
| Для C56H80N4O8Co | ||||
| вычислено, %: | C 67.52; | H 8.09; | N 5.62; | Co 5.92. |
ИК-спектр (ν, см–1): 4500 ш, 1601 сл, 1570 ср, 1558 ср, 1448 о.с, 1360 ср, 1325 с, 1230 ср, 1180 с, 1084 с, 1024 сл, 1001 сл, 980 ср, 966 ср, 893 сл, 763 сл, 731 сл, 696 сл, 652 сл, 555 сл.
ИК-спектры регистрировали на приборе FSM 1201 с Фурье преобразованием в области 7000–400 см–1 (суспензии в вазелиновом масле). Магнитную восприимчивость измеряли на приборе Quantum Design MPMS XL SQUID магнитометре в интервале 2–300 К в магнитном поле 5000 Э. Диамагнитные поправки вносили, используя константы Паскаля. Эффективный магнитный момент рассчитывали по уравнению µэфф(T) = = [(3k/NA${\mu }_{{\text{B}}}^{{\text{2}}}$)χT]1/2 ≈ (8χT)1/2.
РCA кристаллического образца I (0.4 × 0.4 × × 0.1 мм) проведен на дифрактометре Bruker D8 Quest (ω-сканирование, МоКα-излучение, λ = = 0.71073 Å, T = 100 K, 2θ = 50.13°). Измерение и интегрирование экспериментальных наборов интенсивностей, учет поглощения и уточнение структуры проведены с использованием программных пакетов APEX3 [17], TWINABS [18] и SHELX [19]. Кристаллы I моноклинные (C48H78CuN2O9S, 3C2H6OS) пр. гр. P21/c, a = 18.8866(13), b = = 29.781(2), c = 11.3819(8) Å, β = 104.529(2)°, V = = 6197.2(8) Å3, Z = 4, ρ(выч.) = 1.240 мг/м3, μ = = 0.543 мм–1). Структура уточнена как мероэдрический двойник (HKLF 5) с соотношением доменов 0.72 : 0.28; 13 073 независимых отражения (Rint = 0.0789) использованы для уточнения 763 параметров структуры полноматричным МНК по $F_{{hkl}}^{2}$ в анизотропном приближении для неводородных атомов. Атомы водорода помещены в геометрически рассчитанные положения и уточнены изотропно с фиксированными тепловыми параметрами U(H)изо = 1.2U(C)экв (U(H)изо = 1.5U(C)экв для метильных групп). Анализ синтеза электронной плотности показал, что один из трет-бутильных заместителей и все молекулы DMSO, включая координированную молекулу на атоме меди(II), разупорядочены. Для каждого из разупорядоченных фрагментов локализованы два положения. Инструкции DFIX, EADP, ISOR и RIGU использованы для ограничения геометрических и анизотропных параметров атомных смещений в разупорядоченных фрагментах. После финального уточнения S(F 2) = 1.085 и R1 = 13.3% (для всех отражений, удовлетворяющих условию I > 2σ(I)). К сожалению, более низких значений факторов сходимости не удалось достичь из-за недостаточного качества кристаллических образцов (полнота сбора данных составила 90%) и большого количества разупорядоченных фрагментов. Остаточные максимум и минимум электронной плотности составили 1.76 и –0.92 e/Å3 соответственно.
Структура I зарегистрирована в Кембриджском банке структурных данных (CCDC № 1882878; ccdc.cam.ac.uk/getstructures).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
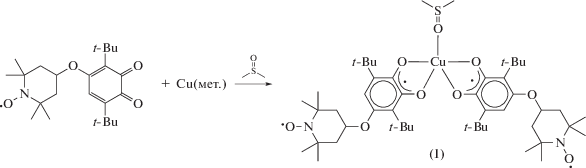
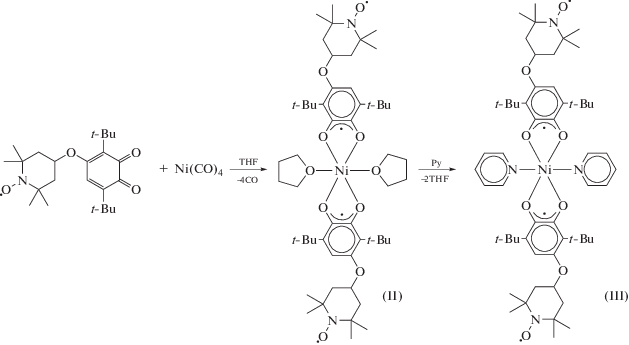
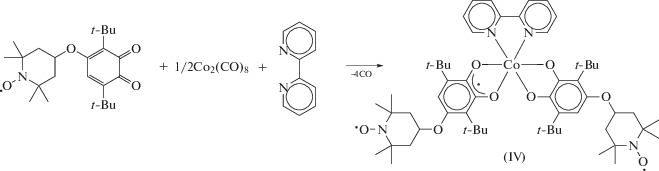
Комплекс меди I получали растворением металлической меди в растворе о-хинона в ДМСО. По реакции тетракарбонила никеля с о-хиноном, содержащим свободно-радикальный нитроксильный заместитель в среде THF получали комплекс II. Взаимодействие II с пиридином приводит к образованию комплексa III. Бис-хиноновый комплекс кобальта с 2,2'-дипиридилом IV получали по реакции соответствующего о-хинона с октакарбонилом дикобальта в присутствии 2,2'-дипиридила (схемы 1–3 ).
Схема 1 .
Схема 2 .
Схема 3 .
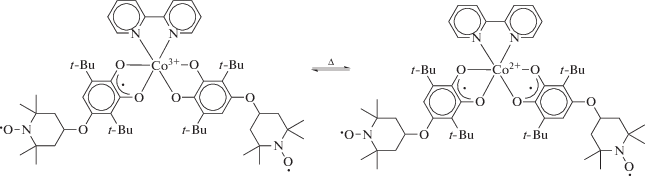
Равновесие редокс-изомерии для комплекса IV можно представить схемой 4 :
Схема 4 .
Все комплексы выделены в индивидуальном состоянии и охарактеризованы элементным анализом, ИК-спектроскопией и магнитометрией. Для комплекса меди I выполнен монокристальный РСА. ИК-спектры комплексов I–IV отражают их состав. Все спектры характеризуются доминирующей по интенсивности полосой в районе 1450 см–1, относящейся к валентным колебаниям полуторной связи С–О, свойственной SQ-лигандам [20]. Нитроксильная группировка фрагмента TEMPO проявляется в ИК-спектрах в виде полосы, отвечающей валентным колебаниям N–O при 1364 см–1 [21]. ДМСО в комплексе I обнаруживается по широкой полосе 3490–3290 см–1, а также по полосам 1020, 950 см–1. ТHF в комплексе II определяется по интенсивной полосе 1090 см–1. Пиридин в III можно характеризовать полосами при 1600, 1082 и 702 см–1. В комплексе IV наблюдается широкая полоса переноса заряда лиганд–лиганд 4500 см–1, характерная для катехолат-о-семихиноновых комплексов кобальта [22], а также полосы 1601, 763 и 732 см–1, относящиeся к дипиридильному лиганду.
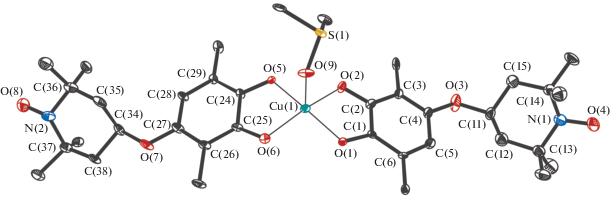
К сожалению, нам не удалось получить кристаллы комплексов II–IV, пригодныe для РСА. По данным РСА, соединение I представляет собой комплекс, в котором катион Cu2+ связан с двумя семихиноновыми лигандами и молекулой DМSО. В независимой области кристаллической ячейки находится одна молекула комплекса и три сольватных молекулы DМSО. Координационный полиэдр двухвалентной меди в комплексе I (рис. 1) – искаженная тетрагональная пирамида, в основании которой лежат атомы кислорода SQ-лигандов, в аксиальной вершине – атом кислорода молекулы DМSО. Каждая молекула DМSО, включая координированную на атоме меди, разупорядочена по двум положениям. Длины связей Cu–O(SQ) лежат в узком интервале значений 1.926(7)–1.951(7) Å, расстояние Cu–O(DМSО) равно 2.237(7) Å. В семихиноновых лигандах наблюдается делокализация электронной плотности по OCCO-фрагменту: длины связей C–O и C–C 1.28(2)–1.31(2) и 1.46(2)–1.47(2) Å соответственно, свидетельствуют об анион-радикальной форме координации [23, 24]. Двугранный угол между плоскостями OCCO семихиноновых лигандов равен 29.5(6)°, углы O(SQ)CuO(DМSО) лежат в интервале 93.1(3)°–100.4(3)°.
Рис. 1.
Молекулярная структура комплекса I. Тепловые эллипсоиды приведены с 30%-ной вероятностью. Атомы водорода и метильные группы трет-бутильных заместителей не приведены для ясности.
Фрагмент TEMPO в семихиноновых лигандах находится в конформации кресла. Двугранные углы между средними плоскостями, проведенными через углеродное кольцо семихинонового фрагмента и гетероцикл фрагмента TEMPO, равны 61.3(4)° и 47.6(4)°. Длины связей O(3)–C(SQ) и O(7)–C(SQ) значительно короче (1.35(2)–1.37(2) Å), чем O(3)–C(TEMPO) и O(7)–C(TE-MPO) (1.45(2)–1.47(2) Å).
В упаковке кристалла I есть множественные контакты O···H и H···H преимущественно между молекулой комплекса и молекулами DМSО. Расстояния O···H и H···H лежат в интервалах значений 2.46(2)–2.64(2) и 2.18(2)–2.40(2) Å соответственно.
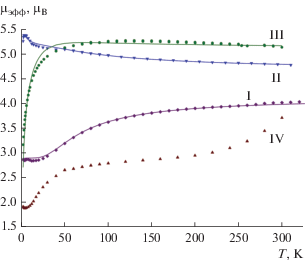
Температурные зависимости магнитного момента комплексов I–IV (pис. 2) аналогичны таковой для описанного ранее бис-семихинонового комплекса Cu(3,6-DBSQ)2 (3,6-DBSQ = 3,6-ди-трет-бутил-о-бензосемихинон) [25], магнитные свойства которого определяются балансом ферромагнитного (металл–лиганд) и антиферромагнитного (лиганд–лиганд) каналов обменных взаимодействий. Значение магнитного момента комплекса I при 300 K составляет 4.03 µB и при понижении температуры уменьшается, выходя на плато ~2.87 µB ниже 30 K. Высокотемпературное значение близко к теоретической величине 3.93 µB для пяти невзаимодействующих парамагнитных центров со спинами S = 1/2 – двух нитроксилов (gR = 2), двух семихиноновых лигандов (gSQ = 2) и одного Cu2+ (gCu = 2.15). Уменьшение при понижении температуры указывает на наличие сильных обменных взаимодействий антиферромагнитного характера. Для анализа зависимости µэфф(T) использовали модель тримера (H = –2JCu-SQ(SSQ1SCu + + SCuSSQ2) – JSQ-SQSSQ1SSQ2) с учетом парамагнитного вклада от спинов нитроксилов согласно закону Кюри. Оптимальные значения параметров gCu, JCu‑-SQ, JSQ-SQ и C составляют 2.31, 336, –212 cм–1 и 0.542 K cм3/моль и сравнимы с соответствующими значениями ранее описанного комплекса Cu(3,6-DBSQ)2 [25]. Значение постоянной Кюри C немного ниже теоретической чисто спиновой величины 0.75 K cм3/моль для двух невзаимодействующих нитроксилов.
Магнитное поведение комплексов II и III характерно для других известных комплексов никеля с ТHF и пиридином. Общий вид кривых µэфф–Т комплексов II и III (рис. 2) схож с описанными в литературе цис-(THF)2Ni(3,6-DBSQ)2 [26] и транс-(Py)2Ni(3,6-DBSQ)2 [27] соответственно. Значения µэфф комплексов II и III при комнатной температуре составляют 4.78 и 5.13 µB соответственно. Оба значения превышают чисто спиновое значение 4.47 µB, вычисленное для системы невзаимодействующих спинов Ni(II) высокоспиновый, d8S = 1; 2 SQS = 1/2; 2 TEMPOS = 1/2, что свидетельствует о преобладании ферромагнитных обменных взаимодействий. С понижением температуры магнитный момент растет, достигая максимума 5.37 µB при 5 К для комплекса II, и 5.25 µB в интервале 100–180 К для III. Дальнейшее снижение температуры приводит к резкому падению магнитного момента для II и плавному для III до 5.25 и 3.16 µB (2 К) соответственно. Такое различие в поведении отражает разное соотношение энергий ферро- и антиферромагнитных взаимодействий в молекулах комплексов. Аппроксимация дает следующие величины:
Рис. 2.
Температурные зависимости магнитных моментов комплексов I–IV (сплошные линии – аппроксимированные кривые).
(THF)2Ni(SQ)2: JNi-SQ = 18.8 см–1; JSQ-SQ = –16.9 см–1; gNi = 2.2 (фиксир.); gSQ = 2.00 (фиксир.); zJ' = = ‒0.01 см–1.
(Py)2Ni(SQ)2: JNi-SQ = 261 см–1; JSQ-SQ = –233 см–1; gNi = 2.2 (фиксир.); gSQ = 2.00 (фиксир.); zJ' = = –0.44 см–1.
Комплекс IV обнаруживает еще более сложное магнитное поведение. Комплекс IV аналогичен по составу редокс-изомерному соединению (Bipy)Co(3,6-DBSQ)2 [28–30], для которого Ткрит = 300 К.
В интервале 50–200 К магнитный момент IV меняется мало и составляет 2.64–2.94 µB. Это значение близко к теоретическому, рассчитанному для трех невзаимодействующих наспаренных электронов (3.0 µB), что соответствует системе спинов Co(III) низкоспиновый, d6S = 0; 1 SQS = 1/2; 2 TEMPOS = 1/2, т.е. низкотемпературному редокс-изомеру. Нагревание приводит к росту магнитного момента до 3.7 µB при 300 К. При охлаждении ниже 50 К магнитный момент падает до 1.87 µB при 5 К. Таким образом, при охлаждении антиферромагнитный обмен приводит к тому, что остается единственный неспаренный электрон, вероятнее всего, на о-семихиноновом фрагменте, участие которого в межмолекулярных взаимодействиях маловероятно. Нагревание выше 200 К ведет к сдвигу равновесия редокс-изомерии к высокоспиновому изомеру Co(II) высокоспиновый d7S = 3/2; 2 SQS = 1/2; 2 TEMPOS = 1/2. Очевидно, что при 300 К редокс-изомерное превращение далеко от завершения.
Спектр ЭПР комплекса I в порошке представляет собой одиночную линию без структуры (gi = = 2.0064, ширина линии ~14 Э), ширина и интенсивность которой существенно не изменяются с температурой. Комплексы II и III в порошке спектров ЭПР не имеют, что неудивительно для высокоспиновых комплексов никеля.
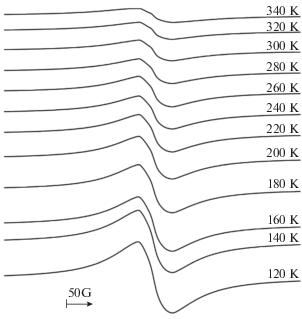
Спектр порошкообразного образца комплекса IV в диапазоне 120–340 К представляет собой широкий (ширина линии ~50 Э) сигнал с gi ≈ 2.0045 со слабо разрешенной сверхтонкой структурой (рис. 3). Интенсивность сигнала уменьшается с ростом температуры без изменения ширины линии.
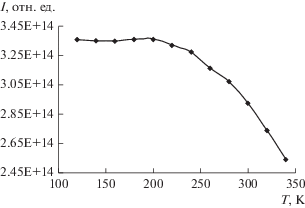
Однако зависимость IT (I = двойная интегральная интенсивность) от температуры (T) (рис. 4) свидетельствует о том, что количество парамагнитных частиц в образце, дающих сигнал ЭПР, в интервале 120–200 К остается приблизительно постоянным. Наблюдающееся резкое уменьшение интенсивности выше 220 К можно объяснить редокс-изомерным превращением, приводящим к образованию высокоспиновых частиц, не имеющих сигнала ЭПР.
Рис. 4.
Зависимость двойной интегральной интенсивности спектра ЭПР комплекса IV в порошке от температуры.
В растворе спектры ЭПР всех комплексов представлены спектром нитроксильного радикала.
Таким образом, восстановление 4-TEMPO-окси-3,6-ди-трет-бутил-о-бензохинона металлической медью, Ni(CO)4 и Co2(CO)8 приводит к образованию соответствующих мультиспиновых металлокомплексов, содержащих в своем составе бирадикальные гетероспиновые лиганды. Анализ молекулярного строения и магнитных свойств новых комплексов свидетельствуют о наличии магнитоструктурных корреляций, свойственных их аналогам, не имеющим нитроксильного заместителя в о-семихиноновом лиганде. Участия нитроксильных радикальных центров в межмолекулярной координации не обнаружено.
Авторы заявляют, что у них нет конфликта интересов.
Список литературы
Eaton S.S. // Coord. Chem. Rev. 1978. V. 26. P. 20.
Eaton S.S., Eaton G.R. // Coord. Chem. Rev. 1988. V. 83. P. 29.
Artemґev A.V., Vysotskaya O.V., Oparina L.A. et al. // Polyhedron. 2016. V. 119. P. 293.
Shultz D.A., Bodnar S.H., Vostrikova K.E. et al. // Inorg. Chem. 2000. V. 39. P. 6091.
Depperman E., Bodnar S.H., Vostrikova K.E. et al. // J. Am. Chem. Soc. 2001. V. 123. P. 3133.
Shultz D., Vostrikova K., Bodnar S. et al. // J. Am. Chem. Soc. 2003. V. 125. P. 1607.
Kirk M.L., Shultz D.A., Depperman E.C. // Polyhedron. 2005. V. 24. P. 2880.
Shultz D.A., Kumar R.K., Bin-Salamon S., Kirk M.L. // Polyhedron. 2005. V. 24. P. 2876.
Stasiw D.E., Zhang J., Wang G., Dangi R. et al. // J. Am. Chem. Soc. 2015. V. 137. P. 9222.
Третьяков Е.В., Толстиков С.Е., Романенко Г.В. и др. // Изв. АН. Сер. хим. 2011. С. 2280.
Егорова Е.Н., Дружков Н.О., Кожанов К.А. и др. // Изв. АН. Сер. хим. 2017. С. 1629.
Dickman M.H., Doedens R.J. // Inorg. Chem. 1982. V. 21. P. 682.
Jaitner P., Huber W., Huitner G., Scheidsteger O. // J. Organometal. Chem. 1983. V. 259. P. C1.
Jaitner P., Huber W., Gieren A. et al. // J. Organometal. Chem. 1986. V. 311. P. 379.
Isrow D., Captain B. // Inorg. Chem. 2011. V. 50. P. 5864.
Armarego W.L.F., Chai C.L.L. Purification of Laboratory Chemicals. Oxford: Elsevier, 2009. 752 p.
APEX3. Version 2016-9. Madison (WI, USA): Bruker AXS Inc., 2016.
TWINABS. Version 2012/1. Madison (WI, USA): Bruker AXS Inc., 2012.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3.
Bubnov M.P. et al. // Z. Anorg. Allg. Chem. 2014. P. 2177.
Kasumov V.T., Uçar I., Bulut A., Yerli Y. // Solid State Sci. 2011. V. 13. P. 1852.
Pierpont C.G., Kelly J.K. Coordination Chemistry of o-Semiquinones. PATAI’S Chemistry of Functional Groups. John Wiley & Sons, Ltd., 2013. P. 13.
Pierpont C.G., Buchanan R.M. // Coord. Chem. Rev. 1981. V. 38. P. 45.
Brown S.N. // Inorg. Chem. 2012. V. 51. P. 1251.
Ovcharenko V.I., Gorelik E.V., Fokin S.V. et al. // J. Am. Chem. Soc. 2007. V. 129. P. 10512.
Piskunov A.V., Fukin G.K., Kurskii Yu.A. et al. // Inorg. Chem. Commun. 2005. V. 8. P. 339.
Bubnov M., Cherkasova A., Teplova I. et al. // Polyhedron. 2016. V. 119. P. 317.
Абакумов Г.А., Черкасов В.К., Бубнов М.П. и др. // Докл. АН СССР. 1993. Т. 330. С. 332.
Lebedev B.V., Smirnova N.N., Abakumov G.A. et al. // J. Chem. Thermodyn. 2002. V. 34. P. 2093.
Bubnov M.P., Skorodumova N.A., Arapova A.V. et al. // Inorg. Chem. 2015. V. 54. P. 7767.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия