Координационная химия, 2020, T. 46, № 8, стр. 451-458
Синтез, строение и магнитные свойства гетероспиновых полимеров MI[MII(Hfac)L2]
О. В. Кузнецова 1, *, Г. В. Романенко 1, А. С. Богомяков 1, В. И. Овчаренко 1
1 Международный томографический центр СО РАН
Новосибирск, Россия
* E-mail: olya@tomo.nsc.ru
Поступила в редакцию 10.01.2020
После доработки 06.02.2020
Принята к публикации 17.02.2020
Аннотация
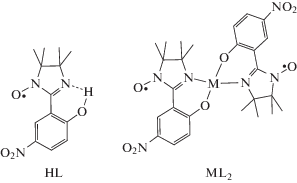
Синтезированы гетероспиновые полимерные комплексы на основе гексафторацетилацетонатов Ni(II) и Co(II) и депротонированного иминонитроксильного радикала 2-(2-гидрокси-5-нитрофенил)-4,4,5,5-тетраметил-4,5-дигидро-1H-имидазол-1-оксила (HL), в которых анионы [MII(Hfac)L2]– (Hfac = = 1,1,1,5,5,5-гексафтор-2,4-пентандионат-ион) связаны в 1D–3D полимеры (I–V) катионами Na+, K+, Rb+ или Cs+. РСА MI[MII(Hac)L2] ∙ n(Me2CO) (n = 0–2.5) показал, что мотив полимера определяется катионом щелочного металла (CIF files CCDC № 1974139–1974143 для I–V). По данным магнитных измерений установлено, что в твердых фазах соединений доминируют ферромагнитные взаимодействия в обменных кластерах {LML}, обусловливающие возрастание эффективного магнитного момента при понижении температуры.
Недавно было показано, что иминонитроксильный радикал 2-(2-гидрокси-5-нитрофенил)-4,4,5,5-тетраметил-4,5-дигидро-1H-имидазол-1-оксил (HL) при взаимодействии с пивалатами переходных металлов способен инициировать redox-процессы, сопровождающиеся частичной восстановительной трансформацией исходного иминонитроксила и последующим образованием координационных соединений, содержащих одновременно как исходный радикал, так и продукт его восстановления – соответствующий нитрон [1, 2]. Обращало на себя внимание существование внутри образующихся моно- или полиядерных молекул ферромагнитных обменных кластеров [2, 3], что обусловливало интерес к разработке синтетических подходов, позволяющих связать ферромагнитные обменные кластеры в структуры высокой размерности, в которых потенциально возможно возникновение кооперативного упорядочения спинов. Следует отметить, что ферромагнитный обмен реализуется и в бис-хелатных молекулярных матрицах со спин-меченым шиффовым основанием [ML2] (M = Ni, Cu, Co), не содержащих дополнительных органических лигандов [4, 5]. Однако гомолептические [ML2], во-первых, малорастворимы в органических средах, во-вторых, обладают малой акцепторной способностью, необходимой для разработки синтеза структур высокой размерности. По этой причине для повышения акцепторной способности металла в [ML2] необходимо либо вводить соответствующие заместители в структуру L, либо дополнять координационную сферу металла акцепторными лигандами. Следует отметить, что в литературе имеются отдельные примеры полимерных комплексов гексафторацетилацетонатов 3d-металлов с нитроксильными радикалами, большинство из них проявляют свойства магнетиков, но они не содержат s-элементов [6–18]. Мы предприняли попытку изучения продуктов взаимодействия сильной акцепторной металлосодержащей матрицы {M(Hfac)2} с HL. Проведенное исследование показало, что моноядерные [M(H2O)2(Hfac)2], где M = Ni или Co, реагируют с HL в органических средах только в присутствии щелочи. При этом в твердую фазу выделяются полимерные гетерометаллические разнолигандные комплексы, размерность которых, как оказалось, зависит от введенного в реакцию иона щелочного металла (Na, K, Rb, Cs). Эти комплексы получены в виде монокристаллов и исследованы их структуры.
В настоящей работе исследовано влияние природы щелочного металла на строение образующегося полимера. Поскольку все выделенные полимерные гетерометаллические комплексы содержат ферромагнитные обменные кластеры, высказано предположение, каким образом можно использовать данные полимеры для получения твердых фаз с кооперативным магнитным упорядочением.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали иминонитроксильный радикал 2-(2-гидрокси-5-нитрофенил)-4,4,5,5-тетраметил-4,5-дигидро-1H-имидазол-1-оксил (HL), синтезированный по методике [4], KOH (“х. ч.”), NaOH (“ч. д. а.”), RbOH (50%-ный раствор в H2O, Sigma-Aldrich), CsOH (50%-ный раствор в H2O, Sigma-Aldrich), ацетон (“ос. ч.”), гептан (эталонный) и метанол (очищенный методом перегонки перед использованием). [Co(H2O)2(Нfac)2] и [Ni(H2O)2(Нfac)2] получали взаимодействием [Co(H2O)4(OAc)2] и [Ni(H2O)4(OAc)2] c 1,1,1,5,5,5-гексафтор-2,4-пентандионом (Hfac) и KOH в воде c последующей перекристаллизацией продукта из EtOAc (“ос. ч.”).
Синтез комплекса K[Ni(Нfac)L2] · Me2CO (I). При комнатной температуре к раствору 0.05 г (0.1 ммоль) [Ni(H2O)2(Нfac)2] в 1 мл ацетона добавляли раствор 0.055 г (0.2 ммоль) HL в 3 мл ацетона, затем раствор 0.011 г (0.2 ммоль) KOH в 0.5 мл MeOH. При этом реакционная смесь приобретала темно-коричневую окраску. Через 2 сут выпадали коричневые призматические кристаллы I, которые отфильтровывали и промывали ацетоном. Выход 0.08 г (45%).
| Найдено, %: | C 44.4; | H 3.9; | N 9.2; | F 12.6. |
| Для C34H37N6O11F6KNi | ||||
| вычислено, %: | C 44.5; | H 4.1; | N 9.2; | F 12.4. |
По аналогичной методике с использованием NaOH, RbOH или CsOH получали, соответственно, Na[Ni(Нfac)L2] · Me2CO (II), Rb[Ni(Нfac)L2] · · 2.5Me2CO (III) и Cs[Ni(Нfac)L2] (IV).
II: красно-коричневые кристаллы в форме призм (выход 60%).
| Найдено, %: | C 45.4; | H 4.4; | N 9.5; | F 12.7. |
| Для C34H37N6O11F6NaNi | ||||
| вычислено, %: | C 45.3; | H 4.1; | N 9.3; | F 12.6. |
III: тонкие красно-коричневые призматические кристаллы (выход 60%).
| Найдено, %: | C 42.6; | H 3.7; | N 8.8; | F 11.5. |
| Для C34H37N6O11F6RbNi (частично десольватированного) | ||||
| вычислено, %: | C 42.4; | H 3.9; | N 8.7; | F 11.8. |
IV: призматические кристаллы коричневого цвета (выход 82%).
| Найдено, %: | C 39.2; | H 3.2; | N 8.7; | F 12.3. |
| Для C31H31N6O10F6СsNi | ||||
| вычислено, %: | C 39.1; | H 3.3; | N 8.8; | F 11.9. |
Синтез K[Co(Нfac)L2] · 2.5Me2CO (V). При комнатной температуре к раствору 0.05 г (0.1 ммоль) [Co(H2O)2(Нfac)2] в 1 мл ацетона добавляли раствор 0.055 г (0.2 ммоль) HL в 3 мл ацетона, затем раствор 0.011 г (0.2 ммоль) KOH в 0.5 мл MeOH. В результате реакционная смесь окрашивалась в черный цвет. Через 2 сут выпадали сростки кристаллов, последующая перекристаллизация которых из смеси ацетон–гептан (5 : 2) приводила к образованию темно-коричневых призматических кристаллов V, которые отфильтровывали и промывали гептаном. Выход 0.049 г (50%).
| Найдено, %: | C 43.8; | H 3.8; | N 9.1; | F 12.9. |
| Для C32.5H34N6O10.5F6KCo (частично десольватированного) | ||||
| вычислено, %: | C 43.9; | H 3.9; | N 9.5; | F 12.8. |
РСА. Массивы отражений от монокристаллов получены на дифрактометрах фирмы Bruker AXS‑Smart Apex II и Apex Duo (поглощение учитывалось по программе SADABS, версия 2.10) [19]. Структуры решены прямыми методами, уточнены полноматричным МНК в анизотропном приближении для всех неводородных атомов. Положения атомов Н рассчитаны геометрически и уточнены в модели “наездника”. Все расчеты по решению и уточнению структур проведены по комплексу программ SHELX. Кристаллографические характеристики соединений, детали экспериментов приведены в табл. 1, значения избранных длин связей и межатомных расстояний – в табл. 2.
Таблица 1.
Кристаллографические данные и параметры уточнения структур I–V
| Параметр | Значение | ||||
|---|---|---|---|---|---|
| I | II | III | IV | V | |
| Брутто-формула | C34H37N6O11F6KNi | C34H37N6O11F6NaNi | C38.50H46N6O12.50F6RbNi | C31H31N6O10F6CsNi | C38.50H46N6O12.50F6KCo |
| М | 917.50 | 901.39 | 1050.99 | 953.24 | 1004.84 |
| T, K | 240 | 295 | 240 | 296 | 240 |
| Сингония; Z | P21/c; 8 | P212121; 8 | P21/c; 8 | P1; 4 | P21/c; 8 |
| a, Å b, Å c, Å α, град β, град γ, град |
19.7547(9) 24.7678(12) 19.8038(10) 90 117.461(3) 90 |
11.0707(13) 21.790(2) 34.756(3) 90 90 90 |
20.196(3) 27.815(5) 18.824(3) 90 115.913(7) 90 |
11.7373(8) 17.2803(12) 20.1143(14) 98.870(4) 101.264(3) 102.339(3) |
20.0833(12) 27.830(2) 18.9399(14) 90 116.796(4) 90 |
| V, Å3 | 8597.8(7) | 8384.3(15) | 9511(3) | 3826.0(5) | 9449.2(12) |
| ρ(выч.), г cм–3 | 1.418 | 1.428 | 1.468 | 1.655 | 1.413 |
| θ Range, deg | 67.234 | 28.278 | 68.229 | 28.173 | 67.768 |
| Интервалы индексов hkl min/max | –22 ≤ h ≤ 23, –29 ≤ k ≤ 29, –23 ≤ l ≤ 22 |
–14 ≤ h ≤ 11, –27 ≤ k ≤ 26, –40 ≤ l ≤ 45 |
–24 ≤ h ≤ 24, –33 ≤ k ≤ 33, –22 ≤ l ≤ 22 |
–15 ≤ h ≤ 15, –22 ≤ k ≤ 22, –26 ≤ l ≤ 26 |
–23 ≤ h ≤ 23, –33 ≤ k ≤ 33, –21 ≤ l ≤ 22 |
| Число измеренных/независимых отражений | 104 203/15 167 | 45 894/19 330 | 131 996/16 581 | 64 338/18 624 | 133 941/16 914 |
| Rint | 0.1694 | 0.0711 | 0.0586 | 0.0616 | 0.1012 |
| Число отражений с I > 2σ(I) | 6328 | 9282 | 12 172 | 10 922 | 9748 |
| Число параметров | 1063 | 1152 | 1273 | 1148 | 1345 |
| GOOF | 0.865 | 0.805 | 1.127 | 0.851 | 1.012 |
| R1/wR2 (I > 2σ(I)) | 0.0601/0.1449 | 0.0456/0.0773 | 0.0755/0.1642 | 0.0343/0.0663 | 0.0823/0.2233 |
| R1/wR2 (все данные) | 0.1443/0.1850 | 0.1188/0.0919 | 0.1013/0.1807 | 0.0739/0.0760 | 0.1346/0.2774 |
| ∆ρmax/∆ρmin, е/Å3 | 0.423/–0.607 | 0.277/–0.292 | 0.759/–0.693 | 0.645/–0.431 | 0.680/–0.532 |
Таблица 2.
Значения избранных длин связей и межатомных расстояний для I–V
| Cвязь | d, Å | ||||
|---|---|---|---|---|---|
| I | II | III | IV | V | |
| M(II)–O | 2.009(3)–2.071(4) | 2.019(3)–2.075(3) | 2.009(3)–2.083(4) | 2.003(2)–2.070(2) | 2.022(4)–2.124(5) |
| M(II)–N | 2.101(3)–2.115(4) | 2.097(4)–2.120(4) | 2.082(4)–2.111(4) | 2.115(2)–2.128(2) | 2.127(4)–2.150(4) |
| M(I)–O | 2.679(3)–3.069(4) | 2.287(5)–2.813(6) | 2.805(3)–3.179(5) | 3.002(2)–3.362(2) | 2.692(4)–3.268(5) |
| Cs–F | 3.341(15)–3.443(14) | ||||
| N–O | 1.258(5)–1.267(5) | 1.265(6)–1.272(6) | 1.259(6)–1.269(7) | 1.262(3)–1.270(4) | 1.255(6)–1.273(7) |
| M(II)···M(I) | 3.684(2), 3.700(1) | 3.331(2), 3.353(2) | 3.857(1), 3.871(1) | 4.0127(6), 4.0751(6) | 3.703(2), 3.708(2) |
Полная информация по структурам I–V содержится в Кембриджском банке структурных данных (CCDC № 1974139–1974143; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk/data_request/cif).
Магнитную восприимчивость (χ) поликристаллических образцов измеряли на SQUID-магнетометре MPMSXL (Quantum Design) в интервале 2−310 K в магнитном поле 5 кЭ. Парамагнитные составляющие χ определяли с учетом диамагнитного вклада, оцененного из констант Паскаля. Эффективный магнитный момент (μэфф) вычисляли по формуле μэфф = [3kχT/(NAμB2)]1/2, где NA, μB и k – число Авогадро, магнетон Бора и постоянная Больцмана соответственно. Анализ экспериментальной зависимости магнитной восприимчивости от температуры проводили с использованием изотропного спин-гамильтониана вида H = –2∑JijSiSj.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
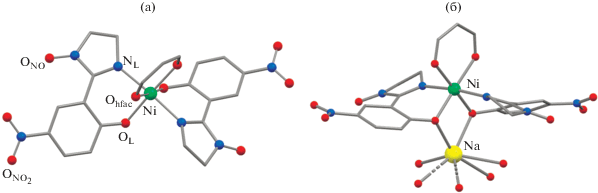
Проведенные исследования показали, что взаимодействие [Ni(H2O)2(Нfac)2] с HL в смеси ацетон–метанол происходит только в присутствии KOH. При этом кристаллизуется комплекс I. В аналогичных условиях с использованием NaOH, RbOH, CsOH были получены II, III и IV соответственно, содержащие фрагменты {Ni(Нfac)L2} (рис. 1). В твердой фазе эти соединения объединены катионами щелочных металлов в полимерные структуры. Кроме того, в кристаллической структуре могут присутствовать молекулы ацетона, связанные с катионом щелочного металла. Окружение атома Ni во всех соединениях – незначительно искаженный октаэдр, образованный двумя OНfac и донорными атомами OL и NL, с расстояниями Ni–O 2.009(3)–2.083(4) Å и Ni–N 2.082(4)–2.128(4) Å (табл. 2). Длины связей N–O в нитроксильной группе L типичны для иминонитроксилов: 1.255(6)–1.273(7) Å [20].
Рис. 1.
Строение координационного аниона [Ni(Нfac)L2]– (а) и фрагмент структуры II (б). Здесь и далее: атомы N –  и O –
и O –  ; CF3, CH3-группы и атомы H не показаны; пунктиром выделены связи, участвующие в образовании
полимерной структуры.
; CF3, CH3-группы и атомы H не показаны; пунктиром выделены связи, участвующие в образовании
полимерной структуры.
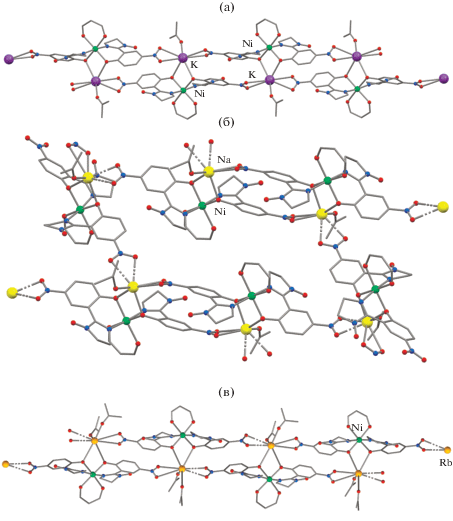
Окружение атомов щелочных металлов различно (рис. 2). В соединении I для атома K – это семивершинник, образованный четырьмя атомами ${{{\text{O}}}_{{{\text{N}}{{{\text{O}}}_{2}}}}}$ от нитрогрупп двух L, двумя мостиковыми OL от двух других L и атомом O молекулы ацетона (K–O 2.679(3)–3.069(4) Å). С учетом всех этих связей в структуре формируются полимерные цепи (рис. 2а).
Соединение II имеет такой же состав, как и I, с аналогичным окружением атомов щелочного металла (Na–O 2.287(5)–3.032(5) Å), но при этом в структуре формируются не цепи, а слои (рис. 2б).
Полимерные цепи образуют и структуру III (рис. 2в). В ней окружение атомов Rb – восьмивершинник из атомов кислорода ${{{\text{O}}}_{{{\text{N}}{{{\text{O}}}_{2}}}}},$ OL и двух молекул ацетона (Rb–O 2.805(3)–3.179(5) Å). Кроме того, между цепочками располагаются сольватные молекулы ацетона. Такое же строение и состав имеет V.
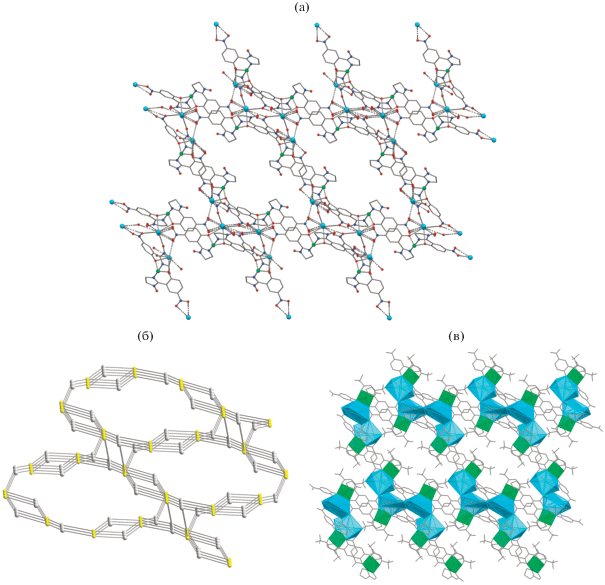
В окружение атома Cs в IV входят атомы O (3.002(2)–3.362(2) Å) и F (3.341(15)–3.443(14) Å), образуя неправильный девятивершинник (рис. 3в). С учетом всех этих контактов структуру можно рассматривать как каркас (рис. 3).
Рис. 3.
(а) Фрагмент каркаса в IV (Нfac-лиганды не показаны, Cs –  , Ni –
, Ni –  ; (б) схематическое представление каркаса: центры парамагнитных лигандов –
; (б) схематическое представление каркаса: центры парамагнитных лигандов – 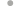 и биядерных фрагментов {Ni···Cs} –
и биядерных фрагментов {Ni···Cs} –  ; (в) изображение каркаса в полиэдрическом представлении для атомов металла.
; (в) изображение каркаса в полиэдрическом представлении для атомов металла.
Исследование магнитных свойств полученных разнометально-разнолигандных комплексов показало наличие ферромагнитных обменных взаимодействий между спинами парамагнитных центров. Значения µэфф при 300 K несколько выше теоретических чисто спиновых (3.74 и 4.58 µB для комплексов Ni(II) и Co(II) соответственно) и возрастают при понижении температуры (рис. 4). Этот результат находится в согласии с данными квантово-химических расчетов, показавших, что координация иминонитроксила посредством атома N парамагнитного фрагмента благоприятна для реализации обменных взаимодействий ферромагнитного характера [21–33]. Анализ экспериментальных зависимостей µэфф(T) для исследованных соединений проводили с использованием модели обменно-связанного тримера (спин-Гамильтониан H = –2J(SL1SM+ SMSL2)) для фрагментов {M(Нfac)L2}. Уменьшение значения µэфф при низких температурах обусловлено более слабыми межкластерными обменными взаимодействиями антиферромагнитного характера и/или расщеплением в нулевом поле, которые учитывали в приближении молекулярного поля. Оптимальные значения g-фактора иона металла (gM) и параметров обменного взаимодействия (J и zJ'), полученные из анализа экспериментальных зависимостей µэфф(T), приведены в табл. 3, значение g-фактора нитроксилов фиксировали равным 2.
Рис. 4.
Экспериментальные зависимости µэфф(T) для I, II, III, IV и V. Сплошные линии – теоретические кривые.
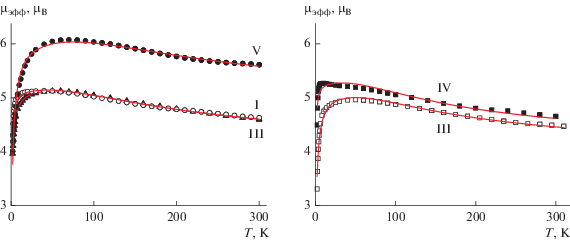
Таблица 3.
Оптимальные значения g-фактора иона металла (gM) и параметров обменного взаимодействия (J и zJ'), полученные из анализа экспериментальных зависимостей µэфф(T)
| Соединение | gM | J, см–1 | zJ ', K |
|---|---|---|---|
| I | 2.24 | 72 | –0.17 |
| II | 2.26 | 70 | –0.34 |
| III | 2.18 | 58 | –0.51 |
| IV | 2.32 | 56 | –0.10 |
| V | 2.17 | 60 | –0.54 |
Таким образом, проведенное исследование показало, что гексафторацетонаты Ni(II) и Co(II) реагируют со спин-меченым основанием Шиффа HL в органических средах в присутствии щелочи. Реакция приводит к кристаллизации из раствора разнолигандных гетерометаллических полимерных комплексов. Тип образующейся полимерной струкутры определяется ионом щелочного металла – слои в случае Na, цепи для K, Rb и каркас в случае Cs. В твердой фазе всех соединений ферромагнитные обменные взаимодействия между парамагнитными центрами локализованы главным образом в обменных кластерах {LML}. Поскольку значения ферромагнитного обмена достаточно велики (табл. 3), представляется целесообразным заменить в составе выделенных соединений щелочные металлы на парамагнитные ионы переходных металлов. Такое исследование мы планируем провести в будущем: в случае, если это удастся реализовать, можно надеяться на получение новой группы гетероспиновых комплексов, способных к кооперативному магнитному упорядочению.
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
Ovcharenko V., Kuznetsova O., Fursova E. et al. // Inorg. Chem. 2014. V. 53. P. 10033.
Кузнецова О.В., Фурсова Е.Ю., Романенко Г.В. и др. // Изв. АН. Сер. хим. 2016. № 5. С. 1167 (Kuznetsova O.V., Fursova E.Yu., Romanenko G.V. et al. // Russ. Chem. Bull. 2016. V. 65. № 5. P. 1167).
Ovcharenko V., Kuznetsova O., Fursova E. et al. // Crystals. 2015. V. 5. P. 634.
Tretyakov E., Eltsov I., Fokin S. et al. // Polyhedron. 2003. V. 22. P. 2499.
Ельцов И.В. Дис. … канд. хим. наук. Новосибирск: ИНХ СО РАН, 2004.
Caneschi A., Gatteschi D., Laugier J. et al. // Inorg. Chem. 1988. V. 27. P. 1553.
Luneau D., Rey P., Laugier J. et al. // Inorg. Chem. 1992. V. 31. P. 3578.
Yoshitomo O., Takashi N., TakayukiI. // Chem. Lett. 2009. V. 38. № 7. P. 740.
Yoshitomo O., Norio I., Takashi N., Takayuki I. // Bull. Chem. Soc. Jpn. 2010. V. 83. № 6. P. 716.
Cassaro R.A.A., Reis S.G., Araujo T.S. et al. // Inorg. Chem. 2015. V. 54. P. 9381.
Ishii N., Okamura Y., Chiba S. et al. // Am. Chem. Soc. 2008. V. 130. P. 24.
Wang J., Li J.-N., Zhang S.-L. et al. // Chem. Commun. 2016. V. 52. P. 5033.
Ishii N., Ishida T., Nogami T. // Inorg. Chem. 2006. V. 45. P. 3837.
Caneschi A., Gatteschi D., Lalioti N. et al. // Angew. Chem. Int. Ed. 2001. V. 40. P. 1760.
Caneschi A., Gatteschi D., Renard J.P. et al. // Inorg. Chem. 1989. V. 28. P. 2940.
Caneschi A., Gatteschi D., Lalioti N. et al. // Dalton Trans. 2000. P. 3907.
Vaz M.G.F., Allão R.A., Akpinar H. et al. // Inorg. Chem. 2012. V. 51. P. 3138.
Catala L., Wurst K., Amabilino D.B., Veciana J. // J. Mater. Chem. 2006. V. 16. P. 2736.
Sheldrick G.M. SADABAS. Program for Empirical X-ray Absorption Correction. Bruker AXS, 1990–2007.
Третьяков Е.В., Овчаренко В.И. // Успехи химии. 2009. Т. 78. № 11. С. 1051 (Tretyakov E.V., Ovcharenko V.I. // Russ. Chem. Rev. 2009. V. 78. № 11. P. 971).
Малиновская С.А., Счастнев П.В., Мусин Р.Н., Икорский В.Н. // Журн. структур. химии. 1993. Т. 34. № 3. С. 70 (Malinovskaya S.A., Schastnev P.V., Musin R.N., Ikorsky V.N. // J. Struct. Chem. 1993. V. 34. P. 398).
Musin R.N., Schastnev P.V., Malinovskaya S.A. // Inorg. Chem. 1992. V. 31. P. 4118.
Овчаренко И.В., Шведенков Ю.Г., Мусин Р.Н., Икорский В.Н. // Журн. структур. химии. 1999. № 1. Т. 40. № 1. С. 36 (Ovcharenko I.V., Shvedenkov Yu.G., Musin R.N., Ikorskii V.N. // J. Struct. Chem. 1999. V. 40. № 1. P. 29).
Cogne A., Laugier J., Dominique L., Rey P. // Inorg. Chem. 2000. V. 39. P. 5510.
Marvilliers A., Pei Y., Boquera J.C. et al. // Chem. Commun. 1999. P. 1951.
Зуева Е.М., Третьяков Е.В., Фокин С.В. и др. // Изв. АН. Сер. хим. 2016. Т. 3. С. 666 (Zueva E.M., Tretyakov E.V., Fokin S.V. et al. // Russ. Chem. Bull. 2016. V. 65. P. 666).
Oshio H., Yamamoto M., Ito T. et al. // Inorg. Chem. 2001. V. 40. № 22. P. 5518.
Luneau D., Rey P., Laugier J. et al. // Inorg. Chem. 1992. V. 31. № 17. P. 3578.
Yamamoto Y., Suzukia T., Kaizaki S. // Dalton Trans. 2001. P. 1566.
Li C., Zhang J., Li L. // Transition Met. Chem. 2015. V. 40. P. 631.
Ishida T., Adachi K., Kawata S. et al. // Polyhedron. 2007. V. 26. P. 2013.
Lanfranc de Panthou F., Luneau D., Musin R. et al. // Inorg. Chem. 1996. V. 35. P. 3484.
Петров П.А., Романенко Г.В., Шведенков Ю.Г. и др. // Изв. АН. Сер. хим. 2004. Т. 53. № 1. С. 98 (Petrov P.A., Romanenko G.V., Shvedenkov Yu.G. еt al. // Russ. Chem. Bull. 2004. V. 53. P. 99).
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия