Координационная химия, 2020, T. 46, № 8, стр. 497-512
Синтез и кристаллическое строение комплексов Cd(II) и Cd(II)–Eu(III) с анионами пентафторбензойной кислоты и N-донорными лигандами
М. А. Шмелев 1, *, Н. В. Гоголева 1, Г. Н. Кузнецова 1, М. А. Кискин 1, Ю. К. Воронина 1, И. А. Якушев 1, Т. М. Иванова 1, Ю. В. Нелюбина 2, А. А. Сидоров 1, И. Л. Еременко 1, 2
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
2 Институт элементоорганических соединений им. А.Н. Несмеянова РАН
Москва, Россия
* E-mail: shmelevma@yandex.ru
Поступила в редакцию 05.03.2020
После доработки 15.03.2020
Принята к публикации 22.03.2020
Аннотация
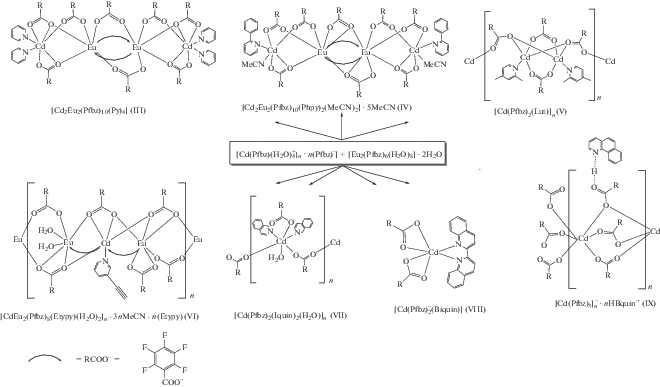
Взаимодействием пентафторбезоатов кадмия(II) [Cd(Pfbz)$\left( {{{{\text{H}}}_{{\text{2}}}}{\text{O}}} \right)_{{\text{4}}}^{ + }$}n · n(Pfbz)–] (I, HPfbz = = пентафторбензойная кислота), европия(III) [Eu2(Pfbz)6(H2O)8] ∙ 2H2O (II) и N-донорного лиганда (пиридин (Py), 2-фенилпиридин (Phpy), 3-этинилпиридин (Etypy)) получена серия новых Cd-‑Ln- комплексов с анионами Pfbz– и пиридином и его замещенными аналогами [Cd2Eu2(Pfbz)10(Py)4] (III), [Cd2Eu2(Pfbz)10(Phpy)2 (MeCN)2] · 5MeCN (IV), [CdEu2(Pfbz)8(Etypy)-(H2O)2]n ∙ 3nMeCN ∙ n(Etypy) (VI). В аналогичных реакциях I и II c 2,4-лутидином (Lut), изохинолином (Iquin), 2,2'-бихинолином (Biquin) и 7,8-бензохинолином (Bquin) основными продуктами кристаллизации из реакционных растворов были комплексы кадмия: [Cd(Pfbz)2(Lut)]n (V), [Cd(H2O)(Pfbz)2(Iquin)2]n (VII), [Cd(Рfbz)2(Biquin)] (VIII) и $[{\text{Cd}}{{({\text{Pfbz}})}_{{\text{3}}}}]_{n}^{--}$ ∙ n(HBquin)+ (IX) соответственно. Данные РСА (CIF files CCDC № 1987805 (I), 1987808 (III), 1987829 (IV), 1987817 (V), 1987822 (VI), 1987823 (VII), 1987824 (VIII), 1987826 (IX)) позволили продемонстрировать примеры образования новых необычных координационных полимеров.
Одно из главных отличий кадмия от 3d-металлов в карбоксилатных системах – выраженная склонность к формированию координационных полимеров из-за увеличения длин связей Сd–X (Х = любой атом координационного окружения кадмия) по сравнению с 3d-металлами. Например, ацетаты Ni(II), Co(II), Zn(II) кристаллизуются из водных растворов в виде моноядерных комплексов [M(OAc)2(H2O)4] (Zn [1], Co [2], Ni [3]) ацетат кадмия кристаллизуется в форме 1D-координационного полимера [Cd(OAc)2(Н2О)2]n [4]. Диаквадикарбоксилаты кадмия с более объемными заместителями имеют молекулярное строение [5–7], поскольку увеличение размеров углеводородного заместителя приводит к созданию стерических затруднений, препятствующих сближению моноядерных фрагментов на расстояния, при которых формируются полиядерные фрагменты. Соединения 3d-металлов, имеющие состав [M(O2CR)2L], где L – пиридин или его монодентатное производное, как правило, имеют биядерное строение (Co [8, 9], Zn [10, 11], Ni [12, 13], тогда как для кадмия известны ацетатные [14] и 3,5-дибромбензоатный [15] координационные полимеры аналогичного состава мономерного фрагмента.
Вероятно, формирование карбоксилатных координационных полимеров может наблюдаться и с другими анионами монокарбоновых кислот, если при этом не возникают стерические затруднения, способствующие формированию молекулярных, а не полимерных структур. Также благоприятным фактором для полимеризации является наличие каких-либо невалентных взаимодействий, способствующих сближению и достижению взаимной ориентации отдельных структурных фрагментов. Причиной этому могут быть водородные связи или ароматических стэкинг-фрагментов.
Рассмотренные примеры демонстрируют, что для преодоления стерических затруднений и формирования полимерных структур очень важна “геометрия” лигандов, в частности, играет роль присутствие заместителей малых размеров или их плоское строение, как в случае ароматических фрагментов.
Следует обратить внимание на известные системы органических соединений, в которых сочетаются перфторированные и нефторированные ароматические фрагменты [16–18]. Для таких систем типично параллельное расположение всех ароматических циклов и их сближение на расстояния до ~3.4–3.6 Å. Это хорошо иллюстрируется кристаллическими упаковками бензола и гексафторбензола, имеющими одинаковый “лестничный” мотив кристаллической упаковки, тогда как их сокристаллизат C6H6 · C6F6 имеет слоистую плотную упаковку [19]. Данный эффект подробно изучен для органических фторзамещенных и незамещенных ароматических молекул [20].
Недавно единственным известным пентафторбензоатным полимером кадмия было соединение [Cd(Рfbz)2(Вipy)(Н2О)]n (Вipy = 2,2'-дипиридил) [21]. Авторы связывают стабилизацию полимерной структуры комплекса c наличием в ней водородных связей, контактов С–H...F–C, а также стэкинг-взаимодействий. Важно обратить внимание на то, что в данном комплексе атомы кадмия одновременно координируют лиганды, содержащие незамещенные и перфторированные ароматические заместители. Факт образования координационного полимера при наличии в составе хелатирующего лиганда Вipy, по-видимому, свидетельствует в пользу того, что для пентафторбензоатных систем, как и в случае ацетатных, вероятно, будет наблюдаться тенденция к образованию координационных полимеров, в состав которых будут входить различные монодентатные, а, возможно, и хелатирующие производные пиридина.
Наши исследования не ограничены комплексами кадмия и в большей степени нацелены на получение Cd-Ln-гетерометаллических координационных соединений, привлекающих внимание нетривиальными фотолюминесцентными свойствами ионов лантанидов, в частности европия(III), эмиссия которого лежит в красной области видимого спектра [22]. Эти соединения могут быть использованы в качестве оптических усилителей, а также сенсорных материалов для люминесцентных пленок, а формирование внутримолекулярных π–π-взаимодействий может положительно сказываться на значениях квантовых выходов люминесценции [23]. Гетерометаллические соединения Cd(II) на сегодняшний день гораздо менее изучены. Они интересны тем, что координационные полимеры на их основе будут построены из трех- или четырехъядерных гетерометаллических фрагментов, типичных для молекулярных гетерометаллических систем [23].
Цель настоящей работы – синтез пентафторбензоатных комплексов кадмия и пиридина или его производных в качестве ароматического N-донорного лиганда для апробации возможности связывания фрагментов комплекса между собой в кристаллической решетке с образованием полимерных структур.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все операции, связанные с синтезом новых комплексов, выполняли на воздухе с использованием ацетонитрила (≥99.5%) и дистиллированной воды. Также в работе использовали следующие реагенты: Cd(NO3)2 · 4H2O (99+%, Acros organics), Eu(NO3)3 · 6H2O (99.99%, Ланхит), KOH (“х. ч.”, “Реахим”), пентафторбензойную кислоту (HРfbz, 99%, P&MInvest), пиридин (Рy, ROTIPURAN® ≥ ≥ 99.5%), 2-фенилпиридин (Рhpy, Sigma-Aldrich, 98%), 2,4-лутидин (Lut, Sigma-Aldrich, 99%), 3-этинилпиридин (Etypy, Sigma-Aldrich, 98%), изохинолин (Iquin, Sigma-Aldrich, 98%), 2,2'-бихинолин (Biquin, Sigma-Aldrich, 98%), 7,8-бензохинолин (Bquin, Sigma-Aldrich, 97%). ИК-спектры соединений регистрировали на ИК-спектрофотометре с Фурье-преобразованием Spectrum 65 (PerkinElmer) методом нарушенного полного внутреннего отражения (НПВО) в интервале частот 4000–400 см–1. Элементный анализ выполняли на CHNS-анализаторе EuroЕА 3000 (EuroVector).
Синтез [{Cd(Pfbz)$\left( {{{{\mathbf{H}}}_{{\mathbf{2}}}}{\mathbf{O}}} \right)_{{\mathbf{4}}}^{ + }$}n · n(Pfbz)–] (I). К свежеосажденному Cd(OH)2 (0.475 г, 3.242 ммоль), полученному при взаимодействии Cd(NO3)2 · 4H2O (1.000 г, 3.242 ммоль) и KOH (0.363 г, 6.484 ммоль) в 100 мл воды, добавляли 1.368 г (6.484 ммоль) HPfbz и перемешивали до полного растворения осадка Cd(OH)2 при 80°С в течение 4 ч. Реакционный раствор выдерживали при комнатной температуре и медленном испарении. Образовавшиеся через 6 сут бесцветные кристаллы, пригодные для РСА, отделяли от маточного раствора декантацией и сушили на воздухе. Выход I 1.494 г (86.3% в расчете на Cd(NO3)2 · 4H2O).
ИК-спектр (НПВО; ν, см–1): 3380 c, 1653 ср, 1706 сл, 1644 ср, 1563 ср, 1529 с,1473 с, 1394 с, 1370 с, 1365 с, 1300 ср, 1121 c, 985 с, 940 ср, 925 ср, 821 сл, 810 сл, 772 ср, 744 ср, 587 cp, 506 ср.
Синтез [Eu2(Pfbz)6(H2O)8] · 2H2O (II). К свежеосажденному Eu(OH)3 (0.603 г, 3.242 ммоль), полученному при взаимодействии Eu(NO3)3 · 6H2O (1.446 г, 3.242 ммоль) и KOH (0.545 г, 9.726 ммоль) в 100 мл воды, добавляли 2.052 г (9.726 ммоль) HPfbz и перемешивали до полного растворения осадка Eu(OH)3 при 80°С в течение 6 ч. Реакционный раствор выдерживали при комнатной температуре и медленном испарении. Образовавшиеся через 10 сут бесцветные кристаллы, пригодные для РСА, отделяли от маточного раствора декантацией и сушили на воздухе. Выход II 1.737 г (61.2% в расчете на Eu(NO3)3 · 6H2O).
ИК-спектр (НПВО; ν, см–1): 3633 cл, 1650 ср, 1590 с, 1522 ср, 1488 сл, 1498 с, 1430 с, 1401 с, 1380 с, 1294 ср, 1115 c, 990 с, 945 ср, 932 сл, 826 сл, 773 с, 745 с, 704 сл, 654 сл, 619 сл, 583 cл, 507 с, 496 cл, 477 cр.
Синтез [Cd2Eu2(Рfbz)10(Рy)4] (III). К раствору комплекса I (0.100 г, 0.166 ммоль) в 5 мл MeCN добавляли навеску соединения II (0.145 г, 0.083 ммоль). Реакционную смесь перемешивали в течение 20 мин при 70°С и к горячему раствору добавляли 27 мкл пиридина (0.322 ммоль, Cd : L = 1 : 2). Полученный бесцветный раствор выдерживали при 70°С в закрытой виале. Образовавшиеся через 3 сут бесцветные кристаллы, пригодные для РСА, отделяли от маточного раствора декантацией, промывали холодным ацетонитрилом (Т ≈ 5°C). Выход III 0.187 г (38.1% в расчете на соединение I).
| Найдено, %: | С 37.05; | Н 0.43; | N 1.75. |
| Для C90H20N4O20F50Cd2Eu2 | |||
| вычислено, %: | C 36.57; | H 0.68; | N 1.90. |
ИК-спектр (НПВО; ν, см–1): 1651 ср, 1585 с, 1525 с, 1488 с, 1449 сл, 1385 с, 1293 ср, 1224 сл, 1142 сл, 1108 ср, 1070 ср, 1040 ср, 991 с, 933 с, 829 ср, 767 ср, 743 с, 700 с, 681 ср, 631 ср, 609 сл, 583 ср, 507 ср.
Синтез [Cd2Eu2(Рfbz)10(Рhpy)2(MeCN)2] · 5MeCN (IV) выполняли по методике, аналогичной для III с использованием 237 мкл Рhpy (1.663 ммоль, Cd : L = 1 : 10) вместо Рy. Образовавшиеся через 10 сут бесцветные кристаллы, пригодные для РСА, отделяли от маточного раствора декантацией, промывали холодным ацетонитрилом (Т ≈ 5°C). Выход IV 0.168 г (62.3% в расчете на соединение I).
| Найдено, %: | C 39.29; | H 1.40; | N 3.61. |
| Для C106H39N9O20F50Cd2Eu2 | |||
| вычислено, %: | C 39.77; | H 1.21; | N 3.87. |
ИК-спектр (НПВО; ν, см–1): 3451 сл, 2630 сл, 2253 сл, 1650 ср, 1627 ср, 1598 с, 1574 ср, 1521 ср, 1493 с, 1454 ср, 1426 ср, 1402 с, 1297 ср, 1158 ср, 1118 ср, 1108 с, 994 с, 942 с, 935 ср, 895 сл, 831 ср, 771 ср, 747 с, 695 с, 639 ср, 626 сл, 582 с, 549 сл, 507 ср, 481 ср.
Синтез [Cd(Рfbz)2(Lut)]n (V) выполняли по методике, аналогичной для III c использованием 193 мкл Lut (1.663 ммоль, Cd : L = 1 : 10) вместо Py. Образовавшиеся через 2 сут бесцветные кристаллы, пригодные для РСА, отделяли от маточного раствора декантацией, промывали холодным ацетонитрилом (Т ≈ 5°C). Выход V 0.109 г (51.1% в расчете на соединение I).
ИК-спектр (ν, см–1): 1647 ср, 1601 с, 1520 ср, 1489 с, 1441 ср, 1371 с, 1305 ср, 1291 сл, 1180 сл, 1140 сл, 1114 ср, 1100 ср, 990 с, 928 с, 831 с, 822 ср, 767ср, 755 ср, 742 с, 701 сл, 692 сл, 619 сл, 582 сл, 561 сл, 541 ср, 506 ср, 481 сл.
Синтез [CdEu2(Pfbz)8(Etypy)(H2O)2]n · 3nMeCN · · n(Etypy) (VI) выполняли по методике, аналогичной для III при комнатной температуре c использованием 0.173 г Еtypy (1.663 ммоль, Cd : L = 1 : 10) вместо Рy. Полученную реакционную смесь выдерживали 30 сут при 3°С. Образовавшиеся бесцветные кристаллы, пригодные для РСА, отделяли от маточного раствора декантацией, промывали холодным ацетонитрилом (Т ≈ 5°C). Выход VI 0.132 г (32.4% в расчете на соединение I).
ИК-спектр (ν, см–1): 2819 сл, 2546 сл, 2294 сл, 2252 ср, 1652 ср, 1610 с, 1523 ср, 1494с, 1392 с, 1293 ср, 1192 сл, 1108 с, 994 с, 931 ср, 826 ср, 769 ср, 742 с, 699 ср, 674 сл, 647 сл, 583 сл, 508 ср, 487 ср, 477 ср, 458 ср, 418 сл.
Синтез [Cd(H2O)(Рfbz)2(Iquin)2]n (VII) выполняли по методике, аналогичной для III c использованием 196 мкл Iquin (1.663 ммоль, Cd : L = 1 : 10) вместо Py. Образовавшиеся через 2 сут бесцветные кристаллы, пригодные для РСА, отделяли от маточного раствора декантацией, промывали холодным ацетонитрилом (Т ≈ 5°C). Выход VII 0.106 г (79.1% в расчете на соединение I).
ИК-спектр (ν, см–1): 3005 сл, 2293 сл, 2253 ср, 1654 ср, 1513 ср, 1492 с, 1443 ср, 1374 с, 1319 ср, 1285 ср, 1109 с, 1038 сл, 992 с, 955 ср, 918 ср, 812 ср, 783 ср, 743 ср, 635 ср, 516 ср, 489 ср, 466 ср.
Синтез [Cd(Pfbz)2(Biquin)] (VIII) выполняли по методике, аналогичной для III c использованием 0.043 мг Biquin (0.166 ммоль, Cd : L = 1 : 1) вместо Рy. Образовавшиеся через 5 сут бесцветные кристаллы, пригодные для РСА, отделяли от маточного раствора декантацией, промывали холодным ацетонитрилом (Т ≈ 5°C). Выход VIII 0.106 г (79.1% в расчете на соединение I).
ИК-спектр (ν, см–1): 2919 сл, 1653 ср, 1584 с, 1520 ср, 1490 с, 1421ср, 1400 ср, 1379 с, 1340 ср, 1296 ср, 1186 сл, 1142 сл, 1103 с, 992 с, 950ср, 936 ср, 824 ср, 767 ср, 747 ср, 694 ср, 656 сл, 619 сл, 584 сл, 507 ср, 488 ср, 479 сл.
Синтез $[{\mathbf{C}}{{{\mathbf{d}}}_{{\mathbf{2}}}}{{({\mathbf{Рfbz}})}_{{\mathbf{3}}}}]_{n}^{--}$ · nHBquin+ (IX) по методике, аналогичной для III c использованием 0.297 г Вquin (1.663 ммоль, Cd : L = 1 : 10) вместо Рy. Образовавшиеся через 8 сут бесцветные кристаллы, пригодные для РСА, отделяли от маточного раствора декантацией, промывали холодным ацетонитрилом (Т ≈ 5°C). Выход IX 0.055 г (35.9% в расчете на соединение I).
ИК-спектр (ν, см–1): 3070 сл, 2628 сл, 2243 сл, 1661 ср, 1643 ср, 1591 с, 1566 ср, 1523 ср, 1490 с, 1480 с, 1443 ср, 1391 с, 1371 с, 1291 с, 1277с, 1269 ср, 1208 с, 1146 сл, 1112 с, 1104 с, 990 с, 928 с, 876 ср, 832 ср, 823 ср, 771 ср, 742 ср, 706 ср, 697 ср, 684 ср, 652 ср, 616 сл, 583 ср, 533 ср, 505 ср, 477 ср.
РСА монокристаллов соединений I–VI, VIII–IX выполнен на дифрактометре Bruker Apex II, оборудованном CCD-детектором (MoKα, λ = 0.71073 Å, графитовый монохроматор) [24]. Для всех соединений введена полуэмпирическая поправка на поглощение по программе SADABS [25]. Структуры расшифрованы прямыми методами и уточнены полноматричным МНК в анизотропном приближении для всех неводородных атомов. Атомы водорода при атомах углерода органических лигандов генерированы геометрически и уточнены в модели “наездника”. Расчеты проведены по комплексу программ SHELX [26] с использованием OLEX2 [27].
Данные рентгеновской дифракции для комплекса VII получены на рентгеновском пучке станции “Белок” Курчатовского центра синхротронного излучения в Национальном исследовательском центре “Курчатовский институт” (Москва, Российская Федерация) в режиме φ-сканирования с использованием CCD детектора Rayonix SX165 при 100 K (λ = 0.79312 Å). Первичное индексирование, уточнение параметров, интегрирование отражений, учет поглощения произведены с использованием программного пакета XDS [28]. Структура расшифрована прямыми методами и уточнены полноматричным МНК по F 2 с параметрами анизотропного приближения для всех неводородных атомов. Атомы водорода помещены в рассчитанные положения и уточнены в модели “наездника”. Расчеты выполнены с помощью программного комплекса SHELXTL [26]. Геометрия полиэдров атомов металлов определена с использованием программы SHAPE 2.1 [29, 30]. Кристаллографические параметры и детали уточнения структур I, III–IX приведены в табл. 1 и табл. 2, основные длины связей и валентные углы для комплекса I – в табл. 3.
Таблица 1.
Кристаллографические параметры и детали уточнения структур I, III–IX
| Параметр | Значение | |||
|---|---|---|---|---|
| I | III | IV | V | |
| Брутто-формула | C14H8O8F10Cd | C90H20N4O20F50Cd2Eu2 | C106H39N9O20F50Cd2Eu2 | C21H9NO4F1Cd |
| М | 606.61 | 2955.82 | 3237.18 | 641.69 |
| Т, K | 296(2) | 173(2) | 120(2) | 296(2) |
| Сингония | Моноклинная | Моноклинная | Триклинная | Триклинная |
| Пр. гр. | C2/C | P21/с | P1 | P1 |
| a, Å | 37.928(18) | 13.368(4) | 14.2202(6) | 6.664(5) |
| b, Å | 7.455(3) | 24.908(7) | 14.6418(6) | 12.817(9) |
| c, Å | 13.217(8) | 15.352(5) | 15.7217(7) | 13.736(15) |
| α, град | 90 | 90 | 78.294(1) | 112.99(3) |
| β, град | 108.07(4) | 109.396(5) | 70.134(1) | 97.46(4) |
| γ, град | 90 | 90 | 67.406(1) | 90.55(2) |
| V, Å3 | 3553(3) | 4822(3) | 2832.4(2) | 1068.5(16) |
| Z | 8 | 2 | 1 | 2 |
| ρ(выч.), г см3 | 2.239 | 2.036 | 1.898 | 1.995 |
| μ, мм–1 | 1.377 | 1.888 | 1.617 | 1.140 |
| θmax, град | 25.43 | 24.999 | 30.61 | 25.669 |
| Tmin/Tmax | 0.601/0.745 | 0.634/0.785 | 0.817/0.855 | 0.620/0.745 |
| Число измеренных рефлексов | 12 422 | 24 257 | 27 883 | 8758 |
| Число независимых рефлексов | 3300 | 7986 | 11 137 | 3998 |
| Число рефлексов с I > 2σ(I) | 2703 | 7980 | 9928 | 3255 |
| Rint | 0.0772 | 0.1600 | 0.019 | 0.0466 |
| Число уточняемых параметров | 2308 | 4017 | 9018 | 2934 |
| GOOF | 1.010 | 0.967 | 1.036 | 1.109 |
| R1 (I > 2σ(I)) | 0.0433 | 0.0767 | 0.0289 | 0.0639 |
| wR2 (I > 2σ(I)) | 0.0901 | 0.2037 | 0.0690 | 0.1298 |
| Δρmin/Δρmax, е Å–3 | –4.660/2.451 | –1.232/1.509 | –1.371/1.537 | –1.156/1.007 |
Таблица 2.
Кристаллографические параметры и детали уточнения структур VI–IX
| Параметр | Значение | |||
|---|---|---|---|---|
| VI | VII | VIII | IX | |
| Брутто-формула | C76H23N5O18F40CdEu2 | C32H16N2O5F10Cd | C32H12N2O4F10Cd | C68H20N2O12F30Cd2 |
| М | 2470.31 | 810.89 | 790.75 | 1851.66 |
| Т, K | 100(2) | 150(2) | 296(2) | 296(2) |
| Сингония | Триклинная | Моноклинная | Моноклинная | Моноклинная |
| Пр. гр. | Р1 | P21/с | C2/C | P21/с |
| a, Å | 15.6773(11) | 20.712(4) | 14.5624(7) | 15.6961(11) |
| b, Å | 16.2440(17) | 5.3510(11) | 24.8057(12) | 7.7640(6) |
| c, Å | 18.5297(18) | 26.889(5) | 8.2876(4) | 26.2157(19) |
| α, град | 83.888(4) | 90 | 90 | 90 |
| β, град | 71.098(3) | 96.56(3) | 106.471(2) | 97.009(2) |
| γ, град | 65.635(3) | 90 | 90 | 90 |
| V, Å3 | 4064.7(7) | 2960.6(10) | 2870.9(2) | 3170.9(4) |
| Z | 2 | 4 | 4 | 2 |
| ρ(выч.), г см3 | 2.018 | 1.819 | 1.830 | 1.939 |
| μ, мм–1 | 1.949 | 1.140 | 0.869 | 0.828 |
| θmax, град | 26.379 | 30.954 | 30.48 | 22.47 |
| Tmin/Tmax | 0.633/0.745 | 0.821/0.956 | 0.728/0.846 | 0.726/0.963 |
| Число измеренных рефлексов | 28 212 | 28 266 | 27 301 | 45 636 |
| Число независимых рефлексов | 16 077 | 21 215 | 9914 | 9919 |
| Число рефлексов с I > 2σ(I) | 8211 | 6715 | 4404 | 5659 |
| Rint | 0.0963 | 0.0439 | 0.0597 | 0.0975 |
| Число уточняемых параметров | 4716 | 5816 | 3956 | 4521 |
| GOOF | 0.964 | 1.054 | 1.065 | 1.083 |
| R1 (I > 2σ(I)) | 0.0903 | 0.0503 | 0.0445 | 0.0533 |
| wR2 (I > 2σ(I)) | 0.2260 | 0.1120 | 0.1098 | 0.1266 |
| Δρmin/Δρmax, е Å–3 | –3.127/2.649 | –1.468/0.737 | –0.758/ 0.700 | –0.599/1.861 |
Таблица 3.
Основные геометрические характеристики комплексов I, V, VII–IX
| Связь | d, Å | ||||
|---|---|---|---|---|---|
| I | V | VII | VIII | IX | |
| Cd–N(L) | 2.295(6) | 2.323(4), 2.371(4) | 2.306(2) | ||
| Cd–O(H2O) | 2.310(4)–2.720(5) | 2.282(4) | |||
| Cd–O(Рfbz) | 2.369(4)–2.497(5) | 2.232(5)–2.512(5) | 2.314(4)–2.381(4) | 2.334(5)–2.392(5) | 2.243(3)–2.351(4) |
| Cd…Cd | 3.903 | 3.376(1), 5.254 | 5.353 | 3.912 | |
| Угол | ω, град | ||||
| CdCdCd | 144.64 | 96.760 | 180.00 | 96.760 | 165.849 |
Полный набор рентгеноструктурных параметров для соединений I, III–IX депонирован в Кембриджском банке структурных данных (CIF files CCDC № 1987805 (I), 1987808 (III), 1987829 (IV), 1987817 (V), 1987822 (VI), 1987823 (VII), 1987824 (VIII), 1987826 (IX); deposit@ ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk/ data_request/cif).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для синтеза комплексов с анионами пентафторбензойной кислоты (HРfbz) реакцией гидроксидов кадмия(II) или европия(III) с HРfbz в воде были получены соединения $[{\text{Cd}}({\text{Рfbz}}){{\left( {{{{\text{H}}}_{{\text{2}}}}{\text{O}}} \right)}_{{\text{4}}}}]_{n}^{ + }$ ∙ n(Рfbz)–] (I) и [Eu2(Рfbz)6(H2O)8] · 2H2O (II). Взаимодействием I, II и N-донорного лиганда (Рy, Рhpy, Lut, Еtypy, Iquin, Biquin, Bquin) в растворе MeCN получена серия гомо- и гетерометаллических комплексов III–IX соответственно (cхема 1). Продукты реакции выделены в виде монокристаллов и охарактеризованы методами CHN-анализа, ИК-спектроскопии и РСА. Основываясь на полученных данных, мы наблюдаем образование гетерометаллических комплексов III–VI, а также комплексов кадмия – VII–IX.
Схема 1 .
Комплекс I кристаллизуется в моноклинной пр. гр. С2/c. Атомы металлов в полимерной цепи транслируются осью 21. Каждый атом Cd связан с соседними парами μ2-мостиковых молекул воды (O(1w) и O(2w), pис. 1а). Атом металла достраивает свое ближайшее окружение (CdO8) до квадратно-антипризматического координацией хелатно связанного Pfbz-аниона и шести молекул воды, две из которых монодентатные (O(3w) и O(4w)). Положительный заряд атома металла компенсируется за счет внешнесферного Pfbz-аниона, формирующего водородные связи с координированными молекулами воды. Молекула воды (O(4w)) образует водородные связи с атомами О координированных Pfbz-анионов внутри одной цепи. Молекулы O(2w) и O(3w) формируют водородную связь между соседними полимерными цепями (рис. 1б). Основные длины связей и углы между атомами, участвующими в водородных связях комплекса I, представлены в табл. 4.
Рис. 1.
Фрагмент полимерной цепи (а) и упаковка (б) комплекса I (aтомы фтора не показаны). Атомы водорода и фтора на рисунке (а) не показаны. Заместители при карбоксильной группе на рисунке (б) не показаны.
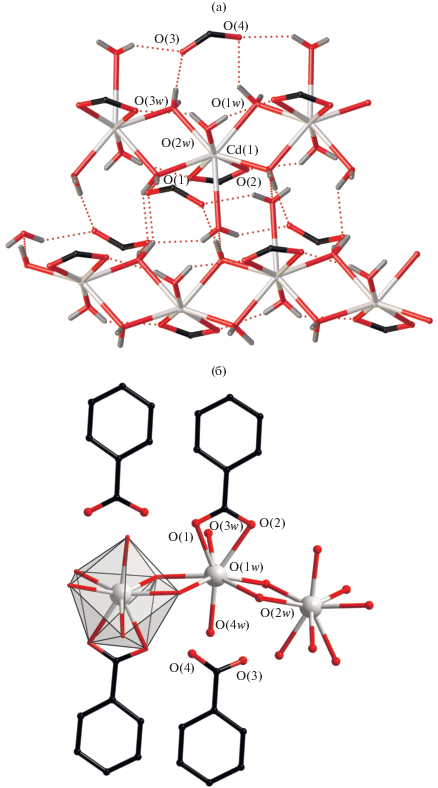
Таблица 4.
Геометрические параметры водородной связи в кристалле соединения I*
| D–H…A | Расстояние, Å | Угол D–Н…A, град | ||
|---|---|---|---|---|
| D–H | H…A | D…A | ||
| O(1w)-H…O(4)i | 0.98 | 1.79 | 2.75 | 151.38 |
| O(2w)-H…O(3) | 0.96 | 1.66 | 2.72 | 174.65 |
| O(3w)-H…O(3) | 0.91 | 1.99 | 2.74 | 139.80 |
| O(3w)-H…O(4) | 0.92 | 1.97 | 2.77 | 144.38 |
| O(4w)-H…O(1)ii | 0.85 | 1.98 | 2.81 | 164.45 |
| O(4w)-H…O(2)iii | 0.93 | 1.98 | 2.57 | 122.92 |
| O(2w)-H…O(3w)iii | 0.85 | 1.99 | 2.75 | 165.23 |
Аналогичный 1D-комплекс формируется при синтезе тетрафтортерефталата кадмия в воде [31], где полимерная цепь формируется мостиковыми молекулами воды, а компенсация положительного заряда полимерной цепи происходит за счет второй депротонированной и не участвующей в координации группы RCOO– координированного тетрафтортерефталатного аниона. В случае анионов 4-гидроксибензойной кислоты (4-OHbnz) образуется моноядерный комплекс [Cd(4-OHBnz)(H2O)5]+(H2O)- (4-OHBnz)– [32], где избыток молекул воды в координационной сфере иона металла препятствует формированию полимерной цепи.
Комплекс II представляет собой известное соединение, структурно описанноe ранее [33, 34].
Взаимодействие соединений I и II в присутствии пиридина (Cd : L = 1 : 2) или 2-фенилпиридина (Cd : L = 1 : 10) приводит к кристаллизации линейных тетраядерных комплексов III, IV, близкого строения (рис. 2а, 2б соответственно). Комплекс III кристаллизуeтся в моноклинной пр. гр. P21/c, IV – в триклинной пр. гр. $P1 - $ в виде сольвата с молекулами MeCN, центр инверсии в обоих соединениях располагается между центральными атомами Eu(1) и Eu(1A). Атомы Eu связаны между собой двумя мостиковыми и двумя хелатно-мостиковыми Рfbz-анионами. Периферийные атомы Cd связаны с атомами Eu одним мостиковым и двумя хелатно-мостиковыми Рfbz-анионами в III и одним хелатно-мостиковым и двумя мостиковыми Рfbz-анионами в IV. В III атом Cd координирует две молекулы Рy, достраивая свое окружение (CdO5N2) до пентагонально-бипирамидального, в IV окружение атома Cd (CdO4N2) достраивается до октаэдрического координацией атомов N молекулы Рhpy и MeCN. По-видимому, присутствие объемного фенильного заместителя в молекуле Рy в α-положении препятствует координации второй молекулы Рhpy и в координационную сферу Cd входит компактная молекула MeCN. Геометрия координационного окружения атома Eu (EuO8) в III и IV соответствует квадратной антипризме. Атомы водорода Рy, Рhpy и координированных молекул MeCN участвуют в формировании межмолекулярных контактов С–H…F с атомами FРfbz-анионов (С…F 1.315–1.415 Å (в III), 1.336–1.348 Å (в IV), H…F 2.59–2.68 Å (в III) и 2.56–2.70 Å (в IV)); углы СHF лежат в диапазоне 111°–127° (для III) и 111°–138° (в IV)). Основные длины связей и углы между атомами, участвующими в водородных связях комплексов III, IV представлены в табл. 5.
Рис. 2.
Молекулярное строение комплексов III (а) и IV(б).Атомы водорода, фтора и сольваты не показаны.
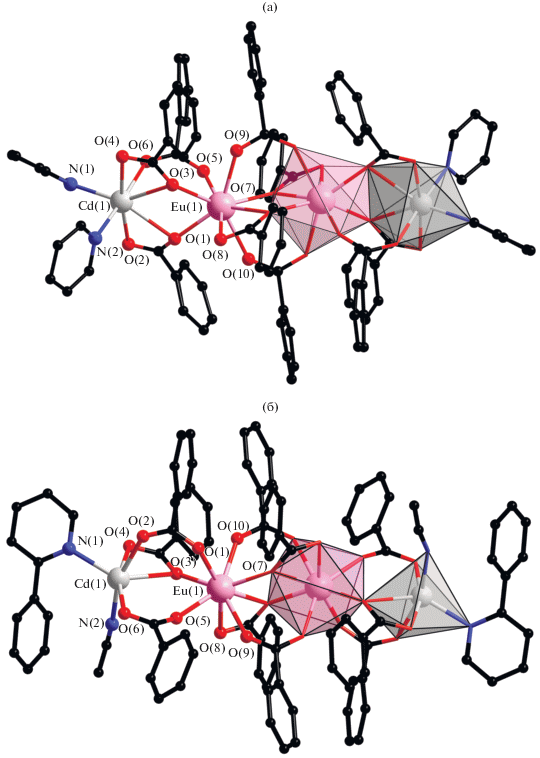
Таблица 5.
Основные геометрические характеристики комплексов III–IV, VI
| Связь | d, Å | ||
|---|---|---|---|
| III | IV | VI | |
| Cd–N(L) | 2.271(11)–2.285(13) | 2.290(3) | 2.340(12) |
| M–X(Solv) | 2.275(3) (MeCN) | 2.414(9)–2.448(9) (H2O) | |
| Cd–O(Pfbz) | 2.293(10)–2.540(9) | 2.253(2)–2.371(3) | 2.225(8)– 2.724(9) |
| Eu–O(Pfbz) | 2.337(10)–2.525(10) | 2.305(2)–2.531(2) | 2.322(9)–2.870(8) |
| Cd…Cd | 11.683 | 12.030 | 10.202, 10.446 |
| Cd…Eu | 3.892 | 4.079 | 3.923, 4.087 |
| Eu…Eu | 3.920 | 3.926 | 4.216(2), 4.254(2) |
| Угол | ω, град | ||
| MMM | 172.80 (CdEuEu) | 168.411 (CdEuEu) | 110.85, 111.45 (EuCdEu) |
Известно несколько примеров координационных соединений с анионами монокарбоновых кислот {Ln2Cd2}, в которых в качестве N-донорного лиганда выступает 1,10-фенантролин (Рhen) ([Cd2Ln2(pTol)10(Рhen)2] (Ln = Nb, Pr, Sm), [Cd2Ho2(pClBnz)10(Phen)2] (H(pTol) = 4-метилбензойная кислота, H(pClBnz) = 4-хлорбензойная кислота) [35]. Известны комплексы состава [Zn2Ln2(O2CR)10(Py)2] с анионами монокарбоновых кислот и пиридином, в этих соединениях каждый атом цинка координирует только одну молекулу пиридина (–O2CR = анион метаакриловой кислоты, Ln(III) = Ce [36] –O2CR = анион 1-нафтиуксусной кислоты, Ln(III) = Eu, Dy, Tb [37].
Координация двух молекул пиридина к атому цинка в LnZn-комплексах наблюдается только в случае биядерного комплекса состава [LnZn-(Piv)5(Py)3] (Ln = Tb, Yb, Dy, Er, HPiv = триметилуксусная килсота) [38]. Гетерометаллические комплексы с молекулами 2-фенилпиридина на данный момент не описаны.
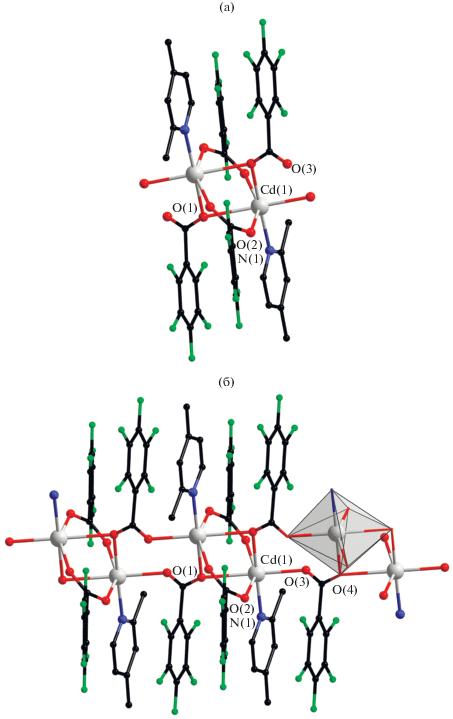
Комплекс V кристаллизуется в триклинной пр. гр. $P\bar {1}.$ Полимерная цепь соединения V построена из центросимметричных биядерных фрагментов {Cd2(Pfbz)4(Lut)2} (центр инверсии располагается между атомами Cd), в которых атомы металла связаны двумя μ2-O,O'-мостиковыми и двумя μ2-O,O-мостиковыми Pfbz-анионами (рис. 3а). Последние Pfbz-анионы участвуют в образовании полимерной структуры (рис. 3б), монодентатно координируясь к атомам Cd двух соседних фрагментов {Cd2(Pfbz)4(Lut)2}, при этом мостиковая функция карбоксилатной группы соответствует η1:η2:μ3. Таким образом, атом кадмия координирует по пять атомов O пяти карбоксилатных групп и одному атому N молекулы Lut, а его окружение (CdO5N) соответствует октаэдрическому.
Рис. 3.
Биядерный фрагмент {Cd2(O2CC6F5)4(Lut)2} (а) и полимерная цепь (б) комплекса V. Атомы водорода не показаны.
В упаковке комплекса V наблюдается близкая к параллельной ориентация ароматических фрагментов C6F5 и Lut внутри одной полимерной цепи (угол между плоскостями, кратчайшее расстояние между плоскостями и расстояние между центроидами составляют 5.2°, 3.287 и 3.769 Å соответственно). Это указывает на формирование стэкинг-взаимодействий между ними. Также наблюдается формирование C–H…F контактов между водородом групп CH3 молекулы Lut и атомом F координированного Pfbz-аниона соседней полимерной цепи (С–H…F 2.61, С…F 3.547 Å, угол С–H…F 166.4°).
Соединения кадмия с 2,4-лутидином и анионами монокарбоновых кислот в литературе представлены только несколькими примерами молекулярных комплексов ([Cd2(Piv)4(Lut)2 [39], [Cd2M(Piv)6(Lut)2] (M = Ca, Sr, Mg) [40].
Комплекс VI кристаллизуется в триклинной пр. гр. Р$\bar {1}$ в виде сольвата с тремя молекулами MeCN и одной молекулой Etypy. Комплекс IV явялется 1D полимером, в котором элементарное звено – трехъядерный фрагмент {Eu2Cd(Рfbz)8-(H2O)2(Еtypy)} (рис. 4а). В этом фрагменте атом Cd(1) связан с каждым атомом европия, Eu(1) и Eu(2), одной мостиковой и двумя хелатно-мостиковыми Рfbz-анионами. Окружение атома кадмия составляют два атома O двух μ2-O,O'-мостиковых Рfbz-анионов, два атома O двух η2,μ3-хелатно-мостиковых Рfbz-анионов, связанные хелатно с атомами Eu, два атома O η2,μ3-хелатно-мостикового Рfbz-аниона, который координирован хелатно атомом Cd, и один атом N молекулы Еtypy. Окружение атомов Eu(1) и Eu(2) отличается. Атом Eu(1) координирует семь атомов O одного хелатно связанного и пяти монодентатно связанных с ним Рfbz-анионов, а также две молекулы воды. Атом Eu(2) координирует семь атомов O двух хелатно связанных и пяти монодентатно связанных с ним Рfbz-анионов. Между собой атомы Eu связаны двумя мостиковыми Рfbz-анионами и двумя атомами O двух хелатно-мостиковых Рfbz-анионов. Окружение атомов Eu (EuO9) соответствует геометрии ‘muffin’, окружение атома Cd (CdO6N) – одношапочной тригональной призме. Основные длины связей и углы представлены в табл. 5.
Рис. 4.
Фрагмент полимерной цепи (а) и фрагмент упаковки (б) комплекса VI. Показаны только атомы водорода, участвующие в формировании водородной связи. Атомы фтора не показаны. На рисунке (а) заместители при карбоксильной группе не показаны, на рисунке (б) показаны только заместители при карбоксильной группе, участвующие в меж- и внутримолекулярных взаимодействиях.
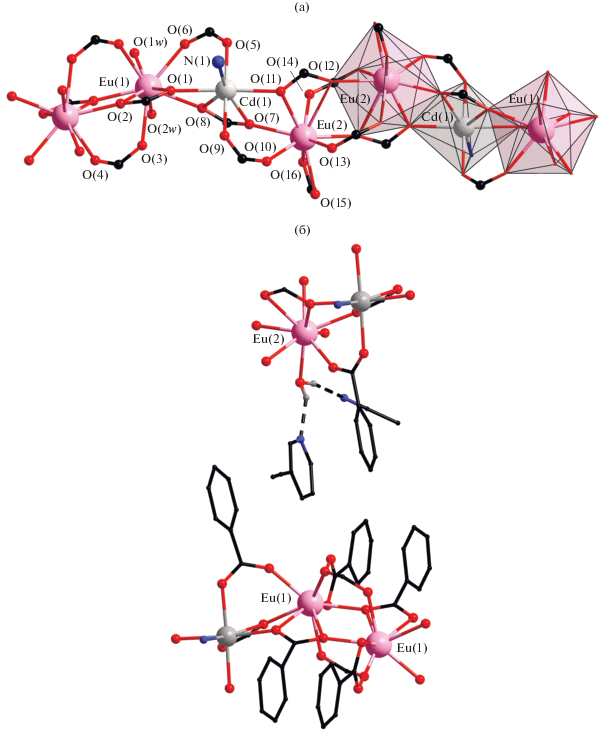
Координированная к атому Eu молекула воды участвует в образовании водородной связи с двумя атомами N сольватных молекул Еtypy и MeCN (N…H 1.918–2.307, N…O 2.717, 2.898 Å, угол N…H–O 148.93° и 166.07° соотвественно) (рис. 4б).
В упаковке комплекса VI наблюдаются стэкинг-взаимодействия между ароматическими фрагментами двух координированных Рfbz-анионов соседних полимерных цепей и сольватной молекулой Еtypy (расстояние между центрами взаимодействующих единиц и угол между плоскостями равны 3.52 Å, 3.23° и 3.55 Å, 5.21° соответственно), а также между ароматическими фрагментами Рfbz-анионов внутри одной полимерной цепи (расстояние между плоскостями и угол между плоскостями равны 3.60 Å и 1.23° соответственно) (рис. 4б). Атомы водорода ацетиленового фрагмента и пиридинового кольца координированных и сольватных молекул Еtypy участвуют в формировании слабых контактов С–H…F с атомами фтора Рfbz-анионов внутри одной или между соседними полимерными цепями (С–H…F–C 2.420–2.628 Å, угол С–H…F 111.3°–168.1°).
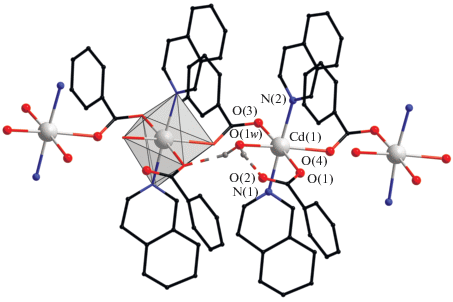
Рис. 5.
Фрагмент полимерной цепи комплекса VII. Показаны только атомы водорода, участвующие в формировании водородной связи. Атомы фтора не показаны.
В отличие от молекулярных комплексов III и IV для полимера VI наблюдается значительное отклонение геометрии металлоостова от линейного (углы CdEuEu для VI 110.85° и 111.45°) тогда как в случае молекулярных комплексов III и IV геометрия металлоостова близка к линейной (CdEuEu 168.38° и 172\\\\.80°). По-видимому, наличие внутри- и межмолекулярных π–π-взаимодействий приводит к искажению геометрии металлоостова комплекса VI, в то время как в кристаллах близких к линейным соединений III и IV стэкинга не наблюдается.
В реакции I, II и Iquin были выделены только кристаллы комплекса VII. Комплекс VII кристаллизуется в моноклинной пр. гр. Р21/с. Атомы кадмия попарно связаны мостиковым Pfbz-анионом, формируя линейную полимерную цепь (pис. 5). Металлоцентр достраивает свое окружение до октаэдрического (CdO5N) координацией атомов О монодентатно связанного Pfbz-аниона, молекулы воды и двух атомов N двух молекул Iquin. Основные длины связей и расстояния представлены в табл. 4.
Координированная молекула воды участвует в образовании водородной связи с двумя атомами O двух монодентатно связанных Pfbz-анионов (O…O 2.658, 2.729, O…H 1.843, 1.949 Å, угол OHO 160.73° и 151.85°). Атомы водорода координированной молекулы изохинолина участвуют в формировании слабых контактов С–H…F с атомами фтора Pfbz-анионов соседних полимерных цепей (С–H…F 2.417–2.645, C...F 1.333–1.339 Å, углы СHF 114.65°–156.92°).
Все описанные в литературе карбоксилатные комплексы с изохинолином {Mx+(O2CR)x(Iquin)y} имеют молекулярное строение, и формирования полимеров не происходит (с ионами меди(II) [41], Ni(II) [42, 43], Co(II) [44, 45] и Cd(II) [Cd(O2CR)2(Iquin)3] [39]).
С хелатирующим Biquin был выделен и структурно охарактеризован моноядерный комплекс кадмия(II) VIII, кристаллизующийся в моноклинной пр. гр. С2/c. В симметричной молекуле комплекса (ось С2 проходит через атом Cd(1) и между атомами углерода C(16) и C(16A)) атом металла достраивает свое окружение (CdN2O4) до тригонально-призматического координацией двух хелатно связанных Рfbz-анионов и двух атомов N хелатной молекулы Вiquin (рис. 6а). В кристалле формируются супрамолекулярные цепочки, образованные за счет межмолекулярных взаимодействий как между ароматическими фрагментами Вiquin (расстояние и угол между плоскостями равны 3.50 Å и 0.00° соответственно), так и между Рfbz-анионами (кратчайшее расстояние и угол между плоскостями равны 3.57 Å и 5.52° соответственно) (рис. 6б).
Рис. 6.
Строение молекулы (а) и фрагмент кристаллической упаковки (б) комплекса VIII. Атомы водорода не показаны.
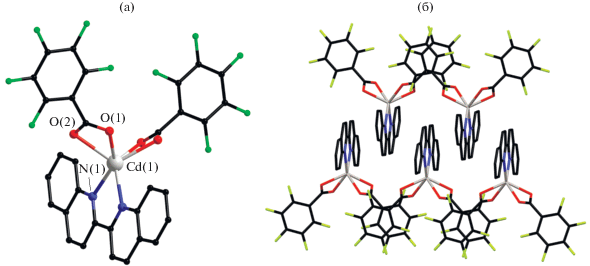
По-видимому, формирование моноядерного комплекса связано с экранированием металлоцентра объемным хелатирующим лигандом.
В случае 7,8-бензохинолина был выделен анионный полимер IX, кристаллизующийтся в моноклинной пр. гр. Р21/с. Полимерная цепь состоит из моноядерных фрагментов {Cd(Рfbz)3}+, связанных между собой одним μ2-O,O,-мостиковым и двумя μ2-O,O',-мостиковыми Рfbz-анионами (рис. 7). Противоионом полимерной цепочки является протонированная сольватная молекула лиганда HВquin+, которая участвует в формировании водородной связи с некоординированным атомом кислорода Рfbz-аниона (H…O 2.749, N…O 2.747 Å, угол NHO 162.8°).
Рис. 7.
Фрагмент полимерной цепи комплекса IX. Показаны атомы водорода, участвующие в водородном связывании. Атомы фтора не показаны.
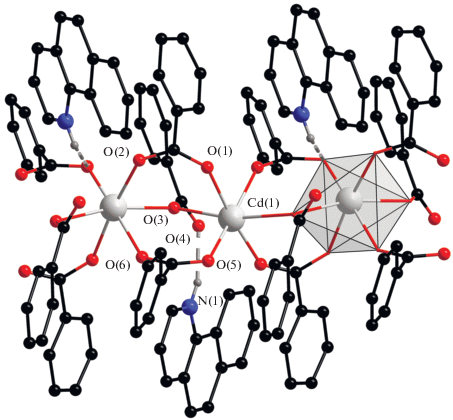
Полученный результат необычен тем, что при подобном с\\оставе, как правило, формируются ионные соединения на основе моноядерного или биядерного анионного карбоксилатного комплекса и соответствующего количества органических катионов [46–49].
В упаковке комплекса IX наблюдается близкая к параллельной ориентация Рfbz-анионов и сольватных молекул HВquin+ (рис. 7, расстояние между центрами взаимодействующих единиц и угол между плоскостями равны 3.56 Å и 6.40° соответственно), а также пар Рfbz-анионов внутри полимерной цепи (расстояние между центрами взаимодействующих единиц и угол между плоскостями равны 3.59 Å, и 5.76° соответственно), что может свидетельствовать о внутримолекулярных стэкинг-взаимодействиях. Атом водорода сольватной молекулы HВquin участвует в формировании слабых контактов С–H…F–C с атомами фтора Рfbz-анионов соседних полимерных цепей (C…F 1.341–1.344, H…F 2.618, 2.620, 2.646 Å, угол СHF 121.82°, 157.86°, 171.27° соответственно).
Полученная серия соединений показывает разнообразие структур с ионами кадмия(II) и анионами пентафторбензойной кислоты, в которых в качестве фактора, определяющего строение комплекса, является N-донорный лиганд. Наблюдаются структурные отличия для карбоксилатных комплексов кадмия и двухвалентных 3d-металлов (из ряда Fe-Zn) с монодентатными производными пиридина, для которых, как правило, образуются моно-, би- или трехъядерные комплексы.
На примере выделенных комплексов показана тенденция образования внутримолекулярных стекинг-взаимодействий между фрагментами C6F5 и C6F5 и пиридиновыми фрагментами координированных лигандов. Тенденция формирования внутримолекулярных взаимоедйствий сохраняется при переходе от полимеров кадмия к Cd-Eu-гетерометаллическим тетраядерным и полимерному комплексам.
Список литературы
Niekerk J.N. van, SchoeningF.R.L., Talbot J.H. // Acta Crystallogr. 1953. V. 6. P. 720.
Niekerk J.N. van, Schoening F.R.L. // Acta Crystallogr. 1953. V. 6. P. 609.
Downie T.C., Harrison W., Raper E.S., Hepworth M.A. // Acta Crystallogr. B. 1971. V. 27. P. 706.
Harrison W., Trotter J. // Dalton Trans. 1972. P. 956.
Amma E.L., Griffith E.A.H., Charles N.G., Rodesiler P.F. // Abstr. Papers Am. Chem. Soc. (Summer). 1983. P. 39.
Rodesiler P.F., Griffith E.A.H., Charles N.G., Amma E.L. // Acta Crystallogr. C. 1985. V. 41. P. 673.
Xiang-HuHuang, Peng-ZhiHong, Wen-DongSong // Acta Crystallogr. E. 2008. V. 64. P. m175.
Golubichnaya M.A., Sidorov A.A., Fomina I.G. et al. // Russ. J. Inorg. Chem. 1999. V. 44. P. 1479.
Burley J.C., Prior T.J. // Acta Crystallogr. E. 2005. V. 61. P. m1422.
Karmakar A., Baruah J.B. // Polyhedron. 2008. V. 27. P. 3409.
Dey D., Roy S., Purkayastha R.N.D. et al. // J. Coord. Chem. 2011. V. 64. P. 1165.
Karmakar A., Sarma R.J., Baruah J.B. // Eur. J. Inorg. Chem. 2006. P. 4673.
Eremenko I.L., Nefedov S.E., Sidorov A.A. // Inorg. Chem. 1999. V. 38. P. 3764.
Saxena P., Thirupathi N. // Polyhedron. 2015. V. 98. P. 238.
Gao Zhu-Qing, Li Hong-Jin, ong GuJin-Zh // Wuji Huaxue Xuebao (Chin.) (Chin. J. Inorg. Chem.). 2004. V. 30. P. 2803.
Stoll I., Brodbeck R., Neumann B. et al.// CrystEngComm. 2009. V. 11. P. 309.
Collings J.C., Roscoe K.P., Robins E.G. et al. // New J. Chem. 2002. V. 26. P. 1740.
Imai Y., Kawaguchi K., Sato T. et al. // Mol. Cryst. Liq. Cryst. 2008. V. 487. P. 153.
Williams J.H., Cockcroft J.K., Fitch A.N. // Angew. Chem Int. Ed. 1992. V. 31. P. 1655.
Cockcroft J.K., Ghosh R.E., Shephard J.J. et al. // Cryst-EngComm. 2017. V. 19. P. 1019.
Kong Y.-J., Li P., Han L.-J et al. // Acta Crystallogr. C. 2017. V. 73. P. 424.
Maas H., Currao A., Calzaferri G. // Angew. Chem. Int. Ed. 2002. V. 41. P. 2495.
Goldberg A., Kiskin M., Shalygina O. et al. // Chem. Asian J. 2016. V. 11. P. 604.
SMART (control) and SAINT (integration). Software. Version 5.0. Madison (WI, USA): Bruker AXS Inc., 1997.
Sheldrick G.M. SADABS. Madison (WI, USA): Bruker AXS Inc., 1997.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Ap-pl. Cryst. 2009. V. 42. P. 339.
Kabsch W. // Acta Crystallogr. D. 2010. V. 66. P. 125.
Alvarez S., Llunell M. // Dalton Trans. 2000. V. 19. P. 3288.
Casanova D., Llunell M., Alemany P., Alvarez S. // Chem. Eur. J. 2005. V. 11. P. 1479.
Chen Sheng-Chun, Zhang Zhi-Hui, Huang Kun-Lin et al. // CrystEngComm. 2013. V. 15. P. 9613.
Nadzhafov G.N., Shnulin A.N., Mamedov Kh.S., Shil’nikov V.I. // Koord. Khim. (Russ.). 1982. V. 8. P. 1276.
Глинская Л.А., Леонова Т.Г., Клевцова Р.Ф., Ларионов С.В. // Журн. структур. химии. 2010. Т. 51. № 3. С. 610 (Glinskaya L.A., Leonova T.G., Klevtsova R.F., Larionov S.V. // J. Struct. Chem. 2010. V. 51. P. 610).
Kalyakina A.S., Utochnikova V.V., Bushmarinov I.S. et al. // Chem. Eur. J. 2015. V. 21. P. 17921.
Chi Yu-Xian, Niu Shu-Yun, Jing Jin et al. // Dalton Trans. 2009. № 37. P. 7653.
Wu Bin, Guo Yong-Sheng // Acta Crystallogr. E. 2004. V. 60. P. m1261.
Kiraev S.R., Nikolaevskii S.A., Kiskin M.A. et al. // Inorg. Chim. Acta. 2018. V. 477. P. 15.
Boyle T.J., Raymond R., Boye D.M. et al. // Dalton Trans. 2010. V. 39. P. 8050.
Гоголева Н.В., Шмелев М.А., Кискин М.А. и др. // Изв. АН. Сер. хим. 2016. № 5. С. 1198 (Gogoleva N.V., Shmelev M.A., Kiskin M.A. et al. // Russ. Chem. Bull. 2016. V. 65. P. 1198).
Гоголева Н.В., Шмелев М.А., Евстифеев И.С. и др. // Изв. АН. Сер. хим. 2016. № 1. С. 181.
Sato Y., Ouchi A., Yukawa Y., Takeuchi T. // Chem. Lett. 1982. P. 1495.
Miklovic J., Packova A., Segla P. et al. // Inorg. Chim. Acta. 2015. V. 429. P. 73.
Ivanikova R., Boca R., Dlhan L. et al. // Polyhedron. 2006. V. 25. P. 3261.
Clegg W., Straughan B.P. // Acta Crystallogr. C. 1992. V. 45. P. 1989.
Hudak J., Boca R., Moncol J., Titis J. // Inorg. Chim. Acta. 2013. V. 394. P. 401.
Niedzielska D., Pazderski L., Wojtczak A. et al. // Polyhedron. 2018. V. 139. P. 155.
Robertson K.N., Bakshi P.K., Lantos S.D. et al. // Can. J. Chem. 1998. V. 76. P. 583.
Ha Kwang-Ho // Z. Kristallogr. 2012. V. 227. P. 33.
Esteruelas M.A., Fernandez-Alvarez F.J., Olivan M., Onate E. // Organometallics. 2009. V. 28. P. 2276.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия