Координационная химия, 2020, T. 46, № 9, стр. 554-561
Синтез и строение дицианодииодоауратов тетра(пара-толил)сурьмы [p-Tol4Sb][Au(CN)2I2] и алкилтрифенилфосфония [Ph3PAlk][Au(CN)2I2], Alk = Me, CH2CN
В. В. Шарутин 1, О. К. Шарутина 1, А. Н. Ефремов 1, *, О. С. Ельцов 2
1 Национальный исследовательский Южно-Уральский государственный университет
Челябинск, Россия
2 Уральский федеральный университет им. первого Президента России Б.Н. Ельцина
Екатеринбург, Россия
* E-mail: efremov_an94@mail.ru
Поступила в редакцию 26.11.2019
После доработки 10.02.2020
Принята к публикации 11.03.2020
Аннотация
Взаимодействием дицианодииодоаурата калия с галогенидами тетра(пара-толил)сурьмы и алкилтрифенилфосфония в водном растворе синтезированы кристаллические комплексы золота красного цвета [p-Tol4Sb][Au(CN)2I2] (I), [Ph3PMe][Au(CN)2I2] (II), [Ph3PCH2CN][Au(CN)2I2] (III), строение которых установлено методами ИК-спектроскопии, спектроскопии ЯМР и РСА (CIF files CCDC № 1901681 (I), 1912903 (II), 1912919 (III)). Катионы тетра(пара-толил)сурьмы и алкилтрифенилфосфония имеют искаженную тетраэдрическую координацию. Дицианодииодоауратные анионы имеют плоское строение с квадратной координацией атома золота. Образование пространственной сетки кристаллов обусловлено слабыми водородными связями СN⋅⋅⋅Н−С между катионами и анионами (2.39, 2.59 Å (I), 2.70, 2.48, 2.52, 2.68 Å (II), 2.73, 2.50, 2.67, 2.44 Å (III)). В комплексе III анионы одного из двух типов взаимодействуют между собой, образуя 1D ступенчатые цепочки вдоль направления кристаллографической оси а благодаря взаимодействиям I⋅⋅⋅I.
Внимание исследователей к дицианидным комплексам золота вызвано их использованием при получении материалов с различными фотохимическими и фотофизическими свойствами [1–8]. Также показано, что они являются действующими метаболитами некоторых лекарственных препаратов [9]. Анионы [Au(CN)2]− могут образовывать каркасные полимеры и олигомеры, обладающие люминесцентными свойствами [4, 5, 8–11]. Цианогалогенидные комплексы трехвалентного золота применяются в качестве сенсоров летучих органических соединений (ДМФА, диоксан, пиридин, этиленгликоль) [12] и как прекурсоры в синтезе дицианидов [13]. В настоящее время известно несколько цианидных комплексов одновалентного золота [14–16] и цианогалогенидных комплексов трехвалентного золота c органическими и неорганическими катионами [12, 13, 17–20], однако комплексы [Kat]+[Au(CN)2Hal2]− с элементоорганическими катионами не изучены.
C целью установления особенностей синтеза и строения дицианодииодоауратных комплексов тетраарилсурьмы и тетраорганилфосфония в настоящей работе впервые синтезированы и структурно охарактеризованы дицианодииодоаураты тетра(пара-толил)сурьмы [p-Tol4Sb][Au(CN)2I2] (I) и алкилтрифенилфосфония [Ph3PAlk][Au(CN)2I2], Alk = Me (II), CH2CN (III).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез дицианодииодоаурата тетра(пара-толил)сурьмы (I). К раствору 100 мг (0.192 ммоль) хлорида тетра(пара-толил)сурьмы в 10 мл воды прибавляли раствор 104 мг (0.192 ммоль) дицианодииодоаурата калия в 5 мл воды, перемешивали и выдерживали при 20°С в течение 14 ч. После испарения воды, твердый остаток сушили и перекристаллизовывали из смеси растворителей ацетонитрил–этиловый спирт (2 : 1 объемн.). При медленном испарении растворителей наблюдали образование красных кристаллов. Выход I 179 мг (94%). Тразл = 161°С.
ИК-спектр (ν, см−1): 3047, 3020, 2980, 2916, 2862, 2166, 2156, 1913, 1643, 1589, 1492, 1442, 1396, 1317, 1211, 1190, 1118, 1068, 1039, 1012, 848, 796, 696, 632, 584, 480, 439, 430.
ЯМР 1H (ДМСО-d6; 600 МГц; δ, м.д.): 2.41 (с., 12H, −CH3), 7.48 (д., 8H, аром. m-H, 3JHH = 7.86 Гц), 7.63 (д., 8H, аром. o-H, 3JHH = 7.86 Гц). ЯМР 13С (ДМСО-d6; 151 МГц; δ, м.д.): 21.16 (−СH3), 102.41 (CN), 124.69 (Сi), 130.97 (Сm), 135.04 (с., Сo), 142.68 (Сp).
Соединения II и III синтезировали по аналогичной методике.
II: темно-красные кристаллы, выход 96%, Тпл = = 143°С.
ИК-спектр (ν, см−1): 3049, 2991, 2978, 2908, 2164, 1585, 1483, 1436, 1334, 1321, 1190, 1159, 1112, 1028, 997, 923, 910, 850, 786, 744, 719, 688, 503, 491, 443, 432, 418.
ЯМР 1H (ДМСО-d6; 600 МГ; δ, м.д.): 3.15 (д., 3H, JH–P = 14.61 Гц, −CH3), 7.79–7.76 (м., 12H, аром. m- и o-H), 7.91–7.89 (м., 3H, аром. p-H). ЯМР 13С (ДМСО-d6; 151 МГц; δ, м.д.): 7.26 (д., СH3, JC–P = 56.07 Гц), 102.45 (СN), 119.86 (д., Сi, JC–P = 88.17 Гц), 130.10 (д., Сo, JC–P = 13.00 Гц), 133.22 (д., Сm, JC–P = 10.75 Гц), 134.82 (д., Сp, JC–P = = 3.16 Гц).
III: темно-красные кристаллы, выход 93%, Тпл = = 128°С.
ИК-спектр (ν, см−1): 3059, 2900, 2866, 2254, 2160, 1585, 1483, 1436, 1382, 1342, 1317, 1247, 1236, 1188, 1163, 1111, 1026, 995, 842, 827, 771, 752, 740, 719, 688, 549, 499, 493, 459, 445, 420.
ЯМР 1H (ДМСО-d6; 600 МГц; δ, м.д.): 5.70 (д., 2H, JH–P = 15.87 Гц, −CH2CN), 7.87–7.83 (м., 12H, аром. m- и o-H), 8.02–8.00 (м., 9H, аром. p-H). ЯМР 13С (ДМСО-d6; 151 МГц; δ, м.д.): 14.04 (д., С-7, JC–P = 55.05 Гц), 102.45 (CN), 112.78 (д., СN, JC–P = = 9.06 Гц), 116.11 (д., Сi, JC–P = 88.64 Гц), 130.65 (д., Сo, JC–P = 13.42 Гц), 133.75 (д., Сm, JC–P = 11.01 Гц), 136.11 (д., Сp, JC–P = 3.07 Гц).
ИК-спектры комплексов I−III регистрировали на ИК-спектрометре Shimadzu IR Affinity-1S в области 4000–400 см–1 (таблетки KBr). Спектры ЯМР 1Н (600 МГц), 13С (151 МГц) регистрировали на ЯМР-спектрометре Bruker AVANCE NEO в ДМСО-d6. Для спектров ЯМР 1Н и 13С использовали в качестве внутреннего стандарта сигналы растворителя.
РСА кристаллов I−III проведен на дифрактометре D8 Quest фирмы Bruker (MoKα-излучение, λ = 0.71073 Å, графитовый монохроматор) при 293 К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [21]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [22] и OLEX2 [23]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положения атомов водорода определены геометрически по модели “наездника”. Кристаллографические данные и результаты уточнения структур приведены в табл. 1, основные длины связей и валентные углы – в табл. 2.
Таблица 1.
Кристаллографические данные, параметры эксперимента и уточнения структур I–III
| Параметр | Значение | ||
|---|---|---|---|
| I | II | III | |
| М | 989.06 | 780.11 | 805.12 |
| Сингония | Моноклинная | Моноклинная | Триклинная |
| Т, K | 293.15 | 293.15 | 293.15 |
| Пр. гр. | P21/c | P21/c | $P\bar {1}$ |
| a, Å | 12.870(7) | 11.225(6) | 8.681(3) |
| b, Å | 15.510(6) | 12.300(4) | 12.433(7) |
| c, Å | 16.600(6) | 17.280(5) | 13.016(6) |
| α, град | 90.00 | 90.00 | 66.61(2) |
| β, град | 104.91(2) | 92.764(17) | 84.32(2) |
| γ, град | 90.00 | 90.00 | 70.89(2) |
| V, Å3 | 3202(3) | 2383.0(16) | 1217.5(10) |
| Z | 4 | 4 | 2 |
| ρ(выч.), г/см3 | 2.051 | 2.174 | 2.196 |
| μ, мм−1 | 7.367 | 8.840 | 8.656 |
| F(000) | 1832.0 | 1432.0 | 740.0 |
| Размер кристалла, мм | 0.23 × 0.18 × 0.15 | 0.3 × 0.15 × 0.08 | 0.22 × 0.19 × 0.12 |
| 2θ, град | 5.72–58.54 | 6.62–67.58 | 5.92–80.7 |
| Интервалы индексов отражений | –17 ≤ h ≤ 17, –21 ≤ k ≤ 21, –22 ≤ l ≤ 22 |
–17 ≤ h ≤ 17, –18 ≤ k ≤ 19, –27 ≤ l ≤ 26 |
–15 ≤ h ≤ 15, –22 ≤ k ≤ 22, –23 ≤ l ≤ 23 |
| Всего отражений | 78 498 | 88 941 | 103 809 |
| Независимых отражений | 8664 (Rint = 0.0422) |
9510 (Rint = 0.0438) |
15 357 (Rint = 0.0623) |
| Отражений с I > 2σ(I) | 6450 | 6193 | 7476 |
| Число уточняемых параметров | 329 | 245 | 265 |
| GOOF | 1.040 | 1.009 | 1.008 |
| R-факторы по F 2 > 2σ(F 2) |
R1 = 0.0490, wR2 = 0.1136 |
R1 = 0.0440, wR2 = 0.0917 |
R1 = 0.0530, wR2 = 0.0806 |
| R-факторы по всем отражениям | R1 = 0.0719, wR2 = 0.1286 |
R1 = 0.0849, wR2 = 0.1084 |
R1 = 0.1465, wR2 = 0.1000 |
| Остаточная электронная плотность (max/min), e/Å3 | 3.56/–2.96 | 2.29/–2.55 | 1.36/–1.50 |
Таблица 2.
Основные длины связей и валентные углы в структурах I−III*
| Связь | Длина, Å | Угол | ω, град |
|---|---|---|---|
| I | |||
| Au(1)–I(1) | 2.6112(10) | I(2)Au(1)I(1) | 176.88(3) |
| Au(1)–I(2) | 2.5977(10) | C(8)Au(1)I(1) | 89.6(3) |
| Au(1)–C(8) | 2.001(8) | C(8)Au(1)I(2) | 90.2(3) |
| Au(1)–C(9) | 1.999(9) | C(9)Au(1)I(1) | 91.1(2) |
| Sb(1)–C(1) | 2.084(7) | C(9)Au(1)I(2) | 89.1(2) |
| Sb(1)–C(21) | 2.088(7) | C(9)Au(1)C(8) | 179.2(4) |
| Sb(1)–C(31) | 2.093(8) | C(1)Sb(1)C(21) | 109.2(3) |
| Sb(1)–C(11) | 2.098(8) | C(1)Sb(1)C(31) | 109.8(3) |
| N(1)–C(8) | 1.133(11) | C(1)Sb(1)C(11) | 109.9(3) |
| N(2)–C(9) | 1.133(11) | C(21)Sb(1)C(31) | 106.4(3) |
| C(34)–C(37) | 1.526(14) | C(21)Sb(1)C(11) | 112.5(3) |
| C(4)–C(7) | 1.497(10) | C(31)Sb(1)C(11) | 108.9(3) |
| II | |||
| Au(1)–I(1) | 2.6030(8) | I(1)Au(1)I(2) | 177.656(18) |
| Au(1)–I(2) | 2.6118(7) | C(9)Au(1)I(1) | 90.92(16) |
| Au(1)–C(9) | 2.002(6) | C(9)Au(1)I(2) | 91.38(16) |
| Au(1)–C(8) | 2.026(6) | C(9)Au(1)C(8) | 178.7(2) |
| P(1)–C(11) | 1.796(4) | C(8)Au(1)I(1) | 88.33(16) |
| P(1)–C(21) | 1.787(5) | C(8)Au(1)I(2) | 89.38(16) |
| P(1)–C(1) | 1.798(5) | C(11)P(1)C(1) | 108.4(2) |
| P(1)–C(7) | 1.791(5) | C(21)P(1)C(11) | 110.8(2) |
| N(2)–C(9) | 1.132(7) | C(21)P(1)C(1) | 109.4(2) |
| N(1)–C(8) | 1.075(8) | C(21)P(1)C(7) | 108.5(2) |
| C(4)–C(3) | 1.364(10) | C(7)P(1)C(11) | 109.9(2) |
| C(1)–C(2) | 1.379(7) | C(7)P(1)C(1) | 109.9(3) |
| III | |||
| Au(1)–I(1)1 | 2.6199(11) | I(1)1Au(1)I(1) | 180.000(14) |
| Au(1)–I(1) | 2.6199(11) | C(9)1Au(1)I(1)1 | 90.51(12) |
| Au(1)–C(9) | 2.004(4) | C(9)Au(1)I(1)1 | 89.49(12) |
| Au(1)–C(9)1 | 2.004(4) | C(9)1Au(1)I(1) | 89.49(12) |
| Au(2)–I(2)2 | 2.6194(11) | C(9)Au(1)I(1) | 90.51(12) |
| Au(2)–I(2) | 2.6194(11) | C(9)1Au(1)C(9) | 180.0 |
| Au(2)–C(10) | 2.008(4) | I(2)2Au(2)I(2) | 180.0 |
| Au(2)–C(10)2 | 2.008(4) | C(10)2Au(2)I(2)2 | 90.30(12) |
| P(1)–C(11) | 1.790(3) | C(10)Au(2)I(2)2 | 89.70(12) |
| P(1)–C(1) | 1.781(3) | C(10)2Au(2)I(2) | 89.70(12) |
| P(1)–C(21) | 1.786(3) | C(10)u(2)I(2) | 90.30(12) |
| P(1)–C(7) | 1.826(3) | C(10)Au(2)C(10)2 | 179.999(1) |
| N(1)–C(9) | 1.137(5) | C(11)P(1)C(7) | 110.26(16) |
| N(3)–C(8) | 1.137(5) | C(1)P(1)C(11) | 108.76(16) |
| N(2)–C(10) | 1.120(5) | C(1)P(1)C(21) | 110.21(15) |
| C(7)–C(8) | 1.452(5) | C(1)P(1)C(7) | 110.41(16) |
| C(2)–C(1) | 1.388(5) | C(21)P(1)C(11) | 111.65(15) |
| C(1)–C(6) | 1.379(5) | C(21)P(1)C(7) | 105.53(16) |
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (CIF files CCDC № 1901681 (I), 1912903 (II), 1912919 (III); deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk/ structures).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Комплекс I синтезировали из дицианодииодоаурата калия и хлорида тетра(пара-толил)сурьмы в водном растворе:
Получение комплексов II и III, содержащих фосфорорганические катионы, осуществляли по аналогичной методике из дицианодииодоаурата калия и бромида или хлорида алкилтрифенилфосфония соответственно:
После испарения воды, высушивания твердого остатка и перекристаллизации его из смеси ацетонитрила с этиловым спиртом получали устойчивые на воздухе кристаллы красного цвета.
ИК-спектроскопия – надежный метод для идентификации органических соединений, содержащих цианогруппу, так как область поглощения данной группы находится в достаточно узком интервале значений от 2200 до 2000 см−1 [24]. Поэтому цианиды легко идентифицировать по наличию полосы средней интенсивности в указанной области. Так, полосы поглощения валентных колебаний связи C≡N обнаружены при 2156, 2164, 2160 см−1 в спектрах соединений I, II и III соответственно. В ИК-спектре соединения I при 480 см−1 наблюдается интенсивная полоса поглощения валентных колебаний связей Sb–C, также присутствуют полосы поглощения асимметричных и симметричных валентных колебаний метильных групп при 2916 и 2862 см−1 соответственно. Полоса поглощения связей P−Ph в спектрах соединений II и III зарегистрирована при 1436 см−1 в обоих случаях, что соответствует области поглощения 1450−1435 см−1, приведенной в [24].
В спектре ЯМР 1H соединения I наблюдаются характерные для толильного фрагмента дублеты m- и o-протонов при 7.48 и 7.63 м.д. соответственно, а также синглет метильной группы при 2.41 м.д. Сигналы протонов фенильных колец комплексов алкилтрифенилфосфония представляют собой мультиплеты р-протонов при 7.91–7.89 (II) и 8.02–8.00 (III) м.д., m- и о-протонов при 7.79–7.76 (II) и 7.87–7.83 (III) м.д. Протоны алкильных фрагментов комплексов II и III обнаруживаются в спектрах ЯМР Н1 в виде дублетов с расщеплением на атоме фосфора при 3.15 и 5.70 м.д. с КССВ 14.61 и 15.87 Гц соответственно. В спектре ЯМР 13С комплекса I все сигналы наблюдаются в виде синглетов, в спектрах ЯМР 13С комплексов II и III – в виде дублетов с соответствующими константами за счет спин-спинового взаимодействия с атомом фосфора. Углерод цианогруппы обнаруживается при 102.41 (I), 102.45 (II) и 102.45 (III) м.д. Сигнал углерода цианогруппы при катионе представляет собой дублет при 112.78 м.д. с КССВ 9.06 Гц.
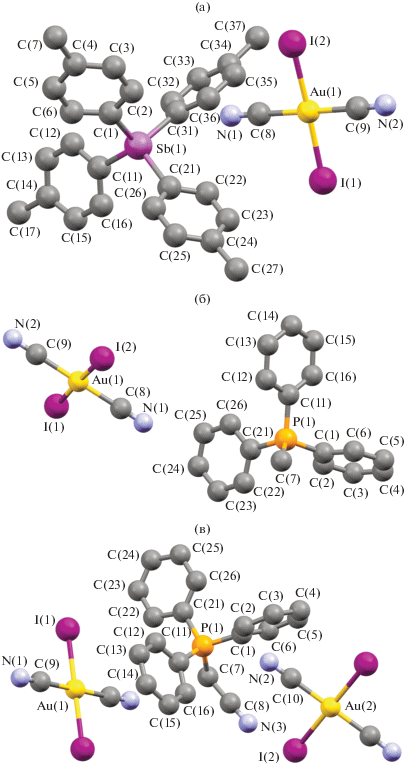
По данным РСА, соединения I–III представляют собой ионные комплексы с тетраэдрической координацией центрального атома в катионе и плоским дицианодииодоауратным анионом. В кристалле III присутствуют по два типа центросимметричных кристаллографически независимых дицианодииодоауратных анионов (рис. 1).
Тетраэдрическая координация атомов сурьмы в катионе соединения I и фосфора – в II и III искажена в незначительной степени. Углы CSbC или CPC отклоняются от теоретического значения и варьируются в пределах 106.4(3)°−112.5(3)° (I), 108.4(2)°−110.8(2)° (II), 105.53(16)°−111.65(15)° (III). В катионе тетра(пара-толил)сурьмы среднее значение длин связей Sb–C составляет 2.091(8) Å. В фосфорорганическом катионе комплекса II расстояния P−С близки между собой вне зависимости от природы заместителя (1.796(4) (Ph), 1.787(5) (Ph), 1.798(5) (Ph), 1.791(5) (СH3) Å). Наличие цианогруппы в катионе структуры III обуслoвливает большую длину связи P–CAlk (1.826(3) Å) по сравнению с расстояниями P–CPh (1.790(3), 1.781(3), 1.786(3) Å). Квадратные анионы [Au(CN)2I2]− отклоняются от плоской конфигурации незначительно, углы СAuC равны 179.2(4)° (I), 178.7(2)° (II), 180.0°, 179.999(1)° (III). Расстояния Au−C в анионах I, II и III меньше суммы ковалентных радиусов атомов золота и углерода (2.03 Å [25]) и составляют соответственно 2.001(8), 1.999(9) Å (I), 2.002(6), 2.026(6) Å (II), 2.004(4), 2.004(4) и 2.008(4), 2.008(4) Å (III). Длины связей Au−I равны 2.6112(10), 2.5977(10) Å (I), 2.6030(8), 2.6118(7) Å (II), 2.6199(11) и 2.6194(11) Å (III).
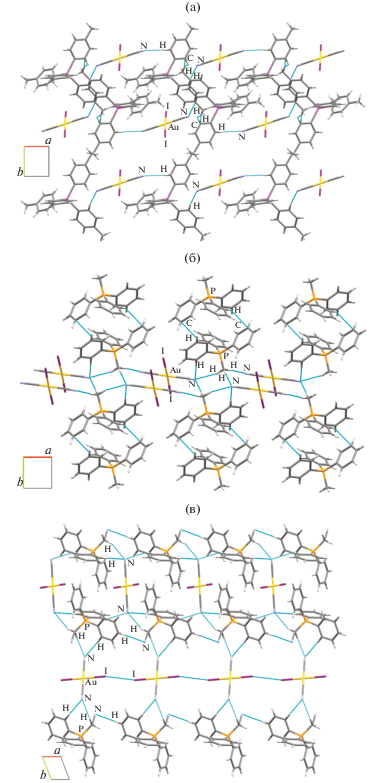
Образование пространственной сетки кристаллов обусловлено слабыми водородными связями СN⋅⋅⋅Н−С между катионами и анионами (2.39, 2.59 Å (I), 2.70, 2.48, 2.52, 2.68 Å (II), 2.73, 2.50, 2.67, 2.44 Å (III)). Катионы комплексов I и II связаны между собой C–H-π-взаимодействиями, расстояние от атома водорода до плоскости бензольного кольца составляет 2.77 и 2.82 Å соответственно (рис. 2а, 2б). Катионы комплекса III взаимодействуют между собой посредством водородных связей СPh–H⋅⋅⋅NCAlk (2.72 Å). В данном комплексе анионы одного из двух типов также взаимодействуют между собой, образуя 1D цепочки вдоль направления кристаллографической оси а благодаря взаимодействиям I⋅⋅⋅I (рис. 2в). Расстояния I⋅⋅⋅I меньше суммы ван-дер-ваальсовых радиусов атомов иода (4.30 Å) и составляют 3.93 Å, что указывает на взаимодействия галоген⋅⋅⋅галоген. Как показано на рис. 2в, анионы одного из двух типов ориентированы таким образом, что иодидные лиганды образуют ступенчатую цепь. Это, в свою очередь, приводит к параллельному выравниванию групп [Au(CN)2I2]− вдоль направления кристаллографической оси а. Углы Au–I⋅⋅⋅I между связанными парами анионов составляют 141.90°, что обеспечивает ступенчатый мотив. Данное I⋅⋅⋅I взаимодействие относится к типу I, так как разность углов Au–I⋅⋅⋅I равна 0° [26].
Таким образом, дицианодииодоауратные комплексы тетра(пара-толил)сурьмы и алкилтрифенилфосфония, полученные из соответствующих галогенидов тетра(пара-толил)сурьмы, алкилтрифенилфосфония и дицианодииодоаурата калия в воде, имеют ионное строение с мономерными дицианодииодоауратными анионами. Структурная организация комплекса III обусловлена не только водородными связями с участием цианогруппы, как и в других комплексах, но и галоген–галогеновыми взаимодействиями между атомами иода.
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
Xiaobo L., Patterson H. // Materials. 2013. V. 6. P. 2595. https://doi.org/10.3390/ma6072595
Dechambenoit P., Ferlay S., Kyritsakas N. et al. // Cryst-EngComm. 2011. V. 13. P. 1922. https://doi.org/10.1039/C0CE00607F
Hill J.A., Thompson A.L., Goodwin A.L. // J. Am. Chem. Soc. 2018. V. 138. P. 5886. https://doi.org/10.1021/jacs.5b13446
Assefa Z., Haire R.G., Sykora R.E. // J. Solid State Chem. 2008. V. 181. P. 382. https://doi.org/10.1016/j.jssc.2007.11.036
Brown M.L., Ovens J.S., Leznoff D.B. // Dalton Trans. 2017. V. 46. P. 7169. https://doi.org/10.1039/C7DT00942A
Chorazy S., Wyczesany M., Sieklucka B. // Molecules. 2017. V. 22. P. 1902. https://doi.org/10.3390/molecules22111902
Shaw C.F. // Chem. Rev. 1999. V. 99. № 9. P. 2589. https://doi.org/10.1021/cr980431o
Roberts R.J., Le D., Leznoff D.B. // Inorg. Chem. 2017. V. 56. № 14. P. 7948. https://doi.org/10.1021/acs.inorgchem.7b00735
Rawashdeh-Omary M.A., Omary M.A., Shankle G.E. et al. // J. Phys. Chem. B. 2000. V. 104. № 26. P. 6143. https://doi.org/10.1021/jp000563x
Colis J.C.F., Larochelle C., Fernández E.J. et al. // J. Phys. Chem. B. 2005. V. 109. № 10. P. 4317. https://doi.org/10.1021/jp045868g
Assefaa Z., Kalachnikova K., Hairec R.G. et al. // J. Solid State Chem. 2007. V. 180. P. 3121. https://doi.org/10.1016/j.jssc.2007.08.032
Ovens J.S., Leznoff D.B. // Chem. Mater. 2015. V. 27. № 5. P. 1465. https://doi.org/10.1021/cm502998w
Ovens J.S., Leznoff D.B. // Dalton Trans. 2011. V. 40. P. 4140. https://doi.org/10.1039/c0dt01772h
Шарутин В.В., Попкова М.А., Тарасова Н.М. // Вест. Южно-Уральского гос. ун-та. Сер. хим. 2018. Т. 10. № 1. С. 55 (Sharutin V.V., Popkova M.A., Tarasova N.M. // Bull. South Ural State Univ. Ser. Chem. 2018. V. 10. № 1. P. 55). https://doi.org/10.14529/chem180107
Sharutin V.V., Sharutina O.K., Popkova M.A. // Russ. J. Inorg. Chem. 2019. V. 64. № 6. P. 607. https://doi.org/10.1134/S0036023619060147
Cambridge Crystallographic Data Center. 2018. http://www.ccdc.cam.ac.uk.
Ovens J.S., Geisheimer A.R., Bokov A.A. et al. // Inorg. Chem. 2010. V. 49. P. 9609. https://doi.org/10.1021/ic101357y
Pitteri B., Bortoluzzi M., Bertolasi V. // Transition Met. Chem. 2008. V. 33. P. 649. https://doi.org/10.1007/s11243-008-9092-9
Marangoni G., Pitteri B., Bertolasi V. et al. // Dalton Trans. 1987. № 1. P. 2235. https://doi.org/10.1039/DT9870002235
Ovens J.S., Truong K.N., Leznoff D.B. // Dalton Trans. 2012. V. 41. P. 1345. https://doi.org/10.1039/c1dt11741f
SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Madison (WI, USA): Bruker AXS Inc., 1998.
SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Madison (WI, USA): Bruker AXS Inc., 1998.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. -Appl. Cryst. 2009. V. 42. P. 339. https://doi.org/10.1107/S0021889808042726
Преч Э., Бюльманн Ф., Аффольтер К. Определение строения органических соединений. М.: Мир, 2006. 440 с.
Бацанов С.С. // Журн. неорган. химии. 1991. Т. 36. № 12. С. 3015 (Batsanov S.S. // Russ. J. Inorg. Chem. 1991. V. 3. P. 1694).
Mukherjee A., Tothadi S., Desiraju G.R. // Accounts Chem. Res. 2014. V. 47. № 8. P. 2514. https://doi.org/10.1021/ar5001555
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия