Координационная химия, 2021, T. 47, № 4, стр. 237-244
Нитратные комплексы кадмия с мостиковым 3-аминохинолином молекулярного и полимерного строения: синтез, структура и люминесцентные свойства
В. В. Ковалев 1, *, Ю. В. Кокунов 1, М. А. Шмелев 1, Ю. К. Воронина 1, М. А. Кискин 1, Л. Д. Попов 2, И. Л. Еременко 1, 3
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
2 Южный федеральный университет
Ростов-на-Дону, Россия
3 Институт элементоорганических соединений им. А.Н. Несмеянова РАН
Москва, Россия
* E-mail: kovavlad@igic.ras.ru
Поступила в редакцию 10.07.2020
После доработки 29.09.2020
Принята к публикации 02.10.2020
Аннотация
При взаимодействии Cd(NO3)2 ⋅ 4H2O c 3-аминохинолином (3-Аq), в зависимости от соотношения реагентов и состава среды, получены молекулярный и полимерный комплексы [Cd(NO3)2(H2O)(3-Аq)] ⋅ 2MeCN (I) и {[Cd(NO3)2(3-Аq)2] ⋅ MeCN}n (II) соответственно. Соединения I, II изучены методами элементного анализа, РCA (CIF files CCDC № 2015059 (I), 2015060 (II)), РФА и люминесценции. В обоих случаях окружение атома кадмия представляет собой пентагональную бипирамиду. Молекулы 3-Аq в димере I являются мостиковыми лигандами, в полимере наряду с указанной функцией имеет место монодентатный характер связывания с Cd(II). Наличие Н-связей между атомами H NH2-группы и атомом N сольватной молекулы MeCN и атомом O NO3-группы приводит к образованию трехмерной супрамолекулярной сетки, которая дополнительно усилена межмолекулярными стекинг-взаимодействиями между ароматическими фрагментами 3-Аq соседних молекул. Оба соединения люминесцируют в красной области спектра. По сравнению со свободным 3-Аq смещение полос эмиссии димера I и полимера II в этой области составляет 93 и 38 нм соответственно.
В последние годы синтез новых координационных полимерных соединений вызывает повышенный интерес. Основные цели в этой области – получение соединений с полезными физическими свойствами и построение корреляций структура–свойства. Топология комплексов во многом зависит от координационного поведения ионов металлов, природы противоионов, электронных и геометрических параметров лигандов, поэтому особый интерес представляет ион кадмия, координационные числа (КЧ) которого изменяются от 4 до 8. При выборе органического лиганда основное внимание уделяется N- и N,O-донорным гетероциклическим соединениям, в частности производным пиридина, что обусловлено устойчивостью образующихся соединений и высокой вероятностью реализации лиганд-центрированной люминесценции.
Хинолини его производные часто используются для получения соединений, обладающих люминесцентными свойствами [1–3]. 3-Аминохинолин (3-Аq) способен связываться ионами металла обеими N-донорными функциональными группами (атомами N гетероцикла и аминогруппы). Два объединенных ароматических цикла могут участвовать в образовании π–π-стэкинг-взаимодействий. Богатая π-система хинолина создает условия для реализации люминесцентных свойств координационных соединений с его участием. Слабые нековалентные взаимодействия (π–π-стэкинг и водородные связи) существенно влияют на образование структуры, растворимость, термическое поведение, электронные и оптические свойства соединения. Наличие NH2-группы и π-системы в комплексах с 3-Аq создает условия для образования межмолекулярных взаимодействий в кристаллах, придавая им и нелинейно-оптические свойства.
Комплексы кадмия(II) вызывают повышенный интерес из-за его способности одновременно образовывать связи с различными донорами, проявляющими разнообразные способы координации. Данные о соединениях кадмия с 3-Аq ограничены работой, в которой описаны синтез и строение комплекса [CdI2(3-Аq)2] с тетраэдрической координацией иона кадмия с монодентатно связанными молекулами 3-Аq [4]. Аналогичное строение имеет комплекс [ZnCl2(3-Аq)2] ⋅ H2O [5]. В обоих случаях координация 3-Аq осуществляется через гетероциклический атом азота. Значительно больше информации о соединениях 3-аминопиридина (3-Аmpy) c ионами кадмия, в которых 3-Аmpy проявляет как монодентатную, так и бидентатно-мостиковую функции, координируясь к иону Cd2+ обоими атомами азота. Характер присоединения 3-Аmpy зависит от состава соединения, координационной сферы иона металла и соотношения 3-Аmpy : Cd в реакционной смеси.
В некоторых координационных полимерах соотношение связывающий лиганд : металл сопровождается изменением его размерности [6]. Ранее мы на примере координационных полимерных соединений нитрата кадмия с 2-амино-5-бромпиридином (Аbp) [7] показали, что изменение соотношения Аbp : Cd приводит к росту размерности продукта реакции от биядерного комплекса к 1D-координационному полимеру.
С целью расширения информации о получении и строении соединений кадмия с 3-Аq и определения факторов, влияющих на характер его координации, мы синтезировали димерный и полимерный соединения нитрата кадмия с 3-Аq с разным соотношением металл : лиганд, определили их состав, структуру и изучили спектры люминесценции.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали Cd(NO3)2 ⋅ 4H2O (“х. ч.”) и 3-аминохинолин (97%; Aldrich), ацетонитрил и метиловый спирт без дополнительной очистки (Химмед).
Синтез [Cd(NO3)2(H2O)(3-Аq)] ⋅ 2MeCN (I). Навески Cd(NO3)2 ⋅ 4H2O (0.68 г, 2.22 ммоль) и 3-Аq (0.32 г, 2.22 ммоль) раздельно растворяли в 10 и 8 мл MeCN соответственно. Растворы смешивали, нагревали до 30–35°С и после охлаждения до комнатной температуры отфильтровывали. Полученный фильтрат выдерживали 2 ч в условиях медленной кристаллизации продукта реакции, затем образовавшиеся призматические кристаллы отделяли декантацией жидкой фазы и высушивали на воздухе. По данным элементного анализа, кристаллы отвечали составу I.
Синтез {[Cd(NO3)2(3-Аq)2] ⋅ MeCN}n (II). Реакцию нитрата кадмия с двукратным избытком 3-Аq и выделение продукта реакции проводили аналогичным для I образом, но в качестве растворителя использовали смесь ацетонитрила с метанолом в объемном соотношении 3 : 1. После окончания реакции раствор фильтровали и выдерживали фильтрат в течение 3 сут в условиях медленного удаления растворителя. Выделенные кристаллы, по данным элементного анализа, отвечали составу комплекса II
.РСА монокристалла соединений I и II выполнен на дифрактометре Bruker SMART APEX II, оборудованном CCD-детектором (MoKα, λ = 0.71073 Å, графитовый монохроматор) [8]. Введена полуэмпирическая поправка на поглощение [9]. Структура расшифрована прямыми методами и уточнена полноматричным МНК в анизотропном приближении для всех неводородных атомов. Атомы водорода при атомах углерода органических лигандов генерированы геометрически и уточнены в модели “наездника”. Расчеты проведены по комплексу программ SHELX-2014/2018 [10]. Кристаллографические параметры и детали уточнения структур для I и II приведены в табл. 1, основные длины связей и углы – в табл. 2.
Таблица 1.
Кристаллографические параметры и детали уточнения структур I и II
| Параметр | Значение | |
|---|---|---|
| I | II | |
| Брутто-формула | C22H26N10O14Cd2 | C20H19N7O6Cd |
| M | 879.33 | 565.82 |
| Т, K | 150(2) | |
| Сингония | Триклинная | |
| Пр. гр. | P1 | |
| Размер кристалла, мм | 0.24 × 0.20 × 0.18 | 0.40 × 0.34 × 0.28 |
| Цвет | Бесцветные | Бесцветные |
| a, Å | 8.3365(2) | 6.5810(12) |
| b, Å | 10.4583(3) | 9.2749(18) |
| c, Å | 10.4888(3) | 17.932(6) |
| α, град | 111.0900(10) | 80.779(11) |
| β, град | 94.8920(10) | 89.001(9) |
| γ, град | 112.9110(10) | 87.983(10) |
| V, Å3 | 758.41(4) | 1079.6(4) |
| Z | 1 | 2 |
| ρ(выч.), г/см3 | 1.925 | 1.741 |
| μ, мм–1 | 1.487 | 1.066 |
| F(000) | 436 | 568 |
| Область сбора данных по θ, град | 2.34–28.99 | 2.66–30.56 |
| Интервалы индексов отражений | –11 ≤ h ≤ 11, –14 ≤ k ≤ 14, –14 ≤ l ≤ 14 |
–8 ≤ h ≤ 9, –13 ≤ k ≤ 11, –25 ≤ l ≤ 25 |
| Tmin/Tmax | 0.410/0.494 | 0.608/0.746 |
| Число измерено отражений | 9191 | 12 664 |
| Число независимых отражений | 4062 | 6536 |
| Число отражений с I > 2σ(I) | 3158 | 6101 |
| Rint | 0.0214 | 0.0217 |
| Количество переменных уточнения | 234 | 324 |
| GООF | 0.996 | 1.080 |
| R-факторы по F 2 > 2σ(F 2) | R1 = 0.0220 wR2 = 0.0490 |
R1 = 0.0317 wR2 = 0.0728 |
| R-факторы по всем отражениям | R1 = 0.0245 wR2 = 0.0499 |
R1 = 0.0355 wR2 = 0.0744 |
| Δρmin/Δρmax, е/Å3 | –0.531/0.475 | –1.179/1.099 |
Таблица 2.
Основные длины связей (Å), углы (град) и параметры водородных связей в I и II*
| I | II | ||
|---|---|---|---|
| Связь | d, Å | Связь | d, Å |
| Cd(1)-O(4) | 2.2771(14) | Cd(1)–O(1) | 2.466(2) |
| Cd(1)-O(21) | 2.3969(13) | Cd(1)–O(2) | 2.510(2) |
| Cd(1)-O(22) | 2.5439(14) | Cd(1)–O(4) | 2.3552(17) |
| Cd(1)-O(31) | 2.3765(14) | Cd(1)–O(5) | 2.5026(18) |
| Cd(1)-O(32) | 2.4525(14) | Cd(1)–N(1) | 2.3426(17) |
| Cd(1)-N(1) | 2.3240(15) | Cd(1)–N(2)a | 2.3818(19) |
| Cd(1)-N(4)a | 2.3877(16) | Cd(1)–N(4) | 2.419(2) |
| Угол | ω, град | Угол | ω, град |
| O(4)Cd(1)N(1) | 108.73(5) | N(1)Cd(1)O(4) | 140.91(6) |
| O(4)Cd(1)O(31) | 89.10(5) | N(1)Cd(1)N(2)a | 92.80(6) |
| N(1)Cd(1)O(31) | 127.63(5) | O(4)Cd(1)N(2)a | 89.27(6) |
| O(4)Cd(1)N(4)a | 160.95(6) | N(1)Cd(1)N(4) | 89.71(7) |
| N(1)Cd(1)N(4)a | 88.52(5) | O(4)Cd(1)N(4) | 84.81(6) |
| O(31)Cd(1)N(4)a | 86.43(5) | N(2)Cd(1)N(4)a | 173.21(6) |
| O(4)Cd(1)O(21) | 82.83(5) | N(1)Cd(1)O(1) | 95.95(6) |
| N(1)Cd(1)O(21) | 99.23(5) | O(4)Cd(1)O(1) | 122.05(6) |
| O(31)Cd(1)O(21) | 132.32(5) | N(2)Cd(1)O(1)a | 100.32(7) |
| N(4)Cd(1)O(21)a | 86.52(5) | N(4)Cd(1)O(1) | 85.68(7) |
| O(4)Cd(1)O(32) | 80.53(5) | N(1)Cd(1)O(5) | 88.06(6) |
| N(1)Cd(1)O(32) | 80.85(5) | N(2)Cd(1)O(5)a | 86.56(6) |
| N(4)Cd(1)O(32)a | 111.04(5) | N(4)Cd(1)O(5) | 87.23(7) |
| O(21)Cd(1)O(32) | 162.41(5) | O(1)Cd(1)O(5) | 171.83(6) |
| O(4)Cd(1)O(22) | 81.61(5) | N(1)Cd(1)O(2) | 147.00(6) |
| N(1)Cd(1)O(22) | 149.16(5) | O(4)Cd(1)O(2) | 71.88(6) |
| O(31)Cd(1)O(22) | 80.18(5) | N(2)Cd(1)O(2)a | 90.90(7) |
| N(4)Cd(1)O(22)a | 79.38(5) | N(4)Cd(1)O(2) | 90.42(7) |
| O(32)Cd(1)O(22) | 129.96(4) | O(5)Cd(1)O(2) | 124.91(6) |
| d(H…A), d(D…A), ∠DHA | |||
| O(4)–H…O(21)b | 2.18, 2.901, 176.7 | N(2)–H…N(3)b | 2.30, 3.172, 173.5 |
| O(4)–H…O(33)c | 2.00, 2.785, 167.6 | N(2)–H…N(1S) | 2.19, 3.001, 171.8 |
| N(4)–H…O(23)d | 2.10, 2.948, 159.6 | N(4)–H…O(2)c | 2.42, 3.236, 158.0 |
| N(4)–H…N(13) | 2.29, 3.093, 166.9 | ||
Полный набор рентгеноструктурных данных депонирован в Кембриджском банке структурных данных (CCDC № 2015059 (I), 2015060 (II); http://www.ccdc.cam.ac.uk/data_request/cif).
РФА мелкокристаллических образцов I и II выполнен на дифрактометре Bruker D8 Advance (CuKα, Ni-фильтр, LYNXEYE детектор, геометрия на отражение).
Спектры возбуждения и эмиссии твердых образцов регистрировали при комнатной температуре в видимом диапазоне спектра с использованием спектрометра Perkin-Elmer LS-55.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Соединение I кристаллизуется в виде сольвата с двумя молекулами MeCN в триклинной пространственной группе $P\bar {1}$, центр инверсии лежит между двумя атомами кадмия, связанными в биядерную молекулу двумя мостиковыми молекулами 3-Аq (рис. 1а). Каждый атом кадмия достраивает свое окружение (CdN2O5) до пентагональной бипирамиды координацией двух хелатных анионов ${\text{NO}}_{{\text{3}}}^{--}$ и молекулы воды (табл. 2). Экваториальные позиции заняты атомами O NO3-групп и пиридиного атома N молекулы 3-Аq. Между атомами H NH2-группы и атомом N сольватной молекул MeCN и атомом O NO3-группы соседней молекулы комплекса образованы H-связи (табл. 2). Координированная молекула образует две H-связи c атомами O NO3-групп соседних молекул комплекса. Такое H-связывание приводит к образованию трехмерной супрамолекулярной сетки, которая дополнительно усилена межмолекулярными стекинг-взаимодействиями между ароматическими фрагментами 3-Аq соседних молекул (расстояние между центроидами пиридинового и бензольногоколецсоставляет 3.686 Å, кратчайшее расстояние – С(4)…С(10) (2 – x, 1 – y, 1 – z) 3.346 Å (рис. 1б).
Рис. 1.
Молекулярное строение (а) и фрагмент кристаллической упаковки (б) комплекса I. Атомы H при атомах углерода 3-Аq не показаны, пунктиром обозначены межмолекулярные H-связи.
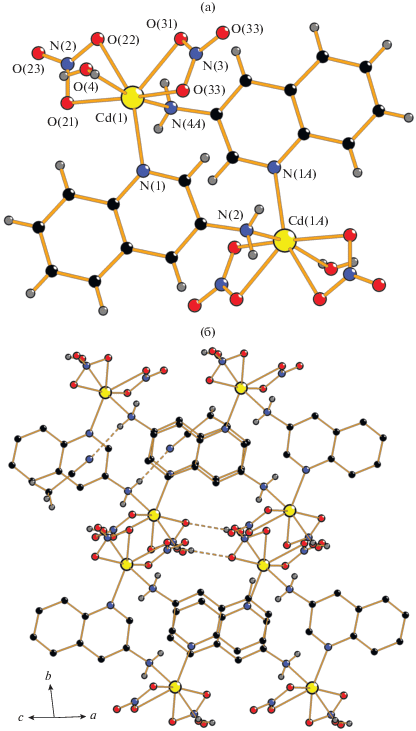
Соединение II кристаллизуется в виде сольвата с одной молекулой MeCN в триклинной пространственной группе $P\bar {1}$. Центр инверсии располагается между атомами Cd двух полимерных цепочек. Элементарным звеном координационного полимера является моноядерный фрагмент, состоящий из двух хелатных анионов ${\text{NO}}_{{\text{3}}}^{--},$ монодентатной молекулы 3-Аq, координированной атомом NH2-группы и двух атомов N двух мостиковых молекул 3-Аq (рис. 2а, табл. 2). Геометрия окружения атома Cd (CdN3O4) соответствует пентагональной бипирамиде с атомами O и атомом N пиридинового цикла в экваториальных позициях. Атомы H NH2-группы мостиковой молекулы Аq участвуют в образовании H-связей с атомами N сольватной молекулы MeCN и некоординированного пиридинового цикла соседней цепочки (табл. 2); также наблюдается внутримолекулярная H-связь между атомом H NH2-группы монодентатно координированной молекулы 3-Аq и атомом O NO3-группы. Дополнительно цепочки связаны между собой межмолекулярными стекинг-взаимодействиями между ароматическими фрагментами 3-Аq (расстояния между центроидами ароматических колец составляют 3.587–3.778 Å, кратчайшее расстояние – N(3)…С(9) (x, –1 + y, z) 3.366 Å.
Рис. 2.
Фрагменты полимерной цепи (а) и кристаллической упаковки (б) комплекса II. Атомы H при атомах углерода 3-Аq не показаны, пунктиром обозначены межмолекулярные H-связи.
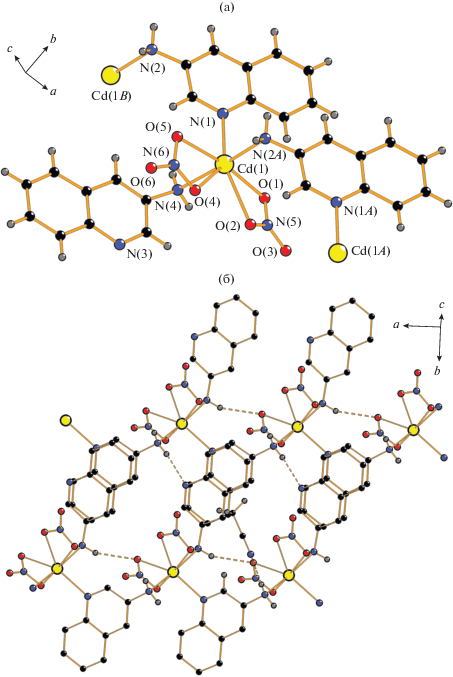
Фазовая чистота образцов I и II подтверждена методом РФА (рис. Sl).
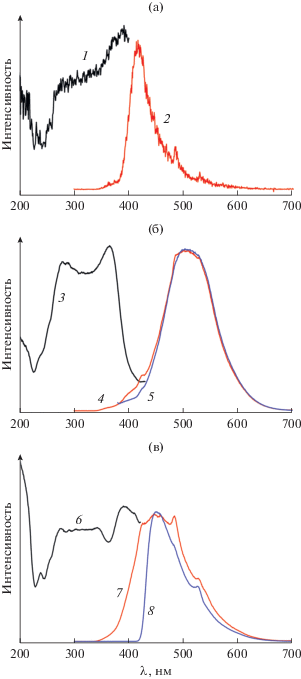
На рис. 3 представлены спектры эмиссии и возбуждения лиганда 3-Аq и комплексов I и II. Спектры эмиссии образцов содержат интенсивные широкие несимметричные линии: 417 нм (λвозб = 280 нм) для 3-Аq, 510 нм (λвозб = 280 и 365 нм) для I и 455 нм (λвозб = 275 и 390 нм) для II. Отмечено смещение полос эмиссии в красную область для I и II на 93 и 38 нм соответственно, по сравнению со свободным 3-Аq. Подобное красное смещение наблюдалось в спектрах эмиссии соединений d0-металлов с 8-аминохинолином [11–13]. Указанная эмиссия связана с π–π-внутрилигандными переходами. Смещение полосы люминесценции в красную область в спектре димера I больше, чем полимера II. Хотя в обоих случаях КЧ иона Cd равно 7, окружение у них различается: в димере I координационныe места у иона Cd занимают аминогруппы 3-Аq, в полимере II – одна NH2-группа 3-Аq и один атом O молекулы воды.
Рис. 3.
Спектры возбуждения (λэм = 417 (1), 510 (3), 455 нм (6)) и эмиссии (λвозб = 280 (2), 280 (4), 365 (5), 275 (7), 390 нм (8)) для твердых образцов 3-Аq (а), I (б) и II (в) соответственно, при комнатной температуре.
Таким образом, при взаимодействии нитрата кадмия с 3-аминохинолином при различных соотношениях реагирующих компонентов и вариации составов растворителей были получены два новых координационных соединения нитрата кадмия, в которых 3-Аq выполняет мостиковую функцию. Полученные соединения представляют собой биядерный комплекс (L : Cd = 1 : 1) и 1D-полимер (L : Cd = 2 : 1). В обоих случаях координационное число атомов кадмия равно семи, геометрия полиэдров соответствует пентагональной бипирамиде. Нитрат-анионы координированы к атомам кадмия по хелатному типу. Оба соединения люминесцируют в красной области спектра.
Авторы заявляют, что у них нет конфликта интересов.
Список литературы
Gao S., Fan R.Q., Wang M. et al. // RSA Advances. 2015. V. 5. № 54. P. 43705.
Mirzaei M., Eshtiagh-Hosseini H., Bolouri Z. et al. // Cryst. Growth. Des. 2015. V. 15. № 3. P. 1351.
Pairu M.K., Dinda J., Lu T.-H. // Polyhedron. 2007. V. 26. P. 4131.
Azam M., Al-Resayes S.I., Pallepogu R. et al. // J. Saudi Chem. Soc. 2016. V. 20. P. 120.
Azam M., Al-Resayes S.I., Pallepogu R. // Helv. Chim. Acta. 2016. V. 99. P. 20.
Nather C., Jess I., Germann L.S. et al. // Eur. J. Inorg. Chem. 2017. P. 1245.
Ковалев В.В., Кокунов Ю.В., Воронина Ю.В. и др. // Коорд. химия. 2020. Т. 46. № 6. С. 376 (Kovalev V.V., Kokunov Yu.V., Voronina Yu.K. et al. // Russ. J. Coord. Chem. 2020. V. 46. № 6. P. 420). https://doi.org/10.1134/S1070328420060032
SMART (control) and SAINT (integration). Software. Version 5.0. Madison (WI, USA): Bruker AXS Inc., 1997.
Krause L., Herbst-Irmer R., Sheldrick G.M., Stalke D. // J. Appl. Cryst. 2015. V. 48. P. 3.
Sheldrick G.M. // Acta Crystallogr. A. 2008. V. 64. P. 112.
Niu C., Wan X., Zheng X. et al. // J. Coord. Chem. 2008. V. 61. P. 1997.
Bai Y., Gao H., Dang D.-B. et al. // Synth. React. Inorg. Met.-Org. Nano-Met. Chem. 2009. V. 39. P. 518.
Xu H., Xue C., Huang R.-Y. // Synth. React. Inorg. Met.-Org. Nano-Met. Chem. 2015. V. 45. P. 1565.
Дополнительные материалы
- скачать ESM.docx
- Рис. S1. Дифрактограммы образцов I и II: порошковые (1 и 3) и теоретически рассчитанные, по данным РСА (2 и 4).
Инструменты
Координационная химия


