Координационная химия, 2022, T. 48, № 4, стр. 238-247
o-бензохиноновые комплексы кобальта, содержащие кремнийорганические радикалы: квантово-химическое исследование
А. А. Старикова 1, *, М. Г. Чегерев 1, А. Г. Стариков 1, В. И. Минкин 1
1 Научно-исследовательский институт физической и органической химии
Южного федерального университета
Ростов-на-Дону, Россия
* E-mail: aastarikova@sfedu.ru
Поступила в редакцию 24.09.2021
После доработки 14.10.2021
Принята к публикации 15.10.2021
- EDN: MSRRRE
- DOI: 10.31857/S0132344X22040053
Аннотация
На основе компьютерного моделирования (DFT UTPSSh/6-311++G(d,p)) электронного строения, геометрических параметров, энергетических характеристик и магнитных свойств моноядерных комплексов кобальта с тетрадентатными N-донорными основаниями (трис(2-пиридилметил)аминами и N,N'-ди-алкил-2,11-диаза[3.3]-(2,6)пиридинофанами) и о-бензохинонами, включающими триангуленовые кремнийорганические радикалы, предсказан парамагнетизм всех состояний изученных молекул. Установлено, что электронные конфигурации и энергетические характеристики изомеров исследованных комплексов регулируются алкильными заместителями во вспомогательных N-донорных лигандах. Выявлены соединения, обладающие потенциалом термически инициированного переключения спиновых состояний по механизмам спин-кроссовера и валентной таутомерии.
В последние десятилетия наблюдается быстрорастущий интерес к координационным соединениям, демонстрирующим переключение спиновых состояний в результате внешних воздействий (температуры, давления, облучения) [1–9]. Такие магнитно-активные металлокомплексы способны существовать в виде двух или более электронных изомеров (электромеров [10]) с различными магнитными свойствами, что создает возможности многообразного применения в устройствах молекулярной электроники и спинтроники [1–4, 7, 11–15]. Поиску перспективных би- и полистабильных молекул посвящены многочисленные научные исследования [2–9, 12–20].
К наиболее распространенному механизму магнитной бистабильности относят спин-кроссовер (СКО), который заключается в индуцируемом внешними факторами изменении спинового состояния координированного иона металла, вызванном перегруппировкой электронов внутри его валентной оболочки [21, 22]. Подходящая для реализации СКО сила поля лигандов достигается в соединениях переходных металлов с электронной конфигурацией d4–d7, в частности в комплексах железа(II/III) [23–27] и кобальта(II) [28–30] с N-донорными лигандами. Другим способом переключения спинового состояния координационных соединений является валентная таутомерия (ВТ), или редокс-изомерия, включающая обратимый внутримолекулярный перенос электрона между металлоцентром и редокс-активным лигандом [31, 32]. Этот феномен всесторонне изучен в комплексах кобальта с о-бензохиноновыми производными; имеются также примеры ВТ-переходов в соединениях иных d-металлов [32, 33], лантанидов [34] и элементов главных групп [35, 36].
Привлекательными объектами с точки зрения молекулярного магнетизма выступают гетероспиновые магнитно-активные соединения с двумя или более различными по природе парамагнитными центрами. Особый интерес представляют комплексы переходных металлов с открытой электронной оболочкой, включающие дополнительные носители спина (лиганды и/или функциональные группы) [18, 37–46]. Классическим примером радикального лиганда является о-бензохинон в семихиноновой (SQ) форме. Выполненные ранее экспериментальные [47–51] и теоретические [50–54] исследования показали, что о-бензохиноновые комплексы кобальта с N-донорными тетрадентатными основаниями способны демонстрировать СКО (LSCoII–SQ ⇄ HSCoII–SQ) и ВТ (LSCoIII–Cat ⇄ ⇄ HSCoII–SQ) перегруппировки (Cat = дианионная катехолатная форма о-бензохинона). С целью придания диамагнитному электромеру LSCoIII–Cat парамагнитных свойств были сконструированы аналогичные соединения, содержащие в четвертом положении хинонового кольца стабильный радикал (1,2,3,5-дитиадиазолил, 1,5-диметил-6-оксо-вердазил, нитронилнитроксил, ТЕМРО) [55, 56]. Согласно результатам квантово-химических расчетов, природа и способ присоединения рассмотренных радикальных заместителей не оказывают существенного влияния на способность комплексов кобальта проявлять магнитную бистабильность, обусловленную различными механизмами.
Недавно нами была теоретически изучена серия ВТ-аддуктов бис-дикетонатов кобальта с о-бензохиноновыми лигандами, содержащими триангуленовые фрагменты [57–60]. Преимущество таких систем по сравнению с предложенными ранее смешанолигандными комплексами [6, 61–63] состоит в уникальном свойстве триангуленов [64] и их тяжелых аналогов [65], заключающемся в увеличении количества неспаренных электронов с ростом числа шестичленных циклов (n) в основании треугольника (схема 1 ) [66, 67], благодаря которому возможно повышение общего спина системы посредством расширения полициклической части. Полученные результаты расчетов [57–60] указывают на незначительное влияние допирования углеводородного полициклического фрагмента атомами кремния или германия на энергетические параметры изомеров и характер обменного связывания. Некоторые парамагнитные триангуленовые производные представлены на схеме 1 .
Схема 1 .
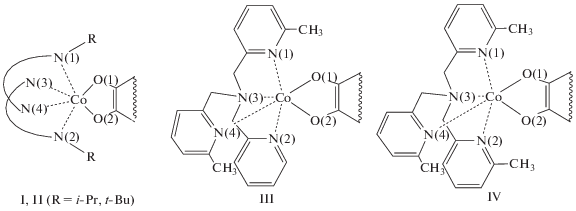
В настоящей работе с целью поиска новых по-лиспиновых систем, склонных к переключению магнитных свойств посредством реализации механизмов СКО и/или ВТ, выполнено компьютерное моделирование координационных соединений ти-па I–IV (схема 2 ) с различным количеством шестичленных колец в основании треугольного полицикла (n = 2–4). Выбор в качестве тетрадентатных N-донорных оснований N,N'-ди-изопропил-2,11-диаза[3.3]-(2,6)пиридинофана, N,N'-ди-трет-бутил-2,11-диаза[3.3]-(2,6)пиридинофана и производных трис(2-пиридилметил)амина (TPA), содержащих две или три CH3-группы в пиридиновых кольцах, обусловлен имеющимися экспериментальными данными, свидетельствующими о возможности проявления спиновых переходов в комплексах кобальта с таким лигандным окружением [47–51]. Гексафторфосфатные анионы, в свою очередь, широко используются при получении подобных солеобразных о-бензохиноновых комплексов кобальта с азотсодержащими лигандами [51].
Схема 2 .
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Расчеты проводили с помощью программы Gaussian 16 [68] методом теории функционала плотности (DFT) с использованием функционала UT-PSSh [69, 70] и расширенного базиса 6‑311++G(d,p), сочетание которых корректно воспроизводит энергетические и магнитные характеристики комплексов, проявляющих магнитную бистабильность [50, 52, 71–74]. Согласно полученным в данном приближении результатам расчетов экспериментально изученных соединений кобальта, СКО реализуется при ΔEHS-LS < 6 ккал/моль, ВТ – при ΔEHS-LS < 8 ккал/моль [50]. Ранее была показана необходимость учета внешнесферных противоионов при DFT-изучении комплексов переходных металлов с редокс-активными лигандами [75]. В этой связи в настоящем исследовании квантово-химические расчеты проведены для соединений, включающих гексафторфосфатный анион, положение и ориентация которого взяты из данных РСА структурно сходных соединений [51]. Локализацию стационарных точек на поверхности потенциальной энергии (ППЭ) осуществляли путем полной оптимизации геометрии молекулярных структур с последующей проверкой стабильности волновой функции DFT и расчетом силовых констант. Вычисление параметров обменного взаимодействия (J, см–1) осуществляли в рамках формализма “нарушенной симметрии” (broken symmetry, BS) [76] с использованием метода обобщенной проекции спина, предложенного К. Ямагучи [77]. Графические изображения молекулярных структур получали при помощи программы ChemCraft [78].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Согласно результатам расчетов, основному состоянию комплекса I (n = 2) отвечает минимум на дублетной ППЭ, в котором единственный неспаренный электрон делокализован по кремнийорганическому фрагменту (рис. 1). Длины координационных связей (табл. 1) и отсутствие спиновой плотности в хиноновом кольце и на металлоцентре позволяют однозначно приписать данному электромеру электронную конфигурацию LSCoIII–Cat–X, где Х – полициклический кремнийорганический радикал. Высокоспиновая форма соединения I (n = = 2) представлена минимумом на секстетной ППЭ. Приведенное на рис. 1 распределение спиновой плотности и вычисленные геометрические характеристики указывают на вхождение в обсуждаемый электромер HSCoII–SQ–X трех парамагнитных центров: высокоспинового двухвалентного иона кобальта, анион-радикальной формы SQ о-бензохинона и полициклического фрагмента. Как следует из пространственного строения изомеров комплекса I (n = 2), полициклический фрагмент располагается в одной плоскости с хиноновым кольцом (рис. 1). Примечательно, что при задании стартовой геометрии с перпендикулярным расположением кремнийорганического радикала оптимизация структуры приводит к развороту Х на 90° и формированию единой сопряженной π-системы Cat/SQ–X. Дестабилизация высокоспинового изомера HSCoII–SQ–X более чем на 10 ккал/моль (табл. 2) свидетельствует о том, что комплекс I (n = 2) будет находиться в основном дублетном состоянии LSCoIII–Cat–X без проявления признаков ВТ-перехода.
Рис. 1.
Пространственное строение и распределение спиновой плотности в электромерах комплексов I–III (n = 2), рассчитанное методом DFT UTPSSh/6-311++G(d,p). Атомы водорода и внешнесферные противоионы не показаны, контурное значение = 0.02 e/Å3.
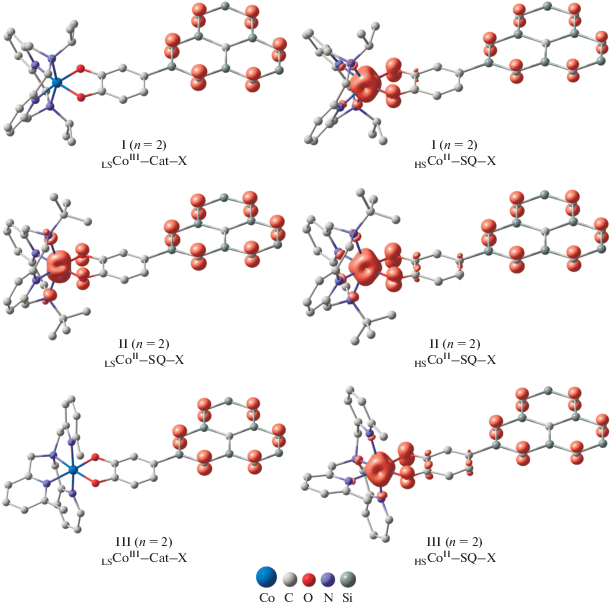
Таблица 1.
Длины координационных связей (Å) в электромерах комплексов I–IV (n = 2–4), рассчитанные методом DFT UTPSSh/6-311++G(d,p)
| Комплекс | Электромер | Co–O(1)* | Co–O(2) | Co–N(1) | Co–N(2) | Co–N(3) | Co–N(4) |
|---|---|---|---|---|---|---|---|
| I (n = 2) | LSCoIII–Cat–X | 1.888 | 1.884 | 2.045 | 2.045 | 1.874 | 1.872 |
| HSCoII–SQ–X | 2.040 | 2.027 | 2.281 | 2.282 | 2.036 | 2.033 | |
| I (n = 3) | LSCoIII–Cat–X | 1.890 | 1.883 | 2.048 | 2.043 | 1.873 | 1.872 |
| HSCoII–SQ–X | 2.039 | 2.026 | 2.284 | 2.278 | 2.035 | 2.032 | |
| I (n = 4) | LSCoIII–Cat–X | 1.890 | 1.884 | 2.048 | 2.044 | 1.873 | 1.872 |
| HSCoII–SQ–X | 2.039 | 2.026 | 2.284 | 2.277 | 2.035 | 2.032 | |
| II (n = 2) | LSCoII–SQ–X | 1.881 | 1.873 | 2.346 | 2.356 | 1.929 | 1.928 |
| HSCoII–SQ–X | 2.039 | 2.031 | 2.353 | 2.371 | 2.038 | 2.037 | |
| II (n = 3) | LSCoII–SQ–X | 1.883 | 1.871 | 2.352 | 2.354 | 1.929 | 1.928 |
| HSCoII–SQ–X | 2.041 | 2.029 | 2.354 | 2.371 | 2.037 | 2.038 | |
| II (n = 4) | LSCoII–SQ–X | 1.881 | 1.873 | 2.350 | 2.354 | 1.929 | 1.928 |
| HSCoII–SQ–X | 2.040 | 2.029 | 2.356 | 2.369 | 2.037 | 2.037 | |
| III (n = 2) | LSCoIII–Cat–X | 1.875 | 1.895 | 2.013 | 1.926 | 1.950 | 2.051 |
| HSCoII–SQ–X | 2.078 | 2.048 | 2.255 | 2.154 | 2.132 | 2.177 | |
| III (n = 3) | LSCoIII–Cat–X | 1.875 | 1.894 | 2.010 | 1.928 | 1.950 | 2.054 |
| HSCoII–SQ–X | 2.082 | 2.042 | 2.258 | 2.157 | 2.131 | 2.177 | |
| III (n = 4) | LSCoIII–Cat–X | 1.874 | 1.896 | 2.012 | 1.927 | 1.949 | 2.053 |
| HSCoII–SQ–X | 2.084 | 2.041 | 2.198 | 2.183 | 2.137 | 2.169 | |
| IV (n = 2) | LSCoIII–Cat–X | 1.871 | 1.885 | 2.016 | 2.018 | 1.949 | 2.060 |
| HSCoII–SQ–X | 2.075 | 2.047 | 2.242 | 2.286 | 2.117 | 2.178 | |
| IV (n = 3) | LSCoIII–Cat–X | 1.871 | 1.888 | 2.019 | 2.018 | 1.950 | 2.060 |
| HSCoII–SQ–X | 2.083 | 2.041 | 2.307 | 2.227 | 2.117 | 2.173 | |
| IV (n = 4) | LSCoIII–Cat–X | 1.870 | 1.889 | 2.019 | 2.020 | 1.950 | 2.059 |
| HSCoII–SQ–X | 2.080 | 2.048 | 2.304 | 2.221 | 2.119 | 2.170 |
Таблица 2.
Спин (S), полная энергия (Е), относительная энергия (ΔE) и спиновая плотность на металлоцентре $(q_{{\text{s}}}^{{{\text{Co}}}})$ в электромерах комплексов I–IV (n = 2–4), рассчитанные методом DFT UTPSSh/6-311++G(d,p)
| Комплекс | Электромер | S | Е, ат. ед. | ΔЕ, ккал/моль | $q_{{\text{s}}}^{{{\text{Co}}}}$ |
|---|---|---|---|---|---|
| I (n = 2) | LSCoIII–Cat–X | 1/2 | –5711.654371 | 0.0 | 0.00 |
| HSCoII–SQ–X | 5/2 | –5711.635697 | 11.7 | 2.62 | |
| I (n = 3) | LSCoIII–Cat–X | 1 | –7062.105189 | 0.0 | 0.00 |
| HSCoII–SQ–X | 3 | –7062.086342 | 11.8 | 2.63 | |
| I (n = 4) | LSCoIII–Cat–X | 3/2 | –8740.208385 | 0.0 | 0.00 |
| HSCoII–SQ–X | 7/2 | –8740.189508 | 11.8 | 2.63 | |
| II (n = 2) | LSCoII–SQ–X | 3/2 | –5790.286545 | 0.0 | 1.26 |
| HSCoII–SQ–X | 5/2 | –5790.273984 | 7.9 | 2.59 | |
| II (n = 3) | LSCoII–SQ–X | 2 | –7140.737126 | 0.0 | 1.27 |
| HSCoII–SQ–X | 3 | –7140.724473 | 7.9 | 2.59 | |
| II (n = 4) | LSCoII–SQ–X | 5/2 | –8818.840317 | 0.0 | 1.25 |
| HSCoII–SQ–X | 7/2 | –8818.827682 | 7.9 | 2.60 | |
| III (n = 2) | LSCoIII–Cat–X | 1/2 | –5708.043783 | 0.0 | 0.00 |
| HSCoII–SQ–X | 5/2 | –5708.030305 | 8.5 | 2.51 | |
| III (n = 3) | LSCoIII–Cat–X | 1 | –7058.494546 | 0.0 | 0.00 |
| HSCoII–SQ–X | 3 | –7058.480643 | 8.7 | 2.62 | |
| III (n = 4) | LSCoIII–Cat–X | 3/2 | –8736.598216 | 0.0 | 0.00 |
| HSCoII–SQ–X | 7/2 | –8736.584781 | 8.4 | 2.61 | |
| IV (n = 2) | LSCoIII–Cat–X | 1/2 | –5747.364131 | 0.0 | 0.00 |
| HSCoII–SQ–X | 5/2 | –5747.360056 | 2.6 | 2.57 | |
| IV (n = 3) | LSCoIII–Cat–X | 1 | –7097.815103 | 0.0 | 0.00 |
| HSCoII–SQ–X | 3 | –7097.810785 | 2.7 | 2.55 | |
| IV (n = 4) | LSCoIII–Cat–X | 3/2 | –8775.918606 | 0.0 | 0.00 |
| HSCoII–SQ–X | 7/2 | –8775.914163 | 2.8 | 2.59 |
Квантово-химическое изучение соединений I (n = 3, 4) показало, что увеличение количества шестичленных колец в кремнийорганическом фрагменте не сопровождается изменением электронной конфигурации найденных изомеров и длин связей в координационном узле (табл. 1). Разности энергий между электромерами комплексов I (n = 3, 4) близки к найденной ΔЕ для соединения I (n = 2) и составляют 11.8 ккал/моль (табл. 2). Учитывая спин-запрещенный характер ВТ-процесса и необходимость преодоления энергетического барьера при переходе LSCoIII–Cat–X ⇄ HSCoII–SQ–X, вероятность реализации внутримолекулярного переноса электрона в обсуждаемых системах крайне мала. Следовательно, комплексы I (n = 3, 4) будут представлены низкоспиновыми электромерами LSCoIII–Cat–X в широком диапазоне температур. Полициклические фрагменты соединений I (n = 3, 4) содержат два и три неспаренных электрона соответственно, которые могут рассматриваться как единый парамагнитный центр благодаря сильным ферромагнитным обменным взаимодействиями внутри кремнийорганического радикала [66, 79–81].
Сравнение данных расчетов соединений I (n = = 2–4) с полученными ранее результатами исследования о-бензохиноновых комплексов кобальта, содержащих N,N'-ди-изо-пропил-2,11-диаза[3.3]-(2,6)пиридинофан [50, 55], показывает увеличение разности энергий между электромерами в системах с кремнийорганическими полициклами. Предсказанное повышение устойчивости изомеров LSCoIII–Cat–X можно объяснить энергетической предпочтительностью образования обобщенной π-системы между триангуленом X и ароматическим Cat фрагментом, в то время как сопряжение с SQ, не являющимся ароматическим, не дает сравнимого энергетического выигрыша. Нумерация атомов в координационном узле комплексов I–IV представлена на схеме 3 .
Схема 3 .
Замена изопропильных заместителей при атомах азота на трет-бутильные группы ожидаемо [50, 51, 55] приводит к тому, что наиболее устойчивыми формами соединений II (n = 2–4) оказываются электромеры LSCoII–SQ–X, включающие низкоспиновый двухвалентный ион кобальта и анион-радикал SQ (рис. 1, табл. 1). Вне зависимости от количества шестичленных колец в кремнийорганическом радикале высокоспиновые изомеры дестабилизированы относительно основного состояния на 7.9 ккал/моль (табл. 2). Предсказанные величины несколько превышают диапазон значений, характерных для протекания СКО [50], что указывает на возможность реализации неполных СКО переходов LSCoII–SQ–Х ⇄ HSCoII–SQ–Х в комплексах II (n = 2–4).
Изучение обменных взаимодействий в электромерах LSCoII–SQ–Х указывает на сильное ферромагнитное связывание в парах LSCoII–SQ и SQ–Х, при этом обмен между металлоцентром и полициклическим фрагментом практически отсутствует ввиду их удаленности (табл. 3). Высокоспиновые электромеры HSCoII–SQ–X характеризуются умеренным антиферромагнитным связыванием спинов неспаренных электронов HSCoII и SQ, а значения параметров J2 и J3 близки к найденным для изомеров LSCoII–SQ–Х. Следует отметить, что обменные взаимодействия между органическими радикалами (J3) ослабляются с увеличением размера триангуленового фрагмента (табл. 3). Эта тенденция обусловлена делокализацией неспаренных электронов полицикла при переходе от комплекса I (n = 2), включающего один электрон на Х фрагменте, к соединению I (n = 4), в котором кремнийорганическая часть содержит три электрона. Можно заключить, что введение радикала Х не оказывает влияния на характер и силу обмена между ионом двухвалентного металла и SQ [50, 51]. В то же время наличие в молекуле полициклического фрагмента способствует формированию дополнительных каналов обмена.
Таблица 3.
Параметры обменных взаимодействий (J, см–1) в электромерах LSCoII–SQ–X, HSCoII–SQ–X комплексов I–IV (n = 2–4), рассчитанные методом DFT UTPSSh/6-311++G(d,p)
| Комплекс | Электромер | J1* | J2 | J3 |
|---|---|---|---|---|
| I (n = 2) | HSCoII–SQ–X | –98 | 2 | 197 |
| I (n = 3) | HSCoII–SQ–X | –96 | 1 | 131 |
| I (n = 4) | HSCoII–SQ–X | –98 | 1 | 80 |
| II (n = 2) | LSCoII–SQ–X | 271 | –9 | 155 |
| HSCoII–SQ–X | –43 | –6 | 181 | |
| II (n = 3) | LSCoII–SQ–X | 264 | –8 | 102 |
| HSCoII–SQ–X | –46 | –4 | 117 | |
| II (n = 4) | LSCoII–SQ–X | 258 | –6 | 64 |
| HSCoII–SQ–X | –49 | –2 | 72 | |
| III (n = 2) | HSCoII–SQ–X | 81 | 0 | 127 |
| III (n = 3) | HSCoII–SQ–X | 78 | –1 | 78 |
| III (n = 4) | HSCoII–SQ–X | 77 | –1 | 47 |
| IV (n = 2) | HSCoII–SQ–X | 85 | –6 | 155 |
| IV (n = 3) | HSCoII–SQ–X | 86 | 2 | 80 |
| IV (n = 4) | HSCoII–SQ–X | 82 | –4 | 65 |
Теоретическое исследование комплексов III (n = 2–4) предсказывает энергетическую предпочтительность низкоспиновых изомеров LSCoIII–Cat–X (рис. 1, табл. 2). Как и в рассмотренных выше системах I и II, варьирование размера полициклического радикала не влияет на геометрические (табл. 1) и энергетические (табл. 2) характеристики электромеров: высокоспиновые структуры HSCoII–SQ–X соединений III (n = 2–4) дестабилизированы по отношению к основным состояниям LS-CoIII–Cat–X на 8.4–8.7 ккал/моль. Вычисленные значения ΔЕ дают основание ожидать ВТ-переходов с низкими степенями превращения. Как и в изученных ранее о-бензохиноновых комплексах кобальта с трис(2-пиридилметил)аминовыми производными [51, 53, 56, 74], в электромерах H-SCoII–SQ–X соединений III (n = 2–4) металлоцентр и SQ радикал взаимодействуют ферромагнитно. Характер и сила магнитного связывания в паре SQ–X аналогичны предсказанным в комплексах I и II (n = 2–4); обмен между неспаренными электронами иона кобальта и кремнийорганического фрагмента практически отсутствует (табл. 3).
Результаты расчетов соединений I и III (n = 2–4) свидетельствуют об увеличении энергетической щели ΔЕ (табл. 2) по сравнению с предсказанными значениями для построенных аналогичным способом производных, не включающих полициклические радикалы [50, 51, 53, 55, 56]. Ранее было показано [49, 53, 74], что в о-бензохиноновых комплексах кобальта с тетрадентатными N-донорными лигандами присутствие электроноактивных заместителей в хиноновом кольце позволяет управлять разностью энергий между электромерами, которая определяет вероятность протекания редокс-процесса. Известно [47, 51], что комплекс кобальта с 3,5-ди-трет-бутил-о-бензохиноном и TPA, содержащим по одной метильной группе в каждом пиридиновом кольце, существует в виде высокоспинового электромера HSCoII–SQ ввиду дестабилизации формы LSCoIII–Cat. Можно ожидать, что обнаруженное в настоящей работе повышение устойчивости низкоспинового состояния при введении кремнийорганического радикала будет благоприятствовать возникновению ВТ-перегруппировок в соединениях IV (n = 2–4) с трис(2-пиридилметил)амином, включающим три CH3-заместителя (cхема 2). С целью проверки данной гипотезы проведено компьютерное моделирование электронного строения и магнитных свойств этих комплексов.
Распределение спиновой плотности в электромерах соединений IV (n = 2–4) имеет схожий вид с найденным в комплексах III (n = 2–4) (рис. 1). Сравнение вычисленных геометрических параметров обсуждаемых систем свидетельствует о том, что наличие дополнительного объемистого алкильного заместителя в пиридиновом кольце приводит к удлинению расстояний Fe–N(2) и небольшому изменению длин координационных связей в соединениях IV (n = 2–4) (табл. 1). Ввиду невозможности формирования коротких межатомных расстояний Fe–N понижается устойчивость низкоспиновых электромеров LSCoIII–Cat–X по сравнению с таковой в комплексах III (n = 2–4) (табл. 2). Однако в отличие от изученных ранее о‑бензохиноновых производных кобальта с триметил-замещенным TPA [47, 51], в координационных соединениях IV (n = 2–4) электромеры LSCoIII–Cat–X отвечают основному состоянию. Это обстоятельство дает предпосылки для протекания ВТ превращений. И действительно, разности энергий между структурами LSCoIII–Cat–X и HS-CoII–SQ–X составляют 2.6–2.8 ккал/моль (табл. 2), что указывает на возможность реализации ВТ-переходов при комнатных температурах. В зависимости от количества шестичленных колец в кремнийорганическом радикале, электромеры LSCoIII–Cat–X характеризуются спиновыми состояниями S, равными 1/2 (n = 2), 1 (n = 3) и 3/2 (n = 4). Благодаря ферромагнитным обменным взаимодействиям (табл. 3) в высокоспиновых структурах ожидается сохранение максимально возможного полного спина S. Следовательно, предсказанные ВТ-перегруппировки будут сопровождаться изменением магнитных свойств, что позволяет рассматривать соединения IV (n = 2–4) в качестве основы молекулярных переключателей.
Таким образом, посредством квантово-химического исследования комплексов кобальта, сконструированных на основе о-бензохинонов, содержащих триангуленовые кремнийорганические заместители и вспомогательные N-донорные лиганды, выявлены молекулы, потенциально способные к проявлению механизмов переключения спиновых состояний (спин-кроссовера и валентной таутомерии). Присутствие полициклического радикала и сильные ферромагнитные взаимодействия обеспечивают парамагнетизм всех изученных молекул. Показано, что энергетические характеристики электромеров соединений I–IV (n = 2–4) не зависят от размера кремнийорганического фрагмента и управляются структурными особенностями тетрадентатных азотсодержащих оснований. Преимущество предложенных систем перед исследованными ранее соединениями с аценовыми фрагментами [82–84] заключается в парамагнетизме всех электромерных форм благодаря наличию ферромагнитно связанных неспаренных электронов в триангуленовом радикале. Кроме того, комплексы I–IV обладают более высоким суммарным спином, который может быть дополнительно увеличен за счет расширения полициклической части, что позволит обогатить функциональные возможности подобных систем.
Авторы заявляют, что у них нет конфликта интересов.
Список литературы
Molecular Switches / Eds. Feringa B.L., Browne W.R. Weinheim: Wiley-VCH, 2011. 824 p.
Witt A., Heinemann F.W., Sproules S., Khusniyarov M.M. // Chem. Eur. J. 2014. V. 20. № 35. P. 11149.
Sato O. // Nature Chem. 2016. V. 8. № 7. P. 644
Senthil Kumar K., Ruben M. // Coord. Chem. Rev. 2017. V. 346. P. 176.
Drath O., Boskovic C. // Coord. Chem. Rev. 2018. V. 375. P. 256.
Старикова А.А., Минкин В.И. // Успехи химии. 2018. Т. 87. № 11. С. 1049 (Starikova A.A., Minkin V.I. // Russ. Chem. Rev. 2018. V. 87. № 11. Р. 1049). https://doi.org/10.1070/RCR4837
Coronado E. // Nat. Rev. Mater. 2020. V. 5. P. 87.
Золотухин А.А., Бубнов М.П., Черкасов В.К., Абакумов Г.А. // Коорд. химия. 2018. Т. 44. № 2. С. 123 (Zolotukhin A.A., Bubnov M.P., Cherkasov V.K. et al. // Russ. J. Coord. Chem. 2018. V. 44. № 4. Р. 272). https://doi.org/10.1134/S1070328418040085
Chegerev M.G., Starikova A.A. // Eur. J. Inorg. Chem. 2021. № 27. P. 2684.
Bally T. // Nature Chem. 2010. V. 2. № 3. P. 165.
Минкин В.И. // Изв. АН. Сер. хим. 2008. № 4. С. 673 (Minkin V.I. // Russ. Chem. Bull. 2008. V. 57. № 4. P. 687). https://doi.org/10.1007/s11172-008-0111-y
Dei A., Sorace L. // Appl. Magn. Reson. 2010. V. 38. № 2. P. 139.
Timco G.A., Carretta S., Troiani F. et al. // Nat. Nanotechnol. 2009. V. 4. № 3. P. 173.
Aromí G., Aguilà D., Gamez P. et al. // Chem. Soc. Rev. 2012. V. 41. № 2. P. 537.
Demir S., Jeon I.-R., Long J.R., Harris T.D. // Coord. Chem. Rev. 2015. V. 289–290. P. 149.
Venkataramani S., Jana U., Dommaschk M. et al. // Science. 2011. V. 331. № 6016. P. 445.
Mörtel M., Seller M., Heinemann F.W., Khusniyarov M.M. // Dalton Trans. 2020. V. 49. № 48. P. 17532.
Овчаренко В.И., Кузнецова О.В. // Успехи химии. 2020. Т. 89. № 11. С. 1261 (Ovcharenko V.I., Kuznetsova O.V. // Russ. Chem. Rev. 2020. V. 89. № 11. P. 1261). https://doi.org/10.1070/RCR4981
Nikovskiy I., Polezhaev A., Novikov V. et al. // Chem. Eur. J. 2020. V. 26. № 15. P. 5629.
Nadurata V.L., Boskovic C. // Inorg. Chem. Front. 2021. V. 8. № 7. P. 1840.
Spin Crossover in Transition Metal Compounds. I. V. 233 / Eds. Gütlich P., Goodwin H.A. Berlin–Heidelberg: Springer-Verlag, 2004.
Spin-Crossover Materials: Properties and Applications / Ed. Halcrow M.A. Chichester: John Wiley&Sons, 2013. 564 p.
Hauser A. // Coord. Chem. Rev. 1991. V. 111. P. 275.
Hauser A., Enachescu C., Daku M.L. et al. // Coord. Chem. Rev. 2006. V. 250. P. 1642.
Halcrow M.A. // Polyhedron. 2007. V. 26. № 14. P. 3523.
Harding D.J., Harding P., Phonsri W. // Coord. Chem. Rev. 2016. V. 313. P. 38.
Khusniyarov M.M. // Chem. Eur. J. 2016. V. 22. № 43. P. 15178.
Krivokapic I., Zerara M., Daku M.L. et al. // Coord. Chem. Rev. 2007. V. 251. P. 364.
Vologzhanina A.V., Belov A.S., Novikov V.V. et al. // Inorg. Chem. 2015. V. 54. № 12. P. 5827.
Taylor R.A., Lough A.J., Lemaire M.T. //J. Mater. Chem. C. 2016. V. 4. № 3. P. 455.
Evangelio E., Ruiz-Molina D. // Eur. J. Inorg. Chem. 2005. № 15. P. 2957.
Tezgerevska T., Alley K.G., Boskovic C. // Coord. Chem. Rev. 2014. V. 268. P. 23.
Rajput A., Sharma A.K., Barman S.K. et al. // Coord. Chem. Rev. 2020. V. 414. P. 213240.
Fedushkin I., Maslova O., Morozov A. et al. // Angew. Chem. Int. Ed. 2012. V. 51. № 42. P. 10584.
Chegerev M.G., Starikova A.A., Piskunov A.V., Cherkasov V.K. // Eur. J. Inorg. Chem. 2016. № 2. P. 252.
Chegerev M.G., Piskunov A.V., Starikova A.A et al. // Eur. J. Inorg. Chem. 2018. № 9. P. 1087.
Kirk M.L., Shultz D.A. // Coord. Chem. Rev. 2013. V. 257. № 1. P. 218.
Tichnell C.R., Shultz D.A., Popescu C.V. et al. // Inorg. Chem. 2015. V. 54. № 9. P. 4466.
Bubnov M., Cherkasova A., Teplova I. et al. // Polyhedron. 2016. V. 119. P. 317.
Artiukhova N.A., Romanenko G.V., Bogomyakov A.S. et al. // J. Mater. Chem. C. 2016. V. 4. № 47. P. 11157.
Bubnov M.P., Teplova I.A., Kopylova E.A. et al. // Inorg. Chem. 2017. V. 56. № 5. P. 2426.
Zolotukhin A.A., Bubnov M.P., Arapova A.V. et al. // Inorg. Chem. 2017. V. 56. № 24. P. 14751.
Черкасова А.В., Кожанов К.А., Золотухин А.А. и др. // Коорд. химия. 2019. Т. 45. № 7. С. 404 (Cherkasova A.V., Kozhanov K.A, Zolotukhin A.A. et al. // Russ. J. Coord. Chem. 2019. V. 45. № 7. P. 489). https://doi.org/10.1134/S1070328419070029
Protasenko N.A., Poddel’sky A.I., Bogomyakov A.S. et al. // Inorg. Chim. Acta. 2019. V. 489. P. 1.
Кузнецова О.В., Романенко Г.В., Богомяков А.С., Овчаренко В.И. // Коорд. химия. 2020. Т. 46. № 8. С. 451 (Kuznetsova O.V., Romanenko G.V., Bogomyakov A.S., Ovcharenko V.I. // Russ. J. Coord. Chem. 2020. V. 46. № 8. P. 521). https://doi.org/10.1134/S1070328420070039
Maryunina K., Yamaguchi K., Nishihara S. et al. // Cryst. Growth Des. 2020. V. 20. № 4. P. 2796.
Beni A., Dei A., Laschi S. et al. // Chem. Eur. J. 2008. V. 14. № 6. P. 1804.
Graf M., Wolmershäuser G., Kelm H. et al. // Angew. Chem. Int. Ed. 2010. V. 49. № 5. P. 950.
Gransbury G.K., Boulon M.-E., Petrie S. et al. // Inorg. Chem. 2019. V. 58. № 7. P. 4230.
Tezgerevska T., Rousset E., Gable R.W. et al. // Dalton Trans. 2019. V. 48. № 31. P. 11674.
Старикова А.А., Чегерев М.Г., Стариков А.Г. // Коорд. химия. 2020. Т. 46. № 3. С. 172 (Starikova A.A., Chegerev M.G., Starikov A.G. // Russ. J. Coord. Chem. 2020. V. 46. № 3. P. 193). https://doi.org/10.1134/S1070328420030070
Стариков А.Г., Старикова А.А., Минкин В.И. // Д-окл. РАН. 2016. Т. 467. № 3. С. 300 (Starikov A.G., Starikova A.A., Minkin V.I. // Dokl. Chem. 2016. V. 467. № 1. Р. 83). https://doi.org/10.1134/S0012500816030113
Starikova A.A., Chegerev M.G., Starikov A.G., Minkin V.I. // Comp. Theor. Chem. 2018. V. 1124. P. 15.
Starikov A.G., Chegerev M.G., Starikova A.A. // Struct. Chem. 2020. V. 31. № 1. P. 37.
Минкин В.И., Старикова А.А., Чегерев М.Г., Стариков А.Г. // Коорд. химия. 2020. Т. 46. № 6. С. 325 (Minkin V.I., Starikova A.A., Chegerev M.G., Starikov A.G. // Russ. J. Coord. Chem. 2020. V. 46. № 6. P. 371). https://doi.org/10.1134/S1070328420060068
Starikova A.A., Chegerev M.G., Starikov A.G. // Chem. Phys. Lett. 2021. V. 762. P. 138128.
Starikov A.G., Starikova A.A., Minyaev R.M. et al. // Chem. Phys. Lett. 2020. V. 740. P. 137073.
Минкин В.И., Старикова А.А., Чегерев М.Г., Стариков А.Г. // Докл. РАН. 2020. Т. 494. № 1. С. 21 (Minkin V.I., Starikova A.A., Chegerev M.G., Starikov A.G. // Dokl. Chem. 2020. V. 494. № 2. P. 149). https://doi.org/10.1134/S001250082010002X
Чегерев М.Г., Старикова А.А., Стариков А.Г., Минкин В.И. // Журн. общ. химии. 2020. Т. 90. № 12. С. 1910 (Chegerev M.G., Starikova A.A., Starikov A.G., Minkin V.I. // Russ. J. Gen. Chem. 2020. V. 90. № 12. P. 2312). https://doi.org/10.1134/S1070363220120142
Стариков А.Г., Чегерев М.Г., Старикова А.А., Минкин В.И. // Изв. АН. Сер. хим. 2021. № 2. С. 309 (Starikov A.G., Chegerev M.G., Starikova A.A., Minkin V.I. // Russ. Chem. Bull. 2021. V. 70. № 2. P. 309). https://doi.org/10.1007/s11172-021-3086-6
Старикова А.А., Миняев Р.М., Минкин В.И. // Изв. АН. Сер. хим. 2014. № 4. С. 812 (Starikova A.A., Minyaev R.M., Minkin V.I. // Russ. Chem. Bull. 2014. V. 63. № 4. P. 812). https://doi.org/10.1007/s11172-014-0514-x
Starikova A.A., Minkin V.I., Starikov A.G. // Mend. Commun. 2014. V. 24. № 6. P. 329.
Фокин С.В., Фурсова Е.Ю., Летягин Г.А. и др. // Журн. структур. химии. 2020. Т. 61. № 4. С. 571 (Fokin S.V., Fursova E.Yu., Letyagin G.A. et al. // J. Struct. Chem. 2020. V. 61. № 4. P. 541). https://doi.org/10.1134/S002247662004006X
Polyarenes I / Eds. Siegel J.S., Wu Y.-T. Berlin–Heidelberg: Springer-Verlag, 2014. 294 p.
Gapurenko O.A., Starikov A.G., Minyaev R.M., Minkin V.I. // J. Comput. Chem. 2015. V. 36. № 29. P. 2193.
Ovchinnikov A.A. // Theor. Chem. Acc. 1978. V. 47. P. 297.
Stable Radicals: Fundamental and Applied Aspects of Odd-Electron Compounds / Ed. Hicks R. Chichester: Wiley, 2011. 588 p.
Frisch M.J., Trucks G.W., Schlegel H.B. et al. Gaussian 16. Revision C. 01. Wallingford: Gaussian, 2016.
Tao J.M., Perdew J.P., Staroverov V.N., Scuseria G.E. // Phys. Rev. Lett. 2003. V. 91. № 14. P. 146401.
Staroverov V.N., Scuseria G.E., Tao J., Perdew J.P. // J. Chem. Phys. 2003. V. 119. № 23. P. 12129.
Cirera J., Ruiz E. // J. Mater. Chem. C. 2015. V. 3. № 30. P. 7954.
Cirera J., Via-Nadal M., Ruiz E. // Inorg. Chem. 2018. V. 57. № 22. P. 14097.
Стариков А.Г., Старикова А.А., Чегерев М.Г., Минкин В.И. // Коорд. химия. 2019. Т. 45. № 2. С. 92 (Starikov A.G., Starikova A.A., Chegerev M.G., Minkin V.I. // Russ. J. Coord. Chem. 2019. V. 45. № 2. Р. 105). https://doi.org/10.1134/S1070328419020088
Gransbury G.K., Livesay B.N., Janetzki J.T. et al. // J. Am. Chem. Soc. 2020. V. 142. № 24. P. 10692.
Minkin V.I., Starikov A.G., Starikova A.A. // Pure Appl. Chem. 2018. V. 90. № 5. P. 811.
Noodleman L. // J. Chem. Phys. 1981. V. 74. № 10. P. 5737.
Shoji M., Koizumi K., Kitagawa Y. et al. // Chem. Phys. Lett. 2006. V. 432. № 1–3. P. 343.
Chemcraft. Version 1.8. 2014: http://www.chemcraftprog.com.
Melle-Franco M. // Chem. Commun. 2015. V. 51. № 25. P. 5387.
Sharma V., Som N., Dabhi S.D., Jha P.K. // ChemSelect. 2018. V. 3. № 8. P. 2390.
Minkin V.I., Starikov A.G., Starikova A.A. et al. // Phys. Chem. Chem. Phys. 2020. V. 22. № 3. P. 1288.
Minkin V.I., Starikov A.G., Starikova A.A. et al. // Dalton Trans. 2018. V. 47. № 44. P. 15948.
Старикова А.А., Метелица Е.А., Минкин В.И. // Коорд. химия. 2019. Т. 45. № 6. С. 350 (Starikova A.A., Metelitsa E.A., Minkin V.I. // Russ. J. Coord. Chem. 2019. V. 45. № 6. Р. 411). https://doi.org/10.1134/S1070328419060095
Minkin V.I., Starikov A.G., Starikova A.A. // J. Phys. Chem. A. 2021. V. 125. № 30. P. 6562.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия