Кристаллография, 2019, T. 64, № 1, стр. 77-80
Кристаллическая структура потенциально мезоморфного 4-нонилоксифенил-4'-метакрилоилокси-бензоата CH2=C(CH3)–COO–C6H4–COO– C6H4–O–С9Н19
Л. Г. Кузьмина 1, *, М. А. Навасардян 1, И. И. Константинов 1, 2, **
1 Институт общей и неорганической химии РАН
Москва, Россия
2 Институт нефтехимического синтеза РАН
Москва, Россия
* E-mail: kuzmina@igic.ras.ru
** E-mail: konst@ipc.ac.ru
Поступила в редакцию 06.03.2018
После доработки 26.03.2018
Принята к публикации 16.04.2018
Аннотация
По данным рентгеноструктурного анализа исследована кристаллическая структура 4,4'-замещенного фенилбензоата CH2=C(CH3)–COO–C6H4–COO–C6H4–O–С9Н19. Кристаллическая упаковка соединения обнаруживает чередование рыхлых алифатических и плотных ароматических областей, что обычно для кристаллов мезогенных соединений. Однако в ароматических областях отсутствуют слабые направленные взаимодействия, ответственные за формирование структурированного расплава. Поэтому соединение не проявляет мезоморфных свойств как при плавлении, так и при охлаждении изотропного расплава.
ВВЕДЕНИЕ
Настоящая работа является продолжением изучения кристаллической структуры потенциально мезогенных алкилзамещенных фенилбензоатов с длинными алкильными цепями. Известно, что линейные молекулы, построенные из жесткого ядра и одной или двух достаточно длинных алифатических цепей, могут проявлять жидкокристаллические свойства, т.е. образовывать мезофазу при плавлении. Поскольку кристаллическая упаковка предшествует мезофазе, естественно предположить, что какие-то специфические особенности кристаллической упаковки являются, с одной стороны, причиной формирования структурированного расплава (мезофазы), а с другой – определяют его специфику.
Поэтому представлялось важным исследовать кристаллическую упаковку потенциально мезоморфных соединений, опираясь на методы рентгеноструктурного анализа и дифференциальной сканирующей калориметрии. Настоящая работа состоит в изучении молекулярной и кристаллической структуры одного из фенилбензоатов, а именно CH2=C(CH3)–COO–C6H4–COO–C6H4–O–С9Н19.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез. Соединение получено этерификацией 4-метакрилоксибензойной кислоты с 4-н-нонилоксифенолом с использованием N,N-дициклогексилкарбодиимина в растворе дихлорметана согласно методике [1]. Продукт очищали в хроматографической колонке, а затем перекристаллизацией из этанола. Чистота продукта проверялась тонкослойной хроматографией: C26H32O5. M 124.542.
Рентгеноструктурный анализ. Кристаллографические характеристики и параметры расшифровки и уточнения структуры приведены в таблице.
Таблица 1.
Кристаллографические характеристики, данные эксперимента и уточнения структуры C26H32O5
| Сингония, пр. гр., Z | Моноклинная, Сc, 4 |
| a, b, c, Å | 54.52(2), 7.341(4), 5.828(3) |
| β, град | 95.820(7) |
| V, Å3 | 2320.2(19) |
| Dx, г/см3 | 1.215 |
| Излучение; λ, Å | MoKα, 0.71073 |
| μ, см–1 | 0.083 |
| Т, К | 120 |
| Размер образца | 0.24 × 0.12 × 0.02 |
| Дифрактометр | Bruker SMART Apex-II |
| Тип сканирования | ω |
| Учет поглощения, Тmin, Tmax | SADABS; 0.65, 0.75 |
| θmax, град | 27 |
| Пределы h, k, l | –69 ≤ h ≤ 28, –9 ≤ k ≤ 19, ‒7 ≤ l ≤ 7 |
| Число отражений: измеренных/независимых (N1), Rint/c I > 2σ(I) (N2) | 10 471/4989, 0.0792/ 2547 |
| Метод уточнения | Полноматричный МНК по F 2 |
| Число параметров | 282 |
| Параметр Флэка | –0.3(17) |
| R1/wR2 по N1 | 0.1562/0.1676 |
| R1/wR2 по N2 | 0.0646/0.1314 |
| S | 0.962 |
| Δρmin/Δρmax | –0.23/0.28 |
| Программы | SAINT [2], SADABS [2], Olex-2 [3] |
Структура расшифрована прямым методом. Уточнение структуры проведено в анизотропном приближении для неводородных атомов. Положения атомов водорода рассчитаны геометрически, и они включены в окончательные этапы уточнения по модели наездника.
Координаты атомов и другие экспериментальные данные депонированы в Кембриджской базе структурных данных (CCDC № 1825117).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Молекулярная структура. Строение молекулы показано на рис. 1. Молекула неплоская. Двугранный угол между плоскостями бензольных колец С2–С7 (кольца А) и С8–С13 (кольцо B) равен 59.2(1)°. Сложноэфирная группа О1–С1–О2 практически копланарна бензольному кольцу А (двугранный угол равен 2.4(2)°) и повернута к плоскости кольца В на угол 60.7(1)°. Таким образом, указанная сложноэфирная группа находится в сопряжении с бензольным кольцом А. Вторая сложноэфирная группа О4–С23–О5 выведена из сопряжения с бензольным кольцом А – двугранный угол между плоскостями О4–С23–О5/C2–C7 составляет 57.6(2)°.
Рис. 1.
Строение молекулы; эллипсоиды среднеквадратичных смещений атомов приведены на уровне вероятности 50%.
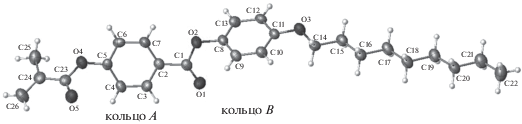
Нонилокси-группа имеет протяженное практически плоское строение. Эта группа повернута к плоскости бензольного кольца В на малый угол (10.5(2)°), что свидетельствует о сопряжении неподеленной пары атома кислорода О3 с бензольным кольцом В. Такая геометрия обычна для кристаллов мезогенных соединений, содержащих алкилокси-заместитель [4–10]. Все длины связей и валентные углы в молекуле обычны для мезогенных фенилбензоатов [6–9].
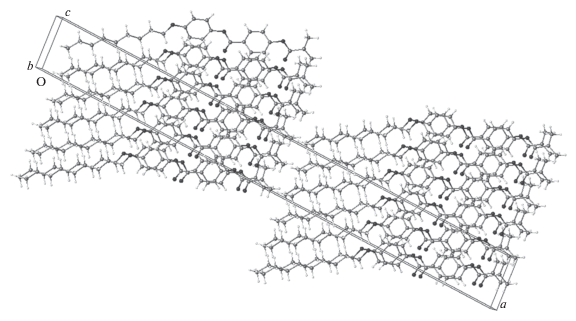
Кристаллическая упаковка. Отличительным свойством кристаллических упаковок мезогенных соединений является чередование в них рыхлых алифатических и плотных ароматических областей [4–10], что может приводить к аномальному плавлению таких соединений – плавление начинается по рыхлым областям.
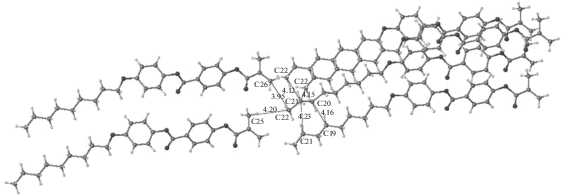
Кристаллическая упаковка исследованного соединения показана на рис. 2. Из рисунка видно, что и в данной структуре упаковка разделяется на чередующиеся алифатические и ароматические области, причем первые из них имеет очень рыхлое строение. На рис. 3 показан фрагмент алифатической области с самыми короткими межмолекулярными расстояниями – короче 4.2 Å. Только одно из них, С2…С26, соответствует ван-дер-ваальсовому контакту.
Рис. 3.
Самые короткие межмолекулярные расстояния в алифатических областях кристалла; расстояния даны в Å.
Но для того чтобы плавление действительно было аномальным, т.е. приводило бы к образованию мезофазы, необходимо выполнение следующего условия – в ароматических областях должны существовать структуроформирующие контакты. Такими контактами являются слабые направленные взаимодействия разных типов. В органических соединениях они представлены обычными водородными связями, слабыми водородными связями С–Н···О, π-стэкинг, С–Н···π, гетероатом···гетероатом взаимодействиями [11–15]. Эти слабые направленные взаимодействия могут не разрушаться при температуре плавления, обусловливая структурированность образовавшегося расплава, т.е. мезофазы.
Анализ ароматических областей кристалла не обнаруживает существования в них указанных направленных взаимодействий. По этой причине плавление данного кристалла не должно сопровождаться формированием мезофазы. Согласно калориметрическим данным соединение не является мезоморфным; оно плавится при температуре 72.2°С, давая изотропный расплав, при охлаждении которого при 59.2° образуется кристаллическая форма [1], т.е. данное соединение не образует мезофазу не только при плавлении, но и при охлаждении расплава.
Таким образом, формирование соединением мезофазы при плавлении кристалла определяется не только спецификой кристаллической упаковки, обусловленной чередованием рыхлых алифатических и плотных ароматических областей, но и наличием в последних элементов структурированности (слабых направленных взаимодействий).
Работа выполнена при финансовой поддержке Российского научного фонда (грант № 16-13-10273).
Список литературы
Hassner A., Alexanian V. // Tetrahedron Lett. 1978. P. 4475.
Bruker (2008). APEX2, SADABS and SAINT. Bruker AXS Inc. Madison, Wiskonsin, USA.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. P. 339.
Кочетов А.Н., Кузьмина Л.Г., Чураков А.В. и др. // Кристаллография. 2006. Т. 51. № 1. С. 59.
Kuz’mina L.G., Navasardyan M.A., Churakov A.V., Howard J.A.K. // Mol. Cryst. Liq. Cryst. 2016. V. 638. P. 60.
Константинов И.И., Чураков А.В., Кузьмина Л.Г. // Кристаллография. 2013. Т. 58. № 1. С. 89.
Kuz’mina L.G., Konstantinov I.I., Lermontova E.Kh. // Mol. Cryst. Liq. Cryst. 2014. V. 588. P. 1.
Kuz’mina L.G., Konstantinov I.I., Churakov A.V., Navasardyan M.A. // Acta Cryst. E. 2017. V. 73. P. 1052.
Кузьмина Л.Г., Константинов И.И., Беззубов С.И. // Химия высоких энергий. 2016. Т. 50. № 6. С. 478.
Кузьмина Л.Г., Кучерепа Н.С. // Кристаллография. 2011. Т. 56. № 2. С. 267.
Nangia A. // Cryst. Eng. Comun. 20024. V. 17. P. 93.
Muller-Dethlefs K., Hobza P. // Chem. Rev. 2000. V. 100. P. 143.
Janiak Ch. // J. Chem. Soc. Dalton Trans. 2000. P. 3885.
Chen Z., Lohr A., Saha-Moller Cr., Wurthner F. // Chem. Soc. Rev. 2009. V. 38. P. 564.
Oxtoby N.S., Blake A.J., Champness N.R., Wilson C. // Cryst. Eng. Commun. 2003. V. 5(17). P. 82.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография