Кристаллография, 2020, T. 65, № 2, стр. 215-222
Новые данные об изоморфизме в минералах группы эвдиалита. VI. Кристаллическая структура члена группы, содержащего сульфидный анион: изоморфизм Cl––S2–
Р. К. Расцветаева 1, *, Н. В. Чуканов 2, И. В. Пеков 3, Д. А. Варламов 2, 4, С. М. Аксенов 1
1 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
2 Институт проблем химической физики РАН
Черноголовка, Черноголовка
3 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
4 Институт экспериментальной минералогии РАН
Черноголовка, Россия
* E-mail: rast@crys.ras.ru
Поступила в редакцию 06.08.2019
После доработки 22.08.2019
Принята к публикации 27.08.2019
Аннотация
Методами рентгеноструктурного анализа, электронно-зондового микроанализа и ИК-спектроскопии исследован представитель группы эвдиалита, содержащий сульфидный анион S2–. Параметры элементарной ячейки: a = 14.2156(3), c = 30.405(1) Å, V = 5321.16(3) Å3, пр. гр. R3m. Кристаллическая структура уточнена до итогового фактора расходимости R = 3.9% в анизотропном приближении атомных смещений с использованием 2158 рефлексов с F > 3σ(F). Идеализированная формула минерала (Z = 3): [(Na,Н3О)14Sr]Ca6(Mn2Na)Zr3[Si26O72](OH)3S2– · 2H2O. Обсуждаются проблемы генезиса минерала и присутствия сульфидной серы в минералах со структурным типом эвдиалита.
ВВЕДЕНИЕ
Минералы группы эвдиалита – широко распространенные в агпаитовых щелочных породах тригональные цирконосиликаты с параметрами элементарной ячейки а ∼ 14 и с ∼ 30 Å и пр. гр. R3, R3m и R$\bar {3}$m. Структура эвдиалита, идеализированная формула которого Na15Ca6Fe$_{3}^{{2 + }}$Zr3(Si26O73) (O,OH,H2O)3(Cl,OH)2 (Z = 3), представляет собой сложную постройку, состоящую из колец Si9O27, Si3O9 и Ca6O24, соединенных изолированными ZrO6-октаэдрами, и ионов Fe2+ в координации плоского квадрата, а также дополнительных тетраэдров SiO4, центрирующих кольца Si9O27. Внекаркасные компоненты представлены ионами Na+, Cl–, OH– и молекулами H2O. Уникальное кристаллохимическое разнообразие минералов группы эвдиалита определяется различными схемами катионного упорядочения, гомовалентного, гетеровалентного и блочного изоморфизма, в который вовлекается широкий круг элементов. Некоторые из них (C, F, K, Ti, Mn, Sr, Nb, Ce, W) могут быть видообразующими для минералов этой группы, другие (Al, S, Y, Ba, La, Hf, Ta, Pb) иногда присутствуют в различных позициях кристаллической структуры в качестве примесей [1, 2]. Кристаллохимическая роль серы в эвдиалитах изучена недостаточно, что обусловлено прежде всего ее присутствием обычно в небольших количествах, не превышающих 0.5 атома на формулу. Так, в [3] отмечался сульфатный тетраэдр SO4, который может располагаться на оси третьего порядка – вблизи центра девятичленных колец Si9O27 (позиции М3 и М4) и между крупными катионами (позиции Х1 и Х2).
В настоящей работе методами рентгеноструктурного анализа, электронно-зондового микро-анализа и ИК-спектроскопии изучен минерал группы эвдиалита, содержащий сульфидную серу, которая располагается, как установлено, в позициях Х1 и Х2. Новый S-содержащий представитель группы эвдиалита найден на горе Кедыкверпахк в Ловозерском щелочном массиве (Кольский п-ов, Россия). Изученный в настоящей работе образец № Кдк-6625 отобран в одной из подземных выработок рудника Карнасурт (участок Кедыкверпахк). Минерал образует светло-желтые (до розовато-желтоватых) прозрачные изометричные зерна, которые достигают 1 мм в поперечнике и находятся в акцессорном количестве в ультраагпаитовом фойяите, непосредственно контактирующем с рудным пластом лопаритового малиньита. Породообразующими минералами этой разновидности фойяита являются калиевый полевой шпат, нефелин, содалит и эгирин, а главные акцессорные минералы – члены группы эвдиалита, лампрофиллит, ломоносовит, лопарит и интерстициальный виллиомит.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Химический состав (табл. 1) исследован методом электронно-зондового микроанализа с применением растрового электронного микроскопа Tescan Vega-II XMU (режим EDS, ускоряющее напряжение 20 кВ, ток 400 пА) и использованием системы регистрации рентгеновского излучения и расчета состава образца INCA Energy 450. Диаметр электронного пучка составил 157–180 нм. Диаметр зоны возбуждения – не более 5 мкм. Время накопления сигнала 100 с. Расстояние от образца до детектора 25 мм. В качестве стандартов использовали: альбит на Na, Al2O3 на Al, SiO2 на Si, NaCl на Cl, санидин на K, волластонит на Ca, монофосфаты Ln на соответствующие лантаноиды и чистые Ti, Mn, Fe, Y, Zr, Nb и Hf на соответствующие элементы. Эмпирическая формула минерала Кдк-6625, рассчитанная на 25.5 атомов Si, для усредненного состава имеет вид (Z = 3): Na13.47K0.03Sr0.76(Ce0.30La0.18Nd0.16Pr0.03Sm0.02)Ca5.16Mn1.36Fe0.39Zr2.85Hf0.03Nb0.26Ti0.25Si25.5S0.48Cl0.21Ox · · n(H3O,H2O). Пределы содержания компонентов, отражающие неоднородность состава изученного образца, следующие: Na12.81–14.02K0–0.11 Sr0.24–1.45(Ce0.20–0.43La0.11–0.27Nd0.10–0.24Pr0–0.09Sm0–0.06) Ca4.94–5.29Mn1.26–1.53Fe0.24–0.52Zr2.59–3.04Hf0–0.05Nb0.14–0.39 Ti0.11–0.38Si25.5S0.37–0.66Cl0.11–0.32Ox · n(H3O,H2O).
Таблица 1.
Химический состав минерала Кдк-6625 (мас. %)
| Компонент | Среднее содержание | Пределы | Стандартное отклонение |
|---|---|---|---|
| Na2O | 13.49 | 13.08–13.90 | 0.33 |
| K2O | 0.05 | 0.00–0.16 | 0.07 |
| CaO | 9.35 | 9.15–9.68 | 0.19 |
| MnO | 3.11 | 2.88–3.50 | 0.21 |
| FeO | 0.92 | 0.55–1.20 | 0.22 |
| SrO | 2.53 | 0.80–4.68 | 1.42 |
| La2O3 | 0.96 | 0.63–1.45 | 0.30 |
| Ce2O3 | 1.60 | 1.08–2.28 | 0.365 |
| Pr2O3 | 0.15 | 0.00–0.52 | 0.20 |
| Nd2O3 | 0.87 | 0.53–1.32 | 0.25 |
| Sm2O3 | 0.12 | 0.00–0.37 | 0.17 |
| SiO2 | 49.54 | 47.84–50.62 | 1.00 |
| TiO2 | 0.64 | 0.30–0.98 | 0.22 |
| ZrO2 | 11.37 | 10.40–12.35 | 0.59 |
| HfO2 | 0.21 | 0–0.48 | 0.41 |
| Nb2O5 | 1.12 | 0.59–1.67 | 0.42 |
| S | 0.50 | 0.38–0.67 | 0.08 |
| Cl | 0.24 | 0.12–0.36 | 0.08 |
| Сумма | 96.77 | 95.65–97.12 |
ИК-спектр образца Кдк-6625, предварительно растертого в агатовой ступке и запрессованного в таблетку с KBr, снят на фурье-спектрометре ALPHA FTIR (Bruker Optics, Германия) в диапазоне волновых чисел 360–3800 см–1 при разрешающей способности 4 см–1 и числе сканирований, равном 16. В качестве образца сравнения использована аналогичная таблетка из чистого KBr.
Для сбора дифракционных данных на монокристальном CCD-дифрактометре Xcalibur Oxford Diffraction (MoKα-излучение) был выбран фрагмент монокристалла изометричной формы. Характеристика кристалла и данные эксперимента приведены в табл. 2. Учитывая близость химического состава образца Кдк-6625 к составу манганоэвдиалита [4], в качестве стартового набора использовали координаты атомов его каркаса. Остальные позиции найдены из серии разностных синтезов электронной плотности. Состав катионов в позициях M1 и N3a уточняли с учетом смешанных кривых атомного рассеяния. Все расчеты выполнены по системе кристаллографических программ AREN [5]. Уточненные структурные параметры и характеристики координационных полиэдров приведены в табл. 3–5 соответственно.
Таблица 2.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структуры
| Идеализированная формула (Z = 3) | [(Na,Н3О)14Sr]Ca6(Mn2Na) Zr3[Si26O72](OH)3S2– · 2H2O |
|---|---|
| a, c, Å | 14.216(3), 30.405(1) |
| V, Å3 | 5321.16(5) |
| Сингония, пр. гр., Z | Тригональная, R3m, 3 |
| Размеры кристалла, мм | 0.1 × 0.1 × 0.25 |
| Дифрактометр | Xcalibur Eos CCD Oxford Diffraction |
| Излучение; λ, Å | MoKα; 0.71073 |
| Тип сканирования | Ω |
| Пределы h, k, l | 0 < h < 19, 0 < k < 19, 0 < l < 48 |
| (sin θ/λ)max | 0.798 |
| Общее количество/число независимых отражений с F > 3σF | 38791/2158 |
| Метод уточнения | МНК по F |
| R, % | 3.9 |
| Программы | AREN [5] |
Таблица 3.
Координаты позиций, кратность (Q) и эквивалентные параметры атомных смещений (Bэкв) атомов каркаса
| Позиция | x/a | y/b | z/c | Q | Bэкв, Å2 |
|---|---|---|---|---|---|
| М | 0.3343(1) | 0.1671(1) | 0.1669(1) | 9 | 1.30(3) |
| М1 | 0.4057(1) | 0.3333(1) | 0.3330(1) | 18 | 0.91(1) |
| Т1 | 0.5261(1) | 0.2631(1) | 0.2517(1) | 9 | 0.8(1) |
| Т2 | –0.0072(1) | 0.6034(1) | 0.0976(1) | 18 | 0.59(7) |
| Т3 | 0.2076(1) | 0.4151(1) | 0.0769(1) | 9 | 0.8(1) |
| Т4 | 0.0839(2) | 0.5419(1) | 0.2572(1) | 9 | 1.0(1) |
| Т5 | 0.0557(1) | 0.3250(1) | 0.2366(1) | 18 | 0.93(7) |
| Т6 | 0.1414(1) | 0.0707(1) | 0.0819(1) | 9 | 0.7(1) |
| О1 | 0.4725(7) | 0.2363(5) | 0.2034(2) | 9 | 2.2(4) |
| О2 | 0.2591(5) | 0.0306(5) | 0.2066(2) | 18 | 2.4(3) |
| О3 | 0.4101(4) | 0.3057(3) | 0.1282(1) | 18 | 1.3(3) |
| О4 | 0.6062(2) | 0.3938(2) | 0.2526(2) | 9 | 1.3(4) |
| О5 | 0.4352(5) | 0.2172(3) | 0.2889(1) | 9 | 1.0(5) |
| О6 | 0.4090(3) | 0.0349(4) | 0.0458(1) | 18 | 1.2(3) |
| О7 | 0.1020(4) | 0.3837(5) | 0.1069(1) | 18 | 2.0(3) |
| О8 | 0.0265(5) | 0.5132(3) | 0.1127(2) | 9 | 1.3(4) |
| О9 | 0.2740(2) | 0.5480(4) | 0.0678(3) | 9 | 3.7(1) |
| О10 | 0.1811(2) | 0.3622(3) | 0.0290(1) | 9 | 0.8(4) |
| О11 | 0.0295(7) | 0.5148(5) | 0.3033(2) | 9 | 1.9(4) |
| О12 | 0.1750(3) | 0.3510(4) | 0.2188(2) | 9 | 1.3(4) |
| О13 | 0.0383(4) | 0.2956(4) | 0.2871(1) | 18 | 1.6(3) |
| О14 | 0.3911(4) | 0.4337(4) | 0.2250(1) | 18 | 1.6(2) |
| О15 | 0.3949(3) | 0.6051(3) | 0.2507(3) | 9 | 2.3(1) |
| О16 | 0.0636(2) | 0.1273(3) | 0.0757(2) | 9 | 1.4(4) |
| О17 | 0.1902(6) | 0.0951(4) | 0.1299(2) | 9 | 1.6(4) |
| О18 | 0.2206(6) | 0.1103(4) | 0.0407(2) | 9 | 1.7(3) |
Таблица 4.
Координаты, кратность (Q) и заселенность (q) позиций и эквивалентные/изотропные параметры атомных смещений (Bэкв/изо) внекаркасных атомов
| Позиция | x/a | y/b | z/c | Q | q | Bэкв/изо*, Å2 |
|---|---|---|---|---|---|---|
| M2a | 0.5118(2) | 0.0238(3) | –0.0017(2) | 9 | 0.22(1) | 1.33(9) |
| M2b | 0.1491(1) | 0.2983(2) | 0.3365(1) | 9 | 0.35(1) | 1.35(5) |
| M2c | 0.4424(5) | 0.5576(5) | 0.0028(3) | 9 | 0.43(2) | 1.9(3) |
| M3a | 0.3334 | 0.6667 | 0.2436(2) | 3 | 0.50(1) | 1.4(1) |
| M3b | 0.3334 | 0.6667 | 0.2768(4) | 3 | 0.26(2) | 1.3(2) |
| M3c | 0.3334 | 0.6667 | 0.2948(1) | 3 | 0.22(2) | 0.99(7) |
| M4a | 0.3334 | 0.6667 | 0.0389(2) | 3 | 0.25(2) | 0.6(2) |
| M4b | 0.3334 | 0.6667 | 0.0571(7) | 3 | 0.22(2) | 1.7(2) |
| M4c | 0.3334 | 0.6667 | 0.0889(2) | 3 | 0.53(1) | 1.0(1) |
| N1a | 0.1149(1) | 0.2299(2) | 0.1523(1) | 9 | 0.20(4) | 1.73(7) |
| N1b | 0.0953(6) | 0.1907(9) | 0.1595(4) | 9 | 0.83(3) | 4.1(2) |
| N2a | 0.5618(2) | 0.4382(2) | 0.1784(2) | 9 | 0.60(3) | 1.2(3) |
| N2b | 0.589(2) | 0.178(2) | 0.161(1) | 9 | 0.20(4) | 2.8(3) |
| N2c | 0.5411(7) | 0.082(1) | 0.1873(6) | 9 | 0.20(1) | 2.1(4) |
| N3a | 0.1885(3) | 0.0942(2) | 0.2873(1) | 9 | 0.38(1) | 1.70(5) |
| N3b | 0.2392(8) | 0.1195(6) | 0.2760(3) | 9 | 0.40(1) | 1.6(1) |
| N3c | 0.220(4) | 0.110(3) | 0.259(3) | 9 | 0.20(1) | 6.1(6) |
| N4a | 0.4602(6) | 0.2301(4) | 0.0480(1) | 9 | 0.60(1) | 1.08(1) |
| N4b | 0.4278(9) | 0.2138(6) | 0.0614(3) | 9 | 0.40(1) | 2.1(2) |
| N5a | 0.4131(8) | 0.5869(8) | 0.1552(4) | 9 | 0.30(2) | 1.7(5) |
| N5b | 0.2655(6) | 0.5309(8) | 0.1895(6) | 9 | 0.30(5) | 2.2(2) |
| N5c | 0.372(2) | 0.551(2) | 0.1593(8) | 18 | 0.20(5) | 2.0(3) |
| X1a | 0 | 0 | 0.2912(3) | 3 | 0.41(1) | 2.0(2) |
| X1b | 0 | 0 | 0.257(3) | 3 | 0.39(5) | 7.5(6) |
| X2a | 0.6667 | 0.3334 | 0.0414(5) | 3 | 0.33(1) | 2.4(1) |
| X2b | 0.6667 | 0.3334 | 0.105(1) | 3 | 0.30(4) | 3.9(8) |
| OH1 | 0.3334 | 0.6667 | 0.1929(9) | 3 | 0.50(2) | 1.8(4) |
| OH2 | 0.3334 | 0.6667 | 0.1413(6) | 3 | 0.50(2) | 0.7(3) |
| OH3 | 0.3334 | 0.6667 | 0.331(1) | 3 | 0.26(4) | 4.0(10) |
| OH4 | 0.3334 | 0.6667 | 0.004(2) | 3 | 0.22(2) | 3.5(9) |
| OH5 | 0.6030(6) | 0.2060(9) | –0.0032(5) | 9 | 0.40(4) | 1.6(3) |
| OH6 | 0.404(3) | 0.596(3) | 0.013(1) | 9 | 0.43(3) | 3.5(5)* |
| H2O | 0.5541(1) | 0.108(1) | –0.0029(5) | 9 | 0.43(4) | 3.7(5) |
Таблица 5.
Характеристика полиэдров в ключевых позициях структуры
| Позиция | Состав (Z = 3) | КЧ | Расстояния катион–анион | ||
|---|---|---|---|---|---|
| Минимальное | Максимальное | Среднее | |||
| М | 3Zr | 6 | 2.028(7) | 2.101(6) | 2.071 |
| М1 | 5.4Ca + 0.6Ln | 6 | 2.289(5) | 2.417(4) | 2.359 |
| T1 | 3Si | 4 | 1.586(5) | 1.622(3) | 1.607 |
| T2 | 6Si | 4 | 1.595(3) | 1.642(7) | 1.616 |
| T3 | 3Si | 4 | 1.618(5) | 1.654(5) | 1.621 |
| T4 | 3Si | 4 | 1.546(8) | 1.665(5) | 1.610 |
| T5 | 6Si | 4 | 1.582(4) | 1.680(6) | 1.622 |
| T6 | 3Si | 4 | 1.574(6) | 1.669(3) | 1.625 |
| М2а | 0.66Mn | 5 | 2.120(9) | 2.24(1) | 2.173 |
| M2b | 1.05(Mn,Fe) | 5 | 1.955(6) | 2.194(6) | 2.132 |
| M2c | 1.29Na | 6 | 2.352(8) | 2.75(1) | 2.604 |
| M3a | 0.52Si | 4 | 1.537(1) | 1.58(5) | 1.55 |
| M3b | 0.26(Si,Al) | 4 | 1.708(8) | 1.65(4) | 1.69 |
| M3c | 0.22Nb | 6 | 1.90(1) | 2.02(1) | 1.96 |
| M4a | 0.25Ti | 6 | 1.707(7) | 1.91(4) | 1.81 |
| M4b | 0.22Si | 4 | 1.504(7) | 1.60(1) | 1.53 |
| M4c | 0.53Si | 4 | 1.590(1) | 1.599(6) | 1.596 |
| N1a | 0.6Sr | 8 | 2.509(6) | 2.708(8) | 2.647 |
| N1b | 2.4H3O | 6 | 2.51(2) | 2.67(1) | 2.57 |
| N2a | 1.8Na | 8 | 2.508(8) | 2.779(7) | 2.634 |
| N2b | 0.6Na | 7 | 2.46(2) | 2.98(3) | 2.59 |
| N2c | 0.6Na | 8 | 2.28(2) | 2.85(1) | 2.60 |
| N3a | 0.74Na + 0.1Sr + 0.3Ce | 10 | 2.311(3) | 2.975(6) | 2.688 |
| N3b | 1.26Na | 6 | 2.40(1) | 2.74(1) | 2.50 |
| N3c | 0.6H3O | 7 | 2.17(1) | 2.88(5) | 2.55 |
| N4a | 1.8Na | 8 | 2.492(8) | 2.97(1) | 2.70 |
| N4b | 1.2Na | 6 | 2.46(1) | 2.88(1) | 2.57 |
| N5a | 0.72Na | 4 | 2.21(2) | 2.94(1) | 2.59 |
| N5b | 0.9Na | 6 | 2.22(1) | 2.95(1) | 2.54 |
| N5c | 0.26Na | 5 | 2.41(2) | 2.86(2) | 2.57 |
ИК-СПЕКТРОСКОПИЯ
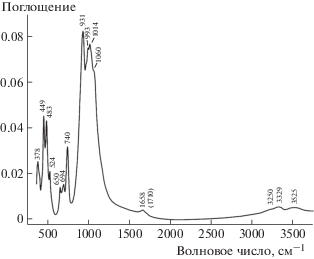
ИК-спектр минерала Кдк-6625 приведен на рис. 1. Спектральные полосы отнесены на основании данных об ИК-спектрах 22 эталонных образцов минералов группы эвдиалита, для которых были изучены химические составы и кристаллические структуры [1]. Полосы в диапазонах 3200–3600 и 1600–1800 см–1 соответствуют O–H-валентным и H–O–H-деформационным колебаниям. Плечи при 3250 и 1710 см–1, предположительно, относятся к ионам H3O+. Поглощение в области 900–1100 см–1 соответствует Si–O-валентным колебаниям. Высокая интенсивность полосы при 931 см–1 свидетельствует о высокой степени заселенности позиций M3 и M4 атомами Si.
Важно отметить отсутствие полос в области 1100–1200 см–1, которые могли бы быть отнесены к асимметричным валентным колебаниям тетраэдров SO4 [мода ν3(F2)]. В ИК-спектрах сульфатов этой моде соответствует интенсивная полоса. Таким образом, можно заключить, что значительные количества сульфатных групп в минерале Кдк-6625 отсутствуют. Деформационные и смешанные колебания групп из кремнекислородных тетраэдров проявляются в интервалах 440–490 и 640–750 см–1 соответственно. Полоса при 524 см–1 относится к валентным колебаниям (Mn,Fe)–O ионов Mn2+ и Fe2+, имеющих координационное число (КЧ) 5. Характерная для эвдиалита полоса валентных колебаний фрагментов Fe2+O4 с конфигурацией плоского квадрата (при 541–546 см–1) в ИК-спектре минерала Кдк-6625 отсутствует. Наиболее низкочастотная полоса при 378 см–1 соответствует решеточной моде, вовлекающей в себя валентные колебания связей Ca–O и колебания тетраэдрических колец как целого.
ОПИСАНИЕ СТРУКТУРЫ И ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Основные особенности состава и строения минерала Кдк-6625 отражены в его кристаллохимической формуле (Z = 3), которая находится в хорошем согласии с эмпирической: [Na9.7(Na,Н3О)2 (H3O)Sr0.7Ln0.3К0.02][Ca5.4Ln0.6] [V(Mn,Fe)1.05) VMn$_{{0.66}}^{{{\text{VI}}}}$Na1.29] [Zr2.95Hf0.05] [Si0.78Nb0.22] [Si0.75Ti0.25] [Si24O72] (OH,O)2.94(S$_{{0.48}}^{{2 - }}$Cl0.22) · 1.98Н2O, где квадратными скобками выделены составы ключевых позиций структуры, а римскими цифрами обозначены КЧ катионов. Идеализированная формула (Z = 3): (Na14Sr)Ca6(Mn2Na)Zr3[Si26O72] (OH)3S2– · 2H2O.
Гетерополиэдрический каркас в структуре данного минерала, как и других представителей группы эвдиалита [1], состоит из колец Si9O27, Si3O9 и Ca6O24, объединенных изолированными ZrO6-октаэдрами. Позиция М полностью занята атомами Zr с небольшой примесью Hf. Недостающее до шести атомов количество Са в М1-позиции восполняется за счет атомов редкоземельных элементов. Полости каркаса заполняются крупными катионами (преимущественно Na+, Sr2+) и оксониевыми группами H3O+ в N-позициях, которые расщепляются на две или три подпозиции, отстоящие друг от друга на расстояниях 0.5–1.4 Å. Атомы Sr находятся в двух полиэдрах – октаэдре и десятивершиннике со средними расстояниями N–O = 2.65 и 2.69 Å соответственно. Позиция N3a в десятивершиннике кроме Sr содержит натрий и лантаноиды.
Одной из особенностей химического состава образца Кдк-6625 является высокое содержание марганца, который занимает одну из ключевых позиций структуры – в пространстве между соседними шестичленными кольцами Са-октаэдров, ребра O–O которых образуют плоский квадрат. По обе стороны квадрата находятся две позиции на расстоянии 0.74 Å друг от друга: одна занята Mn, другая – совместно Mn и Fe. Координирующие их атомы кислорода образуют тетрагональные пирамиды с общим квадратным основанием, развернутые в противоположные стороны со средними расстояниями M2a–О = 2.176 и М2b–О = 2.145 Å соответственно. Третья позиция в этой микрообласти (М2с) отстоит от М2b на 0.99 Å и занята атомом Na, центрирующим шестивершинник со средним расстоянием Na–O = 2.66 Å. Все три полиэдра заполняются статистически, а среди конкурирующих катионов доминирует Mn2+.
Другая видообразующая позиция М3, располагающаяся на оси третьего порядка вблизи центра девятичленного кремнекислородного кольца Si9O27, расщеплена на три подпозиции, находящиеся на коротких расстояниях друг от друга: M3a–M3b = 1.01(1) и M3b–M3c = 0.54(1) Å. Они заняты атомами Si, (Si,Al) и Nb соответственно при доминировании атомов Si. Аналогично позиция М4 вблизи центра второго девятичленного кольца расщеплена на три подпозиции с расстояниями M4a–M4b = 0.53(2) и M4b–M4c = 0.98(2) Å, занятые атомами Ti, Si и Si соответственно, также при доминировании атомов Si.
Таким образом, с учетом 1.55 атомов Si, дополнительных к 24 атомам в кольцах кремнекислородных тетраэдров Т1–Т6 (табл. 3, 5), участвующих в построении гетерополиэдрического каркаса, исследованный образец относится к высококремнистым минералам группы эвдиалита. В нем содержится также 0.49 атома S на приводимую формулу (Z = 3), что превышает отмечавшееся ранее содержание серы в минералах группы эвдиалита (не более 0.46 атомов на формулу).
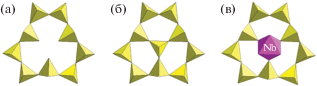
Еще одной особенностью данного образца, новой для группы эвдиалита, является присутствие в нем серы в сульфидной форме S2–. В структуре ряда минералов этой группы сера находится в шестивалентной форме и располагается в тетраэдрах в М3(М4)-позициях наряду с другими тетраэдрическими и октаэдрическими полиэдрами примесных катионов [1]. В ИК-спектрах этих минералов сульфатная группа, присутствующая в количествах более (SO4)0.2, проявляется в виде отчетливого плеча в диапазоне 1100–1200 см–1. Роль сульфатной серы в структурах минералов группы эвдиалита обсуждалась в ряде публикаций [1]. Позиции атомов кислорода в кольцах [Si9O27], координирующих позиции M3 и M4 (рис. 2), могут расщепляться в направлении, перпендикулярном плоскости кольца, на две или три подпозиции вследствие статистического заполнения позиций M3 и M4 различными компонентами [6–9]. Однако исследования большого количества образцов показали, что только на основании расстояний в М3(М4)-тетраэдрах не всегда удается однозначно решить вопрос о нахождении в них атомов S или Si. В ряде образцов, включая аквалит [3] и цирконо-ниобосиликат [4], тетраэдры SО$_{4}^{{2 - }}$ найдены в микрообласти X2, в которой в минералах группы эвдиалита обычно располагаются другие внекаркасные анионы (Cl–, F–, СO$_{3}^{{2 - }}$, РО$_{4}^{{3 - }}$), а также молекулы Н2О.
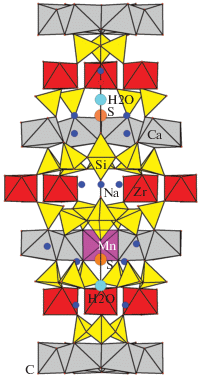
В минерале Кдк-6625 позиции О9 и О15 вследствие неразрешенного расщепления характеризуются параметрами атомных смещений Вэкв = 3.7 и 2.32 Å2, из-за чего в SiO4-тетраэдрах в позициях М3а и М4b расстояния М–О укорочены (средние 1.53 и 1.55 Å соответственно). Однако отнести их к тетраэдрам серы также затруднительно, так как они существенно превышают обычные для сульфатов расстояния 1.44–1.48 Å. Вместе с тем в обеих Х-позициях минерала Кдк-6625 кроме молекул воды присутствуют атомы хлора (0.21 атома на формулу) и серы (0.49 атома на формулу), причем тетраэдрическое окружение этих позиций не зафиксировано. Таким образом, предполагаем, что с большой долей вероятности (и в полном согласии с химическим составом) оба тетраэдра в М-позициях заняты атомами Si, а обе Х1а- и Х2а-подпозиции заселены S2– с небольшой примесью Cl– (рис. 3). Подпозиция Х1а находится на расстояниях 1.05(6) и 1.5(1) Å от молекулы воды и ОН-группы, принадлежащей SiO4-тетраэдру в центре девятичленного кольца соответственно. Позиция Х2а отстоит от другой подпозиции воды на расстоянии 1.92 Å, а от ОН-группы SiO4-тетраэдра в другом кольце – на 1.32 Å. В минерале Кдк-6625 имеет место статистическое заполнение двух Х-областей на оси третьего порядка анионами (S2–, Cl–) и молекулами Н2О приблизительно в равных пропорциях. Анионы S2– в микрообласти Х1 связывают две тройки полиэдров, находясь на расстоянии 2.322 Å от Sr, в микрообласти Х2 они участвуют в объединении трех Na-полиэдров на расстоянии 2.541 Å от центрального атома.
В исследованном образце Mn2+ является доминирующим катионом в микрообласти M2. Поэтому он близок к голотипам манганоэвдиалита [4] и илюхинита [10], а также к гидратированному образцу-6 из Кондерского массива (Хабаровский край) [11] и образцу 7639 из Норра Чер (Norra Kärr, Швеция) [12]. Несмотря на индивидуальные особенности в распределении катионов, в ключевых катионных позициях всех четырех образцов доминируют одни и те же элементы (табл. 6), а основное отличие изученного в работе образца касается заселенности Х-позиций, где S2– является преобладающим анионом. Локальное содержание серы достигает 0.66 атомов на формулу (при Z = 3). Наиболее высокий (по абсолютной величине) отрицательный корреляционный коэффициент для серы равен –0.51 из-за корреляции с Cl, что логично, так как сера замещает именно хлор.
Таблица 6.
Доминирующий состав внекаркасных ключевых позиций в структурах высокомарганцевых минералов группы эвдиалита
| Минерал | N1 | N2 | N3 | N4 | N5 | M2 | M3 | M4 | X1 | X2 | Литература |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Манганоэвдиалит | Na | Na | Na | Na | Na | MnVI | Si | Si | H2O | H2O | [4] |
| Илюхинит | H3O | Na | H3O | Na | H3O | MnV | Si | Si | H2O | H2O | [10] |
| Гидратированный эвдиалит-6 | Na | H3O | H3O | H3O | OH | MnV | Si | Si | Н2О | H2O | [11] |
| Образец-7639 | Na | Na | Na | Na | H3O | MnVI | Si | Si | Н2О | H2O | [12] |
| Образец Кдк-6625 | H3O | Na | Na | Na | Na | MnV | Si | Si | Н2О/S2– | H2O/S2– | Настоящая работа |
Минерал Кдк-6625 намечает новый изоморфный ряд в группе эвдиалита, конечным членом которого является S2–-доминантный минерал. Несмотря на то что анион S2– количественно уступает молекулам H2O в микрообластях Х1 и Х2 минерала Кдк-6625, он является там доминирующим анионом, что позволяет рассматривать этот минерал как потенциально новый минеральный вид, учитывая в качестве прецедента выделение карбокентбруксита (Na,Ce)15Ca6Mn3Zr3Nb(Si25O73) (OH)3(CO3) · H2O в качестве самостоятельного минерала, в котором анион CO32– является видообразующим компонентом. Вхождение серы в состав минерала Кдк-6625 в сульфидной форме может быть связано с восстановительными условиями минералообразования. Ранее [13] обсуждалась роль массовой кристаллизации эгирина на начальной стадии формирования агпаитовых пегматитов в создании восстановительных условий, в которых также образуются органические соединения. Если предположить, что исходный флюид содержал Na, Fe2+ и CO2, то кристаллизация эгирина должна сопровождаться окислительно-восстановительными процессами, которые упрощенно могут быть описаны реакциями, где степень окисления углерода изменяется от +4 до +2 и даже до нуля, а Fe2+ окисляется до Fe3+: Na2O + + 2FeO + 4SiO2 + CO2 → 2NaFeSi2O6 + CO; Na2O + + 2FeO + 4SiO2 + 0.5CO2 → 2NaFeSi2O6 + 0.5C. Заметим, что если исходный флюид беден натрием, но обогащен кальцием, то вместо эгирина в данной системе будет кристаллизоваться геденбергит, а восстановления углерода не произойдет: CaO + FeO + 2SiO2 + CO2 → CaFeSi2O6 + CO2.
Такая ситуация наблюдается, например, в высокощелочных пегматитах Ковдорского массива на Кольском п-ове, секущих кальцитовые карбонатиты и сильно контаминированных кальцием. Вероятно, аналогичную роль (вместо углерода) может играть сера. В этом случае при массовой кристаллизации эгирина – минерала с Fe3+ – будет происходить восстановление S(VI) сначала до S(IV), а затем и до сульфидного аниона. По аналогии с рядом минералов, содержащих сульфидную серу и обладающих ярко-желтой окраской (быстрит, сульфидсодержащий везувиан, Fe-дефицитная разновидность гельвина), можно предположить, что необычный желтый цвет минерала Кдк-6625 связан именно с присутствием аниона S2–.
ВЫВОДЫ
Исследованный в настоящей работе представитель группы эвдиалита является потенциально новым минералом, в котором впервые (с привлечением методов рентгеноструктурного анализа и ИК-спектроскопии) для этой группы зафиксировано присутствие серы в сульфидной форме. Предположительно, вхождение ионов S2– в структуру минерала является следствием его образования в восстановительных условиях. Вполне возможно, что “существенно” сульфидные эвдиалиты не являются редкостью: в большинстве случаев при изучении эвдиалитов серу не включают в анализ из-за низкого содержания: например, в случае Ловозерского массива – от 0.06 до 0.19 мас. % [14]. Между тем можно предположить, что при кристаллизации эвдиалита содержание серы было выше и снизилось до наблюдаемых значений в ходе постмагматических процессов, поскольку в экспериментально закристаллизованном эвдиалите было обнаружено 0.3 мас. % S [15].
Работа выполнена при поддержке Министерства науки и высшего образования в рамках Государственного задания ФНИЦ “Кристаллография и фотоника” РАН в части рентгеноструктурного анализа и Государственного задания по теме 0089-2019-0013 в части ИК-спектроскопии Российского фонда фундаментальных исследований в части кристаллохимического анализа микропористых минералов группы эвдиалита (проект № 18-29-12005) и анализа химического состава (проект № 18-29-12007).
Список литературы
Расцветаева Р.К., Чуканов Н.В., Аксенов С.М. Минералы группы эвдиалита: кристаллохимия, свойства, генезис. Нижний Новгород: Изд-во НГУ, 2012. 229 с.
Johnsen O.E., Grice J.D. // Can. Mineral. 1999. V. 37. № 4. P. 865.
Расцветаева Р.К., Хомяков А.П. // Кристаллография. 2002. Т. 47. № 2. С. 267.
Номура С.Ф., Атенсио Д., Чуканов Н.В. и др. // Зап. Рос. минерал. о-ва. 2010. Ч. 139. № 4. С. 35.
Андрианов В.И. // Кристаллография. 1987. Т. 32. Вып. 1. С. 228.
Расцветаева Р.К., Хомяков А.П. // Докл. РАН. 1998. Т. 362. № 6. С. 784.
Расцветаева Р.К., Хомяков А.П., Некрасов Ю.В. // Кристаллография. 1999. Т. 44. № 5. С. 824.
Расцветаева Р.К., Аксенов С.М., Чуканов Н.В. // Докл. РАН. 2010. Т. 432. № 5. С. 639.
Аксенов С.М., Расцветаева Р.К. // Кристаллография. 2013. Т. 58. № 5. С. 660.
Расцветаева Р.К., Розенберг К.А., Чуканов Н.В., Аксенов С.М. // Кристаллография. 2017. Т. 62. № 1. С. 69.
Rozenberg K.A., Rastsvetaeva R.K., Khomyakov A.P. // Eur. J. Mineral. 2005. V. 17. P. 875.
Расцветаева Р.К., Чуканов Н.В., Мёккель Ш. и др. // Кристаллография. 2020. Т. 65. № 1. С. В печати.
Ермолаева В.Н., Чуканов Н.В., Пеков И.В., Когарко Л.Н. // Зап. Рос. минерал. о-ва. 2008. Ч. 137. № 5. С. 17.
Кузнецова С.Я. Геохимия серы в дифференцированных щелочных массивах. М.: Наука, 1986. 168 с.
Когарко Л.Н. Лазуткина Л.Н. Кригман Л.Д. Условия концентрирования циркония в магматических процессах. М.: Наука, 1988. 119 с.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография