Кристаллография, 2020, T. 65, № 2, стр. 173-179
Трифториды лантана и лантаноидов: лантаноидное сжатие и объем иона фтора
1 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
* E-mail: sobolevb@yandex.ru
Поступила в редакцию 03.04.2019
После доработки 03.04.2019
Принята к публикации 17.06.2019
Аннотация
Лантаноидное сжатие лантана и 14 лантаноидов (Ln), вызывающее уменьшение на ∼15% (к меньшему) ионных радиусов R3+ с ростом атомного номера элемента Z, – способ достижения плотной упаковки ионов F1– в трифторидах тяжелых 4f-элементов Периодической системы элементов. Оценена эффективность лантаноидного (Ln) и актиноидного (An) сжатия для получения кристаллов неорганических фторидов с минимальным объемом элементарной ячейки на один фтор-ион (VF). Для AnF3 (An = Ac–Am) c ростом Z от 89 до 95 величина VF понижается с ∼20 до ∼17.4 Å3. Недоступность тяжелых An делает эту величину окончательной. Плотнейшей упаковки фтор-иона во фторидах, используя эффекты лантаноидного и актиноидного сжатия и увеличения валентности катиона, достичь не удалось. Фториды LnF3 (структурный тип β-YF3) конца ряда от ErF3 (15.86 Å3) до LuF3 (15.48 Å3) ближе всего к плотнейшей упаковке анионов. Последняя величина VF минимальна для всех изученных LnF3 и фторидов актиноидов (простых и комплексных) и близка к насыщению. Ей отвечает оценочное значение ионного радиуса фтор-иона 1.246 Å.
ВВЕДЕНИЕ
Атомные и ионные радиусы R и R3+ в семействе редкоземельных элементов (РЗЭ – R) растут с ростом атомного номера элемента Z при переходе по III группе от 21Sc к 39Y и 57La. Эта общая закономерность Периодической системы впервые нарушается у Ln. У следующего за лантаном церия начинается заполнение 4f-подоболочки. Более сильное взаимодействие электронов 4f-подоболочки с ядром порождает обратную зависимость радиусов R и R3+ – уменьшение с ростом Z. Этот эффект V.M. Goldschmidt (1925) назвал “лантаноидным сжатием”. Лантаноидное сжатие атомов и ионов 14 лантаноидов (и актиноидное сжатие родственного семейства 14 An) является одним из фундаментальных явлений, определяющих изменения свойств и кристаллохимию соединений семейств 4f- и 5f-элементов.
Эффект сжатия ионных радиусов 4f- и 5f-элементов в неорганических фторидах с ионным характером химической связи и простой химической формулой давно представлял фундаментальный кристаллохимический интерес. Он выражался в поиске гомологического ряда соединений Ln или An, в которых при росте атомного номера элемента Z и лантаноидном (4f-элементы) или актиноидном (5f-элементы) сжатии достигается независимость параметров элементарной ячейки соединения от размера катиона (Ln или An соответственно). Это будет означать касание ионов фтора, по которому можно определить занимаемый одним F1– объем VF. При низкой поляризуемости F1– и его сферичности из объема VF можно независимо оценить ионный радиус фтора. Полагается, что VF для фторидов лантаноидов и актиноидов близок или одинаков. Ранее был изучен эффект только актиноидного сжатия, не приводящий к плотнейшей упаковке фтор-ионов.
Задача определения размеров анионов имеет исторические прецеденты, не все из которых завершились успешно. Проблема нахождения размера хотя бы одного иона, чтобы рассчитать размеры другого, образующего с первым химическое соединение, уходит корнями в историю выработки систем ионных радиусов. Для обоснованного деления межатомного расстояния “катион–анион” (абсолютной величины из структурного анализа) надо определить независимым методом размеры одного из них.
В 20-х гг. прошлого столетия А. Ланде предположил, что в кристаллах с “мелкими” катионами и крупными анионами, начиная с некоторого размера аниона А, между ними возникает контакт, и размер катиона перестает влиять на период элементарной ячейки соединения. Объем, приходящийся на один анион в гомологическом ряду соединений (с одинаковой формулой RmAn), становится постоянным. Он определяется расстоянием “анион–анион”, из которого вычисляется размер аниона. Предположение подтверждено на изоструктурных NaCl рядах оксидов, сульфидов и селенидов Mg и Mn. Это направление поиска плотной анионной упаковки для крупных анионов завершилось успехом.
Для самого мелкого аниона, каким является F1–, решение аналогичной задачи сложнее. При фиксированном анионе надо подобрать самые “мелкие” катионы в Периодической системе, образующие фториды. Полагали, что чем выше атомный номер Z, тем меньше размер его высокозарядного катиона [1]. Это предположение направило поиск плотноупакованных по фтору соединений на фториды An. Поиск определялся прогрессом получения 5f-элементов – An = 89Ac, 90Th, 91Pa, 92U и трансурановых элементов до лоуренсия 71Lr. Однако тяжелые 5f-элементы (Bk, Cf, Es, Md, No, Fm, Lr) получены в виде короткоживущих радиоактивных изотопов в очень малых количествах и мало изучены. Для легких An поиск предпринят в конце 50-ых [2]. Он положительного результата не дал, в том числе, из-за недоступности фторидов тяжелых An.
Параллельно с этим направлением проверялось увеличение валентности катионов выше 3+. Оно не учитывало изменения характера химической связи и оказалось неэффективным.
Семейство Ln принадлежит к побочной подгруппе III группы 6 периода Периодической системы элементов, как и семейство актиноидов, располагающееся в 7 периоде. Изменение радиусов rR ионов РЗЭ по ряду меняет знак с положительного (рост rR при 21Sc → 39Y → 57La по III группе) на отрицательный (лантаноидное сжатие по 6 периоду от 57La → 71Lu). Преимущество Ln перед An в полной доступности LnF3 для всего ряда, кроме PmF3. Cейчас его производство налажено и определены температура плавления, тип структуры и параметры элементарной ячейки.
Эффект лантаноидного сжатия уменьшает размеры Ln и позволяет использовать рост Z до крайнего члена семейства – 71Lu. Это может привести к плотной фторной упаковке с катионами в пустотах.
Сравнение лантаноидного и актиноидного сжатия в достижении минимальных VF во фторидах 4f- и легких 5f-элементов проводится впервые.
Цель исследования – оценка возможности лантаноидного сжатия РЗЭ для достижения минимального объема элементарной ячейки VF на один фтор-ион в кристаллах RF3 и сравнение с изученным ранее с этой целью эффектом актиноидного сжатия в простых и комплексных фторидах легких An.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Ионные радиусы R3+во фторидах РЗЭ. Для оценки эффекта лантаноидного сжатия надо выбрать систему ионных радиусов катионов РЗЭ. Подавляющее большинство систем имеют точность ±0.01 Å. С этой точки зрения системы Гольдшмидта (1926), Захариасена (1931), Кордеса (1940), Аренса (1952), Бокия (1954) и другие непригодны для анализа свойств РЗЭ и их соединений. При изменении Z РЗЭ на единицу rR меняется в среднем на ΔrR ∼ 0.014 Å. В абсолютной шкале сомнителен и второй знак, но для анализа свойств РЗЭ по ряду нужна система относительных радиусов до ±0.001 Å.
Для прецизионного анализа лантаноидного сжатия наиболее пригодна «специализированная» система радиусов R3+ в RF3 для КЧ 9 по [3], рассчитанных из высокоточных (±0.0005 Å) измерений параметров решеток RF3 структурных типов LaF3 и β-YF3. В этой системе лантаноидное сжатие монотонно уменьшает rR на 15% (к меньшему) при росте Z от 57 до 71 в отличие от других систем, не обнаруживая “гадолиниевого” скачка (вклада).
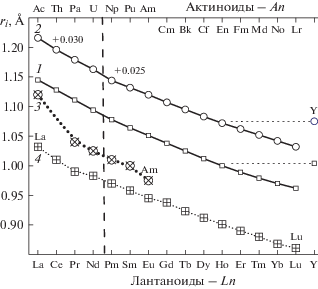
Однако для сравнения лантаноидного и актиноидного сжатия требуется универсальная система “эффективных” ионных радиусов [4], в которой есть ионные радиусы актиноидов. Для РЗЭ эта система использовала их радиусы [3], к которым сделаны поправки: +0.030 Å для ионов La3+–Nd3+ с КЧ 9 и +0.025 Å для остальных РЗЭ с КЧ 9. Поправки обеспечивали универсализацию системы. Последствия поправок видны на рис. 1. Кривая 1 по [3] монотонна на всем интервале La–Lu, показывая изменение rR (КЧ 9) с ростом Z. Кривая 2 по [4] (КЧ 9) с поправками, разными для разных групп РЗЭ. Пунктирная вертикаль разделяет поправки для цериевой (+0.030) и иттриевой (+0.025) подгрупп РЗЭ, порождающие излом между Nd и Pm.
Кривая 3 рис. 1 дает ионные радиусы легких актиноидов от 89Ac до 95Am для состояния 3+ и КЧ 6 по [4]. Эти элементы имеют наиболее долгоживущие изотопы, и их свойства изучены лучше. Все эти AnF3 имеют тип LaF3, и КЧ 6 не соответствует структурным данным. Для сравнения их с Ln пришлось использовать радиусы для Ln по [4] также для КЧ 6, кривая 4. Кривые 3 и 4 показывают, что лантаноидное сжатие приводит к более низким значениям ионных радиусов катионов R3+ (при сопоставимых КЧ). К сравнению лантаноидного и актиноидного сжатия вернемся ниже.
Лантаноидное сжатие в трифторидах РЗЭ. Лантаноидное сжатие проявляется в уменьшении радиуса rR катиона R3+ по ряду РЗЭ. Соответственно, уменьшаются формульный объем Vform и объем VF, приходящийся на один ион. Абсолютные величины влияния одного электрона на размер иона различны на участках 39Y3+–57La3+ (переход по группе, ΔZ = 18) и 57La3+–71Lu3+ (переход внутри 6 периода, ΔZ = 14).
При переходе по III группе прирост ионного радиуса 1.050–1.186 Å дает ∼0.008 Å на одну атомную единицу. Лантаноидное сжатие R3+ уменьшает rR по 6 периоду для 15 РЗЭ от La3+ до Lu3+ от 1.186 до 1.007 Å (радиусы по [3] для КЧ 9), что отвечает ∼0.013 Å на одну атомную единицу. Количественно различие в ∼2 раза усугубляется принципиально – изменением знака. Его связывают с различием между этими двумя участками Периодической системы элементов (Z = 39–57 и 57–71) в принадлежности электронов к внешним оболочкам на первом и “глубинной” 4f-подоболочке на втором. Лантаноидное сжатие велико, и размеры ионов тяжелых РЗЭ (Er–Lu) меньше, чем Y3+ c более низким (на 29 единиц) зарядом ядра. По свойствам YF3 располагается во второй половине ряда LnF3.
Объем иона F1– (VF) в трифторидах лантаноидов. В [5] при анализе внутренней периодичности фазовых превращений в трифторидах иттрия, лантана и лантаноидов (RF3) впервые приведены изменения формульного объема Vform по всему ряду RF3 (R = Y, La, Ln, включая Pm) для структурных типов LaF3 и β-YF3 по [3, 6]. Их Vform состоит из вклада объема катионов (меняется по ряду РЗЭ, определяется лантаноидным сжатием), анионного вклада (постулируется одинаковым для всех LnF3) и вклада плотности структурной упаковки (может быть периодичным и разным для разных структур).
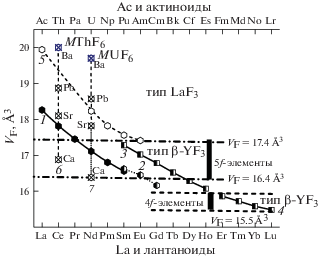
Интересен постоянный вклад – объем элементарной ячейки VF, приходящийся на один ион фтора, рис. 2. Для решения задачи о плотнейшей упаковке фтор-ионов в RF3 надо найти трифторид, у которого VF становится минимальным и остается постоянным при дальнейшем росте Z. Это выявит контакт анионов в структуре фторида. Из минимального VF оценивается ионный радиус F1– как радиус сферы, вписанной в куб с ребром VF. Обоснование величины радиуса F1– требует отдельного рассмотрения.
Информация об изменении VF по обоим рядам фторидов семейств 4f- (нижняя шкала) и 5f-элементов (верхняя шкала) содержится на рис. 2. Для всех лантаноидов, включая Pm, есть данные по Vform и VF. Расчет VF всех RF3 (кривые 1–4 рис. 2) сделан по Vform из параметров решетки. Для RF3 типа LaF3 (R = 57La–62Sm) кривая 1 рассчитана по [3]. Значение VF для α-PmF3, полученное из параметров решетки по [8], хорошо ложится на кривую 1.
Кривая 2 получена [6] для тисонитовых диморфных α-RF3 (R = Sm–Gd) экстраполяцией на RF3 зависимостей параметров решетки от содержания MF2 закаливающихся фаз R1 – yMyF3 – y (M = Ca, Sr).
Выводы. Из изменения VF по ряду лантаноидов (рис. 2) следует: эффект лантаноидного сжатия для RF3 изучен полностью; он приводит к существованию кристаллов β-LuF3 с VF = 15.48 Å3, близким к плотнейшему; лантаноидное сжатие отчетливо на обоих участках ряда RF3 со структурами типов LaF3 (R = La–Gd) и β-YF3 (R = Sm–Lu); в уменьшение VF за счет лантаноидного сжатия дополнительный вклад к катионному вносит полиморфный переход от типа LaF3 к типу β-YF3 с ΔVF в среднем +4.2% (к меньшему); величины VF для RF3 от ErF3 (15.86 Å3) до LuF3 (15.48 Å3) близки к насыщению; этот интервал VF минимален для LnF3. На рис. 2 он обозначен двойной вертикалью и надписью “4f-элементы”.
Актиноидное сжатие в простых и комплексных фторидах An. Семейство 5f-элементов – актиноидов – начинается с родоначальника Ac, после которого с Th идет заполнение 5f-подуровня. Для An эффект актиноидного сжатия аналогичен сжатию у 4f-элементов (58Ce–71Lu). Актиноидное сжатие уменьшает размеры катионов An3+ с ростом Z.
Изучение актиноидного сжатия в отличие от лантаноидного ограничено первой половиной ряда An. Это затрудняет сравнение, так как для легких Ln и An химические различия максимальны из-за электронной структуры последних. Для легких An более устойчивы 6d-орбитали, а для тяжелых – 5f. Для 90Th–95Am энергия 5f- и 6d-подуровней примерно одинакова, и элементы могут находиться в нескольких состояниях окисления. У тяжелых An по мере заполнения 5f-уровней электронные конфигурации стабилизируются, и переход 5f-электронов в 6d-состояние становится все более затрудненным. Поэтому 97Bk–103Lr по свойствам их AnF3 должны приближаться к LnF3 со степенью окисления Ln3+. Однако эти AnF3 недоступны и только можно полагать их подобие LnF3.
Участие в химической связи 5f-электронов у An начала ряда приводит к высоким валентностям, в частности, Th4+ и U4+. Это уменьшает их ионный радиус и открывает возможность получения комплексных фторидов, содержащих, как предполагалось, одни из самых «мелких» катионов – An4+.
На рис. 2 в отличие от автора [2], использовавшего для анализа изменений VF ионные радиусы An (определены неточно и требуют поправки на КЧ, рис. 1), сравнение объемных изменений в рядах LnF3 и AnF3 проводится в абсолютной шкале Z. Прямого сопоставления этих эффектов не было найдено.
Исследования кристаллохимии 5f-элементов вызваны Манхэттенским проектом. В [2] показана принадлежность AcF3 и фторидов актиноидов: UF3, NpF3, PuF3, AmF3 к типу LaF3 и определены параметры их решетки. На рис. 2 на верхней оси – ряд An от 89Ac до 103Lr. Элементы – аналоги двух химических семейств – располагаются друг под другом. Кривая 5 отвечает величинам VF трифторидов начала ряда An. Пропуская фторид Th (не имеет валентности 3+) и Pa (3+), она доходит до Am (3+) включительно [2].
С ростом Z у AnF3 (An = Ac–Am) VF заметно понижается на участке ряда с ~ 20 до ~ 17.4 Å3 и намечается тенденция к насыщению кривой 5 рис. 2. Недоступность тяжелых An делает эксперимент на рис. 2 по влиянию актиноидного сжатия в AnF3 на VF окончательным. Минимальное для изученных AnF3 значение VF = 17.41 Å3 у AmF3 на рис. 2 отмечено верхней штрихпунктирной горизонталью. На этом заканчивается направление поиска [2] плотнейшей упаковки F1– в AnF3, которая не получена.
Минимальное значение VF для AnF3 не предельно среди изученных в [2] соединений типа LaF3. Получены двойные фториды гомологических рядов MThF6 (M = Ba, Pb, Sr, Ca) и MUF6 (M = Ba, Pb, Sr). Пунктирные вертикали 6 и 7 на рис. 2 отвечают изменению их VF. Cоединение СaUF6 синтезировано в [7]. Оно также имеет структуру типа LaF3. Для всех M(Th,U)F6 (вертикали 6 и 7), кроме Ba(Th,U)F6, получены более низкие VF, чем для соответствующих простых трифторидов AcF3–AmF3 (кривая 6).
Предположение [2] о минимизации объемов катиона с ростом валентности An подтверждено в [7] и найдено ограничение на понижение VF у Ba(Th,U)F6 с крупным катионом Ba2+. Переход к двойным соединениям сопровождается уменьшением среднего радиуса катиона (M0.5An$_{{0.5}}^{{4 + }}$)3+ и VF с падением радиуса M2+ по ряду Ba2+ → Pb2+ → → Sr2+ → Ca2+ от 20 до 16.38 Å3. Минимальные VF среди изученных двойных фторидов с мелкими An4+ для CaThF6 [2] и CaUF6 [7] достаточно близки. Однако и для них общий ход зависимости VF от ионного радиуса M2+ не имеет выраженного насыщения.
Минимальный VF ∼ 16.4 Å3 для CaUF6 выделен на рис. 2 второй штрихпунктирной горизонталью. До этой величины расширяется поле значений VF, полученных в простых и комплексных фторидах An начала ряда от Ac до Am. Все фазы в этом поле изоструктурны и принадлежат к плотноупакованному типу LaF3. Интервал минимальных VF для трифторидов и двойных фторидов актиноидов составляет 17.4–16.4 Å3. На рис. 2 он выделен двойной вертикалью и обозначен “5f-элементы”.
Выводы. Из [2], рис. 2 для AnF3 следует: актиноидное сжатие отчетливо на участке первой половины ряда An = AcF3–AmF3, доступной для исследования; минимальные VF в AnF3 составляют 16.4–17.4 Å3 и ниже опубликованного в [1] значения 18 Å3 как предела плотности упаковки F1– во фторидах; эти VF не минимальны для простых и комплексных фторидов An, поскольку есть более тяжелые, но недоступные An.
Лантаноидное и актиноидное сжатие во фторидах. Имеющиеся данные позволяют сравнить лантаноидное и актиноидное сжатие для фторидов 4f- и части легких 5f-элементов. При формальной идентичности заполнения f-подоболочек, химически роднящей семейства лантаноидов и актиноидов, между ними есть различия. Они проявляются для первых членов каждого ряда и выражаются в участии 5f-электронов некоторых актиноидов в химической связи. Оно порождает различие валентностей и химических свойств аналогов семейств, которое к концу рядов минимизируется.
Не углубляясь в различия, выходящие за рамки сообщения, используем данные по лантаноидному и актиноидному сжатию для сравнения. Неважно, из каких фторидов определены VF, важно, чтобы VF было минимальным.
Рассмотрим величину ΔVF уменьшения формульных объемов Vform на 1 Z, приведенную на рис. 3. Для первой группы доступных фторидов актиноидов от AcF3 до NpF3 усредненные изменения ΔVF показаны кривой 1.
Рис. 3.
Изменение объемных эффектов сжатия ΔVF трифторидов на один атомный номер Z по рядам 4f- (лантаноидное) и 5f-элементов (актиноидное).
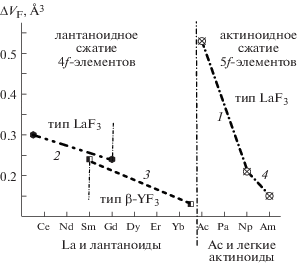
На участке ряда AnF3 (An = Ac–Np) ΔVF падает от 0.53 до 0.21 Å3 на 1 Z. Затем на участке An = = Np–Am падение ΔVF замедляется, приближаясь к 0.21–0.15 на 1 Z. Все изученные AnF3 (An = = Ac–Am) изоструктурны, и морфотропных переходов не содержат. Недоступность оставшихся AnF3 (An = Cf–Lr) оставляет открытым вопрос о близости лантаноидного и актиноидного сжатия для вторых половин рядов.
Для участка ряда RF3 (R = La–Gd) типа LaF3 ΔVF падает от 0.30 до 0.24 Å3 на 1 Z, а для RF3 (R = = Sm–Lu) типа β-YF3 от 0.24 до 0.13 Å3 на 1 Z. У фторидов лантаноидов от Sm до Lu на эффект лантаноидного сжатия накладывается скачок ΔVF (кривые 2, 3) при морфотропной смене структуры типа LaF3 на тип β-YF3. Вклад морфотропии в ΔVF невелик из-за структурного родства типов. Для RF3 типа β-YF3 выделяются тяжелые РЗЭ (рис. 2, 3), для которых эффект лантаноидного сжатия близок к насыщению.
Для AnF3 начала ряда (кривая 1) величина эффекта сжатия ΔVF приблизительно вдвое выше, чем для изоструктурных им LnF3 начала ряда лантаноидов (La–Gd, кривая 2). Отметим, что на этот же участок ряда актиноидов приходится увеличение ионного радиуса An3+ (кривая 3 на рис. 1). По-видимому, это не случайное совпадение, так как оно коррелирует с различием электронного строения элементов именно этих участков рядов.
Дальнейший поиск соединений с плотнейшей фторной упаковкой среди простых фторидов актиноидов для изучения эффекта актиноидного сжатия следует признать бесперспективным по причине недоступности тяжелых актиноидов и большой разнице VF AmF3 (17.41 Å3) и LuF3 (15.48 Å3).
Выводы. Сравнивая поиск [1, 2] наиболее плотноупакованных по фтору простых и комплексных фторидов актиноидов и полученные в настоящей работе данные по LnF3, приходим к выводам: к плотнейшей упаковке F1– приближаются RF3 конца ряда (тип β-YF3): ErF3, HoF3, TmF3, YbF3, LuF3 (в порядке уменьшения ΔVF); на начальных участках рядов LnF3 и AnF3 эффект актиноидного сжатия на ΔVF преобладает над лантаноидным, уравниваясь для начала второй половины обоих рядов.
Ограничения уменьшения размеров катионов во фторидах увеличением их валентности. Рассмотрим еще один путь получения плотнейшей упаковки ионов фтора – уменьшение размера катиона повышением его валентности, предложенный в [1]. Получены и изучены фториды урана с переменной валентностью: UF3, UF4, U4F9, α-UF5, β-UF5, UF6. Ожидалось, что «мелкие» высокозарядные катионы урана должны располагаться в пустотах структуры, а упаковка анионов стать плотнейшей. Средняя величина VF составила для перечисленных шести фторидов 18.3 Å3 на один F1–. Эту величину автор [1] предложил считать некоторой предельной плотностью упаковки анионов в простых фторидах с “мелкими” катионами актиноидов. Его оценка вошла в литературу. Ей отвечает значение ионного радиуса фтора rF = = 1.310 Å, близкое к принятым в нескольких системах ионных радиусов.
Может ли быть принята эта величина для всех фторидов? Из VF для шести фторидов урана (18.1, 19.4, 16.9, 19.0, 17.0, 19.3 Å3 соответственно) следует вывод о большом разбросе (14% к меньшему), не отвечающем точности определения параметров решетки. Главное сомнение вызывает допущение независимости расстояний “катион–фтор” от характера химической связи, которое негласно принимается [1] при усреднении приведенных величин VF.
Влияние характера химической связи на межатомные расстояния “катион–фтор” принципиально для выработки любой системы ионных радиусов. В рассмотренном ряде фторидов урана характер химической связи хорошо изучен в силу областей их применения. Оценка характера связи определяется температурами плавления. Возьмем три наиболее изученных фторида урана:
Ковалентизация связи с ростом валентности урана разительно уменьшает температуры плавления с 1500 до 1036 и 65°С соответственно. При этом VF меняются как 18.1 → 19.4 → 19.3 Å3 по [1]. Все соединения имеют разный характер химической связи и тип структуры. Рост валентности урана не увеличивает плотность упаковки фтор-ионов, как предполагалось. Ковалентизация связей ведет к обратному эффекту – сохранению VF.Эффект стабилизации фтор-ионом предельных состояний валентности металлов путем образования комплексных ионов с экранировкой центрального катиона малым лигандом с высокой электроотрицательностью хорошо известен. В случае урана UF6 становится летучим, что выгодно для его практического применения. Но для оценки объема F1–An6+ не пригоден.
Выводы о влиянии валентности катионов на свойства фторидов урана распространяются и на фториды других высокозарядных катионов. На рис. 4 показано, что фториды 5- и 6-зарядных катионов обладают температурами плавления, более чем на 500°С низкими, чем 1–4-зарядные.
Рис. 4.
Изменение температур плавления некоторых фторидов MFm в зависимости от валентности катиона m+.
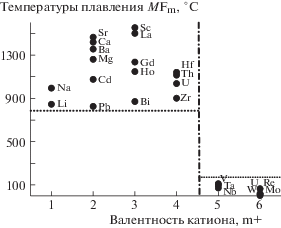
Разрыв происходит резко и не оставляет надежд на продолжение поиска высокозарядных “мелких” катионов для определения размера фтор-иона во фторидах. По-видимому, это направление не имеет перспектив.
В табл. 1 приведены объемы VF (Å3) на один ион фтора, минимальные (min) и максимальные (max) по группам соединений Ln [3, 6] и An [1, 2, 7].
ЗАКЛЮЧЕНИЕ
Достижение плотнейшей упаковки F1– для определения его размера в неорганических фторидах, используя эффекты лантаноидного и актиноидного сжатия и увеличения валентности катиона до 4+, исчерпано. Результата достичь не удалось. Ближе всего к плотнейшей упаковке анионов RF3 конца ряда (структурный тип β-YF3): ErF3, HoF3, TmF3, YbF3, LuF3 (в порядке роста плотности). Полученный минимальный VF составляет 15.48 Å3, что отвечает оценочной величине ионного радиуса F1–rF = 1.246 Å. Анализ кристаллохимии трифторидов РЗЭ приведет к несколько иному значению, вероятно, меньшему и зависящему от координационного окружения.
Автор выражает благодарность П.В. Костоглодову и Н.И. Сорокину за обсуждения.
Работа выполнена при поддержке Министерства науки и высшего образования в рамках работ по Государственному заданию ФНИЦ “Кристаллография и фотоника” РАН.
Список литературы
Zachariasen W.H. // J. Am. Chem. Soc. 1948. V. 70. № 6. P. 2147.
Zachariasen W.H. // Acta Cryst. 1949. V. 2. № 6. P. 388.
Greis O., Petzel T. // Z. Anorg. Allg. Chem. 1974. B. 403. № 1. S. 1.
Shannon R.D. // Acta Cryst. A. 1976. V. 32. № 5. P. 751.
Соболев Б.П. // Кристаллография. 2019. Т. 64. № 5. С. 701.
Соболев Б.П., Гарашина Л.С., Федоров П.П. и др. // Кристаллография. 1973. Т. 18. Вып. 4. С. 751.
Некрасова Н.П., Обломеев Е.Н., Безносикова А.В. // Атомная энергия. 1967. Т. 22. № 4. С. 293.
Волков А.И., Жарский И.М. Большой химический справочник. Минск: Современная школа, 2005. 608 с.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография