Кристаллография, 2020, T. 65, № 3, стр. 379-383
Исследование каталитической системы Fe/γ-Al2O3 при варьировании атмосферы и температуры
А. Р. Бродский 1, *, В. И. Яскевич 1
1 АО “Институт топлива, катализа и электрохимии им. Д.В. Сокольского”
Алма-Ата, Республика Казахстан
* E-mail: albrod@list.ru
Поступила в редакцию 20.05.2019
После доработки 20.09.2019
Принята к публикации 15.10.2019
Аннотация
Проведено исследование каталитической системы Fe/γ-Al2O3 в атмосфере воздуха, СО и Н2 в интервале 293–773 K. В исходном состоянии система содержит как минимум две парамагнитные формы Fe3+ с близкими значениями изомерных сдвигов и различными квадрупольными расщеплениями. В атмосфере СО и Н2 при 423–773 K железо в системе восстанавливается до состояния Fe2+, которое также находится как минимум в двух формах. Обсуждаются процессы, происходящие в системе, и природа обнаруженных форм железа.
ВВЕДЕНИЕ
Система Fe/γ-Al2O3 проявляет каталитическую активность во многих химических процессах, таких как производство аммиака [1–3] и углеродных нанотрубок [4, 5], в реакциях гидрирования СО (синтез Фишера–Тропша) [6, 7], в процессах окисления сероводорода в элементарную серу [8], глубокой переработке твердого ископаемого и возобновляемого органического сырья [9], в реакциях риформинга бензинов [10], а также многих других процессах [11]. Таким образом, являясь практически многофункциональной и удобным объектом для приложения мессбауэровской спектроскопии, система Fe/γ-Al2O3 может быть использована в качестве модельной.
МЕТОДИКА ИССЛЕДОВАНИЙ
В работе проведено исследование с помощью мессбауэровской спектроскопии in situ в условиях, приближенных к реальным условиям работы катализатора, состава системы Fe/γ-Al2O3 в атмосфере воздуха, СО и водорода при варьировании температуры в интервале 293–773 K. Состав атмосферы был выбран исходя из того, что аналогичная газовая среда присутствует в тех или иных перечисленных выше каталитических процессах.
Систему готовили методом пропитки из ацетата железа с 30%-ным обогащением по изотопу Fe57. Источником служил Co57 в матрице Cr активностью 100 мКи. Спектры снимали при комнатной температуре. Изомерные сдвиги (ИС) даны относительно α-Fe.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
На рис. 1 приведены мессбауэровские спектры системы Fe/γ-Al2O3, а в табл. 1 – результаты их обработки.
Рис. 1.
Экспериментальные мессбауэровские спектры системы Fe/γ-Al2O3 при варьировании атмосферы и температуры с расчетными компонентами, соответствующими различным формам Fe; а, б, в, г, д – в атмосфере воздуха; е, ж, з, и, к – в атмосфере водорода; л, м, н, о, п – в атмосфере оксида углерода; а, е, л – 293 K; б, ж, м – 473 K; в, з, н – 573 K; г, и, о – 673 K; д, к, п – 773 K.
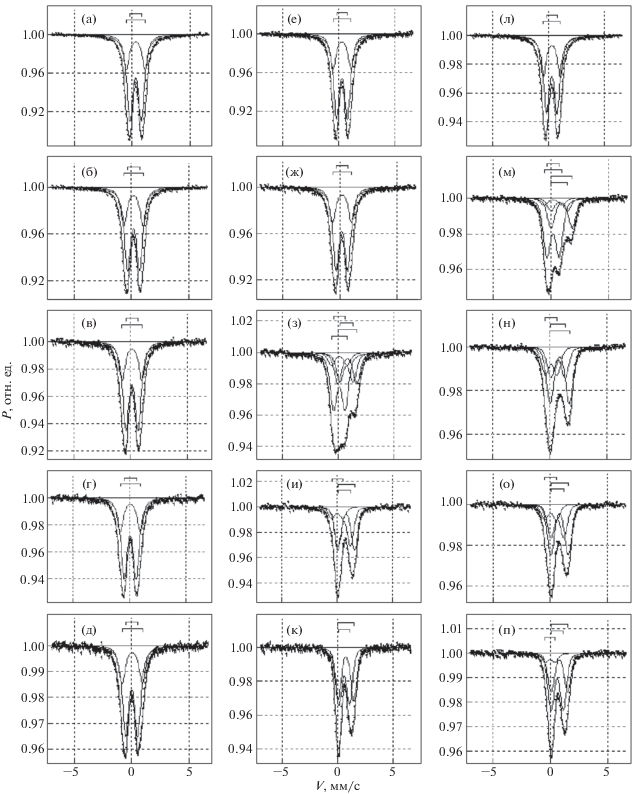
Таблица 1.
Мессбауэровские параметры каталитической системы Fe/γ-Al2O3 при варьировании атмосферы и температуры
| T, К | Fe$_{1}^{{3 + }}$ | Fe$_{2}^{{3 + }}$ | Fe$_{1}^{{2 + }}$ | Fe$_{2}^{{2 + }}$ | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ИС, мм/с | КР, мм/с | S, % | ИС, мм/с | КР, мм/с | S, % | ИС, мм/с | КР, мм/с | S, % | ИС, мм/с | КР, мм/с | S, % | |
| Атмосфера – воздух | ||||||||||||
| 298 | 0.31 | 0.98 | 70 | 0.32 | 1.62 | 30 | ||||||
| 373 | 0.26 | 0.99 | 66 | 0.28 | 1.60 | 34 | ||||||
| 423 | 0.23 | 1.03 | 68 | 0.23 | 1.67 | 32 | ||||||
| 473 | 0.20 | 1.04 | 68 | 0.21 | 1.68 | 32 | ||||||
| 573 | 0.13 | 1.06 | 68 | 0.13 | 1.74 | 32 | ||||||
| 673 | 0.07 | 1.08 | 70 | 0.08 | 1.77 | 30 | ||||||
| 773 | 0.01 | 1.05 | 70 | 0.02 | 1.78 | 30 | ||||||
| Атмосфера – CO | ||||||||||||
| 298 | 0.31 | 0.95 | 64 | 0.32 | 1.55 | 36 | ||||||
| 373 | 0.27 | 0.98 | 69 | 0.28 | 1.60 | 31 | ||||||
| 423 | 0.22 | 1.02 | 60 | 0.22 | 1.62 | 17 | 0.99 | 1.92 | 16 | 0.80 | 1.52 | 7 |
| 473 | 0.21 | 1.05 | 52 | 0.21 | 1.56 | 8 | 0.96 | 1.83 | 28 | 0.76 | 1.41 | 12 |
| 573 | 0.13 | 1.03 | 24 | 0.90 | 1.68 | 49 | 0.74 | 1.23 | 27 | |||
| 673 | 0.05 | 1.03 | 16 | 0.84 | 1.53 | 51 | 0.65 | 1.13 | 33 | |||
| 773 | 0.00 | 0.85 | 8 | 0.79 | 1.44 | 55 | 0.62 | 1.06 | 37 | |||
| Атмосфера – H2 | ||||||||||||
| 298 | 0.31 | 0.99 | 70 | 0.32 | 1.60 | 30 | ||||||
| 373 | 0.26 | 0.99 | 68 | 0.28 | 1.60 | 32 | ||||||
| 423 | 0.22 | 1.01 | 69 | 0.24 | 1.64 | 31 | ||||||
| 473 | 0.19 | 1.03 | 71 | 0.21 | 1.67 | 29 | ||||||
| 573 | 0.13 | 1.03 | 42 | 0.13 | 1.49 | 11 | 0.86 | 1.71 | 24 | 0.78 | 1.20 | 23 |
| 673 | 0.03 | 1.01 | 13 | 0.81 | 1.51 | 46 | 0.69 | 1.15 | 41 | |||
| 773 | 0.75 | 1.43 | 50 | 0.60 | 1.03 | 50 | ||||||
В исходном состоянии спектры представляют собой суперпозицию как минимум двух дублетов, отвечающих двум парамагнитным высокоспиновым формам Fe3+ с близкими значениями ИС и различными квадрупольными расщеплениями (КР).
Поскольку в спектрах системы даже при температуре жидкого азота не наблюдается зеемановского сверхтонкого магнитного расщепления, размеры агрегатов Fe3+ на γ-Al2O3 следует оценивать как не превышающие 5–6 нм.
Можно полагать, что формы Fe$_{1}^{{3 + }}$ и Fe$_{2}^{{3 + }}$ отвечают неэквивалентным положениям ионов железа на носителе (различным конфигурациям ближайшего окружения атомов Fe3+). Значения КР свидетельствуют о значительном отклонении окружения атомов железа от сферической симметрии.
При повышении температуры в атмосфере воздуха у обеих форм наблюдаются температурный (доплеровский) ИС и рост значений КР. Но если у формы Fe$_{1}^{{3 + }}$ увеличение КР – только некоторая тенденция, то у формы Fe$_{2}^{{3 + }}$ (с большим КР) рост является более существенным (табл. 1).
Замена атмосферы воздуха на CO при температурах до 373 K не приводит к существенным изменениям. Начиная с 423 K, наблюдается процесс восстановления Fe3+ до Fe2+, появляются два высокоспиновых состояния Fe$_{1}^{{3 + }}$ и Fe$_{2}^{{3 + }}$, которые имеют различные ИС и КР. С увеличением температуры относительное содержание (S, %) форм Fe2+ растет, а форм Fe3+ падает, причем более существенно для формы Fe$_{2}^{{3 + }}$ (табл. 1).
Начиная с 573 K, остается лишь форма Fe$_{1}^{{3 + }}$, относительное содержание которой с повышением температуры продолжает уменьшаться. С повышением температуры для всех форм железа наблюдается доплеровский ИС и для обеих форм Fe2+ сильное уменьшение величины КР.
Формы Fe$_{1}^{{3 + }}$ и Fe$_{2}^{{3 + }}$ отвечают неэквивалентным положениям ионов железа на носителе. Форма с большим КР, по-видимому, соответствует поверхностным атомам железа, а с меньшим – более глубоко расположенным. В пользу такого допущения может свидетельствовать существенное различие между температурными зависимостями КР для форм Fe$_{1}^{{3 + }}$, Fe$_{2}^{{3 + }}$ (табл. 1). Так, для высокоспинового состояния Fe3+ температурные изменения квадрупольного взаимодействия связаны только с тепловым расширением (тепловыми колебаниями узлов) кристаллической решетки [12]. Поскольку для атомов поверхности средний квадрат смещения перпендикулярно поверхности и вдоль поверхности может в 2 раза и на 30% превышать соответствующие значения для атомов внутри твердого тела [13], то для ионов железа, расположенных ближе к поверхности, можно ожидать более сильной температурной зависимости КР, что и наблюдается для формы Fe$_{2}^{{3 + }}$.
Большее уменьшение относительного содержания формы Fe$_{2}^{{3 + }}$ по сравнению с формой Fe$_{1}^{{3 + }}$ при увеличении температуры в атмосфере CO также является определенным аргументом в пользу того, что именно эта форма расположена ближе к поверхности носителя и поэтому более доступна для CO.
Вероятно, каждой форме Fe2+ должен отвечать свой предшественник – соответствующая форма Fe3+. Логично предположить, что “поверхностная” форма железа будет иметь в ближайшем окружении меньшее количество атомов кислорода носителя, чем более глубоко расположенная. В этом случае последняя форма будет обладать несколько меньшим изомерным сдвигом за счет более значительного переноса электронной плотности с d-орбитали железа на большее количество координированных атомов кислорода. По-видимому, этот эффект заметнее должен проявляться для форм с состоянием Fe2+, чем Fe3+, из-за разницы в плотности (количестве) d-электронов и, как следствие, донорной способности.
Действительно, если ИС обеих форм Fe3+ мало различаются, то ИС для формы Fe$_{1}^{{2 + }}$ заметно меньше, чем у формы Fe$_{2}^{{2 + }}$ (табл. 1). Следовательно, предшественником формы Fe$_{1}^{{2 + }}$ наиболее вероятно является форма Fe$_{1}^{{3 + }}$, а формы Fe$_{2}^{{2 + }}$ – Fe$_{2}^{{3 + }}$.
Замена атмосферы CO на атмосферу H2 (водорода) не приводит к существенным качественным различиям, поскольку как таковой механизм восстановления оксидов железа водородом идентичен механизму восстановления оксидов железа СО [14–16]. Вместе с тем наблюдаются некоторые особенности в процессе восстановления системы Fe/γ-Al2O3 в атмосфере водорода. В частности, восстановление форм Fe3+ начинается при значительно более высокой температуре (рис. 1, табл. 1). Кроме того, восстановление форм Fe3+ приводит к их полному исчезновению при 773 K (табл. 1).
Эти особенности, видимо, связаны с различным химическим сродством у CO и H2 к кислороду. При температурах меньше 1083 K химическое сродство к кислороду выше у CO [14–16], соответственно выше и восстановительная способность.
Исчезновение Fe3+ в атмосфере водорода при 773 K, в том числе формы Fe$_{1}^{{3 + }}$, отнесенной к глубоко расположенным от поверхности носителя атомам железа, можно связать с меньшей молекулярной массой и линейными размерами водорода по сравнению с молекулой CO. Разница в параметрах водорода и CO обусловливает большую проникающую способность первого и, как следствие, восстановление всего Fe3+ до Fe2+ независимо от глубины расположения.
Отметим, что ширина линий для всех обнаруженных форм железа находится в пределах 0.6–0.7 мм/с. Такая ширина, вероятно, связана с тем, что каждая форма железа – суперпозиция близких состояний с близкими мессбауэровскими параметрами, т.е. интегральный спектр формы является суперпозицией подспектров.
ЗАКЛЮЧЕНИЕ
Исследования показали, что система Fe/γ-Al2O3 в зависимости от условий может содержать различные формы железа. Наличие в системе нескольких форм железа указывает на потенциальную возможность образования каталитически активных центров с различными электронными характеристиками и, как следствие, различными каталитическими свойствами (каждая форма катиона железа на носителе может являться специфическим активным центром). Зависимость состава системы от режима восстановления и газовой среды дает возможность путем построения диаграмм типа состав–свойство, параметр–свойство выявить формы железа, играющие определяющую роль в том или ином каталитическом процессе. Такой подход, в свою очередь, может позволить проводить целенаправленный синтез и более точную настройку систем (варьируя условия формирования – температуру, газовую среду, дисперсность и т.д.), обладающих оптимальными каталитическими свойствами для конкретных каталитических процессов.
Работа выполнена при финансовой поддержке ГУ “Комитет науки Министерства образования и науки Республики Казахстан” (грант № AP05130654).
Список литературы
Семенов В.П. Производство аммиака. М.: Химия, 1985. 368 с.
Сибилева С.В., Нефедова Н.В. // Успехи в химии и химической технологии: сб. науч. трудов. 2008. Т. 22. № 10 (90). С. 9.
Сибилева С.В., Нефедова Н.В. Михайличенко А.И. // Химическая промышленность сегодня. 2011. № 6. С. 14.
Царева С.Ю., Жариков Е.В., Аношкин И.В., Коваленко А.Н. // Изв. вузов. Электроника. 2003. № 1. С. 20.
Мищенко С.В., Ткачев А.Г. Углеродные наноматериалы. Производство, свойства, применение. М.: Машиностроение, 2008. 320 с.
Хаджиев С.Н., Лядов А.С., Крылова М.В. // Нефтехимия. 2011. Т. 51. № 1. С. 25.
Sai P., Jong W.B., Ki-Won J. // Catal. Surv. Asia. 2008. V. 12. № 3. P. 170.
Крылов О.В. Гетерогенный катализ. М.: ИКЦ “Академкнига”, 2004. 663 с.
Шарыпов В.И., Кузнецов П.Н., Кричко А.А. и др. Патент РФ 2036950 от 09.06.1995.
Хатмуллина Д.Д. // Молодой ученый. 2014. № 1. С. 136.
Коботаева Н.С., Скороходова Т.С., Сироткина Е.Е. // Нефтепереработка и нефтехимия. 2010. № 2. С. 18.
Вертхейм Г. Эффект Мессбауэра (Принципы и применения). М.: Мир, 1966. 172 с.
Суздалев И.П. Динамичные эффекты в гамма-резонансной спектроскопии. М.: Атомиздат, 1979. 192 с.
Сенин А.В. // Вестн. ЮУрГУ. Сер. Металлургия. 2013. Т. 13. № 1. С. 14.
Jozwiak W.K., Kaczmarek E., Maniecki T.P. et al. // Appl. Catal. A. 2007. V. 326. P. 17.
Дильдин А.Н., Соколова Е.В. Теория металлургических процессов (Учебное пособие к практическим занятиям). Челябинск.: Изд-во ЮУрГУ, 2007. 33 с.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография


