Кристаллография, 2020, T. 65, № 3, стр. 446-448
Структура гидридных фаз на основе интерметаллических соединений ZrMoV и ZrMo1.5V0.5 фаз Лавеса С15
С. А. Лушников 1, *, Л. А. Качалова 1, В. Н. Вербецкий 1, С. С. Агафонов 2
1 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
2 Национальный исследовательский центр “Курчатовский институт”
Москва, Россия
* E-mail: lushnikov@hydride.chem.msu.ru
Поступила в редакцию 18.04.2019
После доработки 18.04.2019
Принята к публикации 10.10.2019
Аннотация
Проведен синтез гидридных фаз на основе псевдобинарных интерметаллических соединений ZrMoV и ZrMo1.5V0.5 с кубической структурой фаз Лавеса С15 (пр. гр. Fd$\bar {3}$m (№ 227), Z = 8). При абсорбции водорода происходит образование гидридных фаз ZrMoVН3.3 и ZrMo1.5V0.5Н3.5. Методом рентгеновской и нейтронной дифракции исследована структура синтезированных гидридов. Установлено, что упорядочение атомов водорода в кубической решетке ZrMoV и ZrMo1.5V0.5 приводит к образованию сверхструктуры с тетрагональной решеткой (пр. гр. I41/a (№ 88), Z = 4). В отличие от гидрида в дейтериде на основе ZrMoV образуется частично упорядоченная сверхструктура (пр. гр. I41/amd (№ 141), Z = 4). Нейтронографические данные позволили установить позиционные параметры атомов металла и водорода.
ВВЕДЕНИЕ
Интерметаллические соединения фаз Лавеса при взаимодействии с водородом образуют гидридные фазы, содержащие до шести атомов водорода на формульную единицу. После понижения температуры или увеличения концентрации происходит упорядочение атомов водорода и образование различных сверхструктур. В случае кубических фаз Лавеса С15 некоторые типы сверхструктур возможно вычислить теоретически [1, 2]. Ранее исследованные гидриды соединений ZrV2 и ZrMo2 значительно различаются как по структуре, так и по термодинамическим характеристикам. Например, на основе соединения ZrV2 в зависимости от количества водорода образуются гидриды с кристаллическими решетками двух типов [3]. При содержании водорода до 4.3 Н/ИМС (4.3 атома водорода на формульную единицу интерметаллического соединения (ИМС)) решетка гидрида кубическая, при концентрации 4.3 Н/ИМС – ромбическая, и при 5 Н/ИМС решетка снова кубическая. Если вместо водорода использовать дейтерий, то разнообразие типов решеток увеличивается [4]. У дейтерида в интервале концентраций до 2 D/ИМС (2 атома дейтерия на формульную единицу ИМС) решетка моноклинная, при 2 D/ИМС – кубическая, при 2.2 D/ИМС – моноклинная и тетрагональная, при 2.3 D/ИМС – кубическая, при 2.7 D/ИМС – моноклинная, при 3.6 D/ИМС – тетрагональная и при 4.9 D/ИМС – кубическая. Взаимодействие ZrMo2 с водородом было исследовано в [5, 6]. Исследование структуры дейтеридной фазы, содержащей около 4 D/ИМС, показало, что кристаллическая решетка ZrMo2 из кубической трансформируется в тетрагональную. В настоящей работе исследовали взаимодействие с водородом соединения ZrMo2, содержащего ванадий. В зависимости от содержания ванадия возможно появление гидридных фаз с типами структур, рассчитанными в [1, 2].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исходные образцы интерметаллических соединений ZrMoV и ZrMo1.5V0.5 были приготовлены из чистых компонентов в электродуговой печи в инертной атмосфере. Для лучшей гомогенизации образцы отжигали при температуре 1500°С в вакууме в течение 50 ч. Гидрирование проводили на установке типа Сивертса с рабочим диапазоном давления до 100 атм. Для улучшения качества дифракционных спектров нейтронографические измерения были проведены на образцах с дейтерием. Нейтронографические данные получены на дифрактометре ДИСК (λ = 1.66 Å) реактора ИР-8 НИЦ “Курчатовский Институт”.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
По данным рентгенофазового анализа и электронной микроскопии полученные образцы содержали незначительные следы соединения на основе раствора молибдена с ванадием и цирконием. Параметр кристаллической решетки ZrMoV a = = 7.502(3) Å, ZrMo1.5V0.5a = 7.549(4) Å. Уменьшение параметра решетки в интерметаллиде с большим содержанием ванадия закономерно и связано с меньшим атомным радиусом ванадия по сравнению с молибденом. Синтезированные образцы ZrMoV и ZrMo1.5V0.5 взаимодействовали с водородом с образованием гидридных фаз, содержащих около 3.1–3.5 Н/ИМС водорода. Увеличение содержания ванадия в интерметаллиде приводит к значительному снижению давления водорода при абсорбции. Образец ZrMoV абсорбировал водород при давлении около 2 атм., а в образце ZrMo1.5V0.5 aбсорбция водорода проходила при давлении около 30 атм.
Данные рентгенофазового анализа образцов гидрида и дейтерида на основе ZrMo1.5V0.5 показали, что у них тетрагональная решетка и одинаковая структура (пр. гр. I41/a (№ 88), Z = 4). Нейтронографические данные дейтерида ZrMo1.5V0.5D3.5 позволили установить, что все атомы дейтерия находятся в позиции 16f с окружением Zr2(Mo,V)2. Периоды решетки дейтерида соответствуют a = 5.556(3), c = 7.968(2) Å (рис. 1, табл. 1).
Рис. 1.
Нейтронограмма образца дейтерида ZrMo1.5V0.5D3.5. Здесь и далее: точки – экспериментальные значения, сплошная кривая – вычисленные значения, внизу показана разностная кривая, штрихи – положения брэгговских рефлексов.
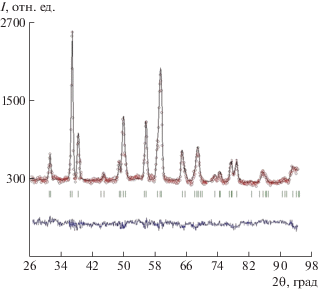
Таблица 1.
Структурные данные образца ZrMo1.5V0.5D3.5
| Атом | Пози-ция | Координаты атомов | Заселен-ность | ||
|---|---|---|---|---|---|
| x/a | y/b | z/c | p | ||
| Zr | 4a | 0 | 0.25 | 0.125 | 1.0 |
| Mo(V) | 8d | 0.25 | 0.25 | 0.75 | 1.0 |
| D | 16f | 0.186(3) | –0.070(2) | 0.060(3) | 0.88(2) |
| Rw = 7.8% | |||||
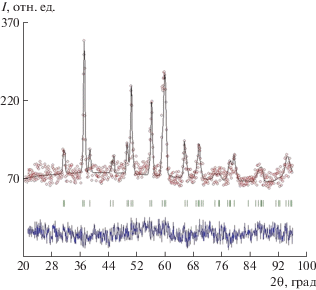
Дифрактограммы образцов гидрида и дейтерида на основе ZrMoV показали, что у них тетрагональная решетка и различная структура. У гидрида ZrMoVН3.3 структура соответствует пр. гр. I41/a (№ 88), Z = 4. На основе анализа сверхструктур [1, 2] было установлено, что дейтерид ZrMoVD3.6 имеет тетрагональную решетку и частично упорядоченную сверхструктуру (пр. гр. I41/amd (№ 141), Z = 4). Нейтронографические данные дейтерида ZrMoVD3.6 показали, что в данной сверхструктуре атомы дейтерия расположены в позиции 32i (рис. 2, табл. 2). Периоды решетки ZrMoVD3.6 составили a = 5.572(3), c = 8.018(8) Å. Такую же сверхструктуру и аналогичное распределение дейтерия имеет дейтерид ZrV2D3.0, исследованный в [7]. В то же время в гидриде на основе ZrV2 (пр. гр. Fd$\bar {3}$m (№ 227), Z = 8) с содержанием водорода 2.7–3.7 Н/ИМС, исследованного в [3], упорядочение атомов водорода приводит лишь к расширению его кристаллической решетки без изменения структуры. Таким образом, различие типа сверхструктуры в гидриде и дейтериде на основе ZrMoV, по-видимому, связано с изотопическим эффектом [8], к которому чувствителен ванадий. В [1] отмечено, что в фазах Лавеса С15, содержащих цирконий, в зависимости от параметра решетки дейтерий может занимать позиции как 96g, так и 32e. В рассматриваемом случае периоды решеток ZrMoV и ZrMo1.5V0.5 позволяют заполнить дейтерием только позицию 96g, которая соответствует позициям 16f и 32i в тетрагональной решетке. Сравнение межатомных расстояний на основе структурных данных показало, что они близки у обоих дейтеридов (табл. 3). Межатомные расстояния в бинарных дейтеридах циркония (2.07 Å [9]) и ванадия (1.65 Å [10]) также близки к аналогичным расстояниям в исследованных соединениях (Zr–D = 2.07 Å, Mo(V)–D = 1.80–1.70 Å). В гидриде молибдена межатомные расстояния больше (2.07 Å [11]), что, по-видимому, связано с характером распределения водорода в металлической подрешетке гидрида.
ВЫВОДЫ
В системах ZrMoV–H2 и ZrMo1.5V0.5–H2 синтезированы гидридные фазы с содержанием водорода 3.3–3.6 Н/ИМС. Увеличение содержания ванадия в интерметаллиде привело к снижению давления реакции гидридообразования. Методами рентгеновской и нейтронной дифракции установлено, что дейтериды ZrMoVD3.6 и ZrMo1.5V0.5D3.5 имеют различную сверхструктуру (пр. гр. I41/amd (№ 141), Z = 4 и пр. гр. I41/a (№ 88), Z = 4). Нейтронографические данные показали, что атомы дейтерия занимают в тетраэдрической решетке дейтеридов позиции 16f и 32i.
Работа выполнена при поддержке Российского научного фонда (грант № 16-12-10065).
Список литературы
Somenkov V.A., Irodova A.V. // J. Less Comm. Met. 1984. V. 101. P. 481.
Irodova A.V. // Solid State Phys. 1980. V. 22. № 9. P. 2559.
Bogdanova A.N., Andre G., Bouree F. // J. Alloys Compd. 2004. V. 379. P. 54.
Irodova A.V., Andre G., Bouree F. // J. Alloys Compd. 2000. V. 302. P. 159.
Lushnikov S.A., Movlaev E.A., Verbetsky V.N. et al. // Int. J. Hydrogen En. 2017. V. 45–32. P. 22330.
Semenenko K.N., Verbetsky V.N., Pilchenko V.A. // Vestn. MGU. Chem. 1986. V. 27. № 3. P. 332.
Fruchart D., Rouault A., Shoemaker C.B., Shoemaker D.P. // Phys. Status Solidi. A. 1980. V. 57. P. 119.
Somenkov V.A. // Ber. Bunsen. Ges. Phys. Chem. 1972. V. 76. P. 724.
Sidhu S.S., Murthy N.S.S., Campos F.P., Zauberis D.D. // Adv. Chem. Ser. 1963.V. 39. P. 87.
Asano H., Hirabayashi M. // Phys. Status Solidi. A. 1973. V. 15. P. 267.
Irodova A.V., Glaskov V.P., Somenkov V.A. et al. // Phys. Crystallogr. 1988. V. 33. P. 453.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография