Кристаллография, 2020, T. 65, № 4, стр. 528-539
Полиморфизм, изоморфизм и морфотропия в трифторидах редкоземельных элементов (R) и системах RF3–R'F3
Б. П. Соболев *
1 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
* E-mail: sobolevb@yandex.ru
Поступила в редакцию 30.07.2019
После доработки 20.01.2020
Принята к публикации 20.01.2020
Аннотация
Взаимосвязь полиморфизма, изоморфизма и морфотропии прослежена для гомологического ряда 16 трифторидов редкоземельных элементов (РЗЭ) (без ScF3) и фаз R1 – xR$_{x}^{'}$F3 (R – РЗЭ) по T–x-диаграммам систем RF3–R'F3. Полиморфизм определяется атомными номерами РЗЭ Z и Т, меняющими соотношение радиусов r+/r– (катион/анион). По полиморфизму и типам структур LaF3, β-YF3 и α-YF3 (α-UO3) выделяют структурные подгруппы RF3: A (R = La–Nd), B (R = Pm–Gd), C (R = Tb–Ho) и D (R = Er–Lu, Y). Сочетания RF3 образуют 10 типов систем RF3–R’F3. Изоморфизм (совершенный и ограниченный) выражается в областях гомогенности фаз R1 – xR$_{x}^{'}$F3. Он влияет на структуру R1 – xR$_{x}^{'}$F3 через соотношение r+/r–, готовя вместе с Т их морфотропные превращения (МП). Морфотропия R1 – xR$_{x}^{'}$F3 регулируется Т и х через r+/r– и реализуется путем фазовых реакций расплава с R1 – xR$_{x}^{'}$F3 и R1 – yR$_{x}^{'}$F3 разной структуры при перитектической МП-I и (или) эвтектической МП-II температурах. Морфотропные превращения структур R1 – xR$_{x}^{'}$F3 происходят на границе GdF3–TbF3 (Z = 64.43–64.51; МП-I; 1186 ± 10°С) и HoF3–ErF3 (Z = 67.67–67.36; МП-II; 1120 ± 10°С). Дано определение истинной морфотропии для систем в координатах T–x.
ВВЕДЕНИЕ
В анализе исторических корней теоретической кристаллохимии [1] изложено формирование в течение около двух сотен лет представлений о ее основных (категорийных) понятиях: полиморфизме (М. Клапрот, 1798), изоморфизме (Е. Митчерлих, 1819) и морфотропии (П.Г. Грот, 1870), которые долгое время развивались независимо. Все они – способы изменения структуры под действием интенсивных параметров состояния систем.
Полиморфизм все эти годы изучался экспериментально, как и изоморфизм. Морфотропия, понятие о которой возникло позже, надолго “застыла” на “мысленном” способе фиксации смены структуры в рядах минералов и солей при изменении качественного (элементного) состава.
Переход от “мысленного” метода выявления морфотропии к экспериментальному необходим в силу объективных причин. Для различения подходов для последнего примем термин “истинной морфотропии”. Между ними нет конфликта – это разные приближения к реальности. Оба существуют, определяясь доступностью физико-химического эксперимента.
Морфотропные ряды минералов и простых (ионных) соединений формируются заменой катионов Mm+ (при одном анионе) по группам Периодической системы. Экспериментальное изучение истинной морфотропии для минералов оказалось невыполнимо. Самый длинный в то время гомологический ряд представлен 10 карбонатами MCO3. Изучение Т–х-фазовых диаграмм “сухих” систем MCO3–M 'CO3 невозможно из-за термического разложения. Недостаток ряда MCO3 и в том, что при большой разнице атомных номеров ΔZ он имеет всего две морфотропные формы.
Информацию об истинной морфотропии дают бинарные (как простейшие) системы, образованные соединениями гомологического ряда MXm с разными (морфотропными) структурами. Переход к таким системам для изучения истинной морфотропии предложил В.М. Гольдшмидт (1925).
Второй компонент системы MXm–M'Xm “строит мост” между разными качественными составами членов гомологического ряда MXm и M’Xm, вводя количественный состав х, пропорциональный содержанию второго катиона M' в фазе M1 ‒ xM$_{x}^{'}$Xm. Это тоже фактор состава, но в дробных долях Z. Постепенный рост х сглаживает различия морфотропных структур MXm и M'Xm, подготавливая морфотропный переход (МП).
Появление в системе MXm–M'Xm второго катиона M' делает в принципе возможным изоморфизм. Для объединения полиморфизма простых соединений ряда MXm (компонентов систем) с изоморфизмом и морфотропией двухкомпонентных фаз M1 – xM$_{x}^{'}$Xm в системах MXm–M'Xm будем считать MXm вырожденными системами с х = 0.
Трифториды редкоземельных элементов (РЗЭ) образуют более длинный гомологический ряд. Согласно IUPAC (International Union of Pure and Applied Chemistry) РЗЭ – 17 элементов от Sc до Lu из 4–6 периодов побочной подгруппы III группы Периодической системы. Исключим ScF3 из-за его отличной от остальных RF3 структуры. Совокупность Y, La и Ln будем обозначать символом R, применяемым ко всему семейству РЗЭ [2, 3].
Исследования трифторидов РЗЭ в бинарных (и более сложных) системах были начаты в нашей стране в начале 70-х годов прошлого столетия на химическом факультете МГУ под руководством академика Александры Васильевны Новоселовой ее сотрудниками и учениками.
Поиск фторидных материалов для квантовой электроники инициировал в 70-х годов постановку автором статьи (дипломником А.В. Новоселовой) в Институте кристаллографии РАН совместно с химическим факультетом МГУ и Институтом химии АН Таджикистана программы изучения Т–х-фазовых диаграмм конденсированного состояния (P = const) систем MFm–RFn (m < n ≤ 4) из 27 фторидов. Она завершилась монографией [2] по более чем 200 системам с ∼480 фазами, ∼370 из которых можно получить в виде монокристаллов [3]. Настоящая монография посвящена А.В. Новоселовой – создателю фторидной школы неоргаников, прививавшей своим ученикам доведение научных исследований до получения материалов с практическим значением.
Полиморфизм, изоморфизм и морфотропия у RF3 и фаз R1 – xR$_{x}^{'}$F3 в системах RF3–R'F3 необычайно развиты [2] и подготовлены для анализа соотношения этой триады в ионных кристаллах.
Приведем определения каждого явления, опираясь на [1].
Полиморфизм – структурный переход при изменении интенсивных параметров состояния. В однокомпонентной системе при постоянном давлении это температура.
Изоморфизм – взаимное замещение атомов разных химических элементов (их групп) в эквивалентных позициях кристаллической структуры.
Морфотропия – резкое изменение кристаллической структуры в закономерном ряду химических соединений при сохранении количественного соотношения структурных единиц. В ряде других определений говорится о дискретности изменения состава и изотермичности.
Последние десятилетия не внесли корректив в определения полиморфизма и изоморфизма, многие вопросы которых для фторидов РЗЭ решены в частных исследованиях. Изучен полиморфизм RF3 [4–9], установлены их три структурных типа: LaF3 [10], β-YF3 [11] и α-YF3 (α-UO3) [12], плавное изменение координационного числа (КЧ) катиона [13–15]. Выявлены четыре структурные подгруппы RF3 [6, 16]. Изоморфизм R3+ и R'3+ изучен в фазах R1 – xR$_{x}^{'}$F3 34 систем RF3–R'F3 [2, 17–21]. Пределы изоморфных замещений в Gd1 – xR$_{x}^{'}$F3 подчиняются геометрическому фактору [18]. Определены условия МП для 11 фаз [17–19]. По температурам плавления ряд RF3 разделен на две морфотропные группы: LaF3–GdF3 и TbF3–LuF3 [22]. Морфотропный переход между GdF3 и TbF3 по оценке [22] совпал с изучением [18] системы GdF3–TbF3. В [23] рассмотрены полиморфизм RF3, изоморфизм R3+ и R'3+ в R1 ‒ xR$_{x}^{'}$F3, фазовые реакции МП и сформулирован подход к изучению триады в системах RF3–R'F3.
Изоморфизму посвящено много работ, из которых по неорганическим фторидам отметим [24]. Изоморфизм ионов РЗЭ в RF3 частично обсуждался в [2]. Современных работ по морфотропии в ионных кристаллах не известно.
Ведущая роль РЗЭ во фторидном материаловедении и фотонике в середине 80-х привлекла внимание к изучению RF3 и систем RF3–R'F3. Большинство систем RF3–R'F3 опубликовано в труднодоступных изданиях. В сборнике “Рост кристаллов” (перевод “Growth of Crystals” [17]) 16 систем, отдельные системы в тезисах докладов. Около трети систем в периодической печати не публиковалось. Недостаток информации показала работа [25] по системе GdF3–LuF3, авторы которой посчитали себя пионерами в этой области химии (критический анализ работы [25] сделан в [26]).
Работа продолжает начатое [6, 7, 18] изучение соотношения полиморфизма, изоморфизма и морфотропии в RF3 и системах RF3–R'F3. Ранее задача стабилизации фаз R1 – xR$_{x}^{'}$F3 со структурой типа β-YF3 изоморфными замещениями решалась [18] изучением систем GdF3–RF3 с близкими по ряду RF3. В данной работе число фаз в МП увеличено вдвое за счет систем из отдаленных по ряду RF3. Полиморфизм, изоморфизм и морфотропия впервые рассматриваются в периодической печати совместно на основе 20 изученных бинарных систем.
Цели сообщения: рассмотреть изменения полиморфизма и плавкости 16 трифторидов Y, La и 14 лантаноидов (Ln) гомологического ряда RF3; обсудить изоморфизм ионов РЗЭ в системах RF3–R’F3 в связи со структурными подгруппами RF3 и 10 типами систем; рассмотреть трансформацию фазовых диаграмм RF3–R'F3 с ростом разницы химического различия компонентов ΔZmax по атомным номерам R3+ и R'3+; обсудить соотношение основных морфотропных типов структур фаз R1 – xR$_{x}^{'}$F3 (LaF3 и β-YF3); выделить типы МП в системах GdF3–TbF3 и HoF3–ErF3; рассчитать границы МП фаз R1 – xR$_{x}^{'}$F3; обсудить соотношение полиморфизма, изоморфизма и морфотропии в некоторых системах RF3–R'F3; внести коррективы в определение истинной морфотропии.
ГОМОЛОГИЧЕСКИЙ РЯД YF3, LaF3 И 14 LnF3
Понятие гомологии, имеющее в химии несколько значений, здесь применено к соединениям RF3 с одинаковой формулой. Трифториды РЗЭ – гомологический ряд простейшего состава (RF3) с ионным характером химической связи и минимальной разницей атомных номеров катионов соседних соединений: ΔZ = 1. Длина ряда RF3 одна из максимальных: 16 соединений. Максимально и число структурных типов RF3 – три (без ScF3).
Ряд RF3 состоит из трех d-элементов: Sc, Y, La, и 14 4f-элементов – лантаноидов (Ln) от Ce до Lu. Химическое родство РЗЭ базируется на электронном строении и выражается в помещении 15 элементов 57La–71Lu в одну клетку Периодической таблицы и их валентности 3+.
Трифториды Y, La и Ln среди неорганических фторидов составляют ∼60% от 27 компонентов систем MFm–RFn (m, n ≤ 4), используемых для получения многокомпонентных кристаллических фторидных материалов [3]. Полиморфизм, изоморфизм и морфотропия обсуждаются на примере многочисленного семейства фторидов, имеющего фундаментальный и практический интерес.
ПОЛИМОРФИЗМ И ПЛАВКОСТЬ В ГОМОЛОГИЧЕСКОМ РЯДУ RF3
Полиморфизм и плавкость RF3 хорошо изучены [4–8]. Полиморфизм вызывается изменением интенсивного параметра состояния – температуры (Т) – через геометрический фактор. C ростом Т размер аниона растет быстрее, чем катиона [1]. Соотношение “r+/r–” падает, уменьшая КЧ и вызывая полиморфизм. При малом размере и низкой поляризуемости иона F1– он может иначе реагировать на рост Т, чем крупные анионы. Хотя зависимость r+/r– от Т играет определяющую роль в триаде, она мало изучена.
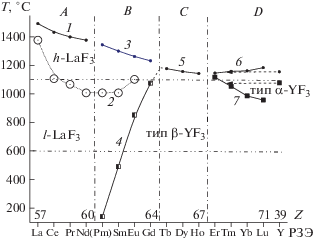
Схема фазовых превращений (полиморфизм и плавление) RF3 (без ScF3) приведена на рис. 1 по [2, 6, 7, 27] в порядке роста Z (кроме YF3). Изменение структур RF3 отражается в разных наклонах их кривых плавления 1, 3, 5, 6. Исключение – кривые 1 и 3, описывающие RF3 одного типа LaF3.
На нижней оси рис. 1 – условной изотерме комнатных температур – ряд RF3 по рентгенографическим данным делится на две части: со структурой типа LaF3 (тисонита) с R = La–Nd; со структурой типа β-YF3 для остальных RF3 c R = = (Pm), Sm–Lu и Y. Положение Pm не было определено.
Повышение Т смещает границу перехода в RF3 на четыре элемента вправо, рис. 1, кривая 4. Действия Т и лантаноидного сжатия независимы, но суммируются в уменьшении относительного (к F1–) размера R3+. Оба фактора приводят к морфотропному переходу: тип LaF3 ↔ тип β-YF3 (МП-I), который смещается с ростом Т. Продолжение кривой 4 до пересечения с 5 на рис. 1 оценивает положение МП-I между GdF3 и TbF3.
Второй раз диморфизм α ↔ β-RF3 появляется у ErF3. Это МП-II: тип β-YF3 ↔ тип α-YF3 (α-UO3), кривая 7 на рис. 1, R = Er–Lu, Y. Причины диморфизма α ↔ β-RF3 противоречивы. Изменение структуры только под действием Т – полиморфизм. Изменение качественного состава (Z), вызывающее ту же структурную перестройку, – признак морфотропии. В.М. Гольдшмидт называл полиморфизм автоморфотропией.
Полиморфная перестройка структуры RF3 провоцируется Т, но ею же и ограничивается: достижение определенной величины r+/r– приводит к потере устойчивости кристаллической фазы и ее плавлению.
ИЗОМОРФИЗМ КАТИОНОВ РЗЭ В СИСТЕМАХ RF3–R'F3
Изоморфизм катионов РЗЭ возможен в бинарных RF3–R'F3 и более сложных системах, требуя как минимум двух разных РЗЭ. Низкие упругости паров RF3 при температурах плавления (кроме ScF3) относят системы RF3–R'F3 к конденсированным с P = const. Переход к системе Т–х увеличивает на единицу степень свободы. Изоморфное замещение – изменение концентрации х интенсивного параметра состояния.
Состав х фаз R1 – xR$_{x}^{'}$F3 в области их гомогенности меняется в пределах одной структуры до некоторого х. Меняя средний радиус катиона и r+/r–, состав готовит МП при х, разном для разных Т. Изовалентный изоморфизм в ионных кристаллах гомологической серии RF3 подчиняется геометрическому фактору в широких пределах Z [2, 17, 18, 20], падая с ростом ΔZ. Совершенный изоморфизм не охватывает все RF3, иначе не было бы МП.
Структурные подгруппы RF3. Изоморфизм ионов РЗЭ в системах RF3–R'F3 зависит от структуры компонентов (двойных соединений не обнаружено). Сочетания типов структур и модификаций делят ряд RF3 на четыре структурные подгруппы (СП): A (R = La–Nd), B (R = Pm–Gd), C (R = Tb–Ho) и D (R = Er–Lu, Y) [6, 7], рис. 1. В СП А RF3 имеют тип тисонита t (LaF3) во всем интервале температур. В СП В – диморфные RF3 c высокотемпературной формой типа t и низкотемпературной типа β-YF3. Подгруппа С с одной формой типа β-YF3. Наконец, RF3 СП D диморфны – к типу β-YF3 добавляется высокотемпературная форма типа α-YF3 (α-UO3).
Структурные подгруппы подчиняются внутрипериодной периодичности (ВП) заполнения 4f-подоболочек Ln [27]. Элементные составы подгрупп и их численность однозначно задаются ВП R3+. Этим СП RF3 выгодно отличаются от классификаций “кристаллохимической нестабильности” и “тетрад-эффекта”. Структурные подгруппы, разделенные тремя штрихпунктирами, не морфотропные группы: при трех типах структур границ должно быть две. Вопрос о числе морфотропных групп у RF3 дискуссионный.
Полиморфизм, изоморфизм и морфотропия связаны со структурными особенностями окружения катионов в структурных типах RF3.
Десять типов систем RF3–R'F3. Анализ взаимного изоморфизма ионов РЗЭ в трех типах структур RF3 основан на фазовых диаграммах систем RF3–R'F3. Из 15 RF3 (без PmF3 и ScF3) формируются 105 систем, из которых изучены 34. Рассмотрение закономерностей изоморфизма в каждой из них – задача, выходящая за рамки этого сообщения. Наиболее полно это сделано в [2, 17]. Серия работ по количественным характеристикам изоморфизма и проявлениям морфотропии в системах RF3–R'F3 начата в [28].
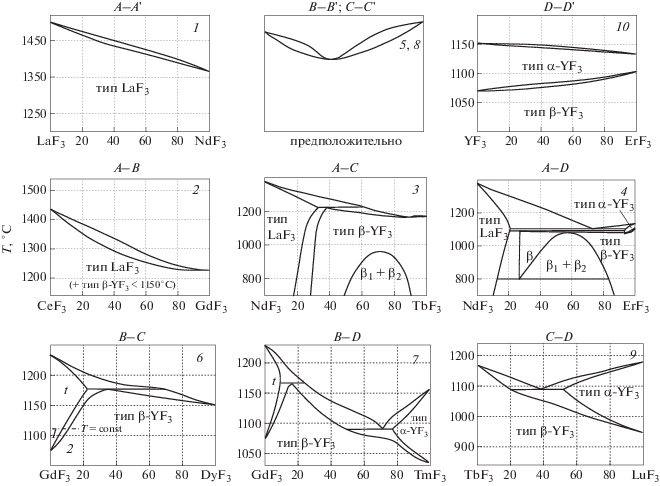
Для настоящего рассмотрения достаточно типовых систем, представляющих парные сочетания RF3 из четырех СП, по одной на каждый из 10 типов систем, представленных на рис. 2. На нем не видны различия некоторых систем в области более низких Т, связанные с полиморфными превращениями. Номера типов систем указаны в правых верхних углах. Нумерация проводится достаточно произвольно, основываясь на алфавитной последовательности буквенных обозначений СП. Фазовые поля ss показаны надписями типов структур. При малых площадях полей тип LaF3 обозначен как t-ss (tysonite), тип β-YF3 как β-ss, а тип α-YF3 (α-UO3) как α-ss.
Различия топологии фазовых диаграмм связаны с фазовым составом – областями гомогенности фаз R1 – xR$_{x}^{'}$F3 и их структурой. Несмотря на пресловутую химическую близость соединений РЗЭ, химические взаимодействия RF3a priori не могут быть тривиальными: изменения размера R3+ дважды приводят к морфотропии, а ∼15%-ная разница радиусов R3+ ограничивает изоморфизм RF3, далеко отстоящих друг от друга по ряду R3+.
Топология фазовых диаграмм RF3–R'F3 подробно рассмотрена в [2]. Здесь обсудим общую оценку изоморфизма, представленную на рис. 2.
Трансформации фазовых диаграмм с ростом ΔZmax R3+ и R'3+. Величина ΔZ определяет степень химического родства трифторидов РЗЭ, их структурные различия, выражающиеся в полиморфизме, а отсюда – степень совершенства изовалентного изоморфизма ионов РЗЭ.
Из 10 типов систем четыре составлены из RF3 одинаковых СП: A–A', B–B', C–C', D–D'. Остальные шесть типов из RF3 разных СП: A–B, A–C, A–D, B–C, B–D, C–D. Иттрий (Z = 39) относится к СП D.
ΔZmax – разница Z между первым компонентом СП и последним последующей СП, из которой берется второй компонент. ΔZmax отражают предельную степень химических различий RF3 в типе систем. Рост ΔZmax вызывает снижение степени совершенства изоморфизма. ΔZmin задается разницей Z между последним компонентом СП и первым компонентом последующей СП. Она характеризует максимальное химическое родство RF3 для данного сочетания.
Для парных сочетаний RF3 из СП (систем) с соседствующими по ряду компонентами ΔZmin = 1. Таких большинство: A–A', B–B', C–C', D–D', A–B, B–C, C–D. Для трех (A–C, B–D, A–D) ΔZmin растет от 4 до 8. Эти же сочетания имеют максимальные ΔZmax (от 9 до 14). В таких системах можно ожидать ограниченный изоморфизм и образование двойных соединений. Низкая изученность систем из далеко отстоящих по ряду RF3 не позволяет оценить ограничения геометрического фактора изоморфизма.
Рисунок 2 показывает, что системы RF3–R'F3 при химическом родстве компонентов проявляют разнообразие типов фазовых диаграмм. Типы различаются по областям гомогенности, структуре твердых растворов (ss), наличию (отсутствию) морфотропных превращений и их типу.
Количественный анализ изоморфизма в системах В–С и В–D. Начало количественным исследованиям изоморфизма и морфотропии в системах B–C и B–D из относительно близких RF3 положила работа [18]. В каждой системе находятся две особые точки: предельный состав t-ss (тип LaF3) и состав с максимальной для данной системы температурой плавления фаз R1 – xR$_{x}^{'}$F3 β-ss типа β-YF3, рис. 2 (типы 6 и 7). Объединение координат особых точек систем GdF3–RF3 (R = Tb, Ho, Er, Yb) в группы приводило к выводам: тип структуры имеет свои значения Zср и радиуса катиона, при которых достигается максимальный изоморфизм; термическая устойчивость (плавление) насыщенных ss с одинаковой структурой близка для фаз с разными Zср; во всех типах структур Zср фаз с максимальной термической устойчивостью и взаимной растворимостью не целочисленны. Близость этих характеристик для разных систем при широком диапазоне изменения концентрации второго компонента в α-(Gd1 – xRx)F3 (от 43 мол. % для TbF3 до 4 мол. % для YbF3) говорит об определяющем влиянии геометрического фактора в системах из относительно близко расположенных RF3 на изоморфизм и термическую устойчивость фаз типа LaF3.
Распространять этот подход к оценке изоморфизма в системах B–C, B–D на все 10 типов систем нельзя. В системах A–C и особенно A–D образуются фазы t-ss, не отвечающие критерию “оптимальных” средних радиусов и Zср, рассчитанных для GdF3–RF3 [18].
Большой материал [2, 17–22] по количественной характеризации изовалентного изоморфизма в системах RF3–R'F3 – предмет отдельной серии публикаций, начатой в [28].
МОРФОТРОПИЯ В ФАЗАХ R1 – xR$_{x}^{'}$F3 СИСТЕМ RF3–R'F3
Морфотропное превращение – основной предмет настоящего рассмотрения. Имеется несколько его определений, но все они расплывчаты. “Дискретно меняющийся состав” ограничен качественным (атомным номером Z). Условие изотермичности МП (Т = const) не говорит о форме его реализации. Структура “меняется резко”, но степень реконструктивности в определении не оговорена. Для RF3 известно плавное изменение КЧ катиона в пределах одного типа структуры, не отменяющее МП. Всеохватывающего определения морфотропного превращения структурного типа в гомологическом ряду ионных соединений не найдено.
Можно полагать, что это вызвано исторической сменой объектов. Первоначально были гомологические ряды соединений (минералов). Температура (из-за ее незнания) как фактор отсутствовала, и “мысленное” определение МП проводили по величине Z катионов.
Первыми сведениями о МП в ряду RF3 были рентгенографические данные 60-х годов, полученные при комнатной температуре. Они делили ряд на две части: RF3 типа LaF3 c R = La–Nd (Pm) и типа YF3 c R = Sm–Lu, Y. Данных о полиморфизме RF3 еще не было. Это деление видно на рис. 1, где горизонтальная ось – приближение к комнатной температуре – для ряда RF3 приводит к единственному МП, что не соответствует действительности.
Это – следствие исключения температуры как фактора. Введем Т и “мысленно” рассмотрим на рис. 1 два изотермических сечения: T = 600°С (нижняя) и T ∼ 1100°С (верхняя штрихпунктирная горизонталь). На нижнем структура меняется между SmF3 (тип LaF3) и EuF3 (тип β-YF3). На верхнем появляется МП между HoF3 и ErF3: тип β-YF3 → тип α-YF3 (α-UO3), но исчезает первый МП. Задав Т наугад в “мысленном” поиске МП, видим, что попадание на него – дело случая.
В 30-х годах прошлого столетия В.М. Гольдшмидт заметил, что истинный МП реализуется только в бинарной Т–х-системе, образованной компонентами разных морфотропных групп гомологического ряда соединений. Между ними образуются ограниченные ss. Химическая система добавляет к “мысленной” морфотропии «качественного состава» величину Т как новый фактор. В системе к качественному (элементному) катионному составу Z прибавляется состав количественный, обычно задаваемый в мольных долях х второго компонента. Состав х не является новым фактором, продолжая шкалу качественного состава Z внутрь системы в долях Z. Для этого выразим х в средних атомных номерах Zср = (1 – x)Z1 + + хZ2 (индексы 1 и 2 – первый и второй катион). На Т–х-диаграмме находятся в равновесии ss с разными морфотропными структурами. Химическая система задает количественный состав х как фактор Zср изменения радиуса катиона и r+/r–.
Морфотропия, согласно определению, протекает при T = const. В изученных Т–х (Р = const) системах RF3–R'F3 фазовые реакции с условием Т = const – перитектическая и эвтектическая. Другие варианты (синтектика, монотектика) в них не найдены. В отличие от “мысленных” границ морфотропии “состава” (по Z) в гомологическом ряду соединений в образованной ими системе в координатах Т–х оба условия истинного МП – Т и х – определяются однозначно.
Истинная морфотропия в системах RF3–R'F3. Следуя В.М. Гольдшмидту, выберем системы для наблюдения истинной морфотропии. Их компоненты должны быть членами гомологического ряда. Желательно минимальное различие Z катионов соседних соединений. Ряды должны быть длинными и с максимальным количеством типов структуры. Всем пожеланиям соответствуют соединения только двух семейств f-элементов – лантаноидов (4f) и актиноидов (5f). Соединения актиноидов по причинам недоступности всего ряда непригодны. Системы RF3–R'F3 остаются единственной в Периодической системе возможностью прецизионного изучения соотношения полиморфизма RF3, изоморфизма в трех (без ScF3) типах структур и морфотропии фаз R1 ‒ xR$_{x}^{'}$F3.
Трифториды РЗЭ играют особую роль в изучении морфотропии, для которой до 80-х годов прошлого века не было объектов для перехода от “мысленного” проведения границы МП к экспериментально определяемому. Причина – искажение фазовых переходов в RF3 примесью кислорода.
Около трети систем RF3–R'F3 изучено, что позволяет “мысленную” взаимосвязь членов триады уточнить экспериментально. Принцип непрерывности Н.С. Курнакова и смена катиона по периоду делают системы RF3–R'F3 уникальными для точного определения границ МП (ΔZ $ \ll $ 1).
Эта точность достигается в системах ZRF3–(Z+1)RF3 из фторидов соседних РЗЭ. Ряд RF3 по Z (рис. 1 и 3) может рассматриваться как “квазисистема” LaF3–LuF3. Она состоит из суммы расположенных подряд вдоль оси “состава” Z от 57 (La) до 71 (Lu) систем с ΔZ = 1. Эта “квазисистема” имеет “фазы” трех типов структуры и два МП между ними.
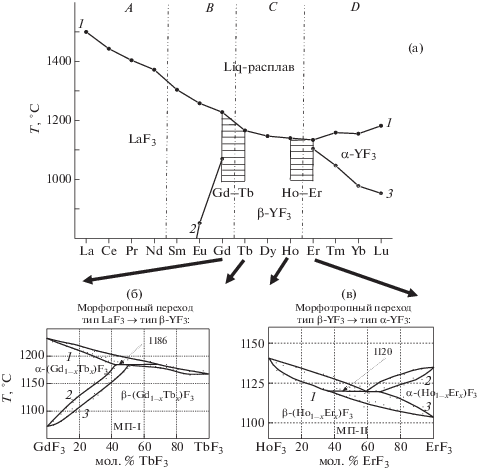
Рис. 3.
Схема фазовых превращений в RF3 (а) и морфотропные переходы типа LaF3 ↔ β-YF3 (МП-I) в системе GdF3–TbF3 (б) и типа β-YF3 ↔ α-YF3 (α-UO3) (МП-II) в системе HoF3–ErF3 (в).
Соотношения морфотропных структурных типов LaF3и β-YF3. Рост Т и Z приводит у RF3 (без ScF3) к трем морфотропным типам структур. Два типа – LaF3 и β-YF3 – являются основными для RF3 и R1 – xR$_{x}^{'}$F3. Третий тип α-YF3 (α-UO3) у RF3 c R = Er–Lu, Y образуется при высоких температурах, не закаливается, и структура его не изучена. Четвертый – ScF3 (тип ReO3) – исключен из рассмотрения из-за отличий от других RF3.
Кристаллохимическое родство типов LaF3 и β-YF3 обсуждалось неоднократно [15, 29–31]. Оно проявляется в исчезающе малых теплотах полиморфных превращений α ↔ β-форм SmF3, EuF3, GdF3 [4, 5]. Прототипом структур типа LaF3 и β-YF3 является высокотемпературная форма h-LaF3 с соотношением параметров “малой” гексагональной ячейки: а/с = √3 = 1.732. Исчезновение тройных осей снижает сингонию до ромбической у типа β-YF3. Степень отклонения β-RF3 от гексагональности дает отличие а/с от идеального. У SmF3а/с = 1.515, у HoF3 – 1.465, а у LuF3 всего 1.374.
Переход от типа LaF3 к типу β-YF3 осуществляется за счет подвижек катионов и анионов. Последние локализованы в плоскости ромбической установки (010). Смещения ионов фтора минимальны вдоль ромбической оси b. Изменения b по ряду β-RF3 минимальны и близки к линейным [13, 15].
Скачок КЧ катиона при скачкообразном изменении его Z и радиуса обычен для гомологических рядов с большими ΔZ. Принадлежность ионов РЗЭ (R3+) к особому химическому семейству Периодической системы f-элементов выделяет кристаллохимию RF3. Благодаря малому ΔZ = 1 между соседними РЗЭ возникает уникальная особенность структуры RF3: КЧ катиона плавно меняется в пределах структурного типа в зависимости от размера R3+ [13, 15]. “Подгонка” КЧ под размер R3+ придает типу β-YF3 толерантность – в нем кристаллизуются 12 RF3. Но это делает поправки ионных радиусов R3+ на КЧ неопределенными. В ряду RF3 тип β-YF3 “центральный”, от которого влево (уменьшение Z) и вправо (рост Z) проходят морфотропные изменения структурного типа RF3.
Таким образом, морфотропные типы структур RF3 чрезвычайно близки. Несмотря на близость типов LaF3 и β-YF3 и отсутствие при МП скачка координационного числа катионов R3+, морфотропия между ними наблюдается.
Морфотропные превращения в системах GdF3–TbF3и HoF3–ErF3. Для нахождения границ истинных МП нужны системы из компонентов по обе стороны границ морфотропных групп RF3 [22]. При трех типах структуры границ две, как и “пограничных” систем. На рис. 3а две границы СП: вертикали между В и С и между С и D. Эти вертикали окружены двумя парами РЗЭ: Gd–Tb и Ho–Er, соединенными горизонтальной штриховкой.
Компоненты системы GdF3–TbF3 из В–С (рис. 3б) – последний фторид из В и первый из С, а системы HoF3–ErF3 из C–D (рис. 3в) – последний из С и первый из D. Система (рис. 3б) моделирует МП: тип LaF3 ↔ тип β-YF3 (МП-I), система (рис. 3в) – МП тип β-YF3 ↔ тип α-YF3 (α-UO3) (МП-II).
Системы из фторидов этих РЗЭ дают информацию о механизмах МП. Системы GdF3–TbF3 и HoF3–ErF3 представлены на рис. 3б и 3в соответственно. Их качественный состав меняется на ΔZ = 1. Количественный состав дробит этот интервал на 0–100 моль. % (0–1 мол. доли х) компонента R'F3.
В системе GdF3–TbF3 МП-I реализуется как перитектическая фазовая реакция при 1186 ± 10°С, описываемая уравнением
В изученных системах условия МП задаются: значениями Т перитектики или эвтектики; составами х и у равновесных фаз R1 – xR$_{x}^{'}$F3 и R1 – yR$_{y}^{'}$F3 с разной структурой при Т перитектики (эвтектики); составом расплава третьей фазы, делающей МП инвариантным.
Сопоставление RF3 и систем RF3–R'F3 с изменением катионов по периоду показывает различие “мысленной” и истинной морфотропии для гомологических рядов RF3 и R1 – xR$_{x}^{'}$F3. Если берется ряд RF3, высшая точность МП ограничивается величиной ΔZ = 1. Термодинамическая оценка [22] дает МП между GdF3 и TbF3 на любом составе 0–100% TbF3. “Мысленная” граница по выделению из расплава GdF3 (тип LaF3) и TbF3 (тип β-YF3), пунктир на рис. 1, имеет ту же точность.
Если берется система ZRF3–(Z+1)RF3, в данном случае GdF3–TbF3, в ней границы МП-I сужаются до ∼8 ± 2 мол. % TbF3 вблизи состава 1 : 1. Для фазы типа LaF3Zср = 64.43. Для фазы типа β-YF3Zср = 64.51. Истинный МП-I имеет ΔZ = 0.08. Система GdF3–TbF3 дает обе границы МП и самый тугоплавкий состав Gd0.49Tb0.51F3 (Z = 64.51). Тип β-YF3 в ряду RF3 не достигает максимальной устойчивости при целочисленных Z.
В системе такого же типа, но с МП-II, разница составов сосуществующих фаз больше и составляет ∼30 мол. % ErF3. Центр тяжести МП-II близок к отношению 2 : 1. Для тисонитовой фазы Zср = 67.67, а для фазы типа β-YF3 – 67.36. Для МП-II ΔZ = 0.31, но и она много меньше единицы.
Изменение катионов в гомологическом ряду MCO3 по второй группе Периодической системы можно осуществить только для “мысленного” способа, поскольку изучение “сухих” систем MCO3–M´CO3 невозможно из-за термического разложения. Для пары MgCO3–CaCO3 ΔZ = 8 (катионы разделяет малый период), а для пары CaCO3–SrCO3 ΔZ = 18 (большой период).
Результаты “мысленного” и экспериментального приемов определения положения границ МП в ряду RF3 не принципиальны. При “мысленном” проведении границы по одному фактору (составу Z) получаем приближение ∼1 между Z и Z + 1. Из эксперимента по системам RF3–R'F3 для двух составов R1 – xR$_{x}^{'}$F3 и R1 – yR$_{y}^{'}$F3 (или Zср) при истинной морфотропии границы много <1. В MCO3 с ΔZ = 18 о точности можно не говорить.
Принципиальна разница между приемами по Т: при “мысленном” способе температура неизвестна, а при экспериментальном имеет определяемые и фиксированные значения.
Границы МП фаз R1 – xR$_{x}^{'}$F3. Дополним данные [18] по температурам МП-I и МП-II для систем GdF3–RF3 (R = Tb, Ho, Er, Yb) из компонентов, близких по ряду РЗЭ, системами из RF3, далеко отстоящих по ряду. Число фаз, участвующих в морфотропных реакциях, увеличивается более чем вдвое. Привести их детально, как для систем GdF3–TbF3 и HoF3–ErF3, в этом сообщении не представляется возможным.
Сравним границы всех обнаруженных МП на графике Т–Z. Обычно сравнение свойств соединений РЗЭ проводят в соответствии со шкалой их ионных радиусов rR. Однако системы rR для R3+ неадекватны. В системе [32] стремление к универсальности привело к поправкам, не приемлемым для R3+ [33]. Заменим относительные величины rR абсолютными средними Zср насыщенных фаз R1 – xR$_{x}^{'}$F3 разных структур (особые точки cистем RF3–R’F3).
Zср в R1 – xR$_{x}^{'}$F3 дает непосредственно качественный и количественный состав фазы, когда компоненты соседствуют. Так, для системы GdF3–TbF3 состав фазы типа LaF3 (64Gd0.5765Tb0.43)F3 описывается Zср = 64.43. Из нее следует, что Z = 64 для катиона 64Gd первого компонента – GdF3, а 0.43 – атомная доля второго компонента 65TbF3. Когда компоненты разнесены по ряду, для расчета Zср необходимо использовать общее уравнение Zср (см. выше).
В R1 – xR$_{x}^{'}$F3 реализуется набор Zср от 57La до 71Lu. На рис. 4 в координатах Т–Zср приведены 23 фазы – участники МП. Они группируются вдоль шести вертикалей. Каждому МП отвечают две вертикали – границы двухфазной области. Рядом указаны соответствующие системы. Рисунок 4 включает в себя данные [18] по системам с RF3 второй половины ряда, дополненные здесь некоторыми сочетаниями А–С и А–D с RF3 начала ряда.
Рис. 4.
Границы морфотропных превращений структурных типов в изученных системах RF3–R'F3 в шкале атомных номеров РЗЭ Z. Шестиугольники – фазы типа LaF3, квадраты – типа β-YF3, кружки – типа α-YF3 (α-UO3).

Первая пара вертикалей (МП-I) лежит вблизи Z = 62 (62Sm) и содержит данные по системам A–C (NdF3–TbF3) и A–D (NdF3–ErF3). Из рис. 2 видно, что в системах проявляется неустойчивость фаз β-(Nd1 – xRx)F3 типа β-YF3 в виде купола распада в первой и частичного обособления β1 во второй. В системе NdF3–YbF3 (на рис. 2 нет) β1 отрывается от β2.
Взаимодействием далеко отстоящих RF3 получены Nd0.7Er0.3F3, Pr0.6Er0.4F3, Pr0.5Dy0.5F3, Ce0.5Dy0.5F3, Nd0.6Ho0.4F3, Nd0.6Ho0.4F3, Nd0.6Y0.4F3 [34, 35]. Все они без оснований трактуются как химические соединения. Природа фазы Nd0.7Er0.3F3 как “обрывка” твердых растворов β-Nd1 – xErxF3 в NdF3–ErF3 показана в [21], рис. 2. Остальные требуют изучения.
Вторая пара вертикалей отвечает МП-I в известной по [18] области Z ∼ 64–65. Системы GdF3–RF3 (R = Er–Lu, Y) из сочетаний В–С и B–D наиболее изучены [17, 18, 20]. Морфотропная смена структуры через двухфазную область выделена на рис. 4 двумя вертикалями между Z = 64 (64Gd) и 65 (65Tb), не совпадающими с целочисленными Z. МП-I имеют близкие Zср и составы фаз, близки и температуры фазовых реакций [18].
Близость средних радиусов РЗЭ (соответственно, Zср) в твердых растворах, участвующих в МП, и Т их разных типов (перитектического, эвтектического) [18] указывает на определяющее влияние геометрического фактора на пределы растворимости и термическую устойчивость фаз R1 – xR$_{x}^{'}$F3. Справедливость этого вывода ограничена сочетаниями В–С и B–D.
Обнаружение в настоящей работе первой (слева) на рис. 4 пары вертикалей в районе 62Sm на сочетаниях A–C (NdF3–TbF3) и A–D (NdF3–ErF3) стало неожиданностью. Это – неизвестный МП, увеличивающий число МП до трех. Число морфотропных групп уравнивается с числом СП, что возможно только в случае существования еще одного типа структуры RF3.
Четвертый тип структуры для RF3 неизвестен. Возможный вариант – признание диморфизма RF3 подгруппы А, отличающегося от диморфизма подгруппы В, – близок к реальности. Фториды типа LaF3 c R = La–Eu по [8] вблизи температуры плавления имеют “размытый” переход между формами h-LaF3 ↔ l-LaF3, рис. 1, кривая 2. Он не является переходом 1-го рода, но подвижки ионов регистрируются структурным анализом и ионной проводимостью.
Предел устойчивости типа LaF3 в фазе Nd0.82Yb0.18F3 (Z = 61.8) отвечает МП между PmF3 и SmF3. Это близко, но не совпадает с границей СП А и В. Вопрос о третьем МП у RF3 остается открытым из-за недостатка данных.
Изученность систем RF3–R'F3 (34 из 105) [17–22] мала для анализа морфотропии в системах с разнесенными по ряду RF3 (СП A–C, A–D).
Выводы. Границы составов и Т МП в RF3 и R1 ‒ xR$_{x}^{'}$F3 из близких по ряду RF3 определены однозначно (рис. 3): МП-I между GdF3 и TbF3 (Zср = = 64.43–64.51; при 1186 ± 10°С), МП-II между HoF3 и ErF3 (Zср = 67.67–67.36; при 1120 ± 10°С) [18]. МП-II дает меньшую точность. МП-I для далеко отстоящих NdF3–YbF3 смещается для t-ss к Z = 61.8 (около 62Sm).
Внутренняя периодичность границ МП-I и МП-II. Структурные подгруппы порождаются ВП заполнения 4f-подоболочки Ln [27]. Определяемая СП морфотропия в RF3 и R1 – xR$_{x}^{'}$F3 может быть связана с ВП Ln. МП-I в системе GdF3–TbF3 на границе СП В и С совпадает с делением внутрипериодной периодичности РЗЭ на Ce- и Tb-подсемейства, на что впервые указали в [22]. МП-II между HoF3 и β-ErF3 коррелирует с изменением хода Vform от Z у изоструктурных RF3, причина которого – немонотонные изменения R3+–F1–-расстояний с ростом Z [13, 15]. Положение этой границы МП совпадает с границей между СП С и D. Положение обоих МП-I и МП-II коррелирует с внутрипериодной периодичностью Ln.
СООТНОШЕНИЕ ПОЛИМОРФИЗМА, ИЗОМОРФИЗМА И МОРФОТРОПИИ В НЕКОТОРЫХ СИСТЕМАХ RF3–R'F3
Порознь полиморфизм и изоморфизм в рядах RF3 и R1 – xR$_{x}^{'}$F3 рассмотрены выше. Сопоставим три категорийных явления в одной системе с обоими типами МП-I и МП-II. Компоненты такой системы должны иметь: полиморфные переходы с модификациями разной структуры; изоморфные замещения во всех типах структур; МП между структурами всех типов.
Трифториды РЗЭ отличаются от гомологических рядов простых соединений со сменой катионов по группе Периодической системы тем, что имеют смену Z катионов по периоду с малыми ΔZ. Гомологический ряд RF3 в системах RF3–R'F3 дал уникальную возможность установить механизмы истинных МП, недоступных для “мысленного” подхода к морфотропии.
В сочетании В–D полиморфны оба компонента. Изоморфизм проявляется в трех типах структур: совершенный в изоморфноемком типе β-YF3 (β-ss) и ограниченный в типах LaF3 (t-ss) и α-YF3 (α-UO3) (α-ss), рис. 5. МП-I и МП-II можно реализовать в любой системе из B–D. Одна из них GdF3–TmF3 на рис. 2 (тип 7) взята за основу схемы рис. 5. Для краткости используем обозначения B и D как компоненты, помня, что в системах за ними стоят соответствующие RF3. Интервал Z на рис. 5 ограничен 64Gd–71Lu – РЗЭ второй половины ряда, системы с фторидами которых изучены.
Рис. 5.
Соотношение полиморфизма в RF3, изоморфизма в R1 – xR$_{x}^{'}$F3 и морфотропных превращений типа МП-I и МП-II в системах сочетания B–D (схема).
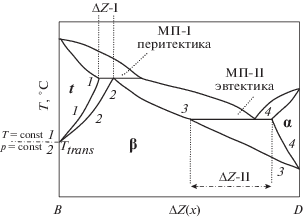
Полиморфизм у В и D инвариантен. В системе В–D на рис. 5 из точки Ttrans полиморфного превращения В выходят моновариантные кривые 1 и 2, описывающие зависимости от состава х температур перехода фазы t-R1 – xR$_{x}^{'}$F3 типа LaF3 и β-R1 ‒ yR$_{y}^{'}$F3 типа β-YF3. Двухкомпонентные твердые растворы β-ss и t-ss наследуют структуры модификаций В и D, стабилизирующиеся в Т–х-координатах изменением х. В β-ss ↔ t-ss-переходе участвуют те же типы структур, что и у В, но он идет через двухфазную область. Кривые доходят до перитектики (жирная линия на рис. 5), где начинается МП-I:
Морфотропия в системе Т–х определена: температурой фазовой реакции (МП-I перитектика и МП-II эвтектика); составами 1 и 2 равновесных фаз t-ss и β-ss разных (морфотропных) структур, насыщенных при Т перитектики, и составами 3, 4 – при Т эвтектики; двухфазной областью превращений t-ss ↔ β-ss или α-ss ↔ β-ss, задающей границы МП.
В исторически первом определении морфотропии для гомологических рядов простых соединений “изотермичность” не могла привязываться к фазовой реакции, которой у них, как у однокомпонентных фаз, нет. Для минералов со сложным катионным составом (аналоги химических систем) температурные условия морфотропии оставались неизвестными, поскольку не были изучены фазовые диаграммы.
На фазовой диаграмме системы Т–х “изотермичность” морфотропии определяется однозначно: это “температура инвариантной фазовой реакции расплава и фаз двух морфотропных типов структур разного состава”. Каждому из составляющих триады на фазовой диаграмме соответствует геометрический образ (принцип соответствия). На рис. 5 это:
– полиморфизм компонента – точка Ttrans;
– полиморфизм фаз R1 – xR$_{x}^{'}$F3 – кривые 1–4;
– изоморфизм – области гомогенности фаз t-ss, β-ss и α-ss;
– морфотропные изменения структуры – горизонтали: МП-I – перитектическая; МП-II – эвтектическая.
Бинарные системы необходимы для определения температур МП и их фазовых механизмов (перитектика или эвтектика). Только в системах Т–х может наблюдаться изоморфизм, а следовательно, и вся триада.
Полиморфизм в RF3 и R1 – xR$_{x}^{'}$F3 регулируется температурой Т через соотношение радиусов “катион/анион” (r+/r–). Изоморфизм в R1 – xR$_{x}^{'}$F3 регулирует структуру составом х через то же соотношение r+/r–, готовя с Т морфотропное превращение. Морфотропию фаз в системах RF3–R'F3 регулируют Т и состав через r+/r–. Изменение r+/r– с Т играет определяющую роль в полиморфизме, изоморфизме, морфотропии. Сжимаемость, термическое расширение и другие аналогичные характеристики RF3 изучены мало.
Выводы. Полиморфизм, изоморфизм и морфотропия в бинарных системах в координатах Т–х (Р = const) различаются степенью свободы. Полиморфизм компонента t-В ↔ β-В инвариантен (вырождение бинарной системы с х = 0). В системе В–D полиморфизм твердых растворов t-R1 ‒ xR$_{x}^{'}$F3 ↔ ↔ β-R1 – yR$_{y}^{'}$F3 моновариантен, изоморфизм бивариантен (поля t-ss, β-ss и α-ss), а МП-I (Liq + t-ss ↔ ↔ β-ss) и МП-II (Liq ↔ α-ss + β-ss) инвариантны.
Отношения полиморфизма RF3, R1 – xR$_{x}^{'}$F3 и МП-I и МП-II в системах RF3–R’F3 из сочетаний В–C и В–D позволяют уточнить определение истинной морфотропии для бинарных систем. Введение в определение истинной морфотропии температуры применимо и к “мысленной”. Проблема в том, что для классических случаев морфотропии карбонатов и им подобных соединений определение Т не всегда выполнимо технически.
Морфотропия – изменение структуры с дискретным изменением состава фаз в T–x-системе (Р = const) из соединений гомологического ряда при температуре инвариантной фазовой реакции.
В определение не внесены “качественного и (или) количественного состава” – они связаны и являются одним фактором. Не внесено “участие расплава”, так как такие реакции возможны и в твердом состоянии. “Резкое изменение структуры” исключено потому, что оно не отвечает, в частности, ряду RF3, в котором МП меняет структуры подвижками ионов без скачка КЧ.
Морфотропные переходы при высоких температурах с участием расплавов затрудняют сравнение морфотропных структур фаз – высокотемпературных структурных исследований RF3 нет, и структурный механизм их мофротропии не ясен.
Гомологические ряды соединений 4f-элементов по периоду определяют морфотропию с точностью выше любых рядов с изменением катионов по группам Периодической системы. “Мысленный” метод проводит границы морфотропии в таких рядах с точностью от ΔZ = 8 (короткий период) до 18 (длинный период). Температуры МП он не определяет вовсе.
Системы RF3–R'F3 дают точность определения истинной морфотропии в RF3 и R1 – xR$_{x}^{'}$F3, по температуре равную точности дифференциально-термического анализа (до ±5°С), а по ΔZ до ∼0.1. Соотношения полиморфизма, изоморфизма и морфотропии основаны на экспериментальных фазовых диаграммах систем RF3–R'F3 из СП В–C и В–D. Изучение систем RF3–R'F3 с далеко отстоящими по ряду РЗЭ (из СП A–C, A–D) углубит информацию по триаде.
Автор глубоко благодарен своему учителю – академику А.В. Новоселовой и выражает признательность В.С. Сидорову, А.К. Галкину и И.Д. Ратниковой за большой вклад в изучение систем RF3–R'F3.
Работа выполнена при поддержке Министерства науки и высшего образования в рамках работ по Государственному заданию ФНИЦ “Кристаллография и фотоника” РАН.
Список литературы
Урусов В.С. Теоретическая кристаллохимия. М.: изд-во МГУ, 1987. 476 с.
Sobolev B.P. The Rare Earth Trifluorides. Part 1. Barcelona: Institut d’Estudis Catalans, 2000. 520 p. (www.books.google.ru/books/rare earth trifluorides).
Sobolev B.P. The Rare Earth Trifluorides. Part 2. Barcelona: Institut d’Estudis Catalans, 2001. 460 p. (www.books.google.ru/books/rare earth trifluorides).
Spedding F.H., Henderson D.C. // J. Chem. Phys. 1971. V. 54. № 6. P. 2476.
Spedding F.H., Beaudry B.J., Henderson D.C. et al. // J. Chem. Phys. 1974. V. 60. № 4. P. 1578.
Sobolev B.P., Fedorov P.P., Steinberg D.V. et al. // J. Solid State Chem. 1976. V. 17. № 2. P. 191.
Sobolev B.P., Fedorov P.P., Seiranian K.B. et al. // J. Solid State Chem. 1976. V. 17. № 2. P. 201.
Greis O., Cader M.S.R. // Thermochim. Acta. 1985. V. 87. № 1. P. 145.
Konings R.J.M., Kovacs A. // Handbook on the Physics and Chemistry of Rare Earths / Ed. Gscheidner K.A. Amsterdam; N.-Y., Oxford. 2003. V. 33. Ch. 213. P. 147.
Oftedal I. // Z. Phys. Chem. 1929. B. 5. № 3–4. S. 272.
Zalkin A., Templeton D.H. // J. Am. Chem. Soc. 1953. V. 75. № 10. P. 2453.
Соболев Б.П., Федоров П.П. // Кристаллография. 1973. Т. 18. Вып. 3. С. 624.
Соболев Б.П., Гарашина Л.С., Федоров П.П. и др. // Кристаллография. 1973. Т. 18. Вып. 4. С. 751.
Буквецкий Б.В., Гарашина Л.С. IV Всесоюз. cимп. по химии неорган. фторидов. Душанбе. 29 сент.–3 окт. 1975. Тез. докл. М.: Наука, 1975. С. 29.
Гарашина Л.С., Соболев Б.П., Александров В.Б., Вишняков Ю.С. // Кристаллография. 1980. Т. 25. № 2. С. 294.
Соболев Б.П., Федоров П.П., Синицын Б.В., Шахкаламян Г.С. IV Всесоюз. cимп. по химии неорган. фторидов. Душанбе. 29 сент.–3 окт. 1975. Тез. докл. М.: Наука, 1975. С. 28.
Соболев Б.П., Федоров П.П., Галкин А.К. и др. // Рост кристаллов. М.: Наука, 1980. Т. 13. С. 198.
Соболев Б.П., Сидоров В.С., Федоров П.П., Икрами Д.Д. // Кристаллография. 1977. Т. 22. Вып. 5. С. 1009.
Sobolev B.P., Fedorov P.P., Ikrami D.D. et al. EUCHEM Conf. on the Chemistry of the Rare Earths. Matinryla-Helsinki. Finland. May 30–June 2. 1978. P. 134.
Сидоров В.С., Федоров П.П., Икрами Д.Д., Соболев Б.П. // V Всесоюз. симп. по химии неорган. фторидов. Днепропетровск. 27–30 июня 1978. Тез. докл. М.: Наука, 1978. С. 258.
Галкин А.К., Сидоров В.С., Икрами Д.Д. и др. // VI Всесоюз. симп. по химии неорган. фторидов. Новосибирск. 21–23 июля 1981. Тез. докл. Новосибирск. 1981. С. 118.
Федоров П.П., Соболев Б.П. // Кристаллография. 1995. Т. 40. Вып. 2. С. 315.
Соболев Б.П. Автореферат дис. “Нестехиометрия в системах из фторидов щелочноземельных и редкоземельных элементов” д-ра хим. наук. М.: Ин-т кристаллографии РАН, 1978. 48 с.
Fedorov P.P. // Russ. J. Inorgan. Chem. 2000. V. 45. Suppl. 3. P. 268.
Ranieri I.M., Baldochi S.L., Klimm D. // J. Solid State Chem. 2008. V. 181. P. 1070.
Fedorov P.P. // Mater. Res. Bull. 2012. V. 47. P. 2700.
Соболев Б.П. // Кристаллография. 2019. Т. 64. № 5. С. 701.
Соболев Б.П. // Журн. неорган. химии. 2020. Т. 65. № 3. С. 373.
Mansmann M. // Z. Kristallogr. 1965. B. 122. № 5–6. S. 375.
Schlyter K. // Arkiv Kemi. 1953. V. 5. № 1. P. 61.
Буквецкий Б.В., Гарашина Л.С. // IV Всесоюз. cимп. по химии неорган. фторидов. Душанбе. 29 сент.–3 окт. 1975. Тез. докл. М.: Наука, 1975. С. 29.
Shannon R.D. // Acta Cryst. A. 1976. V. 32. № 5. P. 751.
Greis O., Petzel T. // Z. Anorgan. Allgem. Chem. 1974. B. 403. № 1. S. 1.
Okamura K. // Chem. Industry. 1972. V. 23. № 5. P. 628.
Okamura K., Yajima S. // Bull. Chem. Soc. Jpn. 1974. V. 46. № 6. P. 1531.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография