Кристаллография, 2020, T. 65, № 5, стр. 725-732
Структура и физические свойства Mg-содержащих оксимолибдатов La2MoO6
Е. И. Орлова 1, Е. П. Харитонова 1, Н. И. Сорокина 2, Т. А. Сорокин 2, А. М. Антипин 2, В. И. Воронкова 1, *
1 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
2 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
* E-mail: voronk@polly.phys.msu.ru
Поступила в редакцию 04.03.2020
После доработки 22.04.2020
Принята к публикации 24.04.2020
Аннотация
Оксимолибдаты La2MoO6, чистые и легированные магнием, получены кристаллизацией из раствора в расплаве и методом твердофазного синтеза в виде монокристаллов и поликристаллических образцов соответственно. Соединения охарактеризованы методами рентгенофазового, рентгеноструктурного анализа, термогравиметрии, дифференциальной сканирующей калориметрии, исследованы их проводящие свойства. Получена модель структуры монокристаллов La2MoO6, легированных магнием. Внедрение атомов двухвалентного магния в позиции атомов шестивалентного молибдена в структуре La2MoO6 приводит к образованию кислородных вакансий и незначительному увеличению проводимости легированных образцов по сравнению с беспримесными кристаллами. Исследованные соединения обладают гигроскопическими свойствами.
ВВЕДЕНИЕ
Бинарные системы Ln2O3–MoO3 (Ln = La, Pr, Nd) в области 25–50 мол. % Ln2O3 перспективны для исследований, поскольку в них образуется ряд соединений с интересными свойствами. Соединения с составом 1 : 3 (соотношение молярных концентраций оксидов) обладают прекрасными люминесцентными свойствами, большими показателями преломления, среди них были впервые обнаружены несобственные сегнетоэлектрики [1]. Обширное семейство LAMOX на основе молибдата La2Mo2O9, открытое в 2000 г. [2], отличается высокой кислородной проводимостью 10–2 См/см при 800°С, которая носит вакансионный характер. Столь высокой проводимостью обладают и соединения с составом 5 : 6, хотя характер проводимости у них иной, интерстиционный (межузельный) [3]. Наконец, соединения Ln2MoO6 состава 1 : 1, так называемые оксимолибдаты, обладают сложным полиморфизмом, зависящим от размера ионного радиуса редкоземельного катиона и от температуры синтеза [4–6].
Рентгеновское исследование беспримесных оксимолибдатов выявило два типа полиморфов в зависимости от величины ионного радиуса [4–7]. В случае крупных катионов La–Nd при температуре синтеза 1200°С соединения кристаллизовались в тетрагональной фазе. Исключение составляло только соединение Nd2MoO6, которое до 1000°С существовало в моноклинной фазе, в этой же фазе при низких и высоких температурах существовали все соединения Ln2MoO6 с редкоземельными катионами с меньшими ионными радиусами. Выше температуры 1010°С соединение Nd2MoO6 необратимо переходило в тетрагональную фазу [4–8].
Структуру оксимолибдатов с крупными катионами La, Pr, Nd исследовали в ряде работ [9–12]. Впервые структура монокристаллов La2MoO6, полученных при температуре 800°С, изучена в [9], для них была установлена полярная пр. гр. I$\bar {4}$2m. Структура каждого монокристалла Nd2MoO6 и La2MoO6, полученного кристаллизацией из раствора в расплаве при 1250°C, была решена в неполярной пр. гр. I41/acd и в ее нецентросимметричной подгруппе I$\bar {4}$c2 [10]. Расположение атомов Мо в обеих моделях структуры одинаково, тогда как позиции атомов Nd(La) и кислорода незначительно различаются. Следует отметить, что для монокристалла La2MoO6 было проведено уточнение четырех ацентричных моделей – I$\bar {4}$c2, I$\bar {4}$2d, I41cd и I4122. При сопоставлении полученных результатов авторы [10] выбрали пр. гр. I$\bar {4}$c2. Структура Ln2MoO6 (Ln = La, Nd) оказалась слоистой, в которой два слоя редкоземельных полиэдров Nd(La)O8 чередуются с одним слоем тетраэдров MoО4, не связанных между собой. Проводимость беспримесных образцов оксимолибдатов Ln2MoO6 (Ln = La, Pr, Nd) невелика и составляет 10–4 См/см [13].
Имеются работы, в которых оксимолибдаты были легированы двухвалентными катионами, такими как Pb [8, 14] и Mg [15]. Допирование Nd2MoO6 и La2MoO6 cвинцом привело к весьма неожиданным результатам. В области 800°С наблюдался обратимый фазовый переход. Выше этой температуры проводимость возрастала скачком на два порядка величины. Переход был обнаружен с помощью калориметрии и исследования электрофизических свойств. Интересно отметить, что при фазовом переходе обнаружены те фазы, которые были определены в [9, 10]: высокотемпературная фаза I41/acd и низкотемпературная фаза I$\bar {4}$2m.
Что касается магния, то его введение не повышало проводимость Nd2MoO6, и заметного изменения свойств этого соединения не наблюдалось. Однако в [15] выявлены гигроскопические свойства образцов Nd2MoO6 с примесями двухвалентного магния, что свидетельствует о возможности существования определенной доли протонной проводимости в таких соединениях.
Таким образом, легирование редкоземельных оксимолибдатов приводит к существенному изменению их физических свойств, что имеет как фундаментальное, так и практическое значение. В настоящей работе получены моно- и поликристаллические образцы в разрезе La2MoO6–MgO тройной системы La2O3–MoO3–MgO, изучены их атомная структура и связь структуры с особенностями свойств соединений, в частности гигроскопических и электрофизических.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Поликристаллические образцы в системе (MgO)x(La2MoO6)(1 – x)/2 (x – мольная доля оксида магния, х = 0, 0.03, 0.05, 0.10, 0.125, 0.15) получены методом твердофазного синтеза на воздухе из оксидов чистоты 99.99%. Оксид лантана La2O3 предварительно обжигали при температуре 1000°С в течение 1 ч с целью удаления воды и углекислого газа. Таблетку нужного состава прессовали с помощью гидравлического пресса с нагрузкой до 0.01 ГПа. Далее использовали двухстадийный обжиг образцов при температурах 800 и 1250°С в течение суток c промежуточным их растиранием и прессованием таблеток. Скорость нагрева и охлаждения составляла 5 град/мин.
Беспримесные монокристаллы La2MoO6 выращивали методом кристаллизации из раствора в расплаве в системе Li2O–MoO3–La2O3. Оксид лития был добавлен в систему для снижения температуры кристаллизации. Оптимальный состав расплава для выращивания беспримесных кристаллов найден методом высокотемпературной микроскопии и составляет: La2O3 = 12.5, Li2O = = 30, MoO3 = 57.5 мол. %. Для получения легированных магнием кристаллов в указанный состав добавляли 40 мол. % MgO. Состав нагревали до температуры 1350°С. Кристаллы были бесцветными, имели пластинчатую форму размером порядка 3 × 5 мм. Плотность синтезированных поликристаллических образцов оценена гидростатическим взвешиванием в толуоле.
Рентгенофазовый анализ проводили при комнатной температуре с помощью дифрактометра Rigaku Miniflex 600 (CuKα-излучение) в интервале углов 2θ = 20°–60° с шагом 0.02°. Параметры элементарных ячеек рассчитаны методом наименьших квадратов.
Интенсивности дифракционных отражений от монокристаллов La2MoO6, беспримесного и с примесью магния, размером не более 0.5 мм, измеряли при комнатной температуре на рентгеновском дифрактометре Xcalibur Eos S2 (Rigaku Oxford Diffraction). Экспериментальные данные обработаны с помощью программы CrysAlisPro [16]. Поглощение в кристаллах учитывали аналитически по огранке [17]. Программа Jana2006 [18] использована для поиска и уточнения параметров структурной модели. Координаты атомов найдены методом charge flipping по программе Superflip [19]. Основные кристаллографические параметры, данные экспериментов и результаты уточнения структур кристаллов La2MoO6, беспримесного и с примесью магния, приведены в табл. 1, значения координат, заселенностей позиций и эквивалентных тепловых параметров – в табл. 2, основные межатомные расстояния – в табл. 3.
Таблица 1.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структурных параметров
| Химическая формула | La2MoO6 | La2Mo0.957Mg0.043O5.83 |
|---|---|---|
| Сингония, пр. гр., Z | Тетрагональная, I$\bar {4}$c2, 8 | |
| а, c, Å | 5.7982(1), 32.0425(6) | 5.7969(1), 32.0371(4) |
| V, Å3 | 1077.24(3) | 1076.58(3) |
| Dх, г/см3 | 5.793 | 5.748 |
| Излучение; λ, Å | 0.71073 | |
| μ, мм–1 | 17.78 | 16.79 |
| Т, K | 293 | |
| Размер образца, мм | 0.37 × 0.199 × 0.14 | 0.415 × 0.361 × 0.051 |
| Дифрактометр | Xcalibur Eos S2 | |
| Тип сканирования | Ω | |
| Тmin, Tmax | 0.065, 0.326 | 0.031, 0.508 |
| θmax, град | 74.45 | 74.39 |
| Пределы h, k, l | –15 ≤ h ≤ 14, –15 ≤ k ≤ 14, –84 ≤ l ≤ 82 |
–15 ≤ h ≤ 15, –12 ≤ k ≤ 13, –86 ≤ l ≤ 86 |
| Число отражений: измеренных/независимых (N1)/I > 3σ(I) (N2) | 40 331/4604/1200 | 40 384/4464/1183 |
| Метод уточнения | МНК по F2 | |
| Число уточняемых параметров | 43 | 58 |
| R(|F |)/wR2(|F |) по N1 | 5.93/3.75 | 6.03/3.80 |
| R(|F |)/wR2(|F |) по N2 | 1.67/1.77 | 1.81/1.89 |
| S | 2.11 | 2.08 |
| Δρmin/Δρmax, э/Å3 | –1.14/1.04 | –1.18/1.42 |
| Программы | CrysAlis [16], Jana2006 [18] | |
Таблица 2.
Координаты атомов, заселенности позиций (q) и эквивалентные параметры атомных смещений (Uэкв) в структурах монокристаллов La2MoO6, беспримесного и с примесью магния
| Атом | x/a | y/b | z/c | q | Uэкв, Å2 |
|---|---|---|---|---|---|
| La1 | 0 | 0 | 0.163(1) | 1 | 0.00502(2) |
| 0 | 0 | 0.164(1) | 0.948(1) | 0.00421(3) | |
| La2 | 0.5 | 0 | 0.086(1) | 1 | 0.00528(2) |
| 0.5 | 0 | 0.087(1) | 0.975(1) | 0.00468(3) | |
| Mo1 | 0.5 | 0 | 0.25 | 1 | 0.00842(3) |
| 0.5 | 0 | 0.25 | 0.927(7) | 0.00707(6) | |
| Mo2 | 0 | 0 | 0 | 1 | 0.00853(3) |
| 0 | 0 | 0 | 0.987(4) | 0.00883(4) | |
| O1 | 0.744(1) | 0.241(1) | 0.125(1) | 1 | 0.0062(1) |
| 0.745(2) | 0.259(2) | 0.125(1) | 0.936(1) | 0.00512(13) | |
| O2 | 0.334(1) | 0.168(1) | 0.215(1) | 1 | 0.0147(3) |
| 0.333(1) | 0.168(1) | 0.215(1) | 1 | 0.0128(2) | |
| O3 | 0.668(1) | 0.331(1) | 0.535(1) | 1 | 0.0127(2) |
| 0.666(1) | 0.331(1) | 0.535(1) | 1 | 0.0130(2) | |
| Mg1 | 0.543(1) | –0.025(7) | 0.255(1) | 0.073 | 0.00707 |
| Mg2 | 0 | 0 | 0.012(5) | 0.013 | 0.00883 |
| La1_1 | –0.001(1) | 0.029(1) | 0.160(1) | 0.052 | 0.00421 |
| La2_1 | 0.448(2) | 0.0009(9) | 0.0848(3) | 0.025 | 0.00468 |
Таблица 3.
Межатомные расстояния (Å) в структурах монокристаллов La2MoO6, беспримесного и с примесью магния
| Химическая связь | Расстояние, Å | |
|---|---|---|
| La2MoO6 | La2Mo0.957Mg0.043O5.83 | |
| La1–O1 × 2 | 2.403(1) | 2.445(1) |
| La1–O1 × 2 | 2.381(1) | 2.346(1) |
| La1–O2 × 2 | 2.722(2) | 2.712(1) |
| La1–O2 × 2 | 2.708(2) | 2.701(1) |
| Среднее | 2.558 | 2.213 |
| La2–O1 × 2 | 2.343(1) | 2.407(1) |
| La2–O1 × 2 | 2.446(1) | 2.376(1) |
| La2–O3 × 2 | 2.705(1) | 2.724(1) |
| La2–O3 × 2 | 2.708(1) | 2.703(1) |
| Среднее | 2.550 | 2.553 |
| Mo1–O2 × 4 | 1.776(2) | 1.780(1) |
| Среднее | 1.776 | 1.780 |
| Mo2–O3 × 4 | 1.787(1) | 1.779(1) |
| Среднее | 1.787 | 1.779 |
Дифференциальную сканирующую калориметрию (ДСК) и термогравиметрию (ТГ) проводили на оборудовании NETZSCH STA 449C в интервале температур 20–1250°С на воздухе при скорости нагрева и охлаждения 10 град/мин.
Для электрофизических измерений на поликристаллические образцы были нанесены платиновые электроды путем вжигания платиновой пасты при 800°С. Проводимость измеряли двухконтактным методом при помощи моста TESLA BM 431 E на частоте 1 МГц в интервале температур от комнатной до 900°С.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
На рис. 1 представлены порошковые дифрактограммы поликристаллических образцов (MgO)x(La2MoO6)(1 – x)/2 (х = 0, 0.03, 0.05, 0.10, 0.125, 0.15). Образец с x = 0.03 изоструктурен беспримесному La2MoO6, при х ≥ 0.05 появляется пик второй фазы, MgO (θ = 43°). Интенсивность этого пика невысока, процентное соотношение второй фазы и основной фазы оксимолибдата не превышает 1.5% в соответствии с количественным рентгенофазовым анализом, данные которого представлены в табл. 4. Там же приведены параметры элементарной ячейки беспримесного и легированных магнием образцов. Параметр с заметно уменьшается с увеличением x вплоть до x = = 0.10, что согласуется с данными рентгеноструктурного анализа беспримесного и легированных магнием монокристаллов La2MoO6. Плотность поликристаллических образцов, измеренная гидростатическим взвешиванием в толуоле, составила в среднем 95% от рентгенографической плотности (табл. 1).
Рис. 1.
Порошковые рентгеновские дифрактограммы измельченных поликристаллических образцов (MgO)x(La2MoO6)(1 – x)/2, x: 0 (1), 0.03 (2), 0.05 (3), 0.10 (4), 0.125 (5), 0.15 (6). Звездочками отмечены рефлексы примесной фазы MgO.
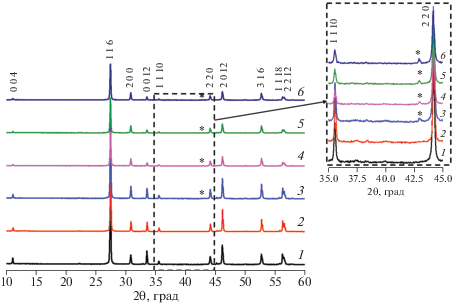
Таблица 4.
Состав, соотношение кристаллических фаз La2MoO6/MgO, параметры элементарной ячейки, потери массы после двух циклов нагрева–охлаждения для оксимолибдатов (MgO)x(La2MoO6)(1 – x)/2, полученных при температуре синтеза 1250°С
| х | La2MoO6/MgO, % | а, Å | с, Å | Потери массы в циклах 1/2, % |
|---|---|---|---|---|
| 0 | 100/0 | 5.795(7) | 32.054(4) | 0.20/0.04 |
| 0.030 | 100/0 | 5.791(2) | 32.03(1) | 0.17/0.04 |
| 0.050 | 99.6(5)/0.43(5) | 5.796(1) | 32.030(7) | 0.25/0.03 |
| 0.100 | 94.4(6)/0.64(7) | 5.800(3) | 32.01(2) | 0.26/0.04 |
| 0.125 | 99.1(5)/0.86(6) | 5.798(1) | 32.047(9) | 0.38/0.07 |
| 0.150 | 98.4(4)/1.58(8) | 5.799(1) | 32.030(8) | 0.43/0.03 |
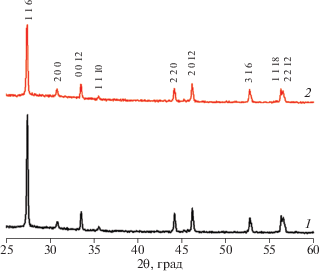
Беспримесные и легированные магнием монокристаллы La2MoO6 имели пластинчатую форму роста и размеры порядка 3–5 мм. На порошковых дифрактограммах (рис. 2), полученных от растертых монокристаллических образцов, значительное увеличение интенсивности рефлекса 0012 (рис. 2) указывает на слоистое строение кристаллов, поскольку наиболее развита в кристаллах грань (00l), перпендикулярная оси с. Исследование образцов с помощью метода ДСК не выявило каких-либо аномалий во всей исследуемой области температур.
Рис. 2.
Порошковые рентгеновские дифрактограммы измельченных монокристаллических образцов La2MoO6: беспримесных (1) и с примесью магния (2).
Уточнение структурных параметров беспримесного монокристалла La2MoO6 и с примесью магния проведено в анизотропном приближении тепловых смещений атомов в рамках пр. гр. I$\bar {4}$c2, установленной ранее авторами [10]. Результаты уточнения структурной модели представлены в табл. 2 и 3. В структуре монокристаллов La2MoO6 установлена 100%-ная заселенность атомами La и Mo своих кристаллографических позиций. При изучении строения монокристаллов La2MoO6 с примесью магния выявлены вакансии в позициях атомов La и Мо. На разностных картах Фурье вблизи этих позиций на расстоянии ∼0.5 и ∼0.3 Å соответственно обнаружены остаточные пики электронной плотности. При уточнении параметров атомов Mg1 и Mg2, замещающих атомы Mo1 и Mo2 и смещенных относительно их положений вдоль оси четвертого порядка на расстояние ∼0.3 Å, были наложены условия равенства параметров тепловых смещений атомов Mg и Mo, а также суммарной заселенности позиции 100% (табл. 2). При внедрении магния в структуру исходной матрицы La2MoO6 решетки атомы лантана подстраиваются под расположение атомов примеси, что приводит к их разупорядочению. При уточнении параметров дополнительных атомов La1_1 и La2_1 были наложены аналогичные условия (табл. 2). На данном этапе уточнения структурной модели построены разностные синтезы электронной плотности вблизи всех позиций атомов кислорода. Однако локализовать и уточнить параметры позиций атомов кислорода, которые окружают атомы Mg, La1_1 и La2_1, не удалось. Невозможность локализации расщепленных позиций атомов кислорода в структуре связана с маленькой концентрацией атомов магния в кристалле (∼4%) и, возможно, недостаточно высоким качеством экспериментального материала. Уточненная химическая формула исследованного монокристалла La2Mo0.957Mg0.043O5.83.
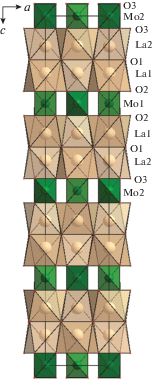
Структура исследуемой тетрагональной модификации беспримесного монокристалла La2MoO6 составлена из LaO8- и MoO4-полиэдров (рис. 3, табл. 3). Атомы La расположены в восьмивершиннике, представляющем собой слегка скрученный по оси четвертого порядка куб. Атомы Mo находятся в вытянутых вдоль оси с и не взаимодействующих друг с другом кислородных тетраэдрах. Структура слоистая. Перпендикулярно оси [001] расположены два слоя LaO8-полиэдров, проложенных одним слоем MoO4-тетраэдров. Позиции атомов La и Mo в ячейке беспримесного кристалла La2MoO6 представлены на рис. 4a. Воображаемая ячейка с атомами магния, замещающими атомы молибдена, показана на рис. 4б. Позиции Mg, как и позиции La, расщеплены. Так как концентрация магния в кристалле невелика (∼4%), таких замещений мало, и трудно судить о распределении магния в кристалле. Ясно лишь, что внедрение в структуру La2MoO6 атомов Mg приводит к разупорядочению решеток атомов La и кислорода.
Рис. 4.
Катионная модель структуры монокристалла La2MoO6 с примесью магния: ячейка основной матрицы La2MoO6 (а) и ячейка, в которой атомы молибдена замещены атомами магния (б).
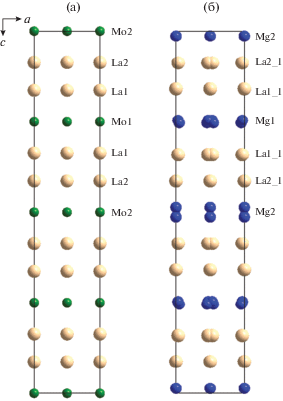
Следует отметить, что процесс вхождения атомов магния в структуру La2MoO6 аналогичен процессу вхождения атомов магния в структуру Nd2MoO6 [15]. Внедрение атомов Mg в структуру монокристалла Nd2MoO6 привело к расщеплению позиций атомов Mo, Nd и O. Атомы Mg, частично замещающие в структуре атомы Mo, располагаются на расстоянии ∼0.3 Å от атома Мо.
Для проверки гигроскопичных свойств нелегированных и легированных магнием соединений (MgO)x(La2MoO6)(1 – x)/2 (x = 0, 0.03, 0.05, 0.10, 0.125, 0.15) образцы были выдержаны около недели в дистиллированной воде при комнатной температуре. Затем было проведено два последовательных цикла нагрева–охлаждения в интервале температур от комнатной до 1250°С на воздухе.
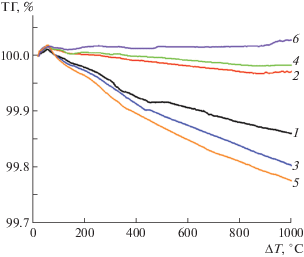
Потери массы вплоть до 1250°С после первого цикла нагрева и охлаждения указаны в табл. 4. На рис. 5 приведены кривые потери массы для образцов с x = 0, 0.05 и 0.10. Потеря воды при высоких температурах порядка 1000°С указывает на наличие воды не только в порах керамики, но и в кристаллической структуре образца [20]. При повторном нагреве потери массы образцами близки к нулю (табл. 4). Отметим, что существенные потери массы при первом нагреве наблюдались как в случае беспримесного образца, так и в случае легированных магнием. Вклад в гигроскопические свойства изучаемых соединений дала также примесь сильно поглощающей воду второй фазы MgO, в незначительных количествах присутствующей в исследуемых образцах (табл. 4).
Рис. 5.
Кривые термогравиметрии поликристаллических образцов (MgO)x(La2MoO6)(1 – x)/2: x = 0 после экспозиции в дистиллированной воде в течение семи дней (1); x = 0, повторный нагрев (2); x = 0.05 после экспозиции в дистиллированной воде в течение семи дней (3); x = 0.05 повторный нагрев образца (4); x = 0.10 после экспозиции в дистиллированной воде в течение семи дней (5); x = 0.10, повторный нагрев образца (6).
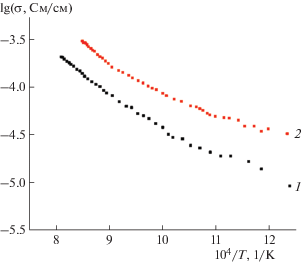
Температурные зависимости электропроводности беспримесного La2MoO6 и легированного образца (MgO)0.03(La2MoO6)0.485, измеренные при нагреве на частоте 1 МГц, приведены на рис. 6. На кривых проводимости нет ярко выраженных аномалий. Она монотонно возрастает с температурой и при 900°С близка к 10–4 См/см для нелегированного образца и примерно на четверть порядка выше в случае образца, содержащего магний. Температурные зависимости электропроводности соединений La2MoO6 и (MgO)0.03(La2MoO6)0.485 нелинейны. Участки, соответствующие области высоких (800–900°C) температур, могут быть аппроксимированы законом Аррениуса. Энергия активации для нелегированного и Mg-содержащего образцов составила 0.87 и 0.97 эВ соответственно, что типично для многих известных материалов с кислородной проводимостью. Незначительное по сравнению с содержащими свинец оксимолибдатами [8, 14] увеличение электропроводности легированного магнием образца можно объяснить образованием кислородных вакансий при вхождении двухвалентного магния в позиции шестивалентного молибдена в структуре оксимолибдата лантана.
ЗАКЛЮЧЕНИЕ
Методами кристаллизации из раствора в расплаве и твердофазного синтеза на воздухе получены моно- и поликристаллические образцы оксимолибдатов La2MoO6, легированные магнием. Рентгеноструктурные исследования монокристаллов La2MoO6, беспримесных и с примесью магния, показали, что атомы магния замещают в структуре атомы молибдена, смещаясь относительно их положений на расстояние ∼0.3 Å вдоль оси четвертого порядка. Обнаружено разупорядочение решетки атомов лантана и кислорода. Вхождение атомов двухвалентного магния в позиции атомов шестивалентного молибдена в структуре La2MoO6 приводит к незначительному увеличению проводимости легированных образцов. Обнаружены гигроскопические свойства исследованных соединений как беспримесных, так и допированных магнием.
Работа выполнена с использованием оборудования ЦКП ФНИЦ “Кристаллография и фотоника” РАН при поддержке Министерства науки и высшего образования РФ (проект RFMEFI62119X0035) в рамках Государственного задания ФНИЦ “Кристаллография и фотоника” РАН в части изучения особенностей строения и Российского фонда фундаментальных исследований (проект № 18-29-12005) в части выращивания кристаллов и исследования их свойств.
Список литературы
Nassau K., Levinstein H.J., Loiacono G.M. // J. Phys. Chem. Solids. 1965. V. 26. P. 1805.
Lacorre P., Goutenoire F., Bohnke O. et al. // Nature. 2000. V. 404. P. 856.
Tsai M., Greenblatt M., McCarroll W.H. // Chem. Mater. 1989. V. 1. P. 253.
Blasse G. // J. Inorgan. Nucl. Chem. 1966. V. 28. P. 1488.
Brixner L.H., Sleight A.W., Licis M.S. // J. Solid State Chem. 1973. V. 5. P. 186.
Покровский А.Н., Рыбаков В.К., Трунов В.К. // Журн. неорган. химии. 1969. Т. 4. С. 2344.
Клевцов П.В., Харченко Л.Ю., Клевцова Р.Ф. // Кристаллография. 1975. Т. 20. Вып. 3. С. 571.
Voronkova V., Orlova E., Kazakov S. et al. // Eur. J. Inorg. Chem. 2016. P. 1022.
Sillen L.G., Lundburg K. // Z. Anorg. Chem. 1943. B. 252. S. 2.
Ефремов В.А., Тулин А.В., Трунов В.К. // Координац. химия. 1987. Т. 13. С. 1276.
Xue J.S., Antonio M.R., Soderholm L. // Chem. Mater. 1995. V. 7. P. 333.
Антипин А.М., Сорокина Н.И., Алексеева О.А. и др. // Кристаллография. 2017. Т. 62. № 4. С. 551.
Yanovskii V.K., Voronkova V.I. // Solid State Phys. 1977. V. 19. P. 3318.
Voronkova V., Kharitonova E., Orlova E. et al. // Eur. J. Inorg. Chem. 2017. P. 5582.
Voronkova V.I., Kharitonova E.P., Orlova E.I. et al. // J. Alloys Compd. 2019. V. 803. P. 1045.
Rigaku Oxford Diffraction, CrysAlisPro Software System, Version 1.171.39.46. 2018. Rigaku Corporation, Oxford, UK.
Clark R.C., Reid J.S. // Acta Cryst. A. 1995. V. 51. P. 887.
Petricek V., Dusek M., Palatinus L. // Z. Kristallogr. 2014. B. 229. № 5. S. 345.
Palatinus L. // Acta Cryst. A. 2004. V. 60. P. 604.
Colomban Ph. // Fuel Cells. 2013. V. 13. № 1. P. 6.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография