Кристаллография, 2020, T. 65, № 5, стр. 733-739
Новые данные об изоморфизме в минералах группы эвдиалита. VIII. Кристаллическая структура Fe2+-аналога фекличевита – потенциально нового минерала из Хибинского массива
Р. К. Расцветаева 1, *, Н. В. Чуканов 2, Л. В. Сипавина 3, М. В. Воронин 3
1 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
2 Институт проблем химической физики РАН
Черноголовка, Россия
3 Институт экспериментальной минералогии им. акад. Д.С. Коржинского РАН
Черноголовка, Россия
* E-mail: rast@crys.ras.ru
Поступила в редакцию 03.04.2020
После доработки 08.04.2020
Принята к публикации 08.04.2020
Аннотация
Методом рентгеноструктурного анализа исследован потенциально новый высококальциевый минерал группы эвдиалита из Хибинского массива. Параметры тригональной элементарной ячейки: a = 14.221(1), c = 30.04(1) Å, V = 5261.3 Å3, пр. гр. R3m. Кристаллическая структура уточнена до итогового фактора расходимости R = 2.8% в анизотропном приближении атомных смещений с использованием 1714 отражений с F > 3σ(F). Идеализированная формула минерала (Z = 3): (Na12Ca3)Ca6Fe$_{3}^{{2 + }}$Zr3NbSi25O75(H2O,OH,F,Cl)3. Преобладающая двухвалентная форма железа подтверждена данными мессбауэровской спектроскопии. Минерал наиболее близок к фекличевиту из Ковдорского щелочного массива и отличается от него, прежде всего, преимущественным содержанием двухвалентного железа по отношению к трехвалентному.
ВВЕДЕНИЕ
Минералы группы эвдиалита широко распространены в щелочных массивах, в частности на Кольском полуострове, и отличаются чрезвычайно сложным составом. Их рассматривают как потенциальное сырье – источник циркония и ряда других редких (в том числе редкоземельных) элементов, в связи с чем проводятся исследования по выщелачиванию эвдиалитового концентрата [1, 2].
Группа эвдиалита состоит из кольцевых цирконо- и титаносиликатов с тригональной симметрией (R3m, R$\bar {3}$m, R3) и включает в себя 29 минеральных видов [3]. Общая формула этих минералов имеет вид: [N1N2N3N4N5]3M16M23M3 M4Z3(Si9O27)2(Si3O9)2Ø4–6X1X2, где буквами обозначены ключевые позиции структуры, вмещающие различные статистически распределенные компоненты, причем 18 компонентов (а именно, Si, Na, K, Ca, Sr, Fe2+, Fe3+, Mn, Ti, Zr, Nb, W, Сe, Н, C, O, F и Cl) могут доминировать в тех или иных позициях [4]. Основой микропористых структур минералов группы является гетерополиэдрический каркас, состоящий из трех- и девятичленных [Si3O9] и [Si9O27] кремнекислородных тетраэдров и шестичленных колец M1О6-октаэдров, соединенных ребрами. Все кольца объединены дискретными ZО6-октаэдрами, которые чаще всего заселены цирконием, и дополнительно – полиэдром M2On (n = 4–7), где M = Fe2+, Fe3+, Mn2+, Na, Zr. Остальные позиции находятся внутри этого уникального каркаса.
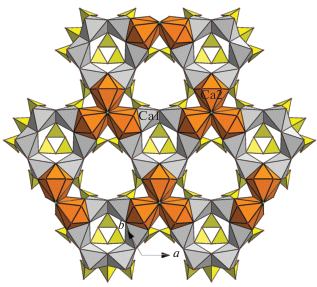
В позицию M1 входят главным образом катионы Ca, а также Mn2+, редкоземельных элементов, Na, Sr, Fe2+. Минералы группы эвдиалита в большинстве случаев характеризуются содержанием CaO 9–10 мас. % (около шести атомов Ca на формулу с Z = 3) и отношением Ca/Zr ≈ 2. Этого количества достаточно для заполнения октаэдров, образующих шестичленное кольцо в структуре эвдиалита. Однако встречаются образцы как с пониженным количеством кальция (3–6 мас. % CaO, т.е. 2.5–4.5 атомов Ca на формулу), например онейллит [5] и раслакит [6], так и высококальциевые – моговидит [7], голышевит [8] и фекличевит [9, 10] с 9–10 атомами Ca на формулу. Все эти высококальциевые минералы происходят из щелочных “пегматитов скрещения” (согласно терминологии А.Е. Ферсмана) Ковдорского массива на Кольском полуострове. В их структурах кальций не только полностью занимает М1О6-октаэдры, но и дополнительно входит в N3(4)-полиэдры (рис. 1), а позиция M2 заселена Fe3+. В настоящей работе изучена структура нового представителя семейства высококальциевых эвдиалитов – аналога фекличевита с Fe2+ в позиции M2, условно названного “феррофекличевитом”.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
“Феррофекличевит” был найден А.П. Хомяковым в виде медово-желтых зон монокристаллических зерен с неоднородной окраской (от желтой и оранжево-желтой до розовой) в пегматитах горы Эвеслогчорр Хибинского щелочного массива и предоставлен для рентгеноструктурного исследования.
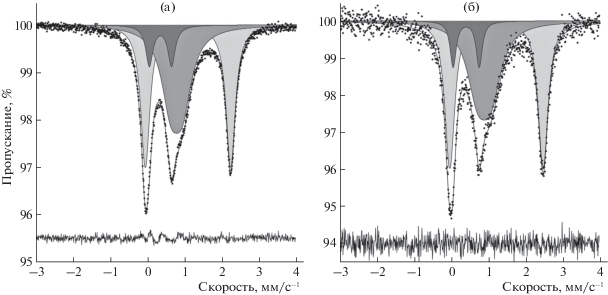
Мессбауэровские спектры получены на спектрометре MS1104Em (Южный федеральный университет, Ростов-на-Дону) с источником 57Co в матрице из родия. Съемку проводили при комнатной температуре и 90 K (рис. 2). В качестве стандарта использовали α-Fe. Спектр обрабатывали с помощью программы UnivemMS. Для измерений брали порошковую пробу массой 115 мг, содержащую фрагменты зон разного цвета. Параметры спектров, определенные в результате обработки, приведены в табл. 1.
Таблица 1.
Компоненты мессбауэровского спектра “феррофекличевита”
| Условия | Компонент | IS, мм/с | QS, мм/с | FWHM, мм/с | S, % |
|---|---|---|---|---|---|
| 293 K | V(Fe2+) | 1.096 ± 0.001 | 2.291 ± 0.002 | 0.297 ± 0.003 | 45.6 |
| IV(Fe2+) | 0.788 ± 0.004 | 0.313 ± 0.013 | 0.597 ± 0.016 | 44.0 | |
| V(Fe3+) | 0.356 ± 0.004 | 0.596 ± 0.008 | 0.236 ± 0.012 | 10.4 | |
| 90 K | V(Fe2+) | 1.223 ± 0.003 | 2.509 ± 0.006 | 0.318 ± 0.012 | 47.8 |
| IV(Fe2+) | 0.892 ± 0.012 | 0.356 ± 0.040 | 0.673 ± 0.068 | 42.8 | |
| V(Fe3+) | 0.408 ± 0.009 | 0.701 ± 0.017 | 0.199 ± 0.026 | 9.4 |
Мессбауэровские cпектры “феррофекличевита”, полученные при разных температурах, представляют собой совокупность трех дублетов, что характерно для минералов группы эвдиалита [11]. Два дублета относятся к ионам Fe2+, имеющим координационные числа 4 (конфигурация, близкая к плоскому квадрату) и 5 (квадратная пирамида). Мессбауэровские параметры третьего дублета малой интенсивности могут соответствовать Fe3+ в квадратной пирамиде или в октаэдре. Учитывая результаты рентгеноструктурного анализа, последний дублет отнесен к VFe3+. Величина коэффициента окисления железа в исследованном образце “феррофекличевита” составляет около 10%. Принципиальных различий в спектрах, полученных при разных температурах с целью выяснения температурного фактора в поведении железа в различных позициях, не зафиксировано.
ИК-спектр зерна желтого цвета, предварительно растертого в агатовой ступке и запрессованного в таблетку с KBr, снят на фурье-спектрометре ALPHA FTIR (Bruker Optics, Германия) в диапазоне волновых чисел 360–3800 см–1 при разрешающей способности 4 см–1 и числе сканирований 16. В качестве образца сравнения использовали аналогичную таблетку из чистого KBr.
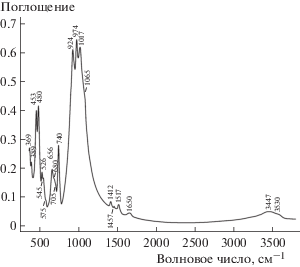
ИК-спектр “феррофекличевита” приведен на рис. 3. Спектральные полосы отнесены на основании данных об ИК-спектрах 22 эталонных образцов минералов группы эвдиалита, для которых были изучены химические составы и кристаллические структуры [3]. Полосы в диапазоне 3400–3600 и при 1650 см–1 соответствуют O–H-валентным и HOH-деформационным колебаниям соответственно. Поглощение в области 900–1100 см–1 соответствует Si–O-валентным колебаниям, причем полоса при 924 см–1 относится к валентным колебаниям тетраэдров M3SiO4 и M4SiO4, центрирующих девятичленные тетраэдрические кольца. Отсутствие полос в области 1100–1200 см–1, где проявляется мода ν3(F2) группы SO$_{4}^{{2 - }}$, свидетельствует о том, что сульфатных групп, являющихся обычными примесными компонентами в минералах группы эвдиалита, в “феррофекличевите” нет. Слабые полосы в диапазоне 1400–1520 см–1 относятся к асимметричным валентным колебаниям групп CO$_{3}^{{2 - }}$. Деформационные и смешанные колебания групп из кремнекислородных тетраэдров проявляются в интервалах 450–490 и 650–750 см–1 соответственно. Полосы при 526 и 545 см–1 относятся соответственно к (Mn,Fe)–O-валентным колебаниям ионов Mn2+ и Fe2+, имеющих координационное число 5, и к валентным колебаниям полиэдра Fe2+O4. Низкая интенсивность полосы Fe2+O4 свидетельствует о низком содержании Fe2+ с координационным числом 4. Еще более слабая полоса (плечо при 575 см–1) отнесена к валентным колебаниям полиэдра Fe3+O5. Это отнесение подтверждено как данными мессбауэровской спектроскопии, так и тем фактом, что катион Fe3+ имеет более высокие “силовые” характеристики, чем Fe2+. Наиболее низкочастотные полосы при 369 и 389 см–1 соответствуют решеточным модам, вовлекающим Ca–O-валентные колебания и колебания тетраэдрических колец как целого.
Химический состав исследовали на зерне желтого цвета методом электронно-зондового микроанализа с применением растрового электронного микроскопа Tescan Vega-II XMU (режим EDS, ускоряющее напряжение 20 кВ, ток 400 пА) и использованием системы регистрации рентгеновского излучения и расчета состава образца INCA Energy 450. Диаметр электронного пучка составил 157–180 нм. Диаметр зоны возбуждения не более 5 мкм. Время накопления сигнала 100 с. Расстояние от образца до детектора 25 мм. В качестве стандартов использовали: альбит на Na, Al2O3 на Al, SiO2 на Si, NaCl на Cl, санидин на K, волластонит на Ca, монофосфаты Ln на соответствующие лантаноиды и чистые Ti, Mn, Fe, Y, Zr, Nb и Hf на соответствующие элементы. Содержание H2O определено методом селективной сорбции газообразных продуктов прокаливания при 1200°С. Эмпирическая формула, рассчитанная на 78 анионов: Na10.95K0.55Sr0.54Ca7.55Fe$_{{1.93}}^{{2 + }}$Mn1.40Zr2.97 Hf0.04Ti0.13Nb0.71Si25.07O75.10OH0.89F0.43Cl0.36(H2O)1.22. В этой формуле железо условно дано в виде Fe2+ с учетом того, что данные мессбауэровской спектроскопии свидетельствуют о резком доминировании Fe2+ над Fe3+. Дополнительно методом ИК-спектроскопии в минерале зафиксировано присутствие небольших количеств карбонатных групп. Общее содержание серы проверяли микрозондовым анализом. Оно ниже предела обнаружения (т.е. менее 0.05 атома на формулу).
Кристаллическая структура “феррофекличевита” исследована методом рентгеноструктурного анализа. Параметры тригональной ячейки: a = = 14.221(1), c = 30.04(1) Å, V = 5261.3 Å3, пр. гр. R3m. Для сбора дифракционных данных использован монокристалл желтого цвета изометричной формы, эксперимент проводили при температуре 120 K. Характеристика кристалла и данные эксперимента приведены в табл. 2.
Таблица 2.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структуры
| Идеализированная формула (Z = 3) | (Na12Ca3)Ca6Fe$_{3}^{{2 + }}$Zr3NbSi25 O75(H2O,OH,F,Cl)3 |
|---|---|
| a, c, Å | 14.221(1), 30.04(1) |
| V, Å3 | 5261.3 |
| Плотность изм./выч., г/см3 | 3.04/2.96 |
| Сингония, пр. гр., Z | Тригональная, R3m, 3 |
| Размеры кристалла, мм | 0.19 × 0.25 × 0.20 |
| Дифрактометр | Bruker SMART-1000, CСD |
| Излучение; λ, Ǻ | MoKα; 0.71073 |
| Тип сканирования | Ω |
| Пределы h, k, l | –20 < h < 17, –20 < k < 19, –42 < l < 42 |
| (sin θ/λ)max | 0.716 |
| Общее количество/число независимых отражений с F > 3σF, Rуср, % | 12 571/1754/2.6 |
| Метод уточнения | МНК по F |
| R, % | 2.8 |
| Программы | AREN [12] |
При определении кристаллической структуры минерала в качестве стартового набора координат использованы координаты атомов каркаса фекличевита [9]. Позиции внекаркасных катионов и анионов, а также позиции M2–M4 найдены из серии разностных синтезов электронной плотности. Ряд позиций уточняли с учетом смешанных кривых атомного рассеяния. Координаты атомов, заселенность позиций, эквивалентные параметры атомных смещений и характеристики координационных полиэдров для изученного минерала приведены в табл. 3–5.
Таблица 3.
Координаты, кратность (Q) позиций и эквивалентные параметры атомных смещений для каркасных атомов
| Позиция | x/a | y/b | z/c | Q | Bэкв, Å2 |
|---|---|---|---|---|---|
| Zr | 0.3409(1) | 0.1704(1) | 0.1668(1) | 9 | 1.04(1) |
| M1 | –0.0011(1) | 0.2603(1) | 0.0009(1) | 8 | 0.82(2) |
| Si1 | 0.5266(1) | 0.2633(1) | 0.2537(1) | 9 | 0.6(2) |
| Si2 | –0.0085(1) | 0.6021(1) | 0.0969(1) | 8 | 0.5(1) |
| Si3 | 0.2061(1) | 0.4122(1) | 0.0789(1) | 9 | 0.6(2) |
| Si4 | 0.0865(1) | 0.5433(1) | 0.2600(1) | 9 | 0.7(2) |
| Si5 | 0.0566(1) | 0.3272(1) | 0.2365(1) | 18 | 0.6(1) |
| Si6 | 0.1412(1) | 0.0706(1) | 0.0835(1) | 9 | 0.5(2) |
| О1 | 0.4856(4) | 0.2428(2) | 0.2033(1) | 9 | 1.0(7) |
| О2 | 0.2673(3) | 0.0334(3) | 0.2066(1) | 18 | 1.5(5) |
| О3 | 0.4188(3) | 0.3088(3) | 0.1270(1) | 18 | 1.0(5) |
| О4 | 0.6048(2) | 0.3952(2) | 0.2603(1) | 9 | 0.9(7) |
| О5 | 0.4329(4) | 0.2160(3) | 0.2900(1) | 9 | 0.9(7) |
| О6 | 0.4128(2) | 0.0342(2) | 0.0446(1) | 18 | 0.8(5) |
| О7 | 0.0922(2) | 0.3675(2) | 0.1073(1) | 18 | 0.9(5) |
| О8 | 0.0286(4) | 0.5143(2) | 0.1135(1) | 9 | 0.9(6) |
| О9 | 0.2707(2) | 0.5414(3) | 0.0860(1) | 9 | 1.2(6) |
| О10 | 0.1836(2) | 0.3672(2) | 0.0290(1) | 9 | 0.8(6) |
| О11 | 0.0261(4) | 0.5131(2) | 0.3059(1) | 9 | 0.9(6) |
| О12 | 0.1736(2) | 0.3482(3) | 0.2188(1) | 9 | 1.0(6) |
| О13 | 0.0380(3) | 0.2938(3) | 0.2882(1) | 18 | 1.0(4) |
| О14 | 0.3855(3) | 0.4383(3) | 0.2278(1) | 18 | 1.7(4) |
| О15 | 0.3926(2) | 0.6074(2) | 0.2673(2) | 9 | 3.2(6) |
| О16 | 0.0618(1) | 0.1236(2) | 0.0822(1) | 9 | 0.9(6) |
| О17 | 0.1998(4) | 0.0999(3) | 0.1310(1) | 9 | 1.3(6) |
| О18 | 0.2216(4) | 0.1108(3) | 0.0429(1) | 9 | 1.3(6) |
Таблица 4.
Координаты, кратность (Q) и заселенность (q) позиций и эквивалентные параметры атомных смещений для внекаркасных атомов
| Позиция | x/a | y/b | z/c | Q | q | Bэкв, Å2 |
|---|---|---|---|---|---|---|
| M2а | 0.4837(1) | 0.5161(1) | 0.0033(1) | 9 | 0.85 | 1.00(2) |
| M2b | 0.4901(6) | 0.5099(6) | 0.0017(3) | 9 | 0.15 | 3.2(2) |
| M3a | 0.3333 | 0.6667 | 0.2450(1) | 3 | 0.93(1) | 0.78(6) |
| M3b | 0.3333 | 0.6667 | 0.281(1) | 3 | 0.07(2) | 1.6(8) |
| M4a | 0.3333 | 0.6667 | 0.0394(1) | 3 | 0.85(1) | 0.81(2) |
| M4b | 0.3333 | 0.6667 | 0.090(1) | 3 | 0.07(1) | 6.1(4) |
| N1 | 0.1008(1) | 0.2016(2) | 0.1597(1) | 9 | 1 | 1.73(6) |
| N2a | 0.5562(2) | 0.4438(2) | 0.1814(1) | 9 | 0.80(1) | 2.09(7) |
| N2b | 0.5896(8) | 0.4104(8) | 0.1629(6) | 9 | 0.20(1) | 1.9(3) |
| N3a | 0.1939(1) | 0.0970(1) | 0.2869(1) | 9 | 0.80(1) | 0.84(2) |
| N3b | 0.1886(5) | 0.0943(4) | 0.2977(2) | 9 | 0.20(2) | 0.7(1) |
| N4a | 0.4393(4) | 0.2199(2) | 0.0506(1) | 9 | 0.69(1) | 1.42(8) |
| N4b | 0.5003(7) | 0.2502(5) | 0.0413(2) | 9 | 0.31(1) | 1.6(1) |
| N5 | 0.1921(3) | 0.5960(2) | 0.1458(1) | 9 | 1 | 2.35(5) |
| C | 0 | 0 | 0.247(2) | 3 | 0.35(7) | 2.1(8) |
| Oc | 0.0514(7) | 0.1028(9) | 0.2403(5) | 9 | 0.35(3) | 2.1(3) |
| O19 | 0.2033(4) | 0.6017(3) | 0.0063(2) | 9 | 0.85 | 1.4(2) |
| Cl1 | 0 | 0 | 0.2281(6) | 3 | 0.24(2) | 2.5(4) |
| Cl2 | 0 | 0 | 0.1805(9) | 3 | 0.19(2) | 2.7(5) |
| F | 0.6667 | 0.3333 | 0.1233(7) | 3 | 0.40(2) | 6.5(5) |
| OH1 | 0.3333 | 0.6667 | 0.1925(3) | 3 | 0.93(2) | 1.0(2) |
| OH2 | 0.3333 | 0.6667 | 0.146(4) | 3 | 0.07(3) | 5.4(8) |
| OH3 | 0.3333 | 0.6667 | 0.337(2) | 3 | 0.07(2) | 2.9(9) |
| H2O1 | 0.6667 | 0.3333 | 0.084(2) | 3 | 0.40(2) | 4.5(5) |
| H2O2 | 0.6667 | 0.3333 | 0.137(3) | 3 | 0.20(2) | 9.2(8) |
Таблица 5.
Характеристики координационных полиэдров
| Позиция | Состав (Z = 3) | КЧ | Расстояния катион–анион, Å | ||
|---|---|---|---|---|---|
| Миним. | Максим. | Среднее | |||
| Zr | 3Zr | 6 | 2.042(5) | 2.092(5) | 2.074 |
| M1 | 5.3Ca + 0.4Mn + 0.3Ce | 6 | 2.287(3) | 2.436(3) | 2.353 |
| M2a | 1.50Fe + 1.05Mn | 5 | 2.091(4) | 2.129(3) | 2.111 |
| M2b | 0.45Fe | 4 | 2.074(9) | 2.106(9) | 2.08 |
| M3a | 0.93Si | 4 | 1.57(1) | 1.608(5) | 1.60 |
| M3b | 0.07Si | 4 | 1.51(1) | 1.67(4) | 1.55 |
| M4a | 0.71Nb + 0.11Ti | 6 | 1.885(6) | 2.080(4) | 1.982 |
| M4b | 0.07Si | 4 | 1.548(4) | 1.60(1) | 1.56 |
| N1 | 3Na | 8 | 2.520(6) | 2.888(5) | 2.656 |
| N2a | 2.4Na | 8 | 2.531(4) | 2.763(6) | 2.640 |
| N2b | 0.6Na | 7 | 2.37(1) | 3.04(4) | 2.64 |
| N3a | 1.8Ca + 0.6Sr | 8 | 2.480(4) | 2.949(5) | 2.711 |
| N3b | 0.6Ca | 7 | 2.373(8) | 2.65(1) | 2.50 |
| N4a | 2.07Na | 7 | 2.475(6) | 2.97(2) | 2.65 |
| N4b | 0.56K +0.37Na | 7 | 2.68(1) | 3.27(1) | 2.96 |
| N5 | 3Na | 6 | 2.233(6) | 3.049(4) | 2.58 |
| C | 0.35C | 3 | 1.28(1) | 1.28(1) | 1.28 |
ОПИСАНИЕ СТРУКТУРЫ И ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Основные особенности состава и структуры минерала отражены в его кристаллохимической формуле (Z = 3):
[Na11.44K0.56]VIII[Ca2.4Sr0.6]VI[Ca5.3Mn0.4Ce0.3][Zr3][V(Fe1.5Mn1.05)IV(Fe0.45)]VI[Nb0.71Ti0.11][Si0.07(OH)0.07][Si(OH)][Si3O9]2[Si9O27]2O3Cl0.43F0.40(CO3)0.35 · 0.6H2O, где квадратными скобками выделены составы ключевых позиций структуры, а римскими цифрами перед скобкой показаны координационные числа полиэдров. Идеализированная формула имеет вид: (Na12Ca3)Ca6Fe$_{3}^{{2 + }}$Zr3NbSi25O75(H2O,OH,F,Cl)3.
Исследованный минерал наиболее близок по составу и структурным особенностям к фекличевиту и голышевиту. Все три минерала характеризуются повышенным содержанием кальция, входящего как в позицию каркаса VIM1, так и во внекаркасные позиции. Сравнительные характеристики этих минералов представлены в табл. 6.
Таблица 6.
Доминирующие компоненты в ключевых позициях структур “феррофекличевита” и высококальциевых минералов группы эвдиалита
Позиция М1 в структуре “феррофекличевита” содержит незначительную примесь Mn и редкоземельных элементов. В отличие от фекличевита, в структуре которого Са целиком занимает позицию N3, в данном минерале он целиком занимает одну из расщепленных позиций N3b (семивершинник, N3b–О = 2.373–2.65 Å, среднее – 2.5 Å) и доминирует (над Sr) в N3а (восьмивершинник, N3а–О = 2.48–2.949 Å, среднее – 2.711 Å). Расщепленные позиции находятся на близком расстоянии друг от друга (N3a–N3b = 0.33(6) Å) и заселяются статистически. От голышевита “феррофекличевит” отличается распределением Са по позициям внекаркасных катионов (в голышевите Са доминирует в позиции N4, в то время как в N3 доминирует Na) и составом позиций дополнительных анионов (табл. 6).
Главное отличие “феррофекличевита” от высококальциевых минералов из Ковдорского массива заключается в доминировании двухвалентного железа над трехвалентным. В структурах фекличевита и голышевита трехвалентное железо занимает две позиции в М2-центрированных пятивершинниках, ориентированных в противоположных направлениях от плоскости основания тетрагональной пирамиды и заселенных неодинаково. В фекличевите наиболее заселенный пятивершинник, содержащий 1.26 атомов Fe3+, характеризуется расстояниями М2–O в пределах 2.08–2.12 Å (среднее – 2.093 Å).
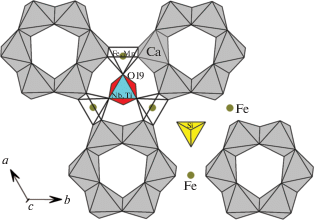
М2-позиция находится в “квадрате”, который может достраиваться до пяти-, шести- или семивершинника. В “феррофекличевите” присутствует М2а-пятивершинник с расстояниями М2a–O 2.088, 2.103, 2.105, 2.127 и 2.129 Å (среднее – 2.111 Å), по ориентации совпадающий с наиболее заселенным в фекличевите, но ориентированный в противоположном направлении по сравнению с наиболее заселенным в голышевите. Это связано с положением Nb на оси 3, в сторону которого ориентированы пятивершинники. М2-пятивершинник занят преимущественно Fe2+ (1.5 атома на формулу) и Mn (1.05 атома). Меньшая часть железа (0.45 атома) располагается в центре искаженного квадрата с расстояниями катион–кислород 2.07 × 2 и 2.11 × 2 Å. Расстояние между их позициями равно 0.17(1) Å. Присутствие Fe2+ в структуре “феррофекличевита” подтверждено данными муссбауэровской и инфракрасной спектроскопии. По данным муссбауэровской спектроскопии ионы Fe2+ распределены практически поровну между двумя позициями. Расхождение с данными рентгеноструктурного анализа может быть связано с зональным распределением железа по позициям в валовой пробе, мессбауэровский анализ которой дал усредненное значение в отличие от рентгеноструктурного анализа, проведенного на монокристалле. Апикальная вершина в пятивершиннике “феррофекличевита” связана с вершиной NbО6-октаэдра на оси третьего порядка, образуя статистические кластеры [NbFe3] и [NbMn3] (рис. 4).
Практически во всех нецентросимметричных минералах группы эвдиалита (в том числе в фекличевите) содержатся значительные количества (более 0.5 формульных единиц, Z = 3) Nb, W или Ti. Атомы этих элементов занимают на оси 3 позицию М3, в то время как в М4 находится кремний [3]. Исключение составляют только голышевит [8] и исследованный в настоящей работе аналог фекличевита из Хибин, в которых Nb заселяет преимущественно позицию М4. В “феррофекличевите” эта особенность (инверсия) проявляется наиболее ярко: весь ниобий вместе с титаном сосредоточен в позиции М4а с общей заселенностью 0.85, а позиции М3а и М3b заняты кремнием. Расщепленные позиции находятся на укороченных расстояниях друг от друга (М3а–М3b = = 1.09 Å, М4а–М4b = 1.52 Å) и заселяются статистически.
В изученном минерале аналогично фекличевиту отсутствует центр симметрии из-за вхождения Са в позицию N3, в то время как позиция, связанная с ней псевдоцентром симметрии (N4), преимущественно натриевая. Она расщепляется на две, расположенные на расстоянии N4a–N4b, равном 0.80(1) Å. Доминирование Nb и Si в двух разных позициях на оси 3 в центре девятичленных колец также усиливает ацентричность структуры.
Отсутствие центра симметрии подчеркивает распределение и внекаркасных анионов (Сl–, F–), и молекул воды по позициям на оси третьего порядка (в их числе найдена и анионная группа СО$_{3}^{{2 - }}$, присутствие которой четко зафиксировано в ИК-спектре изученного образца). В одну группу позиций (обозначенную в литературе как Х1) входят расщепленные позиции, занятые атомами фтора и молекулами воды, в другую (Х2) – атомы хлора Cl1, Cl2 и группа СО$_{3}^{{2 - }}$. Расстояния между частично заселенными позициями молекул воды составляют 1.67(7) Å, а расстояние W1–F = 1.21(6) Å. Аналогично в Х2 микрообласти расстояния между двумя позициями хлора 1.42 Å, а расстояние Cl1–С = 0.57 Å. Анионы Х1 объединяют тройки N1- и N3-полиэдров, в то время как Х2-анионы входят в N2- и N4-полиэдры соответственно. Карбонатные группы содержатся и в других высококальциевых минералах (голышевит и моговодит), но в данном минерале (как и в фекличевите) они не доминируют над Сl и H2O.
ВЫВОДЫ
Таким образом, по химическому составу и структуре изученный минерал наиболее близок к фекличевиту из Ковдорского щелочного массива и отличается от него, прежде всего, преобладанием двухвалентного железа над трехвалентным в позиции M2, что позволяет рассматривать “феррофекличевит” как Fe2+-аналог фекличевита и потенциально новый минерал группы эвдиалита.
В исследовании использованы сборы А.П. Хомякова, который много работал на агпаитовых пегматитах Кольского полуострова и коллекции которого до сих пор представляют материал для исследования.
Авторы выражают благодарность В.С. Русакову за предоставленные предварительные данные муссбауэровской спектроскопии.
Работа выполнена при поддержке Министерства науки и высшего образования РФ в рамках Государственного задания ФНИЦ “Кристаллография и фотоника” РАН в части рентгеноструктурного анализа, Государственного задания (номер государственного учета ААА-А19-119092390076-7) в части ИК-спектроскопического исследования и Российского фонда фундаментальных исследований (проекты № 18-29-12005 и № 18-29-12007-мк) в части кристаллохимического анализа микропористых минералов группы эвдиалита.
Список литературы
Friedrich B., Hanebuth M., Kruse S. Method for Opening an Eudialyte Mineral. Patent EP2995692 A1. 2016.
Davis P., Stopic S., Balomenos E. et al. // Mineral Eng. 2017. V. 108. P. 115.
Расцветаева Р.К., Чуканов Н.В., Аксенов С.М. Минералы группы эвдиалита: кристаллохимия, свойства, генезис. Нижний Новгород: Изд-во НГУ, 2012. 229 с.
Schilling J., Wu F-Y., McCammon C. et al. // Mineral Mag. 2011. V. 75. № 1. P. 87.
Johnsen O., Grice J.D., Gault R.A. // Can. Mineral. 1999. V. 37. № 4. P. 893.
Чуканов Н.В., Пеков И.В., Задов А.Е. // Зап. Всерос. минерал. о-ва. 2003. Т. 132. № 5. С. 22.
Розенберг К.А., Расцветаева Р.К., Чуканов Н.В. и др. // Докл. РАН. 2005. Т. 400. № 5. С. 640.
Розенберг К.А., Расцветаева Р.К., Чуканов Н.В. и др. // Кристаллография. 2005. Т. 50. № 4. С. 590.
Расцветаева Р.К., Екименкова И.А., Пеков И.В. // Докл. РАН. 2005. Т. 368. № 5. С. 636.
Пеков И.В., Екименкова И.А., Чуканов Н.В. и др. // Зап. Всерос. минерал. о-ва. 2001. Т. 130. № 3. С. 551.
Pol'shin E.V., Platonov A.N., Borutzky B.E. // Phys. Chem. Minerals. 1991. V. 18. № 2. P. 117.
Андрианов В.И. // Кристаллография. 1987. Т. 32. Вып. 1. С. 228.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография