Кристаллография, 2021, T. 66, № 1, стр. 104-111
Новые данные об изоморфизме в минералах группы эвдиалита. IХ. Блочный изоморфизм в ключевых позициях: кристаллическая структура Fe-дефицитного эвдиалита из Хибинского массива
Р. К. Расцветаева 1, *, Н. В. Чуканов 2, 3, Д. В. Лисицин 4
1 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
2 Институт проблем химической физики РАН
Черноголовка, Роcсия
3 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
4 Музей Самоцветы Федерального агентства по недропользованию
Москва, Россия
* E-mail: rast@crys.ras.ru
Поступила в редакцию 02.05.2020
После доработки 10.05.2020
Принята к публикации 12.05.2020
Аннотация
Методами рентгеноструктурного анализа, электронно-зондового микроанализа и ИК-спектроскопии исследованы кристаллическая структура и кристаллохимические особенности Fe-дефицитного высокомарганцевого эвдиалита из Хибинского массива (Кольский п-ов). Параметры элементарной тригональной ячейки минерала: a = 14.199(1), c = 30.305(1) Å, V = 5291.2(2) Å3, пр. гр. R3m. Кристаллическая структура уточнена до итогового фактора расходимости R = 4.46% в анизотропном приближении атомных смещений с использованием 1937 рефлексов с F > 3σ(F). Упрощенная кристаллохимическая формула минерала (Z = 3, римскими цифрами указаны координационные числа катионов в ключевых позициях): N1–5(Na,H3O)$_{{15}}^{{{\text{V}}--{\text{X}}}}$ M1(Ca,Mn)$_{6}^{{{\text{VI}}}}$ M2(FeIV,NaVI,NaV,MnVII,MnV)3M3(SiIV,NbVI) M4SiIV Z(Zr,Ti) $_{3}^{{{\text{VI}}}}$[Si24O72] (OH,Cl,SO4)3 (H2O,OH) ⋅ 1.5H2O. Обсуждаются закономерности блочного изоморфизма в минералах группы эвдиалита.
ВВЕДЕНИЕ
Характерной особенностью минералов с микропористыми гетерополиэдрическими структурами является разнообразие реализующихся в них механизмов гомовалентного, гетеровалентного и блочного изоморфизма [1]. Наиболее ярко эта особенность проявляется в минералах группы эвдиалита (МГЭ), уникальных по сложности кристаллических структур и кристаллохимическому разнообразию входящих в эту группу минеральных видов и разновидностей [2].
Под блочным изоморфизмом понимается способность групп атомов или ионов, имеющих различные конфигурации, замещать друг друга в кристаллических структурах [3]. В МГЭ можно выделить три ключевые позиции, в окрестностях которых такой изоморфизм проявляется наиболее ярко. Прежде всего это позиция M2, которая находится между кольцами M16O24, состоящими из связанных через общие ребра октаэдров M1O6 (M1 = Ca, Mn, Fe, Na, REE, Sr, Y). Позицию M2 могут заселять катионы, имеющие различные радиусы и координацию – от плоского квадрата до семивершинника: (Fe2+)IV, (Fe2+)V, (Fe3+)V, (Fe3+)VI, (Mn2+)V, (Mn2+)VI, ZrIV, TaIV, NaV, NaVI, NaVII (римскими цифрами указаны координационные числа). В основе координационных полиэдров M2O5 и M2O7 находится квадрат, образуемый четырьмя атомами кислорода (ребрами двух октаэдров соседних колец M16O24). Его дополняют одна или несколько ОН-групп, расположенных по одну или обе стороны квадрата. Пяти- или семивершинники, если они одновременно присутствуют в структуре, заполняются статистически.
Блочный изоморфизм в МГЭ реализуется также в микрообластях в окрестности позиций M3 и M4, располагающихся вблизи центров двух неэквивалентных девятичленных колец Si9O27. Эти микрообласти могут быть заполнены как тетраэдрами SiO4 или (реже) AlO4, так и октаэдрами (чаще всего NbO6 и TiO6, редко – WO6, MnO6, NaО6). [2]. Таким образом, заряд катиона в этих позициях может варьироваться от +1 (Na) до +6 (W), что возможно только при блочном изоморфизме. В настоящей работе изучен образец МГЭ с особенностями блочного изоморфизма в окрестности позиции M2.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Изученный в настоящей работе МГЭ происходит из ультраагпаитового пегматита, вскрытого подземными выработками рудника Олений Ручей. Минерал найден одним из авторов (Д.В. Лисицин) в отвалах рудника в двух различающихся по минеральному составу пегматитовых глыбах, представляющих, по всей видимости, разные зоны единого пегматитового тела. В одном случае МГЭ образует изометричные зерна коричневого и коричневато-желтого цвета размером до 30 мм, реже – четкие блестящие кристаллы размером до 5 мм в мелких полостях в ассоциации с лампрофиллитом, виллиомитом, пектолитом, джерфишеритом, эгирином и микроклином. В другом случае он образует массивные каймы (толщиной до 1 см) темно-коричневого цвета вокруг зерен красного эвдиалита обычного (“классического”) состава в почти мономинеральной (с редкими включениями пластинчатых кристаллов лампрофиллита) эгириновой породе. Для рентгеноструктурного анализа (РСА) использован обломок кристалла первого типа. Минерал исследован с применением комплекса методов – микрозондового анализа, ИК-спектроскопии и РСА.
Химический состав определяли методом рентгеноспектрального микроанализа с помощью растрового электронного микроскопа Tescan Vega-II XMU (режим EDS, ускоряющее напряжение 20 кВ, ток 400 пА) и с использованием системы регистрации рентгеновского излучения и расчета состава образца INCA Energy 450. Диаметр электронного пучка составил 157–180 нм. Пределы содержания компонентов, отражающие неоднородность состава изученного образца, следующие (в расчете на сумму Si + Nb = 26 атомов на формулу): Na11–13K0.5–0.7Ln0.1–0.3Ca4.8–5.3Mn1.3–1.7Fe0.8–1.1 Zr2.3–2.7Ti0.3–0.6Hf0–0.05Nb0.1–0.2Si25.8–25.9Cl0.5–0.6S0.2–0.3Ox ⋅ ⋅ n(H3O,H2O,OH).
Для сбора дифракционных данных на CCD-дифрактометре Xcalibur Oxford Diffraction (MoKα-излучение) использован фрагмент монокристалла изометричной формы. Характеристика кристалла и данные эксперимента приведены в табл. 1. Параметры тригональной элементарной ячейки: a = 14.199(1), c = 30.305(1) Å, V = 5291.2(2) Å3, пр. гр. R3m.
Таблица 1.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структуры
| Идеализированная формула | [Na12(H3O)3][Ca5Mn1]Zr3 [(Fe,Mn)1.7Na1.3] [Si26O72](OH,H2O)4 ⋅ 1.5H2O |
|---|---|
| a, c, Å | 14.199(1), 30.305(1) |
| V, Å3 | 5291.2(2) |
| Сингония, пр. гр., Z | Тригональная, R3m, 3 |
| Размеры кристалла, мм | 0.15 × 0.12 × 0.27 |
| Дифрактометр | Xcalibur Eos CCD Oxford Diffraction |
| Излучение; λ, Å | MoKα; 0.71073 |
| Тип сканирования | ω |
| Пределы h, k, l | 0 ≤ h ≤ 19, 0 ≤ k ≤ 19, 0 ≤ l ≤ 48 |
| (sin θ/λ)max | 0.8 |
| Общее количество/ число независимых отражений с F > 3σF | 29635/1937 |
| Метод уточнения | МНК по F |
| R, % | 4.6 |
| Программа | AREN [4] |
В качестве стартового набора использованы координаты атомов каркаса низкожелезистого эвдиалита [5]. Остальные позиции найдены из серии разностных синтезов электронной плотности. Состав катионов в некоторых позициях уточняли с учетом смешанных кривых атомного рассеяния. Все расчеты выполнены по системе кристаллографических программ AREN [4]. Уточненные структурные параметры и характеристики координационных полиэдров приведены в табл. 2–4.
Таблица 2.
Координаты, кратность позиций (Q) и эквивалентные параметры смещений (Bэкв) атомов каркаса
| Позиция | x/a | y/b | z/c | Q | Bэкв, Å2 |
|---|---|---|---|---|---|
| Z | 0.3293(1) | 0.1646(1) | 0.1669(1) | 9 | 1.48(2) |
| Si1 | 0.5259(2) | 0.2630(1) | 0.2509(1) | 9 | 1.5(1) |
| Si2 | –0.0071(1) | 0.6036(1) | 0.0970(1) | 18 | 1.29(7) |
| Si3 | 0.2065(1) | 0.4130(2) | 0.0778(1) | 9 | 1.4(1) |
| Si4 | 0.0866(2) | 0.5433(2) | 0.2592(1) | 9 | 1.6(1) |
| Si5 | 0.0554(1) | 0.3256(1) | 0.2359(1) | 18 | 1.24(7) |
| Si6 | 0.1411(2) | 0.0705(1) | 0.0821(1) | 9 | 1.1(1) |
| O1 | 0.4709(7) | 0.2355(5) | 0.2015(2) | 9 | 2.0(4) |
| O2 | 0.2617(6) | 0.0299(6) | 0.2058(2) | 18 | 2.7(2) |
| O3 | 0.4074(6) | 0.3034(6) | 0.1274(2) | 18 | 2.4(3) |
| O4 | 0.6054(3) | 0.3946(3) | 0.2518(3) | 9 | 1.7(4) |
| O5 | 0.4391(8) | 0.2191(6) | 0.2884(2) | 9 | 2.2(4) |
| O6 | 0.4086(5) | 0.0349(5) | 0.0454(1) | 18 | 1.8(2) |
| O7 | 0.0958(6) | 0.3767(7) | 0.1081(2) | 18 | 2.4(2) |
| O8 | 0.0200(8) | 0.5100(5) | 0.1111(2) | 9 | 1.7(3) |
| O9 | 0.2728(5) | 0.5456(7) | 0.0657(4) | 9 | 4.3(4) |
| O10 | 0.1814(4) | 0.3629(6) | 0.0282(3) | 9 | 2.1(3) |
| O11 | 0.0247(7) | 0.5123(5) | 0.3025(3) | 9 | 1.7(4) |
| O12 | 0.1750(4) | 0.3509(6) | 0.2161(2) | 9 | 2.1(4) |
| O13 | 0.0385(6) | 0.2962(6) | 0.2870(2) | 18 | 2.4(2) |
| O14 | 0.3882(6) | 0.4390(5) | 0.2262(2) | 18 | 2.8(2) |
| O15 | 0.3936(4) | 0.6064(4) | 0.2540(4) | 9 | 3.4(4) |
| O16 | 0.0634(4) | 0.1269(6) | 0.0756(3) | 9 | 2.5(4) |
| O17 | 0.1891(9) | 0.0945(6) | 0.1297(3) | 9 | 2.8(3) |
| O18 | 0.2242(7) | 0.1121(5) | 0.0417(3) | 9 | 2.1(3) |
Таблица 3.
Координаты, кратность (Q) и заселенность (q) позиций и эквивалентные параметры смещений атомов ключевых и внекаркасных позиций
| Позиция | x/a | y/b | z/c | Q | q | Bэкв/*изо, Å2 |
|---|---|---|---|---|---|---|
| M1a | 0.4094(1) | 0.3352(1) | 0.3332(1) | 18 | 0.82(1) | 0.74(2) |
| M1b | 0.0041(7) | 0.2731(5) | –0.0022(2) | 18 | 0.18(1) | 1.09(6) |
| M2a | –0.0097(8) | 0.4952(5) | –0.0008(3) | 9 | 0.30(1) | 1.35(6) |
| M2b | 0.4812(4) | 0.5188(4) | –0.0003(3) | 9 | 0.10(1) | 0.4(1) |
| M2c | 0.5281(3) | 0.4719(3) | –0.0038(2) | 9 | 0.19(1) | 1.51(9) |
| M2d | 0.166(1) | 0.332(2) | 0.3257(5) | 9 | 0.21(2) | 3.0(4) |
| M2e | 0.557(1) | 0.443(1) | –0.005(1) | 9 | 0.20(5) | 5.6(4) |
| M3a | 0.3334 | 0.6667 | 0.2451(3) | 3 | 0.49(2) | 1.1(3) |
| M3b | 0.3334 | 0.6667 | 0.2714(3) | 3 | 0.42(2) | 2.3(1) |
| M3c | 0.3334 | 0.6667 | 0.2897(3) | 3 | 0.09(1) | 1.9(2) |
| M4a | 0.3334 | 0.6667 | 0.0339(7) | 3 | 0.11(1) | 2.0(2) |
| M4b | 0.3334 | 0.6667 | 0.0504(5) | 3 | 0.53(3) | 4.3(1) |
| M4c | 0.3334 | 0.6667 | 0.0889(7) | 3 | 0.36(3) | 2.4(1) |
| S | 0.6667 | 0.3334 | 0.047(1) | 3 | 0.25(5) | 7.2(3) |
| N1a | 0.1091(5) | 0.2176(8) | 0.1545(3) | 9 | 0.50(2) | 2.4(3) |
| N1b | 0.0958(9) | 0.192(1) | 0.1664(6) | 9 | 0.49(3) | 5.3(3) |
| N2a | 0.5586(4) | 0.4414(4) | 0.1801(2) | 9 | 0.49(1) | 4.88(7) |
| N2b | 0.5898(6) | 0.1797(9) | 0.1640(6) | 9 | 0.30(1) | 2.4(3) |
| N2c | 0.546(1) | 0.454(1) | 0.188(1) | 9 | 0.18(2) | 3.8(4) |
| N3a | 0.225(1) | 0.1125(9) | 0.2823(3) | 9 | 0.48(2) | 2.8(4) |
| N3b | 0.191(1) | 0.096(1) | 0.2840(5) | 9 | 0.34(2) | 2.1(2) |
| N3c | 0.224(4) | 0.112(3) | 0.271(1) | 9 | 0.18(3) | 2.8(5) |
| N4a | 0.445(1) | 0.2224(8) | 0.0544(5) | 9 | 0.45(3) | 2.8(3) |
| N4b | 0.475(1) | 0.2373(9) | 0.0388(5) | 9 | 0.33(1) | 1.3(2) |
| N4c | 0.433(2) | 0.216(1) | 0.0498(9) | 9 | 0.26(2) | 2.6(3) |
| N5a | 0.246(2) | 0.491(3) | 0.172(1) | 9 | 0.1(1) | 3.8(9)* |
| N5b | 0.415(1) | 0.585(1) | 0.163(1) | 9 | 0.2(1) | 6.9(9) |
| N5c | 0.258(1) | 0.515(2) | 0.181(1) | 9 | 0.1(1) | 4.9(5)* |
| N5d | 0.194(3) | 0.597(2) | 0.148(2) | 9 | 0.2(1) | 7.7(5) |
| N6 | 0 | 0 | 0.0004(1) | 3 | 0.5(1) | 4.42(1) |
| ОS1 | 0.619(2) | 0.238(2) | 0.035(3) | 9 | 0.23(4) | 7.0(5) |
| ОS2 | 0.6667 | 0.3334 | 0.093(2) | 3 | 0.24(6) | 2.8(9) |
| OH1 | 0.3334 | 0.6667 | 0.3200(1) | 3 | 0.4(5) | 3(1) |
| OH2 | 0.3334 | 0.6667 | 0 | 3 | 0.4(5) | 3(1) |
| OH3 | 0.3334 | 0.6667 | 0.1926(7) | 3 | 0.51(4) | 1(1)* |
| OH4 | 0.3334 | 0.6667 | 0.143(2) | 3 | 0.5(1) | 3.6(5)* |
| (H2O,OH)1 | 0.147(6) | 0.574(4) | 0.006(1) | 9 | 0.27(4) | 6.2(4) |
| (H2O,OH)2 | 0.208(5) | 0.604(3) | 0.002(1) | 9 | 0.26(4) | 5.2(4) |
| (H2O,OH)3 | 0.281(3) | 0.564(5) | 0.325(3) | 9 | 0.46(7) | 3.8(5)* |
| X1a | 0 | 0 | 0.2361(7) | 3 | 0.49(4) | 5.6(3) |
| X1b | 0 | 0 | 0.262(1) | 3 | 0.3(6) | 5(1) |
| X1c | 0 | 0 | 0.293(1) | 3 | 0.21(6) | 2.2(8) |
| X2a | 0.6667 | 0.3334 | 0.109(1) | 3 | 0.38(8) | 4(1)* |
| X2b | 0.6667 | 0.3334 | 0.136(2) | 3 | 0.38(1) | 3.9(8)* |
Таблица 4.
Характеристики координационных полиэдров
| Позиция | Состав (Z = 3) | КЧ | Расстояния катион–анион, Å | ||
|---|---|---|---|---|---|
| Мин. | Макс. | Среднее | |||
| Z | 2.6Zr + 0.4Ti | 6 | 2.032(7) | 2.088(8) | 2.054 |
| M1а | 4.9Ca | 6 | 2.253(7) | 2.419(5) | 2.356 |
| M1b | 1.1Mn | 6 | 2.195(9) | 2.439(9) | 2.338 |
| M2а | 0.9Fe | 4 | 2.10(1) | 2.15(1) | 2.12 |
| M2b | 0.3Mn | 5 | 2.090(9) | 2.258(8) | 2.157 |
| M2c | 0.5(Mn,Fe) | 7 | 2.14(4) | 2.53(4) | 2.31 |
| M2d | 0.7Na | 6 | 2.02(3) | 2.74(7) | 2.35 |
| M2e | 0.6Na | 5 | 2.30(3) | 2.90(2) | 2.54 |
| M3a | 0.49Si | 4 | 1.507(9) | 1.58(2) | 1.525 |
| M3b | 0.42Si | 4 | 1.47(1) | 1.574(5) | 1.548 |
| M3c | 0.09Nb | 6 | 1.7(1) | 1.83(7) | 1.77 |
| M4a | 0.01Nb | 6 | 1.77(1) | 1.82(5) | 1.80 |
| M4b | 0.53Si | 4 | 1.52(1) | 1.56(1) | 1.55 |
| M4c | 0.36Si | 4 | 1.64(1) | 1.64(5) | 1.64 |
| N1a | 1.5Na | 9 | 2.48(1) | 2.74(1) | 2.64 |
| N1b | 1.5Na | 7 | 2.35(1) | 2.86(2) | 2.53 |
| N2a | 1.2Na + 0.3Ce | 9 | 2.45(1) | 2.96(3) | 2.68 |
| N2b | 0.9Na | 8 | 2.43(2) | 3.00(2) | 2.62 |
| N2c | 0.6Na | 8 | 2.47(1) | 2.79(1) | 2.62 |
| N3a | 1.44Na | 10 | 2.41(1) | 2.88(4) | 2.69 |
| N3b | 1.0Na | 10 | 2.36(1) | 2.90(1) | 2.75 |
| N3c | 0.56H3O | 9 | 2.45(5) | 2.95(4) | 2.67 |
| N4a | 1.35Na | 10 | 2.43(2) | 2.96(3) | 2.63 |
| N4b | 1.0Na | 10 | 2.37(3) | 2.87(2) | 2.64 |
| N4c | 0.65Na | 8 | 2.42(2) | 2.76(2) | 2.72 |
| N5a | 0.3H3O | 7 | 2.18(3) | 2.97(3) | 2.59 |
| N5b | 0.6H3O | 5 | 2.19(2) | 2.80(3) | 2.57 |
| N5c | 0.3H3O | 9 | 2.18(4) | 2.91(2) | 2.47 |
| N5d | 0.6H3O | 9 | 2.18(4) | 2.96(5) | 2.60 |
| N6 | 0.5K | 9 | 2.76(2) | 3.02(1) | 2.89 |
| S | 0.25S | 4 | 1.22(3) | 1.38(8) | 1.26 |
КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА Fe-ДЕФИЦИТНОГО ОБРАЗЦА
Основные особенности состава и строения изученного МГЭ отражены в его кристаллохимической формуле (Z = 3), которая хорошо согласуется с эмпирической: N1–5[(Na11.1(H3O)2.4Ln0.3] N6[K0.5] M1[Ca4.9(Mn1.1)] M2[Fe$_{{0.9}}^{{{\text{IV}}}}$Na$_{{0.6}}^{{{\text{VI}}}}$Na$_{{0.6}}^{{\text{V}}}$Mn$_{{0.5}}^{{{\text{VII}}}}$ (Mn,Fe)$_{{0.3}}^{{\text{V}}}$] M3,M4[Si1.8Nb0.2] Z[Zr2.6Ti0.4][Si24O72][SO4]0.25(OH)2.4 Cl0.5(H2O,OH) ⋅ 1.5H2O, где квадратными скобками выделены составы ключевых позиций структуры, а римскими цифрами обозначены координационные числа катионов. Идеализированная формула (Z = 3): [Na12(H3O)3][Ca5Mn1]Zr3[(Fe, Mn)1.7Na1.3][Si26O72](OH,H2O)4 ⋅ 1.5H2O.
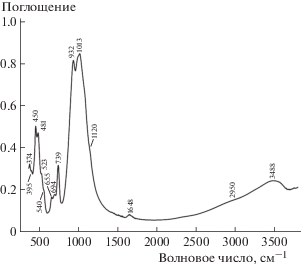
Кристаллическая структура изученного образца хорошо согласуется с его ИК-спектром (рис. 1). Полоса при 3488 см–1 относится к O–H-валентным колебаниям молекул воды и ОН-групп. Широкое плечо при 2950 см–1 свидетельствует о присутствии в минерале кислотных групп (предположительно, ионов H3O+). Полоса при 1648 см–1 относится к деформационным колебаниям молекул воды. Присутствие сульфатных анионов проявляется в виде слабо выраженного плеча при 1120 см–1. Четкая полоса при 932 см–1 отражает высокое содержание кремния в позициях M3 и M4. Полосы валентных колебаний полиэдров FeO4 и (Mn,Fe)O5 (соответственно при 540 и 523 см–1) имеют низкие интенсивности, что, очевидно, связано с низким содержанием этих полиэдров вследствие вхождения значительных количеств Na в позицию M2. Полосы ИК-спектра отнесены в соответствии с [2].
Особенностью химического состава изученного образца является пониженное содержание кальция, железа и циркония при высоком содержании кремния. Для построения шестичленного кольца необходимы шесть атомов кальция на формулу (Z = 3), и в данном случае при его недостатке (пять атомов) в позицию октаэдра статистически входит марганец. Центральная позиция расщеплена на две с расстояниями между ними 0.207(7) Å. Са-подпозиция характеризуется расстояниями M1а–O в пределах 2.253(7)–2.419(5) Å. Для второй подпозиции с заселенностью 18% Mn расстояния М1b–О = 2.195(9)–2.439(9) Å. Расщепление позиции в октаэдре шестичленного кольца со смешанной заселенностью наблюдалось и ранее, но его уточнение выполнено впервые.
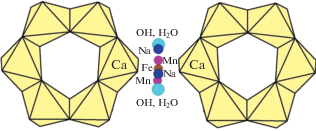
Параллельные ребра октаэдров, принадлежащих соседним шестичленным кольцам, образуют полиэдр, по своей конфигурации близкий к плоскому квадрату и координирующий ключевую позицию М2а. По обе стороны от квадрата локализовано 10 пиков на коротких расстояниях друг от друга, отвечающих катионам Fe, Mn и Na, а также ОН- и Н2О-группам (рис. 2). Центр квадрата занят катионами Fe с расстояниями до атомов О квадрата в пределах М2а–O = 2.10(1)–2.15(1) Å. По одну сторону квадрата расположены две подпозиции, смещенные из его центра на расстояния M2a–M2d = 0.24(2) и M2a–M2b = 0.58(1) Å, занятые атомами Na и Mn соответственно. Их координация на основе квадрата дополнена до шести со средним расстоянием 2.35 Å и до пяти при среднем расстоянии 2.157 Å соответственно. По другую сторону квадрата находятся также две подпозиции на расстояниях M2a–M2c = 0.57(1) и M2a–M2e = 1.29(1) Å. Их координацию также составляют атомы кислорода в квадрате, в первом случае дополненную до октаэдра (статистически – семивершинника за счет Х-аниона на оси третьего порядка) со средним расстоянием M2c–О = = 2.31 и во втором – до пятивершинника с расстоянием 2.54 Å. Полиэдры заселены атомами Mn (с примесью Fe) и атомами Na соответственно. С учетом заселенности этих подпозиций преобладающим катионом в M2-микрообласти является железо при его общем пониженном содержании (табл. 4).
Видообразующие позиции М3 и М4 располагаются на оси третьего порядка вблизи центров двух неэквивалентных девятичленных кремнекислородных колец Si9O27 и расщеплены на три подпозиции, находящиеся на коротких расстояниях друг от друга: M3a–M3b = 0.79(1), M3а–M3c = = 1.35(1), M3b–M3c = 0.55(1), M4a–M4b = 0.49(2), M4а–M4c = 1.66(1), M4b–M4c = 1.16(2) Å. Все подпозиции заселены статистически и содержат атомы кремния при небольшой примеси ниобия (табл. 5 ).
Крупные катионы распределяются по шести цеолитоподобным полостям каркаса, в которых N-позиции (кроме N6) расщепляются на две–четыре подпозиции (табл. 3, 4). В одной полости подпозиции отстоят друг от друга на расстояниях N1a–N1b = 0.48(2) Å. В другой позиция расщепляется на три с расстояниями между ними N2a– –N2b = 0.90(1), N2a–N2c = 0.38(2) и N2b–N2c = = 1.28(2) Å. В третьей полости центральная позиция расщепляется на три, разнесенные на расстояния N3a–N3b = 0.41(2), N3a–N3c = 0.33(3) и N3b–N3c = 0.55(4) Å. Расстояния в четвертой полости N4a–N4b, N4a–N4c и N4b–N4c равны 0.59(2), 0.20(2) и 0.61(3) Å соответственно. Полость, ограниченная сверху и снизу кольцами Si9O27, содержит четыре подпозиции, разнесенные на расстояния от 0.40 до 2.1 Å, а также ОН-группы в апикальных вершинах SiО4-тетраэдров, развернутых внутрь полости. Оксониевые группы в подпозициях N1–N5 формируют пяти-, семи- и девятивершинные полиэдры, а атомы K находятся в центре шестерного кольца из M1-октаэдров в позиции N6 с КЧ = 9 и заселенностью 0.5. Все N-подпозиции заняты атомами натрия и группами Н3О. В N2a-подпозицию входят в виде примеси атомы лантаноидов.
Анионная позиция X1, расположенная на оси третьего порядка, расщеплена на три подпозиции. Атом хлора в X1a находится на расстояниях Х1a–X1b = 0.77(4), Х1a–X1с = 1.71(4) Å от подпозиций, заселенных молекулами воды. Расстояние между молекулами воды Х1b–X1с = 0.93(5) Å. Все три подпозиции входят в окружение полиэдров N3a, N3b и N3c. Позиция X2 также расщеплена на три, находящиеся на расстояниях Х2a–X2b = = 0.83(8), X2a–Os = 0.49(8), X2b–Os = 1.32(9) Å друг от друга и статистически занятые атомом кислорода в вершине SО4-тетраэдра и молекулами воды, входящими в полиэдры N2а, N2b, N4a и N4b (табл. 3, 4).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
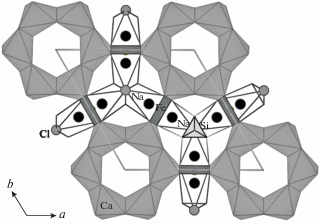
Катионы М2-микрообласти располагаются в плоскости шестичленных колец, перпендикулярной оси третьего порядка. Их полиэдры объединяют М1-октаэдры шестичленных колец и М3(М4)-октаэдры на осях 3. Позиция М2 находится в центре квадрата (рис. 3), образованного ребрами октаэдров соседних шестичленных колец, и может расщепляться на две и больше подпозиций, которые формируют полиэдры нескольких типов на базе квадрата с добавлением ОН-групп, принадлежащих осевым M3(M4)-октаэдрам. В высококремниевых образцах этот квадрат достраивается до M2-полиэдров при добавлении ОН-групп осевых тетраэдров SiO3(OH) и/или молекул воды.
Рис. 3.
Фрагмент слоя, образованного шестичленными кольцами октаэдров и ионами Fe2+ в координации плоского квадрата.
М2-квадрат заполняется атомами Fe2+, реже – Na; в качестве подчиненных и примесных компонентов в этой позиции могут присутствовать также Zr, Hf и Ta. Двухвалентное железо в квадратной координации – “визитная карточка” эвдиалита sensu stricto [6], а аналогичная координация натрия – специфическая особенность структуры аллуайвита [7]. Элементы в центре квадрата различны по своей валентности и ионным радиусам, что влияет на размеры и форму квадратов. Наиболее крупный полиэдр – NaO4 (среднее расстояние Na–O = 2.2 Å), самый маленький – FeO4 (Fe–О = = 2.0–2.1 Å), а форма этих полиэдров может трансформироваться – от квадрата до прямоугольника или трапеции [2]. Если атомы железа и натрия в квадратной координации не вызывают возражений, то вопрос о Zr и Та относится к разряду дискуссионных. В соответствии с локальным балансом зарядов на анионах, образующих квадрат, для центрального катиона предпочтительнее заряд меньше +4, и тем более он не может быть выше. Однако в гиперциркониевых образцах избыток циркония входит в позицию в центре квадрата наряду с другими элементами. Методом РСА было зафиксировано присутствие в центре плоского квадрата (Zr + Hf) в гидратированном эвдиалите [8], а также Ta в высокотанталовом МГЭ [9]. Cильные связи, отвечающие самым коротким расстояниям 2.035(7) и 2.116(8) Å, осуществляются между атомами Та и четырьмя атомами кислорода, координирующими Та по квадрату, и гораздо более слабые взаимодействия Та с двумя другими лигандами (ОН-группами) на расстояниях 2.44(2) и 2.66(1) Å соответственно. В этом случае отклонение от локального баланса зарядов смягчается за счет дальнодействующих кулоновских взаимодействий с двумя атомами кислорода (с расстояниями Та–О до 2.66 Å), формально дополняющими координационную сферу Та до искаженного октаэдра.
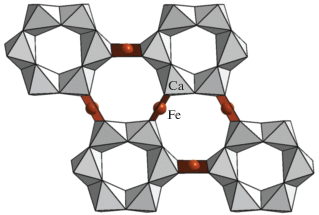
М2-полуоктаэдр, или квадратная пирамида, – пятивершинник, образующийся на базе квадрата с добавлением ОН-группы, принадлежащей М3- или М4-октаэдрам на осях третьего порядка (рис. 4). Этот полиэдр могут заселять ионы Mn2+, Fe3+, Fe2+, Na+ и Zr4+. “Визитной карточкой” кентбруксита можно считать Mn-пятивершинник [10]. Замещение марганца железом в пятивершинниках установлено в близких по строению к кентбрукситу минералах – феррокентбруксите [11], георгбарсановите [12], тасеките [13], фекличевите [14], голышевите [15] и ряде разновидностей МГЭ [2]. В этих минералах пятые вершины координационных полиэдров располагаются по одну сторону от плоскости квадрата, что подчеркивает ацентричный характер структуры (приводящий к стойкому проявлению пьезоэффекта в георгбарсановите) в отличие от близкой к центросимметричной структуры эвдиалита и его аналогов. В большинстве случаев в микрообласти M2 статистически реализуются ориентированные различным образом пятивершинники [2].
Рис. 4.
M2-пятивершинники, ориентированные в противоположные стороны, статистически замещаемые M2-октаэдром в структуре манганоэвдиалита.
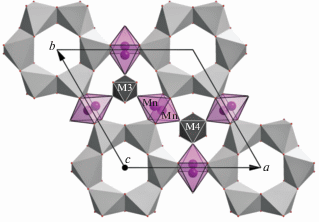
М2-октаэдр образуется, когда квадратная координация дополняется двумя ОН-группами осевых M3(M4)-октаэдров либо молекулами воды (рис. 4). В эти полиэдры могут входить атомы Fe2+, Fe3+, Ti, Hf, Zr, Mn, Na, Mg. Примерами минералов с М2-октаэдрами являются манганоэвдиалит (Mn) [16] и икранит (Fe) [17, 18]. Наиболее крупные M2-полиэдры – семивершинники, построенные на основе квадрата и атомов кислорода каркаса. В них чаще всего располагаются атомы Na, а иногда Mn и Zr (рис. 5). Na-семивершинники доминируют в структурах [5, 19], а также зафиксированы в структурах промежуточного члена изоморфного ряда манганоэвдиалит–илюхинит [20] и минерала ряда эвдиалит–сергеванит [21] с расстояниями Na–O 2.23(4)–2.96(3) и 2.33(1)–3.01(1) Å соответственно. Чаще всего разнообразные полиэдры находятся в комбинации друг с другом и имеют общие с М1-октаэдрами ребра, а с осевыми октаэдрами – вершины, в результате формируются локальные полиэдрические фрагменты пяти типов, которые заполняют статистически катионы с разными ионными радиусами и зарядами:
1. М2IV + M1VI + M1VI;
2. М2V + M1VI + M1VI + М3VI;
3. М2V + M1VI + M1VI + М4VI;
4. М2VI + M1VI + M1VI + М3VI + М4VI;
5. М2VII + M1VI + M1VI + М3VI + М4VI.
В заполнении M1VI-октаэдра могут участвовать Ca, Mn, Fe, Na, REE, Sr, Y (в дуалите в одном модуле статистически присутствует вся эта группа элементов, кроме Y) [2]. В результате в каждом минерале реализуется определенная комбинация локальных составов для пар M1- и M2-полиэдров, отвечающая условиям локального баланса валентностей на атомах кислорода, общих для этих полиэдров. Общие вершины полиэдров М2 и М3VI (М4VI) могут быть реализованы при всех вариантах их заселения. Например, в минералах ряда кентбруксит–феррокентбруксит и барсановите установлены комбинации Mn(Fe)-пятивершинников с NbО6-октаэдрами (в частности, Fe-пятивершинник в таскеите из Одихинча [22] образует кластер [NbFe3]), а в вольфрамсодержащих аналогах кентбруксита (хомяковит и манганхомяковит [23] и йонсенит-(Се) [24]) эти же пятивершинники сочетаются с WО6-октаэдрами. Заряд в таких случаях регулируется за счет О или ОН-группы в общей вершине. Большая избирательность возможна при распределении катионов с учетом наличия общего ребра М2-полиэдров и M1-октаэдров. Для высококальциевых минералов (моговидит [25], фекличевит [14], голышевит [15], феррофекличевит [26]) возможно заселение М2-полиэдров всех типов не только двухвалентными, но и четырех- и пятивалентными элементами. В других случаях реализуются комбинации одно-, двух- и трехвалентных элементов в М1-октаэдре и элементов с зарядом от +1 до +5 в М2-полиэдрах.
ВЫВОДЫ
Особенностью изученного образца является высокая структурная сепарация химических элементов в микрообласти М2, приводящая к статистической реализации четырех типов полиэдров и пяти типов локальных полиэдрических фрагментов со статистическим заполнением их катионами Са, Fe, Mn и Na. Минерал представляет яркий пример блочного изоморфизма в окрестности позиции M2. В изученном минерале локализована сульфатная группа в Х-анионной части структуры и впервые установлено расщепление смешанной позиции в октаэдре шестичленного кольца.
Работа выполнена с использованием оборудования ЦКП ФНИЦ “Кристаллография и фотоника” при поддержке Минобрнауки РФ (проект RFMEFI62119X0035) в рамках Государственного задания ФНИЦ “Кристаллография и фотоника” РАН в части рентгеноструктурного анализа и Российского фонда фундаментальных исследований (проект № 18-29-12005) в части кристаллохимического анализа микропористых минералов группы эвдиалита. Исследования методом ИК-спектроскопии проведены в соответствии с темой Государственного задания (номер государственного учета ААА-А19-119092390076-7). Работы по анализу химического состава и диагностики ассоциирующих минералов выполнены при поддержке Российского фонда фундаментальных исследований (проект № 18-29-12007_мк).
Список литературы
Chukanov N.V., Pekov I.V. // Micro- and Mesoporous Mineral Phases. Series: Reviews in Mineralogy and Geochemistry / Eds. Ferraris G., Merlino S. Washington: Mineralogical Society of America, 2005. V. 57. P. 105.
Расцветаева Р.К., Чуканов Н.В., Аксенов С.М. Минералы группы эвдиалита: кристаллохимия, свойства, генезис. Нижний Новгород: Изд-во НГУ, 2012. 229 с.
Солодовников С.Ф. Основные термины и понятия структурной кристаллографии и кристаллохимии. Новосибирск: Изд-во ИНХ СО РАН, 2005. 114 с.
Андрианов В.И. // Кристаллография. 1987. Т. 32. Вып. 1. С. 228.
Расцветаева Р.К., Хомяков А.П. // Докл. РAH. Химия. 1998. Т. 362. № 6. С. 784.
Голышев В.М., Симонов В.И., Белов Н.В. // Кристаллография. 1972. Т. 17. Вып. 6. С. 1119.
Расцветаева Р.К., Хомяков А.П., Андрианов В.И., Гусев А.И. // Докл. АН СССР. 1990. Т. 312. № 6. С. 1379.
Rozenberg K.A., Rastsvetaeva R.K., Khomyakov A.P. // Eur. J. Mineral. 2005. V. 17. P. 875.
Расцветаева Р.К., Чуканов Н.В., Меккель Ш. // Кристаллография. 2003. Т. 48. № 2. С. 250.
Johnsen O., Grice J.D., Gault R.A. // Eur. J. Mineral. 1998. V. 10. P. 207.
Johnsen O., Gault R.A., Grice J.D. // Can. Mineral. 2003. V. 41. P. 55.
Хомяков А.П., Нечелюстов Г.Н., Екименкова И.А., Расцветаева Р.К. // Зап. Всерос. минерал. о-ва. 2005. № 6. С. 47.
Екименкова И.А., Расцветаева Р.К., Чуканов Н.В. // Кристаллография. 2000. Т. 45. № 6. С. 1010.
Расцветаева Р.К., Екименкова И.А., Пеков И.В. // Докл. РАН. 1999. Т. 368. № 5. С. 636.
Розенберг К.А., Расцветаева Р.К., Чуканов Н.В., Верин И.А. // Кристаллография. 2005. Т. 50. № 4. С. 590.
Номура С.Ф., Атенсио Д., Чуканов Н.В. и др. // Зап. Рос. минерал. о-ва. 2010. Т. 139. № 4. С. 35.
Екименкова И.А., Расцветаева Р.К., Чуканов Н.В. // Докл. РАН. 2000. Т. 371. № 5. С. 625.
Расцветаева Р.К., Чуканов Н.В. // Кристаллография. 2003. Т. 48. № 5. С. 775.
Розенберг К.А., Расцветаева Р.К., Верин И.А. // Кристаллография. 2009. Т. 54. № 3. С. 446.
Расцветаева Р.К., Чуканов Н.В., Меккель Ш. и др. // Кристаллография. 2020. Т. 65. № 1. С. 32.
Расцветаева Р.К., Чуканов Н.В., Ван К.В. // Кристаллография. 2020. Т. 65. № 4. С. 555.
Расцветаева Р.К., Чуканов Н.В., Зайцев В.А. и др. // Кристаллография. 2018. Т. 63. № 3. С. 392.
Johnsen O., Gault R.A., Grice J.D., Ercit T.S. // Can. Mineral. 1999. V. 37. P. 893.
Grice J.D., Gault R.A. // Can. Mineral. 2006. V. 44. P. 105.
Розенберг К.А., Расцветаева Р.К., Чуканов Н.В., Верин И.А. // Докл. РАН. 2005. Т. 400. № 5. С. 640.
Расцветаева Р.К., Чуканов Н.В., Сипавина Л.В., Воронин М.В. // Кристаллография. 2020. Т. 65. № 5. C. (в печати).
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография