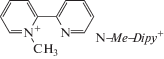Кристаллография, 2021, T. 66, № 3, стр. 412-416
Структура и свойства анион-радикальной соли 7,7,8,8-тетрацианохинодиметана с катионом N-метил-2,2'-дипиридила
Т. Н. Стародуб 1, *, Д. Фенске 2, 3, 4, О. Фур 3, 4, С. Мишкевич 1, О. Н. Кажева 5, В. А. Стародуб 1
1 Институт химии Университета им. Яна Кохановского
Кельце, Польша
2 Институт неорганической химии Технологического института
Карлсруэ, Германия
3 Институт нанотехнологии и Карлсруэ наномикроотделение Технологического института Карлсруэ
Еггеншттайн-Деопольдсгафен, Германия
4 Лен-институт функциональных материалов Института химии и химической инженерии Университета Сень-Ят-Сена
Гуанчжоу, Китай
5 Институт проблем химической физики РАН
Черноголовка, Россия
* E-mail: tstarodub@ujk.edu.pl
Поступила в редакцию 02.06.2020
После доработки 02.06.2020
Принята к публикации 22.07.2020
Аннотация
Синтезирована анион-радикальная соль 7,7,8,8-тетрацианохинодиметана с катионом N-метил-2,2'-дипиридила. Методами электронной спектроскопии и элементного анализа установлен ее состав. Методом рентгеноструктурного анализа определена кристаллическая и молекулярная структура соли. Соль содержит однородные стопки частиц 7,7,8,8-тетрацианохинодиметана, что является необходимым условием высокой электрической проводимости. В ИК-спектре соли наблюдаются особенности, характерные для органических металлов – непрерывное поглощение (электронный континуум) и проявление электронно-фононного взаимодействия. Это позволяет отнести данную соль к органическим металлам.
ВВЕДЕНИЕ
Анион-радикальные соли (АРС) на основе 7,7,8,8-тетрацианохинодиметана (TCNQ) вызывают большой интерес с конца 60-х годов прошлого столетия, когда на основе TCNQ были получены первые органические металлы [1, 2]. После открытия органических металлов, а затем и сверхпроводников на основе катион-радикальных солей [2] интерес к АРС на основе TCNQ ослабел, однако во второй половине 80-х годов прошлого столетия он вновь возник и с тех пор не ослабевает. Это связано прежде всего с открытием плавких проводящих органических проводников на их основе.
Исследования магнитных свойств АРС на основе TCNQ привели к открытию магнитоупорядоченных структур – ферро- и антиферромагнитных [3, 4]. Использование в качестве противоионов органических катионов, содержащих в своем составе более одного донорного атома, привело к открытию квазидвумерных органических проводников на основе АРС [5]. Наличие в составе катиона некватернизованных донорных атомов создает возможность косвенного магнитного обмена между спинами анион-радикалов соседних стопок, что было продемонстрировано на примере АРС TCNQ с катионами на основе пиразина [6–8].
С целью расширения подобных исследований было проведено исследование АРС TCNQ с катионом N-метил-2,2'-дипиридила:
Комплексы 2,2'-дипиридила проявляют свойства антиоксидантов, а также антибактериальные и антигрибковые свойства [9]. На основе Dipy могут быть сконструированы эффективные биосенсоры для обнаружения патогенной биофлоры в продуктах питания [10]. Поэтому АРС TCNQ с катионами на основе Dipy могут найти применение в биотехнологии.
В работе описано получение монокристаллов АРС (N-Me-Dipy)(TCNQ)2 (1), их кристаллическая и молекулярная структура, а также данные, полученные на основе ИК-спектров.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
7,7,8,8-тетрацианохинодиметан, 2,2'-дипиридил, хлористый метил и йодид лития фирмы Aldrich использовали без дополнительной очистки. Соль LiTCNQ синтезировали в ацетонитриле, реакцию кватернизации дипиридила проводили также в ацетонитриле.
Для синтеза АРС использовали реакцию
Кристаллы 1 отфильтровывали, промывали диэтиловым эфиром и сушили на воздухе. Состав АРС был установлен спектрофотометрически по методике [11]. Он был подтвержден элементным анализом. Найдено: C 71.53, H 3.74, N 24.91 мас. %. Получена химическая формула C37H22N11. Вычислено: C 71.60, H 3.57, N 24.82 мас. %.
Для определения структуры синтезированной АРС использовали дифрактометр Stoe StadiVari. Съемку проводили при температуре 140.15 К. Для решения структуры использовали программы Olex2 [12] и ShelXT [13]. Уточнение проводили методом наименьших квадратов по программе ShelXL [13].
Основные кристаллографические параметры C37H22N11 (M = 620.65 г/моль): ромбическая пр. гр. P212121 (№ 19), a = 7.5644(4), b = 12.7028(7), c = = 31.7026(15) Å, V = 3046.3(3) Å3, Z = 4, Т = 140.15 К, μ(GaKα) = = 0.442 мм–1, Dвыч = 1.353 г/см3, 20 772 измеренных отражений (6.522° ≤ 2θ ≤ 119.978°), 6779 независимых отражений (Rint = 0.0514, Rsigma = = 0.0790), которые были использованы во всех расчетах. Финальные значения: R1 = 0.0477 (I > > 2σ(I)) и wR2 = 0.1272 (по всем данным).
Длины связей и валентные углы приведены в табл. 1 и 2, на рис. 1 представлена структура соединения 1 с нумерацией атомов. Кристаллографические данные депонированы в Кембриджский банк структурных данных (CCDC № 2006758) и могут быть получены через www.ccdc.cam.uk.conts/retrieving (CCDC, 12 Union Road, Cambridge CB21EZ, UK; факс: +44 1223 336 033; deposit@ccdc.cam.ac.uk).
Таблица 1.
Длины связей в структуре 1
| Связь | Длина, Å | Связь | Длина, Å |
|---|---|---|---|
| N1–C1 | 1.367(5) | C27–C33 | 1.404(5) |
| N1–C5 | 1.363(4) | C28–C29 | 1.356(4) |
| N1–C11 | 1.490(5) | C30–C31 | 1.430(6) |
| N2–C6 | 1.356(4) | C30–C32 | 1.424(6) |
| N2–C10 | 1.338(5) | C33–C34 | 1.420(6) |
| C1–C2 | 1.358(5) | C33–C35 | 1.421(5) |
| C2–C3 | 1.374(6) | N3–C19 | 1.142(5) |
| C3–C4 | 1.373(5) | N4–C20 | 1.146(5) |
| C4–C5 | 1.381(5) | N5–C22 | 1.154(5) |
| C5–C6 | 1.483(5) | N6–C23 | 1.139(5) |
| C6–C7 | 1.383(5) | C12–C13 | 1.445(5) |
| C7–C8 | 1.381(5) | C12–C17 | 1.439(5) |
| C8–C9 | 1.367(6) | C12–C18 | 1.390(5) |
| C9–C10 | 1.379(5) | C13–C14 | 1.347(5) |
| N7–C31 | 1.142(5) | C14–C15 | 1.438(5) |
| N8–C32 | 1.150(5) | C15–C16 | 1.435(5) |
| N9–C34 | 1.149(5) | C15–C21 | 1.389(5) |
| N10–C35 | 1.150(5) | C16–C17 | 1.345(4) |
| C24–C25 | 1.435(5) | C18–C19 | 1.436(6) |
| C24–C29 | 1.429(5) | C18–C20 | 1.436(6) |
| C24–C30 | 1.398(5) | C21–C22 | 1.427(6) |
| C25–C26 | 1.350(5) | C21–C23 | 1.431(5) |
| C26–C27 | 1.431(5) | N11–C36 | 1.138(6) |
| C27–C28 | 1.425(5) | C36–C37 | 1.450(6) |
Таблица 2.
Валентные углы в структуре 1
| Связь | Угол, град | Связь | Угол, град |
|---|---|---|---|
| C1–N1–C11 | 116.3(3) | C32–C30–C31 | 117.04(3) |
| C5–N1–C1 | 120.7(3) | N7–C31–C30 | 178.3(5) |
| C5–N1–C11 | 123.0(3) | N8–C32–C30 | 178.6(5) |
| C10–N2–C6 | 116.3(4) | C27–C33–C34 | 122.0(4) |
| C2–C1–N1 | 120.6(4) | C27–C33–C35 | 122.6(4) |
| C1–C2–C3 | 120.1(4) | C34–C33–C35 | 115.3(3) |
| C4–C3–C2 | 118.7(4) | N9–C34–C33 | 178.5(5) |
| C3–C4–C5 | 121.5(3) | N10–C35–C33 | 177.7(5) |
| N1–C5–C4 | 118.3(3) | C17–C12–C13 | 117.6(3) |
| N1–C5–C6 | 122.1(3) | C18–C12–C13 | 120.9(3) |
| C4–C5–C6 | 119.6(3) | C18–C12–C17 | 121.4(3) |
| N2–C6–C5 | 112.9(3) | C14–C13–C12 | 120.9(3) |
| N2–C6–C7 | 122.8(3) | C13–C14–C15 | 121.2(3) |
| C7–C6–C5 | 124.0(3) | C16–C15–C14 | 117.9(3) |
| C8–C7–C6 | 118.8(4) | C21–C15–C14 | 120.9(3) |
| C9–C8–C7 | 119.5(4) | C21–C15–16 | 121.2(3) |
| C8–C9–C10 | 118.2(4) | C17–C16–C15 | 121.2(3) |
| N2–C10–C9 | 124.4(4) | C16–C17–C12 | 121.2(3) |
| C29–C24–C25 | 117.4(3) | C12–C18–C19 | 121.9(4) |
| C30–C24–C25 | 121.2(4) | C12–C18–C20 | 121.6(4) |
| C30–C24–C29 | 121.4(3) | C19–C18–C20 | 116.5(3) |
| C26–C25–C24 | 121.2(3) | N3–C19–C18 | 179.3(4) |
| C25–C26–C27 | 121.3(3) | N4–C20–C18 | 179.6(5) |
| C28–C27–C26 | 117.6(3) | C15–C21–C22 | 122.4(4) |
| C33–C27–C26 | 121.1(3) | C15–C21–C23 | 123.0(3) |
| C33–C27–C28 | 121.3(3) | C22–C21–C23 | 114.6(3) |
| C29–C28–C27 | 121.3(3) | N5–C22–C21 | 177.4(4) |
| C28–C29–C24 | 121.2(3) | N6–C23–C21 | 177.3(4) |
| C24–C30–C31 | 121.6(4) | N11–C36–C37 | 178.7(6) |
| C24–C30–C32 | 121.4(4) |
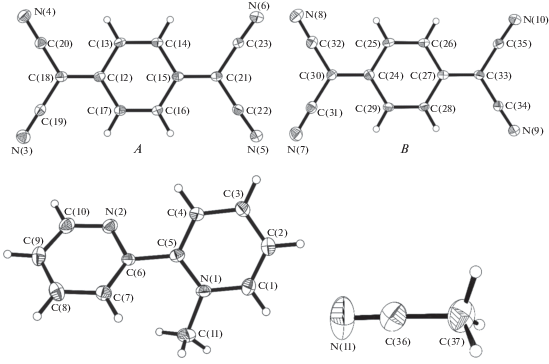
Рис. 1.
Строение анион-радикалов (А и В), катиона и молекулы ацетонитрила в структуре 1, эллипсоиды изображены с вероятностью 30%.
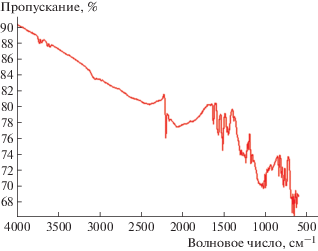
ИК-спектры получали на приборе Nicoletis 10 (Thermo Scientific) с приставкой SmartMIRacle в интервале 600–4000 см–1. На рис. 2 представлен ИК-спектр соли 1.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
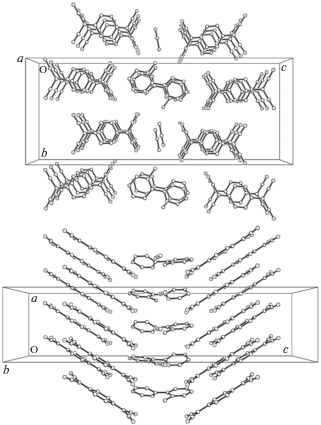
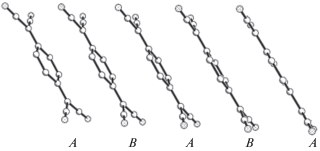
Кристаллическая структура АРС 1 образована двумя анион-радикалами ${\text{TCN}}{{{\text{Q}}}^{{-- \bullet }}}$ (А и В), катионом N-метил-2,2'-дипиридила и молекулой растворителя, расположенными в общих позициях элементарной ячейки (рис. 3). Геометрия катиона отклоняется от планарной, что, видимо, обусловлено стерическим эффектом метильной группы – двугранный угол между плоскостями N-циклов равен 41.3°. Анион-радикалы ${\text{TCN}}{{{\text{Q}}}^{{-- \bullet }}}$ характеризуются планарным строением – максимальный выход всех атомов, кроме атомов водорода, из их усредненных плоскостей не превышает 0.06 и 0.03 Å (атомы N(3) и N(9) соответственно). Соль характеризуется слоистой кристаллической структурой, в которой вдоль оси c происходит чередование слоев, образованных катионами и молекулами растворителя, со слоями анион-радикалов ${\text{TCN}}{{{\text{Q}}}^{{-- \bullet }}}$ (рис. 3). Анион-радикалы образуют стопки (рис. 4), в которых чередуются в последовательности A…B…A…B. Расстояние между усредненными плоскостями анион-радикалов в стопке составляет 3.19 Å, двугранные углы между этими плоскостями равны 179.9°. Соседние стопки в слое сдвинуты друг относительно друга вдоль длинной оси анион-радикала примерно на половину его длины, а стопки из слоев, разделенных катионами, еще различаются углом наклона катион-радикалов в стопке (рис. 4).
На основании химической формулы 1 можно сделать вывод, что усредненная величина заряда на частицах TCNQ–q равна –0.5 или –1.0 на две формульные единицы TCNQ. Учитывая наличие в структуре АРС 1 двух кристаллографически неэквивалентных частиц TCNQ, заряды на них можно оценить на основании предложенного Кистенмахером соотношения:
где параметры c, b и d – длины соответствующих связей (схема 1) [14, 15]:Используя данные табл. 1, находим для двух типов частиц TCNQ следующие заряды: –0.55 и ‒0.32. Учитывая приближенность метода, эти величины можно считать удовлетворительными; в кристаллах АРС существует слабое альтернирование заряда частиц TCNQ.
Как известно [1, 2], в ИК-спектрах проводящих АРС TCNQ проявляются особенности, об-условленные электронно-фононным взаимодействием. В частности, проявляется непрерывное поглощение, начало которого соответствует ширине запрещенной зоны, и на его фоне проявляются линии полносимметричных колебаний (эти линии в отсутствие такого взаимодействия запрещены в ИК-спектрах).
Как видно из рис. 2, в спектре АРС 1 наблюдается непрерывное поглощение во всем исследованном интервале волновых чисел, линии в области 900–1400, 1800–2100 см–1 сильно уширены. Эти особенности характерны для высокопроводящих АРС TCNQ и обусловлены электронно-фононным взаимодействием [1, 2]. Следствием этого взаимодействия является “возгорание” запрещенных правилами отбора полносимметричных колебаний TCNQ и их значительное уширение. Они проявляются на фоне электронного континуума, начало которого определяется шириной запрещенной зоны. Это позволяет сделать вывод, что данная АРС является органическим металлом либо узкозонным полупроводником. Ширина запрещенной зоны ограничена соотношением [2]:
где Δ – ширина запрещенной зоны, ν0 – начало непрерывного поглощения. В данном случае получаем оценку: Δ ≤ 0.07 эВ.ЗАКЛЮЧЕНИЕ
Синтезированная в работе АРС содержит изолированные стопки анион-радикалов TCNQ, в которых наблюдается слабое альтернирование заряда. Структура и строение АРС благоприятствуют образованию проводящего состояния соли. Это подтверждают ИК-спектры соли: непрерывное поглощение в спектре позволяет отнести данную АРС к органическим металлам либо к узкозонным полупроводникам (ширина запрещенной зоны не превышает 0.07 эВ).
Список литературы
Стародуб В.А., Стародуб Т.Н. // Успехи химии. 2014. Т. 83. № 5. С. 391.
Стародуб В.А., Стародуб Т.Н., Кажева О.Н., Брегадзе В.И. Материалы современной электроники и спинтроники. М.: Физматлит, 2018. 424 с.
Ueda K., Sugimoto T., Endo S. et al. // Chem. Phys. Lett. 1996. V. 261. P. 295. https://doi.org/10.1016/0009-2614(96)00982-7
Sugimoto T., Ueda K., Tsujii M. et al. // Chem. Phys. Lett. 1996. V. 249. P. 304. https://doi.org/10.1016/0009-2614(95)01418-7
Ziolkovsky D.V., Kravchenko A.V., Starodub V.A. et al. // Funct. Mater. 2005. V. 12. P. 577.
Ziolkovskiy D.V., Kazheva O.N., Shilov G.V. et al. // Funct. Mater. 2006. V. 13. P. 119.
Barszcz B., Graja A., Ziolkovskiy D.V., Starodub V.A. // Synth. Met. 2008. V. 158. P. 246. https://doi.org/10.1016/j.synthmet.2008.01.010
Radvakova A., Ziolkovskiy D.V., Cheranovskii V.O. et al. // J. Phys. Chem. Solids. 2009. V. 70. P. 1471. https://doi.org/10.1016/j.jpcs.2009.09.004
Piotrowska A., Drzeżdżon J., Jacewicz D., Chmurzyński L. // Wiadomości Chemiczne. 2017. V. 71. P. 220. http://www.dbc.wroc.pl/dlibra/docmetadata?id=36712&from=publication
Tichoniuk M., Ligaj M., Filipiak M. // Sensors. 2008. V. 8. P. 2118. https://doi.org/10.3390/s8042118
Starodub V.A., Gluzman E.M., Kaftanova Yu.A., Olejniczak J. // Theor. Experim. Chem. 1997. V. 33. № 2. P. 95. https://doi.org/10.1007/BF02765953
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. P. 339. https://doi.org/10.1107/S0021889808042726
Sheldrick G.M. // Acta Cryst. A. 2015. V. 71. P. 3. https://doi.org/10.1107/S2053273314026370
Üngör Ö., Phan H., Sang Choi E. et al. // J. Magn. Magn. Mater. 2020. V. 497. P. 165984. https://doi.org/10.1016/j.jmmm.2019.165984
Kistenmacher Th.J., Emge Th.J., Bloch A.N., Cowan D.O. // Acta Cryst. B. 1982. V. 38. P. 1193. https://doi.org/10.1107/S0567740882005275
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография