Кристаллография, 2021, T. 66, № 5, стр. 750-758
Кристаллизация в условиях микрогравитации и структура атомного разрешения уридинфосфорилазы из Vibrio cholerae
П. А. Эйстрих-Геллер 1, С. В. Рубинский 1, В. Р. Самыгина 1, 2, А. Г. Габдулхаков 1, М. В. Ковальчук 1, 2, А. С. Миронов 3, А. А. Лашков 1, *
1 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
2 Национальный исследовательский центр “Курчатовский институт”
Москва, Россия
3 Институт молекулярной биологии им. В.А. Энгельгардта РАН
Москва, Россия
* E-mail: alashkov83@gmail.com
Поступила в редакцию 08.09.2020
После доработки 22.09.2020
Принята к публикации 28.09.2020
Аннотация
Уридинфосфорилазы известны в качестве одной из ключевых мишеней при разработке новых противоопухолевых и антипаразитарных препаратов. В условиях микрогравитации на Международной космической станции методом встречной диффузии в капиллярах выращены кристаллы уридинфосфорилазы из патогенной бактерии Vibrio cholerae. Определена ее пространственная структура атомного (1.04 Å) разрешения (RCSB ID PDB: 6Z9Z). Впервые в пространственной структуре уридинфосфорилазы в отсутствие связанных специфических лигандов обнаружены альтернативные конформации протяженных областей (β-стрендов и смежных петель) белковой молекулы. Эти альтернативные конформации, возможно, связаны с функционированием фермента. Методами конформационного анализа с использованием марковских моделей показано, что переход между конформациями возможен и без связывания фермента с лигандом.
ВВЕДЕНИЕ
При развитии опухолевых заболеваний в клетках человека повышается потребность в азотистых пиримидиновых основаниях, к которым относятся уридин и тимидин. Азотистые основания можно получить с помощью обратимой каталитической реакции фосфоролитического расщепления пиримидиновых нуклеозидов. Катализатором этой реакции выступает уридинфосфорилаза (UPh). Экспрессия этого белка возрастает в опухолевых клетках [1–3], поэтому действие некоторых противоопухолевых лекарственных препаратов направлено на регуляцию метаболизма азотистых оснований и их производных. К одному из типов таких препаратов относят лекарства, основанные на ингибировании фермента UPh. Эти лекарства регулируют метаболизм азотистых оснований, а именно уридина и тимидина, в ре-синтезе которых принимает участие UPh.
В настоящее время активно изучается энзиматическая специфичность UPh, разрабатываются обратимые конкурентные ингибиторы, снижение концентрации которых приводит к восстановлению активности UPh. Изучены и описаны структуры белка и его комплексов из разных организмов с разнообразными лигандами с разрешением до 1.2 Å [4–13].
Для разработки новых лекарственных препаратов – ингибиторов UPh – необходимо понимание механизмов функционирования белка, чему способствует более точное исследование структуры белка и его комплексов методом рентгеноструктурного анализа (РСА). Как показывает практика авторов работы, анализ структур атомного и субатомного разрешения позволяет выявить не только структурные особенности белка и его комплексов, но и с помощью анализа альтернативных конформаций, анизотропных температурных факторов и системы протонирования активного центра приблизиться к экспериментальному определению механизма функционирования фермента как биологической машины [6, 10, 11].
Одним из перспективных методов кристаллизации макромолекул является кристаллизация в условиях микрогравитации. Согласно [14–16] кристаллы, выращенные в невесомости, имеют более упорядоченную внутреннюю структуру, более низкую степень двойникования и лучшую рассеивающую способность по сравнению с кристаллами, выращенными в наземных условиях.
В работе представлены результаты РСА кристаллов уридинфосфорилазы из Vibrio cholerae (VchUPh), выращенных в условиях микрогравитации на Международной космической станции (МКС). Приведен анализ обнаруженных альтернативных конформаций протяженных элементов (β-стрендов и петель) третичной структуры белка при отсутствии связанных специфических лигандов. Подобные альтернативные конформации в структурах UPh атомного разрешения наблюдались лишь в ее комплексах с функционально значимыми лигандами, имеющими неполную заселенность [6, 10, 11].
МАТЕРИАЛЫ И МЕТОДЫ
Выделение и очистка VchUPh. Очистку препарата VchUPh проводили методом двухэтапной ионообменной хроматографии с использованием наполнителя Бутил-сефароза на первом этапе и Q-сефароза (Amersham Pharmacia Biotech) – на втором. По результатам SDS-гель-электрофореза гомогенность препарата VchUPh составляла 96%. Методика наработки биомассы продуцента, выделения и очистки VchUPh описана в [8].
Кристаллизация. В [8, 10] описана кристаллизация белка методом диффузии в парах при концентрации белка 15 мг/мл (в 0.1 M Трис-HCl), состав противораствора: 0.2 M МgCl2 ⋅ 6H2O, 15% (w/v) полиэтиленгликоля (ПЭГ) 4000, 0.1 M Трис-HCl, pH 8.5.
Для эксперимента в условиях микрогравитации условия кристаллизации методом диффузии в парах первоначально были адаптированы к методу встречной диффузии в капиллярах. В качестве начальных взяты известные условия кристаллизации, варьировались лишь концентрация хлорида магния от 0.1 до 0.4 М и концентрация ПЭГ 4000 от 15 до 25% с шагом 2%. При кристаллизации использовали метод встречной диффузии в капиллярах [17]. Кристаллизацию проводили на МКС. Параллельно в лаборатории проходил наземный контрольный эксперимент с идентичными кристаллизационными условиями. В контрольном эксперименте пригодные для РСА кристаллы выросли в течение двух недель. Для сбора рентгенодифракционных данных использовали кристаллы, выращенные в условиях микрогравитации в 0.3 M MgCl2 ⋅ 6H2O, 19% (w/v) ПЭГ 4000, 0.1 M Трис-HCl, pH 8.5 при температуре 293 K (рис. 1).
Сбор и обработка данных. Дифракционные данные с кристалла VchUPh получены при температуре 100 K на станции BL41XU синхротрона SPring-8 (Хёго, Япония). В качестве криопротектанта использовали раствор, содержащий 20% глицерина и все компоненты кристаллизационного раствора. С помощью программ комплекса XDS [18] проведена обработка экспериментального набора интенсивностей отражений. Шкалирование интенсивностей и расчет модулей структурных факторов проведены в программе SCALA [19]. Параметры съемки и итоговая статистика дифракционных данных приведены в табл. 1.
Таблица 1.
Характеристики получения экспериментального набора интенсивностей, обработки данных, решения и уточнения структуры
| Характеристика набора данных | |
| Длина волны, Å | 0.7 |
| Детектор | EIGER 16M |
| Расстояние от кристалла до детектора, мм | 190 |
| Угол осцилляции, град | 0.1 |
| Пр. гр. | P21 |
| a, b, c, Å | 93.186, 97.061, 93.227 |
| α = γ; β, град | 90.00; 119.965 |
| Разрешение, Å | 46.59–1.04 (1.08–1.04)* |
| Полное число отражений | 2 680 710 (268 036)* |
| Число независимых отражений | 682 103 (67 467)* |
| Полнота набора, % | 99.15 (98.57)* |
| Повторяемость | 3.9 (4.0)* |
| Среднее значение 〈I/σ(I)〉 | 12.64 (1.56)* |
| Общий температурный фактор Вильсона, Å2 | 10.16 |
| Rmerge, % | 5.56 (82.41)* |
| Rmeas, % | 6.41 (94.98)* |
| Rpim, % | 3.16 (46.72)* |
| CC1/2, % | 99.8 (63.6)* |
| Уточнение структуры | |
| Срезка набора, min(σ(|F |)/|F |) | 2.0 |
| Число рефлексов в рабочем наборе | 679 672 (67 460)* |
| Число рефлексов в тестовом наборе | 33 812 (3492)* |
| Rwork, % | 12.56 (23.27)* |
| Rfree, % | 14.20 (24.36)* |
| Cruickshank DPI, Å | 0.029 |
| Число уточняемых неводородных атомов | |
| Белка | 12 501 |
| Лигандов | 105 |
| Воды | 1688 |
| R.m.s.d. от “идеальной” геометрии | |
| по длинам валентных связей, Å | 0.007 |
| по валентным углам, град | 0.96 |
| Среднее значение B-фактора для всех атомов, Å2 | 16.27 |
| Макромолекулы | 14.39 |
| Лигандов | 32.47 |
| Воды | 29.23 |
| Статистика Рамачандрана | |
| Число а.о. в наиболее благоприятных областях, % | 98.79 |
| Число а.о. в разрешенных областях, % | 0.81 |
| Число а.о. в неблагоприятных областях, % | 0.4 |
| Число редко встречающихся ротамеров, % | 0.73 |
| ID PDB | 6Z9Z |
Решение и уточнение структуры. Структура решена методом молекулярного замещения по программе Molrep [20]. В качестве стартовой модели использована структура VchUPh (ID PDB: 6EYP). Структура уточнена при помощи программы phenix.refine [21] в сочетании с ручной коррекцией в программе Coot [22]. В структуре локализованы связанные с белком неспецифические лиганды: глицерин, 1,2-этандиол, диэтиленгликоль, ионы магния, натрия. Температурные факторы атомов рассчитывали в анизотропном приближении. На последних этапах уточнения к модели добавлены атомы водорода. Корректность результатов уточнения структуры оценивали в программах ProСheck [23], MolProbity [24] и PDB Validation Server (https://validate-rcsb.wwpdb.org). Основные значения параметров уточнения структуры приведены в табл. 1. Структура комплекса депонирована в RCSB PDB (ID PDB: 6Z9Z).
Молекулярное моделирование методом классической молекулярной динамики (МД). Для определения наиболее вероятных конформаций участков основной цепи, формирующих активный центр молекулы, и оценки стабильности связывания фермента с молекулой глицерина проводили МД-моделирование в пакете программ GROMACS (версия 2018.8) [25] с использованием набора полноатомных силовых полей CHARMM [26] версии C36m [27]. Обработку моделей лигандов осуществляли с помощью WEB-сервиса CGenFF [28]. Молекулы воды описывали трехцентровой моделью TIP3P. К системе были добавлены ионы магния и хлора в концентрации, соответствующей 0.3 M MgCl2. Расчет дальних электростатических взаимодействий проводили методом частица–сетка, используя функцию кубической интерполяции. Для описания ван-дер-ваальсовых взаимодействий использовали функцию сглаживания “force-switch” в интервале 10–12 Å. Давление в системе контролировали с помощью баростата Паринелло–Рахмана [29] на уровне 1 бар. Температура МД-системы поддерживалась постоянной с помощью термостата шкалирования скоростей частиц (V-rescale [30]) на уровне 293 K, что соответствовало температуре роста кристаллов. Длину траектории МД задавали равной 100 нс. Для интегрирования с шагом 2 фс уравнений движения Ньютона использовали алгоритм с перескоками. Всего было получено четыре траектории димера СD: две траектории А-конформера с молекулой глицерина и без нее и две траектории В-конформера также с молекулой глицерина и без нее.
Определение относительной аффинности связывания глицерина с активным центром VchUPh методом расчета линейной энергии взаимодействия (LIE, [31]) осуществляли в программе gmx_lie программного пакета GROMACS. Траектории МД-симуляции белок–лиганд вновь обрабатывали, используя метод поля реакции при отсечке 15 Å для расчета потенциальной энергии, кулоновского взаимодействия лиганда с окружением. Новую обработку траекторий осуществляли в пределах времени, в течение которого глицерин не покидал область активного центра UPh (4.2 нс для альтернативной A-конформации и 1 нс для B-конформации).
Для дальнейшего исследования результатов молекулярного моделирования использовали метод марковских состояний [32] с помощью программного комплекса PyEmma [33]. Для первоначального понижения размерности данных до набора переменных, определяющего конформационные свойства полипептидной цепи, использовали значения синуса и косинуса двугранных углов основной цепи D VchUPh для участков аминокислотных остатков (а.о.) 90–107, 144–153, 215–226. Для дальнейшего понижения размерности конформационного пространства использовали метод анализа независимых компонентов с запаздыванием по времени [34]. На этом этапе корреляционные функции рассчитывали таким образом, чтобы коэффициенты автокорреляции были максимальными, а корреляции между различными переменными были равны нулю, что позволило дополнительно понизить размерность путем преобразования к так называемым “независимым координатам”. Выбор времени запаздывания основывался на знании аналогичных времен, типичных для схожих конформационных изменений в других белках [35], поэтому дальнейшее “подстраивание” проводили после анализа предполагаемых временных интервалов переходов между основными состояниями полученной марковской модели [36]. Для рассматриваемых участков молекулы (а.о. 90–107, 144–153, 215–226) устанавливали времена запаздываний 3, 4 и 3 нс соответственно.
Перед построением марковской модели проводили дискретизацию траекторий при помощи алгоритма кластеризации k-средних. Число кластеров, равное тридцати для всех трех рассматриваемых участков полипептидной цепи, подбиралось с помощью эвристического метода, описанного в документации PyEmma на основе функции оценки VAMP-2 Score [37]. На основе проведенной кластеризации построена марковская модель, а именно: осуществлен подсчет количества переходов из одного состояния в другое, построена матрица переходов, вычислены ее собственные значения и собственные векторы. Проекции центроидов кластеров, полученных на этапе дискретизации, на собственные векторы с наибольшими собственными значениями определяли положение основных состояний.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Кристаллы VchUPh и данные их рентгеноструктурного анализа. В условиях микрогравитации на МКС выращены высокосовершенные кристаллы уридинфосфорилазы из патогенной бактерии Vibrio cholerae. Определена пространственная структура VchUPh с рекордно высоким разрешением – 1.04 Å.
Пространственная организация структуры фермента VchUPh аналогична рассмотренным ранее структурам VchUPh [6, 8–10]. Каждая субъединица молекулы VchUPh, представляющей собой тороидальный гомогексамер диаметром ~106 Å, включает в себя 253 а.о. (молекулярная масса = 27.5 кДа). По данным программы DSSP [38] вторичная структура мономера представлена восемью β-стрендами (28% а.о.) и восемью α-спиралями (32% а.о.). В межмономерной области каждого гомодимера гексамерной молекулы локализован ион Na+, координирующий три пары одноименных а.о. смежных субъединиц гомодимера. В каждом димере находится по два идентичных активных центра фермента, образованных а.о. соседних субъединиц гомодимера.
Активный центр VchUPh. Активные центры молекулы свободны от специфических лигандов, но большинство рибозосвязывающих участков нуклеозидсвязывающих сайтов, образованных а.о. Glu197, Thr93 и His7 соседней субъединицы в гомодимере [10], заняты неспецифически связанными молекулами этандиола и глицерина. Это можно объяснить схожестью химической природы многоатомных спиртов и моносахаридных остатков, являющихся альдегидо- или кето-спиртами. В большинстве активных центров молекулы глицерина связаны водородными связями лишь с одним аминокислотным остатком рибозосвязывающего сайта (Glu197 или His7).
В ранее решенной с разрешением 1.22 Å структуре нелигандированной VchUPh – 6EYP – в большинстве активных центров глицерин находится в двойном положении: один из конформеров связан водородными связями лишь с карбоксильной группой Glu197, другой конформер связан с обоими а.о. (Glu197, His7).
В рассматриваемой структуре связанные с рибозосвязывающими участками активного центра молекулы спиртов находятся в одной конформации, но иногда с неполной заселенностью. В активном центре субъединицы D молекула глицерина связана как с имидазольной группой His7 соседней субъединицы (NE2_His7/C – 3.0 Å – O1_GOL), так и с карбоксильной группой Glu197 (OE2_Glu197/D – 2.7 Å – O3_GOL, OE1_Glu197/D – 3.3 Å – O3_GOL) (рис. 2).
Рис. 2.
Пространственная организация ферментативного центра D(C) VchUPh (ID PDB: 6Z9Z). Показан фрагмент карты электронной плотности 2Fo – Fc. Пунктиром показаны полярные контакты доноров и акцепторов водородных связей. Аминокислотные остатки углеродного остова и ход главной цепи в разных альтернативных конформациях структуры показаны разными цветами; * – а.о. C-субъединицы; L11 – петля-“шлагбаум” (а). Структура активного центра фермента (D-субъединица, A-конформация) с минимальным значением ΔGLIE относительной аффинности связывания глицерина с VchUPh (б).
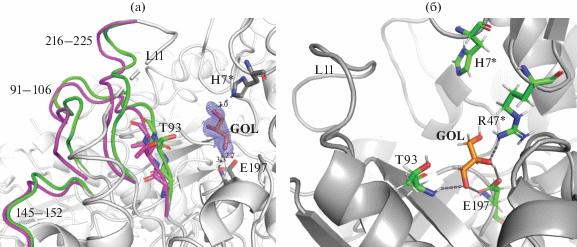
В случае связывания молекулы глицерина одновременно с His7 и Glu197 ее конформация и расположение в сайте связывания UPh похожи на конформацию части C3'–O3'–C4'–O4'–C5'–O5' рибозной компоненты субстратов, псевдосубстратов или ингибиторов UPh (уридин, тимидин, цитидин, 2,2-ангидроуридин). Но имеется и существенное отличие: Thr93, формирующий подвижную стенку активного центра [6, 10, 11], не образует водородных связей с молекулой спирта ни в одном активном центре как рассматриваемой структуры, так и 6EYP, а его боковая цепь находится на расстоянии > 4–5 Å от атомов лигандов. В отличие от глицерина субстраты и ингибиторы связываются с боковой цепью Thr93 посредством O4'-гидроксигруппы, положению которой в молекуле глицерина соответствует O2-гидроксигруппа.
Дополнительное исследование связывания молекулы глицерина в активном центре проведено методом МД. В качестве стартовых моделей для МД брали гомодимер CD в разных альтернативных положениях а.о. 91–106, образующих “стенку” активного центра D-cубъединицы. Именно в этом гомодимере разница между альтернативными конформациями наибольшая. В обоих случаях лиганд лишь небольшую часть времени траектории находился в связанном состоянии (∼4.2 нс и 1 нс для A и B-конформаций соответственно) (рис. 3).
Рис. 3.
График зависимости среднеквадратичного отклонения координат неводородных атомов глицерина в сравнении с их начальным значением от времени молекулярной динамики (первые 6 нс) в случае A-конформации фрагментов структуры VchUPh (а); B-конформации (б).
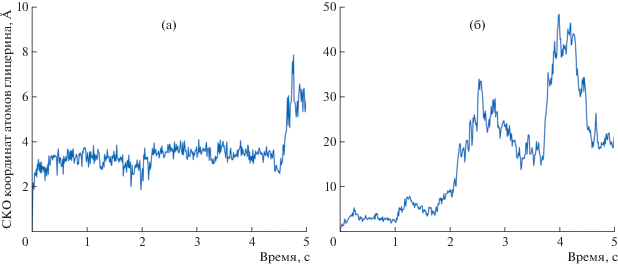
В случае A-конформации, когда фрагмент 91–106 находился ближе к лиганду (рис. 2а), связывание с активным центром было относительно стабильным в течение ∼4.2 нс (рис. 3а), и средняя оценка свободной энергии связывания составляла 〈ΔGLIE〉 = –14.4 кДж/моль. Однако в течение нескольких первых пикосекунд конформация лиганда принципиально менялась по отношению к экспериментально определенной, и минимальное значение оценки свободной энергии ($\Delta G_{{{\text{LIE}}}}^{{\min }}$ = = –38.8 кДж/моль) соответствовало этой новой конформации глицерина в сайте связывания (рис. 2б). В этой конформации лиганд не связан водородными связями с атомами боковой цепи His7/С, зато связывается с аминогруппой основной цепи Thr93/D и атомами боковой цепи Arg47/C. Arg47 входит в фосфатсвязывающий сайт активного центра, а Thr93 в β5-стренд, образующий стенку активного центра.
В случае B-конформации фрагмента 91–106, когда тот находился дальше от лиганда (рис. 2а), связывание было стабильным в течение значительно меньшего времени (∼1 нс) (рис. 3б), и средняя оценка свободной энергии выше (〈ΔGLIE〉 = = –7.9 кДж/моль) в сравнении с A-конформацией. В течение всего времени пребывания в активном центре фермента молекула глицерина не образовывала устойчивых водородных связей с Thr93, однако, так же как и для А-конформации, связывалась с Arg47/C фосфатсвязывающего сайта. Учитывая все изложенное выше, можно сделать вывод о зависимости стабильности и аффинности связывания глицерина от положения и конформации β5-стренда, образующего стенку активного центра, однако в любом случае стабильность связывания глицерина с ферментом ниже, чем у его субстратов и конкурентных ингибиторов.
Петля-“шлагбаум” L11 [10] во всех активных центрах находится в открытом положении, как и в структуре 6EYP, что логично, так как этандиол и глицерин не являются субстратами UPh, а фосфатсвязывающий сайт свободен от ортофосфат-аниона.
Анализ альтернативных конформаций функционально значимых областей VchUPh в нелигандированном состоянии. В субъединицах A, C, F боковая цепь Arg47 фосфатсвязывающего сайта находится в альтернативных конформациях. Альтернативные конформации этого а.о. наблюдались ранее [6, 10, 11] во всех структурах, где фосфатсвязывающий сайт не лигандирован ортофосфат- либо сульфат-анионом. Подвижность боковых цепей аргинина фосфатсвязывающего сайта, как было показано ранее, играет важную роль в связывании и позиционировании ортофосфат-аниона относительно молекулы нуклеозида [10].
Больший интерес вызывают альтернативные конформации пространственно близко расположенных участков 91–106, 145–152 и 216–225 а.о. D-субъединицы. В альтернативных конформациях находятся не только боковые цепи этих а.о., но и главная цепь этих фрагментов (рис. 2).
В рассмотренных прежде структурах высокого разрешения комплексов VchUPh с субстратами [10], псевдосубстратом – 6-метилурацилом [6], ингибитором – 2,2'-ангидроуридином [11] также наблюдаются двойные положения фрагментов β5- и β8-стрендов при связывании фермента с лигандом, имеющим неполную заселенность. При этом одно из двойных положений фрагментов элементов третичной структуры соответствует лигандированному состоянию, а второе – нелигандированному. Однако, во-первых, в двойной конформации находились значительно меньшие участки структуры (92–95 и 217–219 а.о. в структуре комплекса VchUPh с 2,2'-ангидроуридином [11]). Во-вторых, двойные положения наблюдались при частичной заселенности лиганда. В-третьих, а.о. одного из двойных положений фрагмента β5-стренда связывались с молекулой лиганда либо непосредственно (уридин, тимидин, 2,2'-ангидроуридин), либо через одну молекулу воды (6-метилурацил). В структуре, описываемой в данной работе, заселенность молекулы глицерина в активном центре D-субъединицы полная, и ее атомы не образуют значимых связей с атомами а.о. 92–94.
Фрагментам субъединицы D, находящимся в альтернативных конформациях, соответствуют следующие элементы вторичной структуры:
участок 91–96 β5-стренда, неупорядоченные фрагменты с поворотными элементами 97–106 и 145–149, начальный фрагмент 150–152 β7-стренда, концевой фрагмент 216–221 β8-стренда, начальный фрагмент петли-“шлагбаума” L11 (221–225).
Атомы главной цепи этих фрагментов взаимодействуют друг с другом посредством сети водородных связей (рис. 4а), и их движения в молекуле, по-видимому, согласованы. В [10] предложена схема конформационных изменений, индуцированных связанным специфическим лигандом, которые приводят к закрытию активного центра. Изменения происходят в результате согласованного сдвига β5-стренда, β8-стренда и связанной с последним петлей-“шлагбаумом” L11. Однако в рассматриваемой структуре, судя по всему, имеет место не зависимое от связывания рибозосвязываюшим сайтом специфического лиганда движение β5- и β8-стрендов. При этом не происходит полного перехода сайта связывания в закрытую конформацию, так как, во-первых, нет взаимодействия фосфатсвязывающего сайта с фосфат-анионом и, во-вторых, возможно, для фиксации закрытой конформации необходимо значимое взаимодействие молекулы нуклеозида или его аналога с атомами а.о. 93–95 β5-стренда (рибозной части с Thr93, а пиримидиновой – с основной цепью Gly95).
Рис. 4.
Сеть водородных связей между атомами главной цепи фрагментов пространственной структуры субъединицы D VchUPh в области альтернативных конформаций. Альтернативные конформации показаны разными цветами углеродного остова молекулы (а). Наложение пространственных структур фрагментов β5- и β8-стрендов нелигандированной VchUPh (ID PDB: 6Z9Z) и ее комплекса с уридином ((ID PDB: 5M2T) (б).
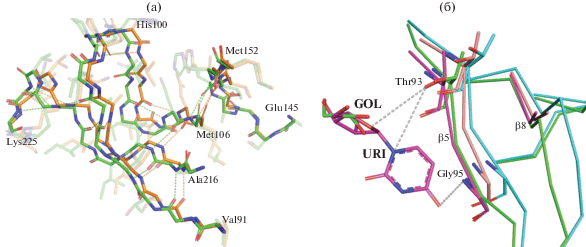
Менее вероятная гипотеза состоит в том, что в рассматриваемой структуре молекула глицерина, связываясь в рибозосвязывающем сайте, индуцирует конформационные изменения элементов структуры. Однако никаких значимых взаимодействий ни напрямую, ни через молекулы воды между атомами молекулы глицерина и атомами фрагмента 93–95 β5-стренда обнаружено не было. Кроме того, даже в случае, когда молекула глицерина связывается лишь с одним а.о. нуклеозидсвязывающего сайта (субъединица A), все равно обнаруживаются аналогичные наблюдаемым в субъединице D альтернативные конформации фрагмента β5-стренда.
Сравнение альтернативных конформаций в структурах атомного разрешения нелигандированной VchUPh и ее комплекса с уридином (ID PDB: 5M2T, 1.03 Å) выявило, что альтернативные конформации β5- и β8-стрендов в целом соответствуют наблюдаемым в рассматриваемой структуре (рис. 4б). Но атомы β5-стренда в конформации, соответствующей в структуре 5M2T закрытому состоянию активного центра, в особенности участка 93–94, находятся ближе к лиганду и противоположной стенке активного центра (рис. 4б). Это подтверждает гипотезу о том, что согласованные изменения конформации β5- и β8-стрендов возможны и без специфического связывания активного центра с субстратами или конкурентными ингибиторами, но переход в полностью закрытое состояние и его фиксация возможны лишь при связывании с атомами а.о. β5-стренда со специфическими лигандами фермента. Атомы уридина образуют в свою очередь водородные связи лишь с атомами а.о. 93–95 β5-стренда одной (более “закрытой”) конформации.
С целью доказательства или опровержения гипотезы о спонтанном, не зависимом от связывания с лигандом, переходе между конформациями рассматриваемых фрагментов структуры проведен конформационный анализ с использованием моделей марковских состояний. На рис. 5 (левый столбец) изображена карта свободной энергии кластеров конформаций фрагментов структуры в зависимости от значения первых двух (самых “медленных”) независимых компонент. Обе экспериментально определенные конформации соответствуют субминимальному значению свободной энергии, обе находятся в пределах одной потенциальной ямы, потенциальных барьеров между ними не наблюдается. При анализе основных стационарных самых «долгоживущих» состояний марковской модели выявлено, что экспериментально определенные конформации относятся к одному стационарному состоянию (рис. 5, правый столбец), однако для участка 90–107 точки находятся близко к границе другого марковского состояния. Из этих данных можно сделать вывод об относительно свободном переходе между экспериментально определенными конформациями фрагментов структуры (а.о. 91–106, 145–152 и 216–225), который не индуцируется связыванием с лигандом, а происходит самопроизвольно.
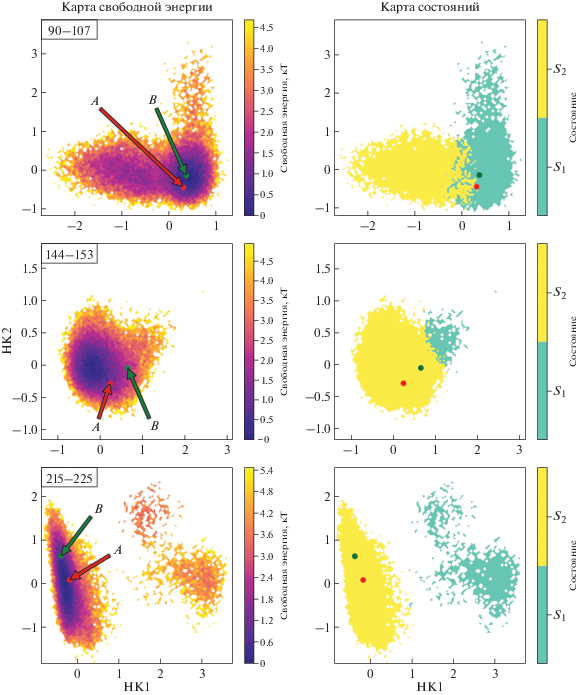
Рис. 5.
Карта свободной энергии конформаций трех фрагментов пространственной структуры VchUPh, построенная по данным марковских моделей как функция двух самых медленных независимых компонент (левый столбец). Карта самых долгоживущих метастабильных состояний (правый столбец). Конформации (A и B) фрагментов, полученные из данных рентгеноструктурного анализа, выделены стрелками.
ЗАКЛЮЧЕНИЕ
Методом встречной диффузии в капиллярах в условиях микрогравитации на МКС выращены высокосовершенные кристаллы уридинфосфорилазы из патогенной бактерии Vibrio cholerae. Определена ее пространственная структура атомного (1.04 Å) разрешения. Это рекордно высокое разрешение для данного фермента. Впервые в пространственной структуре уридинфосфорилазы в отсутствие связанных специфических лигандов обнаружены альтернативные конформации протяженных областей (β5-, β7-, β8-стрендов и смежных неупорядоченных участков) белковой молекулы. На основании анализа рентгеноструктурных данных и конформационного анализа методами молекулярной динамики и марковских моделей установлено, что согласованные изменения конформации β5-, β7- и β8-стрендов возможны и без специфического связывания аминокислотных остатков активного центра с субстратами, псевдосубстратами или конкурентными ингибиторами. Переход активного центра в полностью закрытое состояние и его фиксация возможны лишь при связывании лигандов с атомами а.о. β5-стренда со специфическими лигандами фермента.
Выявлено, что молекулы глицерина могут связываться в рибозосвязывающем участке активного центра уридинфосфорилазы в конформации, близкой к конформации фрагментов природных субстратов и ингибиторов фермента. Но аффинность и стабильность подобного связывания невелики в сравнении с субстратами и конкурентными ингибиторами и зависят, помимо всего прочего, от конформации и положения β5-стренда фермента.
Работа выполнена в рамках Федеральной космической программы 2016–2025 (МКС “Наука”) (в части кристаллизации методом встречной диффузии и сбора дифракционных данных), при финансовой поддержке Российского фонда фундаментальных исследований (проект № 19-29-12054) в части поиска условий кристаллизации, при поддержке Министерства науки и высшего образования в рамках выполнения работ по Государственному заданию ФНИЦ “Кристаллография и фотоника” РАН (в части решения, уточнения и анализа пространственной структуры, в том числе с использованием молекулярной динамики и марковских моделей). Работа выполнена с использованием инфраструктуры ЦКП “Информатика” ФИЦ ИУ РАН [39].
Список литературы
Katsumata K., Tomioka H., Sumi T. et al. // Cancer Chemother. Pharmacol. 2003. V. 51 (2). P. 155. https://doi.org/10.1007/s00280-003-0583-2
Kanzaki A., Takebayashi Y., Bando H. et al. // Int. J. Cancer. 2002. V. 97 (5). P. 631. https://doi.org/10.1002/ijc.10105
Luccioni C., Beaumatin J., Bardot V. et al. // Int. J. Cancer. 1994. V. 58 (4). P. 517. https://doi.org/10.1002/ijc.2910580411
Лашков А.А., Жухлистова Н.Е., Сотниченко С.Е. и др. // Кристаллография. 2010. Т. 55. С. 44.
Caradoc-Davies T.T., Cutfield S.M., Lamont I.L. et al. // J. Mol. Biol. 2004. V. 337. P. 337. https://doi.org/10.1016/j.jmb.2004.01.039
Прокофьев И.И., Лашков А.А., Габдулхаков А.Г. и др. // Кристаллография. 2018. Т. 63. С. 415. https://doi.org/10.7868/S0023476118030116
Lashkov A.A., Zhukhlistova N.E., Gabdoulkhakov A.G. et al. // Acta Cryst. D. 2010. V. 66. P. 51. https://doi.org/10.1107/S0907444909044175
Lashkov A.A., Gabdulkhakov A.G., Prokofev I.I. et al. // Acta Cryst. F. 2012. V. 68. P. 1394. https://doi.org/10.1107/S1744309112041401
Prokofev I.I., Lashkov A.A., Gabdulkhakov A.G. et al. // Acta Cryst. F. 2014. V. 70. P. 60. https://doi.org/10.1107/S2053230X13031877
Прокофьев И.И., Габдулхаков А.Г., Балаев В.В. и др. // Кристаллография. 2016. Т. 61. С. 919. https://doi.org/10.7868/S0023476116060138
Эйстрих-Геллер П.А., Рубинский С.В., Прокофьев И.И. и др. // Кристаллография. 2020. Т. 65. С. 271. https://doi.org/10.31857/S002347612002006X
Daa Silva Neto A.M., Torini de Souza J.R., Romanello L. et al. // Biochimie. 2016. V. 125. P. 12. https://doi.org/10.1016/j.biochi.2016.02.007
Roosild T.P., Castronovo S., Villoso A. et al. // J. Struct. Biol . 2011. V. 176. P. 229. https://doi.org/10.1016/j.jsb.2011.08.002
Куранова И.П., Ковальчук М.В. // Природа. 2014. № 3. С. 12.
Snell E.H., Helliwell J.R. // Rep. Prog. Phys. 2005. V. 68 (4). P. 799. https://doi.org/10.1088/0034-4885/68/4/r02
Бойко К.М., Тимофеев В.И., Самыгина В.Р. и др. // Кристаллография. 2016. Т. 61. С. 691.
Абрамчик Ю.А., Тимофеев В.И., Муравьева Т.И. и др. // Кристаллография. 2016. Т. 61. № 6. С. 940.
Kabsch W. // Acta Cryst. D. 2010. V. 66. P. 125. https://doi.org/10.1107/S0907444909047337
Evans P. // Acta Cryst. D. 2006. V. 62. Pt. 1. P. 72. https://doi.org/10.1107/S0907444905036693
Vagin A., Teplyakov A. // J. Appl. Cryst. 1997. V. 30 (6). P. 1022. https://doi.org/10.1107/S0021889897006766
Afonine P.V., Grosse-Kunstleve R.W., Echols N. et al. // Acta Cryst. D. 2012. V. 68. P. 352. https://doi.org/10.1107/S0907444912001308
Emsley P., Lohkamp B., Scott W.G. et al. // Acta Cryst. D. 2010. V. 66. P. 486. https://doi.org/10.1107/S0907444910007493
Laskowski R.A., MacArthur M.W., Moss D.S. et al. // J. Appl. Cryst. 1993. V. 26 (2). P. 283. https://doi.org/10.1107/S0021889892009944
Davis I.W., Leaver-Fay A., Chen V.B. et al. // Nucl. Acids Res. 2007. V. 35. P. 375. https://doi.org/10.1093/nar/gkm216
Van Der Spoel D., Lindahl E., Hess B. et al. // J. Comput. Chem. 2005. V. 26. P. 1701. https://doi.org/10.1002/jcc.20291
MacKerell A.D. // Abstracts Papers Am. Chem. Soc. 1998. V. 216. P. 696.
Huang J., Rauscher S., Nawrocki G. et al. // Nature Methods. 2016. V. 14. P. 71. https://doi.org/10.1038/nmeth.4067
Vanommeslaeghe K., Hatcher E., Acharya C. et al. // J. Comput. Chem. 2010. V. 31. P. 671. https://doi.org/10.1002/jcc.21367
Parrinello M., Rahman A. // J. Appl. Phys. 1981. V. 52. P. 7182. https://doi.org/10.1063/1.328693
Bussi G., Parrinello M. // Comput. Phys. Commun. 2008. V. 179. P. 26. https://doi.org/10.1063/1.3073889
Aqvist J., Marelius J. // Comb. Chem. High Throughput Screen. 2001. V. 4 (8). P. 613. https://doi.org/10.2174/1386207013330661
Schutte C., Fischer A., Huisinga W., Deuflhard P. // J. Comput. Phys. 1999. V. 151. P. 146. https://doi.org/10.1016/S1570-8659(03)10013-0
ehmeyer C., Scherer M.K., Hempel T. et al. // Living J. Comp. Mol. Sci. 2019. V. 1. P. 5965. 10.33011/livecoms.1.1.596
Perez-Hernandez G., Paul F., Giorgino T. et al. // J. Chem. Phys. 2013. V. 139. P. 015102. https://doi.org/10.1063/1.4811489
Husic B.E., Pande V.S. // J. Chem. Phys. 2017. V. 147. P. 176101. https://doi.org/10.1063/1.5002086
Trendelkamp-Schroer B., Wu H., Paul F., Noé F. // J. Chem. Phys. 2015. V. 143. P. 174101. https://doi.org/10.1063/1.4934536
McGibbon R.T., Pande V.S. // J. Chem. Phys. 2015. V. 142. P. 124105. https://doi.org/10.1063/1.4916292
Kabsch W., Sander C. // Biopolymers. 1983. V. 22. P. 2577. https://doi.org/10.1002/bip.360221211
Положение о ЦКП “Информатика”. http://www.frccsc.ru/ckp
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография



