Кристаллография, 2022, T. 67, № 4, стр. 571-577
Синтез и кристаллическая структура нового представителя семейства водных дифосфатов – (NH4)2[Mg3(P2O7)2(H2O)2]
А. И. Евдокимов 1, 2, *, А. М. Антипин 2, О. А. Гурбанова 1, А. С. Волков 1, О. В. Димитрова 1
1 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
2 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
* E-mail: andrewevd17@gmail.com
Поступила в редакцию 26.11.2021
После доработки 08.02.2022
Принята к публикации 08.02.2022
- EDN: BNHTXO
- DOI: 10.31857/S0023476122040075
Аннотация
Впервые методом гидротермального синтеза при T = 553 К и P = 7 МПа получены монокристаллы нового соединения (NH4)2[Mg3(P2O7)2(H2O)2], относящегося к семейству водных дифосфатов с общей формулой A2M3[P2O7]2(H2O)2, где A = K, NH4, Rb, Na, M = Mn, Fe, Co, Ni. Новое соединение имеет параметры элементарной ячейки a = 9.3047(2), b = 8.0843(2), c = 9.3655(3) Å, β =100.225(1)°. Модель кристаллической структуры определена в рамках пр. гр. P21/c с точностью до R = 0.0235. Впервые для соединений этого структурного типа получены спектры комбинационного рассеяния, подтверждены вхождение молекулы воды в структуру (NH4)2[Mg3(P2O7)2(H2O)2] и образование сложных фосфатных групп P2O7.
ВВЕДЕНИЕ
Долгое время считали, что в природе могут образовываться только ортофосфаты, однако эксперименты по синтезу полифосфатов в условиях, соответствующих природным гидротермам [1], а также открытия гипергенных минералов – канафита Na2CaP2O7 ⋅ 4H2O [2], вулдриджита Na2CaCu2(P2O7)2 ⋅ 10H2O [3], канонеровита MnNa3P3O10 ⋅ 12H2O [4] и хилброунита MgNa3P3O10 ⋅ 12H2O [5] – продемонстрировали возможность образования сложных фосфатов.
Впервые структурный тип, к которому относится новое соединение (NH4)2[Mg3(P2O7)2 (H2O)2], был описан в 1990 г. [1]. Он включает в себя дифосфаты с общей формулой A2M3[P2O7]2 (H2O)2, где A = K, NH4, Rb, Na, M = Mn, Fe, Co, Ni. Катионы М имеют октаэдрическое окружение и вместе с группировками P2O7 и молекулами воды формируют слои. Межслоевое пространство занимает щелочной катион А. Известно, что соединения этого структурного типа могут обладать функциональными свойствами. Так, в работе [6], посвященной исследованию аммоний-марганцевого члена данного семейства, показано, что при температуре выше 30 К магнитная восприимчивость соединения отвечает уравнению Кюри–Вейса с μэф = 5.74(1)μB и θ = –21.3 К, что согласуется с наличием высокоспиновых ионов Mn2+ и антиферромагнитных взаимодействий.
Таким образом, синтез, исследование строения и физических свойств новых дифосфатов представляют значительный интерес и могут помочь в изучении минералообразования фосфатов в природных гидротермальных обстановках. В настоящей работе представлены результаты синтеза и комплексных исследований нового магниевого представителя данного семейства кристаллов методами рентгеноспектрального, рентгеноструктурного анализов и спектроскопии комбинационного рассеяния света (КРС).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Новый гидратированный дифосфат магния-аммония (NH4)2[Mg3(P2O7)2(H2O)2] получен в гидротермальных условиях в системе MgCl2 : NH4 H2PO4 при массовом соотношении компонентов 1 : 1, что соответствует 1 г (10.503 ммоль) MgCl2 и 1 г (8.69 ммоль) NH4H2PO4. Эксперимент проведен в течение 14 дней в стальных автоклавах объемом 6 мл, футерованных фторопластом, при T = 553 К и P = 7 МПа, степень заполнения автоклава водой составляла 80%. После выключения печи кристаллы были промыты теплой дистиллированной водой, просушены и отобраны для дальнейших исследований с использованием бинокулярного микроскопа. Монокристаллы новой фазы представляют собой моноклинные бесцветные прозрачные призмы длиной до 0.2 мм.
Качественный химический анализ проведен с помощью электронного микроскопа Jeol JSM-6480LV, оснащенного энергодисперсионным рентгеновским спектрометром INCA Energy-350. Показано, что в состав фазы входят атомы N, Mg, P и O.
Рентгеноструктурные исследования монокристалла проведены на дифрактометре Xcalibur Eos S2 (MoKα, λ = 0.71073 Å) при комнатной температуре. Для проведения рентгенодифракционного эксперимента были отобраны монокристаллы, линейные размеры которых не превышали 0.1 мм. Образцы подвергали первичному рентгеноструктурному исследованию, в результате которого был выбран кристалл с наилучшими профилями дифракционных пиков и сходимостью интенсивностей эквивалентных по симметрии дифракционных отражений. По результатам предварительных экспериментов составлено задание для проведения полного дифракционного эксперимента. Обработка экспериментальных данных, поиск и интегрирование пиков, введение поправок на фактор Лоренца, поляризацию и поглощение (по форме образца) проведены с помощью пакета программ CrysAlisPro [7]. Модель кристаллической структуры определена и уточнена с применением метода charge flipping (переброски заряда) [8] с помощью программного комплекса Jana2006 [9]. Данные эксперимента, кристаллографические характеристики и результаты уточнения структуры представлены в табл. 1. Информация об исследованной структуре депонирована в Банк данных неорганических структур: ICSD/CCDC № 2150548.
Таблица 1.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структуры (NH4)2[Mg3(P2O7)2(H2O)2]
| Химическая формула | (NH4)2[Mg3(P2O7)2(H2O)2] |
|---|---|
| Сингония, пр. гр., Z | Моноклинная, P21/c, 2 |
| a, b, c, Å | 9.3047(2), 8.0843(2), 9.3655(3) |
| β, град | 100.225(1) |
| V, Å3 | 693.30(1) |
| D, г/см3 | 2.3611 |
| μ, мм–1 | 0.779 |
| Излучение λ, Å | MoKα, 0.71073 |
| Т, К | 295 |
| Размер образца, мм | 0.1 × 0.06 × 0.025 |
| Дифрактометр | Xcalibur Eos S2 |
| Тип сканирования | ω |
| θмин–θмакс, град | 3.35–53.6 |
| Пределы h, k, l | –21 ≤ h ≤ 21, –18 ≤ k ≤ 18, –20 ≤ l ≤ 20 |
| Число отражений: измеренных/независимых, Rint/I > 3σ(I) | 58981/2172, 0.069/1872 |
| Метод уточнения | МНК по F 2 |
| Число уточняемых параметров | 120 |
| Экстинкция, k | 0.17 (тип II, изотропная [10]) |
| R1/wR2 | 0.0235/0.0537 |
| S | 1.05 |
| Δρmin/Δρmax, э/Å3 | –0.28/0.26 |
| Программы | CrysAlisPro [7], Jana2006 [9], VESTA [11] |
Спектры КРС получены на спектрометре LabRam HR800 Evolution, оснащенном конфокальным микроскопом Olympus BX-FM. Съемку образца проводили при комнатной температуре с использованием Ar-лазера (λL = 488 нм) и дифракционной решетки с разрешением 1800 штр/мм при пятидесятикратном увеличении.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Рентгеноструктурный анализ. Структура соединения определена в рамках пр. гр. P21/c. Наиболее тяжелые атомы структуры – Mg и P – локализованы с помощью утилиты Superflip [8]. Кислородное окружение атомов магния и фосфора определено исходя из положений максимумов электронной плотности на картах разностных синтезов Фурье, расположенных на расстояниях 2.00–2.20 и 1.50–1.64 Å соответственно. При дальнейшем анализе карт разностных синтезов Фурье в полости, образованной восемью атомами кислорода, на расстоянии 3.54 Å от позиции P1 выявлен максимум электронной плотности. Положение данного пика соответствует позиции щелочного металла в структуре K2Co3[P2O7]2 (H2O)2 [1] или позиции азота в катионе ${\text{NH}}_{4}^{ + }$ в структуре (NH4)2Mn3[P2O7]2(H2O)2 [6]. Исходя из этого и данных химического анализа в настоящей работе сделано предположение, что обнаруженный максимум соответствует позиции азота в ионе ${\text{NH}}_{4}^{ + }$. Атомы водорода локализованы геометрически как вершины тетраэдра с атомом N1 в центре. Учет этих позиций привел к существенному снижению факторов расходимости и величин остаточной электронной плотности. Согласно [1, 6] в кристаллах данного структурного типа атом O2, участвующий в окружении Mg2, образует молекулу воды. В настоящей работе положения атомов водорода, участвующих в образовании молекулы воды, рассчитаны геометрически. Введение молекулы воды в модель структуры сделало итоговую формулу соединения электронейтральной – (NH4)2[Mg3(P2O7)2(H2O)2]. На заключительном этапе уточнения структурной модели введена поправка на вторичную экстинкцию согласно формализму Беккера–Коппенса [10]. Координаты базисных атомов, эквивалентные параметры атомных смещений структуры даны в табл. 2. Значения межатомных расстояний приведены в табл. 3.
Таблица 2.
Координаты атомов, значения заселенности позиций (q) и параметры атомных смещений (Uэкв) атомов в структуре (NH4)2[Mg3(P2O7)2(H2O)2]
| Атом | Позиция Уайкова |
x/a | y/b | z/c | Uэкв, Å2 |
|---|---|---|---|---|---|
| P1 | 4e | 0.208(1) | 0.436(1) | 0.261(1) | 0.008(1) |
| P2 | 4e | 0.403(1) | 0.699(1) | 0.209(2) | 0.007(1) |
| Mg2 | 4e | 0.372(1) | 0.359(1) | 0.001(1) | 0.009(1) |
| Mg1 | 2b | 0.5 | 0.5 | 0.5 | 0.009(1) |
| O1 | 4e | 0.056(1) | 0.445(1) | 0.294(1) | 0.015(1) |
| O2 | 4e | 0.767(1) | 0.518(1) | 0.164(1) | 0.018(1) |
| O3 | 4e | 0.213(1) | 0.347(1) | 0.119(1) | 0.012(1) |
| O4 | 4e | 0.322(1) | 0.376(1) | 0.388(1) | 0.012(1) |
| O5 | 4e | 0.247(1) | 0.629(1) | 0.233(1) | 0.011(1) |
| O6 | 4e | 0.461(1) | 0.577(1) | 0.110(1) | 0.010(1) |
| O7 | 4e | 0.493(1) | 0.702(1) | 0.363(1) | 0.010(1) |
| O8 | 4e | 0.371(1) | 0.866(1) | 0.139(1) | 0.011(1) |
| N1 | 4e | 0.942(1) | 0.219(1) | 0.019(1) | 0.023(1) |
| H1n1 | 4e | 0.931(1) | 0.141(1) | 0.080(1) | 0.033(1) |
| H2n1 | 4e | 1.021 | 0.275 | 0.052 | 0.027 |
| H3n1 | 4e | 0.950 | 0.176 | –0.065 | 0.027 |
| H4n1 | 4e | 0.867 | 0.284 | 0.008 | 0.027 |
| H1o2 | 4e | 0.718 | 0.467 | 0.232 | 0.045 |
| H2o2 | 4e | 0.860 | 0.540 | 0.216 | 0.036 |
Таблица 3.
Межатомные расстояния в структуре (NH4)2[Mg3(P2O7)2(H2O)2]
| Связь | Длина, Å | Связь | Длина, Å |
|---|---|---|---|
| Mg1О6-октаэдр | Mg2О6-октаэдр | ||
| Mg1–O4 | 2.055(1) × 2 | Mg2–O2 | 2.076(1) |
| Mg1–O7 | 2.072(1) × 2 | Mg2–O3 | 2.000(1) |
| Mg1–O8 | 2.199(1) × 2 | Mg2–O4 | 2.186(1) |
| 〈Mg1–O〉 | 2.109 × 2 | Mg2–O6 | 2.126(1) |
| P1О4-тетраэдр | Mg2–O6 | 2.079(1) | |
| P1–O1 | 1.502(1) | Mg2–O7 | 2.065(1) |
| P1–O3 | 1.518(1) | 〈Mg2–O〉 | 2.089 |
| P1–O4 | 1.529(1) | H2O (∠H–O–H = 104.02°) | |
| P1–O5 | 1.630(1) | O2–H1o2 | 0.945(1) |
| 〈P1–O〉 | 1.545 | O2–H2o2 | 0.934(1) |
| P2О4-тетраэдр | NH4-тетраэдр (∠N–H = 109.47°) | ||
| P2–O5 | 1.636(1) | N1–H1n1 | 0.813 |
| P2–O5 | 1.523(1) | N1–H2n1 | 0.87 |
| P2–O5 | 1.528(1) | N1–H3n1 | 0.87 |
| P2–O5 | 1.511(1) | N1–H4n1 | 0.87 |
| 〈P2–O〉 | 1.545 | 〈N1–H〉 | 0.856 |
Новое соединение (NH4)2[Mg3(P2O7)2(H2O)2] является членом семейства дифосфатов с общей формулой A2M3[P2O7]2(H2O)2, где A = K, NH4, Rb, Na, M = Mn, Fe, Co, Ni, Mg. В [12] представлена зависимость изменения параметров a и b от типа катиона в позициях А и М. Параметр а элементарной ячейки зависит от сорта одновалентного катиона, занимающего межслоевое пространство. Для соединений с аммонием характерен больший параметр а, для соединений с калием – меньший. Кроме того, прослеживается зависимость параметра b элементарной ячейки от величины ионного радиуса катиона М. С увеличением ионного радиуса в ряду Ni2+–Mg2+–Co2+–Fe2+–Mn2+ увеличивается параметр b в структурах от 7.98 Å в дифосфатах никеля до 8.36 Å в дифосфатах марганца. Таким образом, новый магниевый дифосфат, изученный в настоящей работе, хорошо укладывается в эту закономерность (табл. 4).
Таблица 4.
Кристаллографические характеристики соединений A2M3 [P2O7]2(H2O)2
| Соединение | a, b, c, Å; β, град | 〈M–O〉, Å | rM/rA, Å | Ссылка |
|---|---|---|---|---|
| (NH4)2[Ni3(P2O7)2(H2O)2] | 9.408(7), 7.985(9), 9.235(3); 100.26(1) |
2.064 | 0.69/1.55 | [13] |
| (NH4)2[Mg3(P2O7)2(H2O)2] | 9.304(7), 8.084(3), 9.365(5); 100.22(5) |
2.099 | 0.72/1.55 | Настоящая работа |
| K2[Co3(P2O7)2(H2O)2] | 9.122(4), 8.110(1), | 2.110 | 0.74/1.51 | [1] |
| 9.229(2); 99.31(4) | ||||
| K2Fe3(P2O7)2(H2O)2 | 9.152(2), 8.174(2), 9.315(2); 98.86(3) |
2.140 | 0.78/1.51 | [14] |
| (NH4)2Fe3(P2O7)2(H2O)2 | 9.413(1), 8.194(1), | 2.147 | 0.78/1.55 | [15] |
| 9.399(1); 99.65(1) | ||||
| (NH4)2[Mn3(P2O7)2(H2O)2] | 9.477(1), 8.356(6), 9.461(1); 99.91(9) |
2.194 | 0.83/1.55 | [6] |
| Rb2[Mn3(P2O7)2(H2O)2] | 9.374(1), 8.367(1), 9.437(1); 99.12(1) |
2.193 | 0.83/1.61 | [16] |
Примечание. Оригинальные данные [1] преобразованы в соответствии со стандартной установкой пр. гр. P21/c, Z = 2.
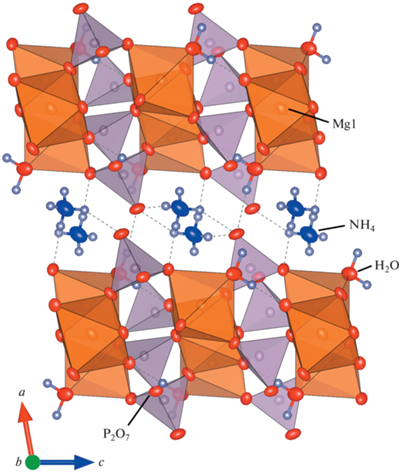
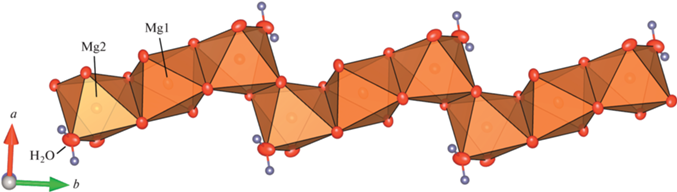
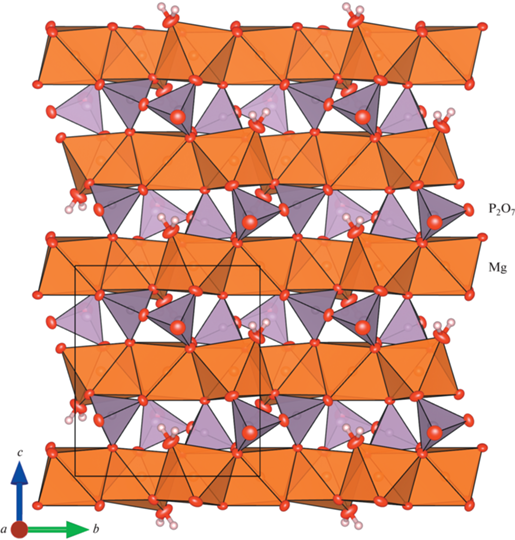
Модель кристаллической структуры дифосфата магния состоит из слоев [Mg3(P2O7)2(H2O)2]2–, параллельных плоскости bc, и катионов ${\text{NH}}_{4}^{ + }$, занимающих полости межслоевого пространства. Отметим, что в [1] выбрана нестандартная установка P21/a, что приводит к несоответствию ориентации слоев относительно осей a, b, c в настоящей работе и в [1]. Слои сложены направленными вдоль оси b зигзагообразными цепочками, состоящими из MgO6-октаэдров двух типов. Атом Mg1 расположен в центре инверсии, а Mg2 – в общей позиции. Кислородные октаэдры Mg2O6 более искаженные (рис. 2, табл. 3). Октаэдры двух типов соединяются друг с другом по ребрам (рис. 2), а сами цепочки соединяются по вершинам с диортогруппами P2O7, в которой фосфор занимает две разные общие позиции (рис. 3). Атомы водорода, входящие в катион ${\text{NH}}_{4}^{ + }$, образуют водородные связи с атомами кислорода – вершинами фосфорных тетраэдров, а также с атомами кислорода, соединяющими полиэдры MgO6 и PO4 (рис. 1). Атомы водорода молекулы воды связаны со “свободными” вершинами PO4-тетраэдров и с общими вершинами MgО6-октаэдров и PO4-тетраэдров. Таким образом осуществляется связывание слоев.
Рис. 3.
Слой [Mg3(P2O7)2(H2O)2]2– с диортогруппами P2O7 и зигзагообразными цепочками из MgO6 в проекции bc.
Спектроскопия комбинационного рассеяния света. Для нового соединения (NH4)2[Mg3(P2O7)2 (H2O)2] в пределах волновых чисел от 0 до 4000 см–1 получен спектр КРС (рис. 4). Обработка экспериментального спектра проведена по программе Spectragryph [17]. В литературе не обнаружено спектров КРС, относящихся к данному структурному типу. В связи с этим интерпретация пиков возможна только на основе данных рентгенодифракционных экспериментов и спектров КРС других дифосфатов. Наиболее интенсивные пики находятся в диапазоне частоты сдвига КРС 720–820 см–1 (табл. 5). Линии 734 и 758 см–1 относятся соответственно к асимметричным (νas) и симметричным (νs) растяжениям мостиковых связей P–O–P [18, 19]. Пики, лежащие в интервале до 350 см–1, скорее всего связаны с внешними, торсионными и деформационными колебаниями [19], а пик при 3722 см–1 связан с колебаниями связи O–H в молекулах воды [20, 21].
Рис. 4.
Спектр КРС (NH4)2[Mg3(P2O7)2(H2O)2. На вставке – увеличенная область, выделенная прямоугольником.
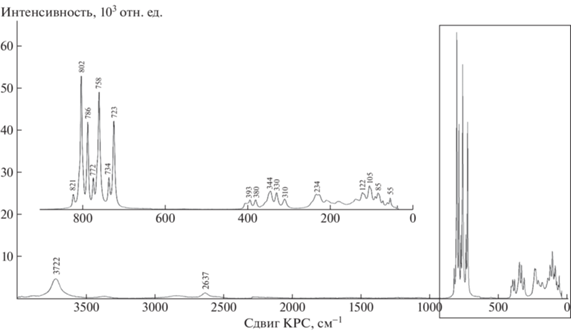
Таблица 5.
Частота сдвига и интенсивность спиральных линий (NH4)2[Mg3(P2O7)2(H2O)2] по результатам спектроскопии комбинационного рассеяния света
| Сдвиг КРС, см–1 | Интенсивность | Отнесение |
|---|---|---|
| 55 | Очень слабый | τ-колебания, внешние колебания |
| 85 | Очень слабый | |
| 105 | Средний | |
| 122 | Слабый | |
| 234 | Слабый | |
| 310 | Очень слабый | |
| 330 | Слабый | δ POP |
| 344 | Слабый | |
| 380 | Очень слабый | ρ POP |
| 393 | Очень слабый | |
| 723 | Очень сильный | |
| 734 | Сильный | νas POP |
| 758 | Очень сильный | νs POP |
| 772 | Сильный | |
| 786 | Очень сильный | |
| 802 | Очень сильный | |
| 821 | Слабый | |
| 2637 | Слабый | ν NH4 |
| 3722 | Слабый | ν H2O |
Таким образом, в работе впервые синтезировано новое магниевое соединение из группы A2M3[P2O7]2(H2O)2, изучены его химический состав и структура. Показано, что модель кристаллической структуры состоит из слоев, сложенных октаэдрами MgO6 и группировками P2O7 и разделенных крупными катионами ${\text{NH}}_{4}^{ + }$. Впервые методом спектроскопии КРС получены данные о соединении структурного семейства, к которому относится новая фаза (NH4)2[Mg3(P2O7)2(H2O)2], подтверждающие вхождение молекулы воды в структуру, а также наличие группировки P2O7. В дальнейшем представляет интерес продолжить изучение фазообразования полимеризованных фосфатов в различных системах.
Рентгеноструктурные исследования выполнены с использованием оборудования ЦКП ФНИЦ “Кристаллография и фотоника” РАН при поддержке Министерства науки и высшего образования РФ в рамках госзадания ФНИЦ “Кристаллография и фотоника” РАН.
Список литературы
Lightfoot P., Cheetham A.K., Sleight A.W. // J. Solid State Chem. 1990. V. 85 (2). P. 275.
Rouse R.C., Peacor D.R., Freed R.L. // Am. Mineral. 1988. V. 73. P. 168.
Cooper M.A., Hawthorne F.C. // Can. Mineral. 1999. V. 37. P. 73.
Popova V.I., Popov V.A., Sokolova E.V. et al. // N. Jb. Miner. Mh. 2002. V. 3. P. 117.
Elliott P., Brugger J., Caradoc-Davies T., Pring A. // Mineral. Mag. 2013. V. 77. № 3. P. 385.
Chippindale A.M., Gaslain F.O.M., Bond A.D., Powell A.V. // J. Mat. Chem. 2003. V. 13. № 8. P. 1950.
Agilent Technologies. CrysAlisPro Software System, Version 41_64.119a. Agilent Technologies Limited. Oxford. England.
Palatinus L. // Acta Cryst. A. 2004. V. 60. P. 604.
Petricek V., Dusek M., Palatinus L. // Z. Krist. 2014. B. 229. № 5. S. 345.
Becker P.J., Coppens P. // Acta Cryst. A. 1974. V. 30. P. 129.
Momma K., Izumi F. // J. Appl. Cryst. 2011. V. 44. P. 1272.
Кирюхина Г.В. Кристаллические структуры ряда синтетических аналогов минералов с амфотерными металлами: Дис. … канд. геол.-мин. наук. М.: МГУ, 2016.
Wei Y., Gies H., Tian Zh. et al. // Inorg. Chem. Commun. 2010. V. 13. P. 1357.
Yang J., Zhang X., Liu B. et al. // Acta Cryst. E. 2012. V. 68. P. 47.
Liu B., Zhang X., Wen L., Huang Y.-X. // Acta Cryst. E. 2012. V. 68. P. 5.
Кирюхина Г.В., Якубович О.В., Димитрова О.В., Волков А.С. // Кристаллография. 2016. Т. 61. № 5. С. 774.
Menges F. Spectragryph – Optical Spectroscopy Software. Version 1.2.15. 2020. http://www.effemm2.de/spectragryph
Parajón-Costa B.S., Mercader R.C., Baran E.J. // J. Phys. Chem. Solids. 2013. V. 74. № 2. P. 354.
Harcharras M., Ennaciri A., Capitelli F., Mattei G. // Vibr. Spectr. 2003. V. 33. № 1. P. 189.
Raman Data and Analysis. Raman Spectroscopy for Analysis and Monitoring. Horiba Limited. Japan.
Stefov V., Soptrajanov B., Kuzmanovski I. et al. // J. Mol. Struct. 2005. V. 752. P. 60.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография