Микробиология, 2020, T. 89, № 5, стр. 604-611
Разнообразие планктонных бактерий Дургунского и Тайширского водохранилищ (Западная Монголия)
Е. В. Кузнецова a, *, Д. Б. Косолапов a, b, Н. Л. Белькова c
a Институт биологии внутренних вод им. И.Д. Папанина РАН
152742 Некоузский район, Ярославская область, Борок, Россия
b Череповецкий государственный университет
162600 Вологодская область, Череповец, Россия
c Научный центр проблем здоровья семьи и репродукции человека
664003 Иркутск, Россия
* E-mail: elivic.rum@gmail.com
Поступила в редакцию 21.02.2020
После доработки 08.04.2020
Принята к публикации 29.05.2020
Аннотация
С помощью метода пиросеквенирования фрагмента гена 16S рРНК получены первые данные о разнообразии бактериопланктона двух крупнейших и сравнительно молодых водохранилищ Монголии – Тайширского, образованного на реке Завхан, и Дургунского, образованного на протоке Чонохарайх. Выявлено 145 филотипов (при кластерном расстоянии 0.03), принадлежащих 18 филам. Доля ОТЕ, не идентифицированных на уровне филы, варьировала в пределах 0.6–3.0%. Видовое богатство бактериопланктона, согласно индексам разнообразия ACE и CHAO1, было максимальным на эвтрофном участке протоки Чонохарайх ниже плотины Дургунской ГЭС и минимальным – на мезотрофном участке р. Завхан выше Тайширского вдхр. Согласно индексам Шеннона и Симпсона, обилие разных видов в сообществе характеризовало мезотрофный и эвтрофный участки пелагиали Тайширского и Дургунского водохранилищ, соответственно, как участки с наибольшей выравненностью. Системы водохранилищ достоверно отличались по таксономическому разнообразию бактериопланктона, о чем свидетельствует соотношение общих и уникальных ОТЕ, которое изменялось по продольному профилю водотоков.
Бактериопланктон – постоянный, многочисленный и разнообразный компонент водных экосистем. Оценка разнообразия бактериальных сообществ находится в ряду приоритетных задач микробиологии и гидробиологии (Azam et al., 1990; Kato, 1996). В основе классификации бактерий и архей лежит сходство по 16S рРНК. Микроорганизмы группируются в так называемые операционные таксономические единицы (ОТЕ), поскольку для них до сих пор отсутствует адекватное определение вида (Achtman, Wagner, 2008). Соответственно, альфа-разнообразие прокариот – это богатство их сообществ, т.е. количество ОТЕ, которые можно найти в определенном местообитании. Другой аспект разнообразия прокариот – это бета-разнообразие, т.е. различия в составе сообществ, например, между разными водными экосистемами (Limolino et al., 2006).
Представленность бактериальных таксонов в водоемах может быть различной: количество некоторых фиотипов очень велико, однако значительная часть сообществ сформирована редкими филотипами, которые мало исследованы (Pedrós-Alió, 2012). Наибольшим распространением в пресноводных экосистемах характеризуются эубактерии из филумов Proteobacteria, Actinobacteria и Bacteroidetes. Менее распространенные филотипы принадлежат, главным образом, к филумам Acidobacteria, Firmicutes, Cyanobacteria, Planctomycetes, Verrucomicrobia и Chloroflexi (Gracas et al., 2011; Lymperopoulou et al., 2012; Kaushik et al., 2014; Lliros et al., 2014). ОТЕ из этих филумов лежат в основе разнообразия сообщества водных бактерий. Однако внутри таксонов высокого ранга сосредоточено разное количество филотипов. Наиболее разнообразными в этом отношении считаются филумы Proteobacteria и Actinobacteria (Ruiz-González et al., 2015).
Для оценки разнообразия сообществ водных бактерий используются различные индексы. Среди них индекс Шеннона, который хорошо характеризует разнообразие и выравненность сообщества. Чем больше в сообществе видов и чем меньше отличается их численность, тем выше значение индекса Шеннона. При учете разнообразия эукариот этот индекс обычно варьирует в пределах от 1.5 до 3.5, очень редко превышая 4.5 (Лебедева и соавт., 2002). В результате исследования водных бактерий было установлено, что их разнообразие по индексу Шеннона варьирует в диапазоне от 2.0 до 8.0 и более. Были выявлен ряд интересных закономерностей, что пресноводный бактериопланктон обычно разнообразнее морского (Матишов и соавт., 2015; Newton et al., 2011; Fortunato et al., 2012; Eiler et al., 2014; Lee, Eom, 2016), что бактериопланктон разнообразнее бактерионейстона (Галачьянц и соавт., 2017), что в теплый период года в сообществах пресноводных бактерий выявляется больше ОТЕ, чем в холодный (Qu et al., 2018), что во влажный сезон микробное разнообразие выше, чем в сухой (Avila et al., 2017).
Существует множество методов определения состава микробных сообществ (Kolmakova et al., 2014; Boulund, 2015). К настоящему времени проведены исследования таксономического состава и разнообразия бактерий водоемов разного типа на основе различных технологий секвенирования следующего поколения, отличающихся производительностью (Logares et al., 2012; Lee, Eom, 2016). Один из них – метагеномный анализ вариабельных участков гена 16S рРНК с помощью высокопроизводительного 4, 5, 4-пиросеквенирования (Lliros et al., 2014; Yang et al., 2015; Раднагуруева и соавт., 2016; Ma et al., 2016; Галачьянц и соавт., 2017).
Изучение пространственного распределения и разнообразия водных бактерий особенно актуально при исследовании водных экосистем в засушливых регионах, к которым относится Котловина Больших озер, расположенная в Западной Монголии (Крылов и соавт., 2014). В этом регионе в первое десятилетие XXI века построены две крупнейшие в МНР ГЭС, в результате чего образованы два водохранилища – Дургунское и Тайширское.
Цель работы – изучить таксономическое разнообразие бактериопланктона Дургунского и Тайширского водохранилищ с помощью метагеномного анализа ампликонов вариабельных районов гена 16S рРНК.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Отбор проб. Пробы воды для исследования таксономического состава бактериопланктона водохранилищ и водотоков, на которых они образованы, отбирали, и их концентрацию проводили 21–25 августа 2015 г. Интегральные пробы получали, смешивая воду, отобранную с каждого метра глубины плексигласовым батометром Рутнера.
В Дургунском вдхр., длина которого составляет около 4 км, пробы отбирали в пелагиали и литорали приплотинного участка (станции Д2 и Д3 соответственно) (табл. 1), а также в прот. Чонохарайх, на которой образовано это водохранилище, примерно в 1 км выше водохранилища (ст. Д1) и в 1 км ниже плотины ГЭС (ст. Д4). В Тайширском вдхр., длина которого около 35 км, воду отбирали в пелагиали и литорали приплотинного участка (ст. Т2 и Т3), а также в р. Завхан примерно в 1 км выше водохранилища (ст. Т1) и в 1 км ниже плотины (ст. Т4). Дургунская электростанция мощностью 12 МВт построена в 2008 году на протоке Чонохарайх, соединяющей озера Хар-Ус и Хар. Высота плотины составляет 20 м, длина по гребню 252 м. Тайширская электростанция построена в 2007 году в верховьях крупнейшего водотока Западной Монголии – р. Завхан. Высота плотины 50 м, длина по гребню 190 м, мощность ГЭС – 11 МВт (Крылов и соавт., 2014).
Таблица 1.
Разнообразие бактериопланктона систем Дургунского и Тайширского водохранилищ в августе 2015 г. (кластерное расстояние 0.03)
| Станция | Общее число последователь-ностей | Число ОТЕ | Индекс разнообразия | |||
|---|---|---|---|---|---|---|
| ACE | CHAO1 | Шеннона | Симпсона | |||
| Д1 | 1050 | 64 | 86.0 | 77.2 | 3.60 | 0.79 |
| Д2 | 1143 | 85 | 92.0 | 90.6 | 5.00 | 0.94 |
| Д3 | 1490 | 89 | 97.7 | 95.6 | 4.77 | 0.92 |
| Д4 | 1472 | 91 | 119.7 | 118.1 | 4.37 | 0.88 |
| Т1 | 949 | 34 | 40.2 | 38.0 | 2.51 | 0.66 |
| Т2 | 1536 | 73 | 83.0 | 79.0 | 4.67 | 0.93 |
| Т3 | 632 | 57 | 70.7 | 66.6 | 4.30 | 0.90 |
| Т4 | 815 | 54 | 64.3 | 62.7 | 4.36 | 0.92 |
Примечание. Здесь и далее: Д1 – прот. Чонохaрайх выше Дургунского вдхр., Д2 – пелагиаль водохранилища, Д3 – литораль водохранилища, Д4 – прот. Чонохарайх ниже плотины ГЭС; Т1 – р. Завхан выше Тайширского вдхр., Т2 – пелагиаль водохранилища, Т3 – литораль водохранилища, Т4 – р. Завхан ниже плотины ГЭС.
Бактерии концентрировали на нитроцеллюлозных фильтрах SterivexTM-GS “Millipore” (США) с диаметром пор 0.22 мкм. Перед этим пробы воды подвергали префильтрации через поликарбонатные фильтры с диаметром пор 1.5 мкм. После фильтрования фильтры замораживали и хранили при –25°С.
Выделение бактериальной ДНК вели с помощью комплекта реагентов для экстракции и элюции ДНК Bacterial Genomic DNA kit (“Axygen”, США) согласно протоколу производителей. Амплификацию фрагмента гена 16S рРНК, содержащего пять вариабельных районов V4–V8, проводили на бактериальных праймерах 5'‑CCATCTCATCCCTGCGTGTCTCCGAC-TCAG- Х-CCAGCAGCYGCGGTAAN-3', где X – 10‑нуклеотидный бар-код, уникальный для каждого отдельного образца и 5'-CCTATCCCCTGTGTGCCTTGGCAGTC-TCAG-GACGGGCGGTGTGTACAAG-3'. Метагеномное секвенирование ампликонов 16S pДНК проводили на реактивах GS Junior+ и пиросеквенаторе 454 GS Junior System (“Roche”, США). Результаты анализа зарегистрированы в международной базе данных NCBI.
Биоинформационную обработку данных разнообразия и таксономического состава бактериальных сообществ проводили с использованием сервиса RDP Pipeline (https://pyro.cme.msu.edu) (Wang et al., 2007; Cole et al., 2009). Средняя длина последовательностей составила 496 нуклеотидов, химерные последовательности и последовательности короче 300 нуклеотидов были исключены из дальнейшего анализа. Выделение филотипов (операционных таксономических единиц, OTЕ) проводили при кластерном расстоянии 0.03.
Для оценки видового богатства и обилия видов были рассчитаны индексы разнообразия (ACE, CHAO1, Шеннона и Симпсона). Для определения сходства и различий между бактериальными сообществами строили диаграммы Венна, а также применяли метод главных компонент (Галачьянц и соавт., 2017).
РЕЗУЛЬТАТЫ
На исследованных участках водоемов и водотоков в период отбора проб температура воды варьировали в пределах 15.2–22.6°С, электропроводность – в пределах 265–280 мкСм/см, концентрация растворенного кислорода – в пределах 7.21–9.26 мг/л, рН – в пределах 7.22–9.01. Скорость течения воды не превышала 0.2 м/с. Общая численность бактериопланктона составляла (2.51–11.23) × × 106 кл./мл, биомасса – 50–249.3 мг С/м3. Эти показатели в обоих водохранилищах достигали уровня эвтрофных вод, но в среднем были выше в Дургунском вдхр. по сравнению с Тайширским (Косолапов, Косолапова, 2018). Трофический статус Дургунского вдхр. можно охарактеризовать как эвтрофный, а Тайширского – как мезотрофный (Крылов и соавт., 2014).
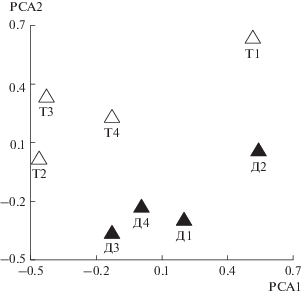
В ходе молекулярно-генетического анализа было выполнено 9087 прочтений нуклеотидных последовательностей со средней длиной 496 нуклеотидов. Количество прочтений в пробах варьировало от 632 до 1536. Всего было выделено 145 бактериальных филотипов при кластерном расстоянии 0.03, при этом число ОТЕ в каждой пробе воды изменялось от 34 до 91. Наибольшим разнообразием согласно индексам ACE и CHAO1 характеризуется бактериальное сообщество прот. Чонохорайх на участке ниже Дургунского вдхр. (ст. Д4) (табл. 1), а согласно индексам Шеннона и Симпсона – сообщество Дургунского вдхр. (ст. Д3). Наименее разнообразными по всем показателям оказались бактериальные сообщества участков водотоков, особенно р. Завхан, расположенных выше водохранилищ (ст. Д1, ст. Т1) (табл. 1). Богатство таксонов на уровне рода различалось между двумя системами водохранилищ (достоверность формирования групп по индексам АСЕ и CHAO1 оказалась равной 0.025 и 0.031 соответственно). В свою очередь, обилие таксонов различалось по типу водных масс вдоль прот. Чонохарайх и р. Завхан (достоверность формирования групп по индексам Шеннона и Симпсона составляла 0.015 и 0.009 соответственно) (рис. 1).
Рис. 1.
Применение метода главных компонент для сравнительного анализа бактериальных сообществ участков двух водных систем: прот. Чонохарайх–Дургунское вдхр. и р. Завхан–Тайширское вдхр.
В бактериальных сообществах всех участков по количеству последовательностей и филотипов преобладали пять фил: Bacteroidetes (6.2–81.2%), Actinobacteria (6.8–48.8%), Proteobacteria (8.1–39.1%), Verrucomicrobia (0.5–14.4%) и Cyanobacteria (0.1–14.7%) (табл. 2). Если в сообществе прот. Чонохорайх выше Дургунского вдхр. доминировали представители фил Actinobacteria и Proteobacteria, то в сообществе р. Завхан выше Тайширского вд-хр. – представители филы Bacteroidetes. В водохранилищах и на участках водотоков ниже плотин ГЭС доминирующие филы были представлены более выравнено.
Таблица 2.
Состав сообществ бактериопланктона водохранилищ
| Таксон | Доля (%) в сообществе | |||||||
|---|---|---|---|---|---|---|---|---|
| Д1 | Д2 | Д3 | Д4 | Т1 | Т2 | Т3 | Т4 | |
| Доминирующие филы | ||||||||
| Bacteroidetes | 6.2 | 4.7 | 8.8 | 10.4 | 81.2 | 17.8 | 15.3 | 17.8 |
| Actinobacteria | 48.8 | 21.0 | 27.9 | 33.0 | 6.8 | 26.3 | 23.6 | 30.8 |
| Proteobacteria: | 26.4 | 34.2 | 26.8 | 30.4 | 8.1 | 31.1 | 39.1 | 27.0 |
| alpha- | 10.0 | 7.9 | 13.0 | 19.9 | 0.5 | 15.2 | 28.3 | 14.8 |
| beta- | 15.0 | 21.4 | 9.1 | 7.2 | 7.4 | 10.2 | 4.9 | 6.9 |
| gamma- | 0.5 | 4.2 | 3.2 | 2.0 | 0.2 | 2.1 | 2.4 | 4.9 |
| delta- | 0.7 | 0.3 | 1.3 | 1.1 | 0 | 0.3 | 0.5 | 0 |
| Verrucomicrobia | 10.4 | 11.4 | 10.9 | 14.4 | 0.5 | 9.8 | 7.6 | 14.0 |
| Cyanobacteria | 0.4 | 5.2 | 14.7 | 3.7 | 0.1 | 5.5 | 5.1 | 0.4 |
| Минорные филы | ||||||||
| Planctomycetes | 2.0 | 1.6 | 1.7 | 1.6 | 0.2 | 3.7 | 3.8 | 2.3 |
| Cloroflexi | 0.4 | 0.5 | 0.3 | 0.4 | 0.1 | 2.0 | 2.1 | 0.7 |
| TM7 | 0.1 | 0.3 | 0.4 | 0.1 | 0.2 | 0.4 | 0.2 | 0.1 |
| OD1 | 1.2 | 0.8 | 2.6 | 1.0 | 0.2 | 0.1 | 0 | 0.1 |
| Firmicutes | 0 | 9.3 | 0.4 | 0.4 | 0 | 0.3 | 0.3 | 0.6 |
| OP3 | 1.0 | 0.6 | 0.8 | 0.8 | 0.3 | 0 | 0 | 0.1 |
| Clamydiae | 1.0 | 0.4 | 1.0 | 1.3 | 0 | 0 | 0 | 0 |
| Clorobi | 0 | 0 | 0 | 0 | 0 | 1.0 | 0.6 | 3.1 |
| GNO2 | 0.2 | 0.1 | 0.3 | 0.2 | 0 | 0 | 0 | 0.7 |
| Acidobacteria | 0 | 0.8 | 0 | 0 | 0 | 1.3 | 0.9 | 0.5 |
| ZB3 | 0 | 0 | 0 | 0.1 | 0 | 0.2 | 0 | 0 |
| Elusmicrobia | 0 | 0 | 0.1 | 0 | 0 | 0 | 0 | 0 |
| [Thermi] | 0 | 7.5 | 0 | 0 | 0 | 0 | 0 | 0 |
| Не идентифицированные на уровне филы | 1.8 | 1.5 | 3.0 | 2.0 | 2.1 | 0.6 | 1.4 | 1.7 |
Выявлено 13 минорных фил бактерий, некоторые из которых отличались низкой представленностью в сообществах всех исследуемых участков водоемов, например, фила ТМ7. Доли Planctomycetes и Chloroflexi в системе Дургунского вдхр. менее отличались по участкам отбора проб, чем в системе Тайширского вдхр., где они были на порядок меньше в речных водах по сравнению с водами водохранилища. Firmicutes и Acidobacteria отсутствовали в сообществах участков прот. Чонохарайх и р. Завхан выше плотин и появлялись в водохранилищах, особенно в их пелагиали. В литорали Дургунского вдхр. определили филу OD1, а в литорали Тайширского вдхр. она отсутствовала. ОP3, Chlamidae, GNO2 были специфичны для прот. Чонохарайх, в Дургунском вдхр. их обилие снижалось. Clorobi, напротив, была характерна для системы Тайширского вдхр. Фила [Thermi] была представлена только в пелагиали Дургунского вдхр.
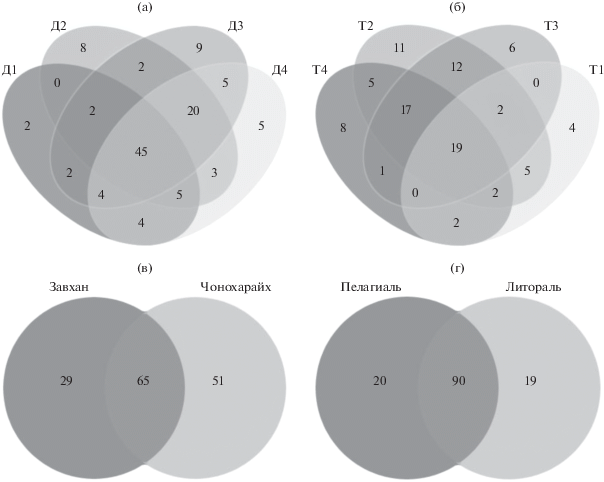
Вклад доминирующих фил в системе Дургунского вдхр. составил 76.5–92.2%, а в системе Тайширского вдхр. – 90.0–96.7%. При сравнении бактериальных сообществ между собой было выявлено, что для системы Дургунского вдхр. 45 ОТЕ являются общими (рис. 2а), а для системы Тайширского вдхр. общими являются только 19 ОТЕ (рис. 2б). Для мелководных и глубоководных участков общими оказались 90 ОТЕ (рис. 2в). Несмотря на большое количество уникальных ОТЕ, доля последовательностей, относящихся к ним, низкая. Количество уникальных филотипов в прот. Чонохарайх (51 ОТЕ) было больше, чем в р. Завхан (29 ОТЕ) (рис. 2г).
Рис. 2.
Бета-разнообразие бактериопланктона водохранилищ, охарактеризованное с помощью диаграмм Венна (кластерное расстояние 0.03): а – в системе прот. Чонохарайх–Дургунское вдхр; б – в системе р. Завхан–Тайширское вдхр.; в – между системами прот. Чонохарайх–Дургунское вдхр и р. Завхан–Тайширское вдхр.; г – между пелагиалью и литоралью водохранилищ.
Участки водотоков выше водохранилищ отличались по обилию доминирующих филотипов. Так, в бактериопланктоне прот. Чонохарайх преобладал филотип АСК-М1 (42.9%), но его доля в сообществе р. Завхан составляла только 5.3%. В Дургунском вдхр. и протоке ниже плотины доля этого таксона уменьшалась в 1.5–2 раза, а в Тайширском вдхр. – увеличивалась в 2–4 раза. Такая же закономерность наблюдалась с родом Flavobacterium, составляющим 54.3% в р. Завхан и значительно уменьшающим свою представленность в Тайширском вдхр.
Самой богатой таксонами была фила Proteobacteria (60 филотипов при кластерном расстоянии 0.03). Однако их представленность была невелика. Выделялось сем. Pelagibacteraceae, обилие которого было значительным в Дургунском и Тайширском водохранилищах, особенно в их литоральной зоне (11 и 25% соответственно).
Фила Verrucomicrobia была представлена десятью филотипами при кластерном расстоянии 0.03. Доля в сообществах некоторых из них была значительной. Так, в системе Дургунского вдхр. выделялся р. Candidatus Xiphinematobacter (2.4–4.4%). В Тайширском вдхр. обильно представленным было сем. [Cerasicoccaceae] (до 6.1%), а в реке ниже Тайширского вдхр. – сем. R4-41B (7.2%).
Из представителей минорных фил определяли филотипы Thermus и Staphylococcus (7.2 и 8.9% в Дургунском вдхр. соответственно), а также пор. Phycisphaerales (2.9–3.2% в Тайширском вдхр.).
ОБСУЖДЕНИЕ
В число абиотических факторов, контролирующих разнообразие водных бактериальных популяций, входят температура, содержание растворенных органических и неорганических веществ и соединений биогенных элементов, рН среды, концентрация растворенного кислорода (Simek et al., 2008; Lindstrom et al., 2010; Berdjeb et al., 2011; Ruiz-Gonzalez et al., 2013; Скопина и соавт., 2016). Абиотические параметры исследованных нами водных экосистем представляют собой адекватные фундаментальные ниши для выявленных ОТЕ (Jia, Whalen, 2020). В этих условиях выявленные нами виды сохраняются и поддерживают стабильные популяции. Так, значительная доля видов (39%) выявлена на всех участках системы Дургунского водохранилища. При этом еще больше видов (45%) – общие среди двух различных водных систем, отличающихся набором абиотических параметров. И, наконец, пелагиаль и литораль водохранилищ в большинстве (70%) заселена общими видами. Однако численность и биомасса бактериопланктона выше в системе Дургунского водохранилища (в пределах одного порядка), где для ряда доминирующих видов, вероятно, сложились более благоприятные условия, в том числе, и абиотические.
Оценка с помощью индексов разнообразия видового богатства и обилия видов бактериопланктона систем двух крупнейших Монгольских водохранилищ и водотоков, на которых они образованы, показала, что наиболее разнообразен по всем показателям бактериопланктон самих водохранилищ. При этом абсолютные значения индексов указывают на высокую степень разнообразия. Несмотря на то, что Дургунское и Тайширское водохранилища образованы недавно, и сообщества гидробионтов в них находятся на стадии формирования, экосистемы этих двух водоемов с замедленным водообменом резко выделяются. Особенно развиты сообщества пелагиали водохранилищ, хотя различий между глубоководными и мелководными зонами меньше, чем сходств.
В процессе исследования между бактериопланктоном Дургунского и Тайширского водохранилищ установлен ряд различий. Так, по числу ОТЕ и их представленности сообщество Дургунского вдхр. значительно превосходило соответствующие показатели Тайширского вдхр. По-видимому, это определяется тем, что прот. Чонохарайх вытекает из эвтрофного оз. Хар-Ус, которое служит основным источником формирования вод Дургунского вдхр. Видовое сходство между бактериальными сообществами р. Завхан и Тайширского вдхр. гораздо ниже, что свидетельствует о различных условиях обитания бактерий на зарегулированных и незарегулированных участках этой реки. Видовое богатство и обилие видов бактериопланктона в эвтрофном Дургунском вдхр. выше таковых в мезотрофном Тайширском вдхр.
Таксономическая структура незарегулированных участков водотоков также различается. Таксоны системы Дургунского вдхр. и системы Тайширского вдхр. образуют два кластера на диаграмме распределения видов. Сходство между участками прот. Чонохарайх, расположенными выше и ниже водохранилища, больше, чем между такими же участками р. Завхан. По-видимому, это можно объяснить различиями в формировании и морфометрии этих двух водохранилищ. Ширина приплотинной части Дургунского вдхр., расположенной в скальных породах, составляет не более 0.3 км, а ширина приплотинной части Тайширского вдхр., затопившего почвы с растительностью, существенно больше – около 2.5 км. Кроме того, площадь и водосбор Дургунского вдхр. значительно меньше таковых Тайширского вдхр.
Интересно отметить, что закономерности распределения бактериопланктона по продольному профилю водохранилищ (Simek et al., 2001; Ruiz-Gonzales et al., 2013) выявлены и при изучении разнообразия сообществ зоопланктона Дургунского и Тайширского водохранилищ. Увеличение объемов воды в водохранилищах, а также повышение процессов биологического самоочищения от верховьев к приплотинным участкам приводят к снижению значений коэффициента трофности, рассчитанного на основе показателей зоопланктона. Поступление богатых биогенными и органическими веществами вод водохранилищ на участки водотоков ниже плотин приводят к резкому увеличению коэффициента трофности (Крылов и соавт., 2014).
Структура бактериопланктона испытывает значительные сезонные изменения. Однако в конце лета в пресных водоемах Европы и Азии, так же как в Дургунском и Тайширском водохранилищах доминирующими филами являются Proteobacteria, Actinobacteria и Cyanobacteria, что свидетельствует об устойчивости экосистем этих водоемов в позднелетний период (Yang et al., 2015; Sun et al., 2017).
Многие ОТЕ на исследованных участках водохранилищ и водотоков Монголии идентифицированы только на уровне крупных таксонов. Это свидетельствует о специфичности бактериальных сообществ водных экосистем Котловины Больших озер, которые входят в Центрально-Азиатский бессточный бассейн. Имеющиеся в литературе сведения о таксономической структуре бактериопланктона водохранилищ аридной зоны ограничены, но можно утверждать, что состав и пропорции доминирующих фил сопоставимы с полученными нами данными. В трех крупнейших эвтрофных водохранилищах Китая (Шиян, Ксикенг, Луотиан) (22°24′ с.ш. и 114°08′ в.д.) зарегистрированы четыре из пяти отмеченных нами доминирующих фил (Bacteroidetes, Actinobacteria, Proteobacteria и Cyanobacteria). В этих китайских водохранилищах отсутствовала только фила Verrucomicrobia. Вместо нее идентифицированы филы Acidobacteria, Firmicutes и Planctomycetes (Li et al., 2016). Возможно, кроме географического расположения, выявленные различия объясняются различиями в возрасте водохранилищ, потому что в нашем исследовании указанные филы были характерны именно для зарегулированных участков. По-видимому, со временем в Дургунском и Тайширском водохранилищах состав бактериопланктoна и представленность в нем разных таксонов претерпят изменения.
Таким образом, установлено, что в конце лета в бактеропланктоне на зарегулированных и незарегулированных участках систем (река–водохранилище), функционирующих в условиях аридного климата, доминировали пять бактериальных фил: Bacteroidetes, Actinobacteria, Proteobacteria, Verrucomicrobia и Cyanobacteria, что характерно для большинства пресных водоемов. Подавляющее большинство в бактериальных сообществах составляли некультивируемые формы. Выявлены различия видового разнообразия бактериопланктона как между двумя водными системами, так и вдоль продольного профиля каждой системы. Микробные сообщества сходны по составу доминирующих фил, однако существенно отличаются на уровне родов по составу и представленности крупных таксонов. Сообщества водохранилищ отличаются большей устойчивостью и разнообразием, чем сообщества незарегулированных участков водотоков.
Список литературы
Галачьянц А.Д., Белькова Н.Л., Суханова Е.В., Галачьянц Ю.П., Морозов А.А., Парфенова В.В. Особенности таксономического состава бактерионейстонных сообществ озера Байкал // Микробиология. 2017. Т. 86. С. 229–238.
Galach’yants A.D., Bel’kova N.L., Sukhanova E.V., Galach’yants Y.P., Morozov A.A., Parfenova V.V. Taxonomic composition of Lake Baikal bacterioneuston communities // Microbiology (Moscow). 2017. V. 86. P. 241–249.
Косолапов Д.Б., Косолапова Н.Г. Пико- и нанопланктон водных экосистем Долины Озер и Котловины Больших Озер (Монголия) // Биол. внутр. вод. 2018. № 3. С. 36–44. https://doi.org/10.1134/S0320965218030099
Kosolapov D.B., Kosolapova N.G. Pico- and nanoplankton in aquatic ecosystems in the Valley of the Lakes and Great Lakes Depression (Mongolia) // Inland Water Biol. 2018. V. 11. P. 269–277. https://doi.org/10.1134/S1995082918030094
Крылов A.В., Солонго Д., Мэндсайхан Б. Зоопланктон Дургунского и Тайширского водохранилищ (Западная Монголия) в конце периода наполнения // Аридные экосистемы. 2014. Т. 20. № 2(59). С. 48–55.
Krylov A.V., Solongo D., Mendsaikhan B. Zooplankton of the Durgun and the Taishir reservoirs (Western Mongolia) by the end of impoundment period // Arid Ecosystems. 2014. V. 4. № 2. P. 85–90.
Лебедева Н.В., Криволуцкий Д.А., Пузаченко Ю.Г., Дьяконов К.Н., Алещенко Г.Н., Смурнов А.В., Максимов В.Н., Тикунов В.С., Огуреева Г.Н., Котова Т.В. География и мониторинг биоразнообразия. М.: Издательство научного и учебно-методического центра, 2002. 432 с.
Матишов Д.Г., Стахеев В.В., Чирак Е.Л., Глущенко Г.Ю. Метагеномный анализ структуры бактериального сообщества Азовского моря // Океанология. 2015. Т. 55. С. 770–775.
Matishov D.G., Stakheev V.V., Glushchenko G.Y., Chirak E.L. Metagenomic analysis of the bacterial community of the Sea of Azov // Oceanology. 2015. V. 55. P. 696–700.
Раднагуруева А.А., Лаврентьева Е.В., Будагаева В.Г., Бархутова Д.Д., Дунаевский Я.Е., Намсараев Б.Б. Органотрофные бактерии горячих источников Байкальской рифтовой зоны // Микробиология. 2016. Т. 85. С. 347–360.
Radnagurueva A.A., Lavrentieva E.V., Budagaeva V.G., Barkhutova D.D., Namsaraev B.B., Dunaevsky Y.E. Organotrophic bacteria of the Baikal Rift Zone hot springs // Microbiology (Moscow). 2016. V. 85. P. 367–378.
Скопина М.Ю., Васильева А.А., Першина Е.В., Пиневич А.В. Разнообразие малочисленности: феномен “разреженной бактериальной биосферы” // Микробиология. 2016. Т. 85. С. 248–260.
Skopina M.Y., Pinevich A.V., Vasileva A.A., Pershina E.V. Diversity at low abundance: The phenomenon of the rare bacterial biosphere // Microbiology (Moscow). 2016. V. 85. P. 272–282.
Achtman M., Wagner M. Microbial diversity and the genetic nature of microbial species // Nat. Rev. Microbiol. 2008. V. 6. P. 431–440.
Avila M.P., Staehr P.A., Barbosa F.A.R., Chartone-Souza E., Nascimento A.M.A. Seasonality of freshwater bacterioplankton diversity in two tropical shallow lakes from the Brazilian Atlantic Forest // FEMS Microbiol. Ecol. 2017. V. 93. Art. fiw218.
Azam F., Cho B.C., Smith D.C., Simon M. Bacterial cycling of matter in the pelagic zone of aquatic ecosystems // Large Lakes – Ecological Structure and Function / Eds. Tilzer M.M., Ser-ruya C. Berlin: Springer-Verlag, 1990. P. 477–488.
Berdjeb L., Ghiglione J.F., Domaizon I., Jacquet S. A 2-year assessment of the main environmental factors driving the free-living bacterial community structure in Lake Bourget (France) // Microb. Ecol. 2011. V. 61. P. 941–954.
Boulund F. Computational methods for analysis of fragmented sequence data. Göteborg, 2015. 68 p.
Cole J.R., Wang Q., Cardenas E., Fish J., Chai B., Farris R.J., Kulam-Syed-Mohideen A.S., McGarrell D.M., Marsh T., Garrity G.M., Tiedje J.M. The Ribosomal Database Project: improved alignments and new tools for rRNA analysis // Nucleic Acids Res. 2009. V. 37. P. 141–145.
Eiler A., Zaremba-Niedzwiedzka K., Martinez-Garcia M., McMahon K.D., Stepanauskas R., Andersson S.G., Bertilsson S. Productivity and salinity structuring of the microplankton revealed by comparative freshwater metagenomics // Environ. Microbiol. 2014. V. 16. P. 2682–2698.
Fortunato C.S., Herfort L., Zuber P., Baptista A.M., Crump B.C. Spatial variability overwhelms seasonal patterns in bacterioplankton communities across a river to ocean gradient // ISME J. 2012. V. 6. P. 554–563.
Gracas D.A., Miranda P.R., Barauna R.A., McCulloch J.A., Jr. R.G., C. Schneider M.P., Silva A. Microbial diversity of an anoxic zone of a hydroelectric power station reservoir in Brazilian Amazonia // Microb. Ecol. 2011. V. 62. P. 853–861.
Jia Y., Whalen J.K. A new perspective on functional redundancy and phylogenetic niche conservatism in soil microbial communities // Pedosphere. 2020. V. 30. P. 18–24.
Kato K. Bacteria – a link among ecosystem constituents // Res. Popul. Ecol. 1996. V. 38. P. 185–190.
Kaushik R., Balasubramanian R., Dunstan H. Microbial quality and phylogenetic diversity of fresh rainwater and tropical freshwater reservoir // PLoS ONE. 2014. V. 9. Art. e100737.
Kolmakova O.V., Gladyshev M.I., Trusova M.Y., Rozanov A.S., Peltek S.E. Spatial biodiversity of bacteria along the largest Arctic river determined by next generating sequencing // FEMS Microbiol. Ecol. 2014. V. 89. P. 442–450.
Lee S.-Y., Eom Y.-B. Analysis of microbial composition associated with freshwater and seawater // Biomed. Sci. Lett. 2016. V. 22. P. 150–159.
Li J., Chen C., Lu J., Lei A., Hu Z. Temporal patterns in bacterioplankton community composition in three reservoirs of similar trophic status in Shenzhen, China // Int. J. Environ. Res. Public Health. 2016. V. 13. Pii. E599. https://doi.org/10.3390/ijerph13060599
Limolino M.V., Riddle B.R., Brown J.H. Biogeography. 3d edn. Sunderland, MA: Sinauer Associates, Inc., 2006.
Lindstrom E.S., Feng X.M., Graneli W., Kritzberg E.S. The interplay between bacterial community composition and the environment determining function of inland water bacteria // Limnol. Oceanogr. 2010. V. 55. P. 2052–2060.
Lliros M., Inceoglu O., Garcıa-Armisen T., Anzil A., Leporcq B., Pigneur L.-M., Viroux L., Darchambeau F., Descy J.-P., Servais P. Bacterial community composition in three freshwater reservoirs of different alkalinity and trophic status // PLoS One. 2014. V. 9. Art. e116145. https://doi.org/10.1371/journal.pone.0116145
Logares R., Haverkamp T.H.A., Kumar S., Lanzén A., Nederbragt A.J., Quince C., Kauserud H. Environmental microbiology through the lens of high-throughput DNA sequencing: synopsis of current platforms and bioinformatics approaches // J. Microbiol. Meth. 2012. V. 91. P. 106–113.
Lymperopoulou D.S., Kormas K.A., Karagouni A.D. Variability of prokaryotic community structure in a drinking water Reservoir (Marathonas, Greece) // Microbes Environ. 2012. V. 27. P. 1–8.
Ma L., Mao G., Liu J., Gao G., Zou C., Bartlam MG., Wang Y. Spatial-temporal changes of bacterioplankton community along an exhorheic river // Front. Microbiol. 2016. V. 7. Art. 250. https://doi.org/10.3389/fmicb.2016.00250
Newton R.J., Jones S.E., Eiler A., McMahon K.D., Bertilsson S. A guide to the natural history of freshwater lake bacteria // Microbiol. Mol. Biol. Rev. 2011. V. 75. P. 14–49.
Pedrós-Alió C. The rare bacterial biosphere // Annu Rev. Mar. Sci. 2012. V. 4. P. 449–466.
Qu J., Jia C., Liu Q., Li Z., Liu P., Yang M., Zhao M., Li W., Zhu H., Zhang Q. Dynamics of bacterial community diversity and structure in the terminal reservoir of the South-to-North water diversion project in China // Water. 2018. V. 10. Art. 709.
Ruiz-Gonzalez C., Proia L., Ferrera I., Gasol J.M., Sabater S. Effects of large river dam-regulation on bacterioplankton community structure // FEMS Microb. Ecol. 2013. V. 84. P. 316–331.
Ruiz-Gonzalez C., Salazar G., Logares R., Proia L., Gasol J.M., Sabater S. Weak coherence in abundance patterns between bacterial classes and their constituent OTUs along a regulated river // Front. Microbiol. 2015. V. 6. Art. 1293.
Simek K., Armengol J., Comerma M., Garcia J.C., Kojecka P., Nedoma J., Hejzlar J. Changes in the epilimnetic bacterial community composition, production, and protist-induced mortality along the longitudinal axis of a highly eutrophic reservoir // Microb. Ecol. 2001. V. 42. P. 359–371.
Simek K., Hornak K., Jezbera J., Nedoma J., Znachor P. Spatio-temporal patterns of bacterioplankton production and community composition related to phytoplankton composition and protistan bacterivory in a dam reservoir // Aquat. Microb. Ecol. 2008. V. 51. P. 249–262.
Sun W., Xia C., Xu M., Guo J., Sun G. Seasonality affects the diversity and composition of bacterioplankton communities in Dongjiang river, a drinking water source of Hong Kong // Front. Microbiol. 2017. V. 8. Art. 1644.
Wang Q., Garrity G.M., Tiedje J.M., Cole J.R., Bayesian N. Naive Bayesian classifier for rapid assignment of rRNA sequences into the new bacterial taxonomy // Appl. Environ. Microbiol. 2007. V. 73. P. 5261–5267.
Yang X., Huang T., Zhang H. Effects of seasonal thermal stratification on the functional diversity and composition of the microbial community in a drinking water reservoir // Water. 2015. V. 7. P. 5525–5546.
Дополнительные материалы отсутствуют.


