Микробиология, 2021, T. 90, № 5, стр. 618-622
Ингибирующее действие норадреналина на рост биопленок комменсала кожи человека Kytococcus schroeteri H01
Н. Д. Данилова a, О. В. Гераськина b, Е. В. Дювенжи a, А. В. Феофанов b, В. К. Плакунов a, А. В. Ганнесен a, *
a Федеральный исследовательский центр “Фундаментальные основы биотехнологии”
Российской академии наук
119071 Москва, Россия
b Московский государственный университет им. М.В. Ломоносова
119991 Москва, Россия
* E-mail: andrei.gannesen@gmail.com
Поступила в редакцию 22.03.2021
После доработки 20.05.2021
Принята к публикации 23.05.2021
Аннотация
Впервые исследовано действие норадреналина на рост планктонных культур и биопленок комменсального микроорганизма Kytococcus schroeteri H01. Показан дозозависимый ингибирующий эффект норадреналина на биопленки после 24 и 72 ч инкубации K. schroeteri H01 на тефлоне: наибольшее подавление роста биопленок отмечено при концентрации гормона 3.5 × 10–7 М после 24 ч инкубации (71 ± 13% от контроля) и 3.5 × 10–6 М после 72 ч роста (78 ± 10% от контроля). Биопленки на стекле в присутствии норадреналина становились значительно более плоскими и тонкими. Значимого воздействия на метаболическую активность клеток в составе биопленок не обнаружено. По-видимому, норадреналин влияет на начальные этапы перехода к биопленочному способу существования и синтез матрикса у K. schroeteri.
Биопленки микроорганизмов играют важную роль в глобальных биогеохимических циклах элементов, в функционировании различных природных экосистем, иммунной системы человека и поддержании гомеостаза комменсальной микробиоты кожи, кишечника и других органов (Ножевникова и соавт., 2015). Представители филума Actinobacteria широко используются в биотехнологии, а также широко представлены как комменсалы человека, в частности, кожи (Fourniere et al., 2020). В настоящее время все возрастающий интерес представляют исследования взаимодействия гуморальных систем человека и его микробиоты (в особенности, биопленок комменсалов и патогенов) с точки зрения потенциальной регуляции гомеостаза микробиоты гормонами. Катехоламины являются наиболее исследованными гормонами, однако их влияние на грамположительные микроорганизмы исследовано слабо, в частности, мало изучен эффект воздействия на актинобактерии. Недавно было показано, что катехоламины (норадреналин, адреналин) способны оказывать значительный стимулирующий эффект на рост биопленок C. acnes и M. luteus (Borrel et al., 2019; Данилова и соавт., 2020). Помимо этого, сравнительно мало сведений о жизнедеятельности и формировании биопленок некоторых грамположительных микроорганизмов, обитающих на коже и их взаимодействии с организмом человека. В этом аспекте интересно исследование Kytococcus schroeteri – микроорганизма, выделенного из рода Micrococcus по ряду биохимических признаков и отнесенного, согласно современной классификации, к семейству Kytococcaceae порядка Micrococcales класса Actinobacteria (Becker et al., 2002, Nouioui et al., 2018). Этот микроорганизм является крайне мало исследованным с точки зрения биохимии и физиологии, что затрудняет понимание механизмов вызываемых им клинических случаев эндокардитов, пневмоний и обрастаний имплантатов, приводящих к распространению инфекции (Shah et al., 2019). В недавнем исследовании полного генома (Boukerb et al., 2019) K. schroeteri H01, выделенного с кожи, показано, что для него характерно высокое содержание Г + Ц, как и для других актинобактерий, а также наличие около 2200 кодирующих генов и 2.5 млн пар оснований. Таким образом, этот организм является типичным представителем данной физиологической группы, несмотря на особенности его экотопа (Boukerb et al., 2019). О биопленках K. schroeteri H01 практически ничего не известно, поэтому, а также из-за того, что этот потенциально опасный и малоизученный микроорганизм обитает на здоровой коже человека, важно исследовать его биопленки и связь с гуморальными системами человека.
В настоящей работе использовали штамм K. schroeteri H01, выделенный ранее с кожи добровольца (Журина и соавт., 2017; Boukerb et al., 2019), и воздействие на него норадреналина (“Merck”, США), показавшее, что данный гормон является одним из существенных факторов регуляции метаболизма указанного обитателя кожи человека. В работе опирались на данные о содержании гормона в плазме крови человека в норме (верхний предел нормы, согласно Boyanova, 2017, – 3.5 × 10–9 М). Помимо этого исследовали также концентрации 3.5 × 10–8, 3.5 × 10–7, 3.5 × 10–6 М. Бактерии выращивали на обогащенной клостридиальной среде (Gannesen et al., 2018). Инкубацию проводили при 33°С, что соответствует температуре кожи, где обитает этот микроорганизм (Boutcher et al., 1995; Lange-Asschenfeldt et al., 2011). Результаты представляли в виде средних абсолютных и относительных значений (% от контроля). Эксперименты проводили не менее чем в трех независимых повторностях. Статистическую достоверность данных характеризовали непараметрическим критерием Манна–Уитни при р < 0.05 с использованием пакета Microsoft Excel 2010.
Биопленки выращивали в модельных системах с тефлоновыми кубиками и в планшетах со стеклянным дном, как описано ранее (Журина и соавт., 2017; Gannesen et al., 2018). В обоих случаях биопленки формировались в равновесии с планктонной культурой. Одну часть образцов окрашивали кристаллическим фиолетовым для определения общей биомассы, а другую часть окрашивали метаболизируемым красителем 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромидом (МТТ) по методике, разработанной ранее (Журина и соавт., 2017). Это позволило оценить метаболическую активность клеток в составе биопленок, а именно работу электрон-транспортных цепей и НАДН-дегидрогеназ, поскольку акцептор электронов МТТ является универсальным инструментом для подобной оценки, как в случае клеток животных, так и бактерий (Berridge at al., 2005). В планшетах анализировали трехмерную структуру биопленок (плотность биомассы, т.е. объем на единицу площади поля зрения, и среднюю толщину) с помощью конфокальной лазерной сканирующей микроскопии (КЛСМ).
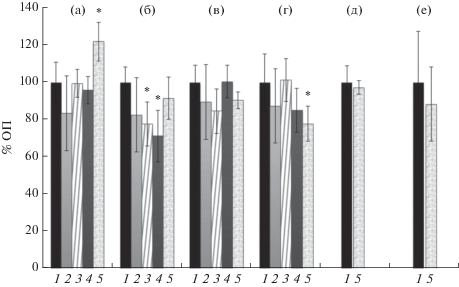
Перед началом основных экспериментов предварительно определили время инкубации для получения формирующихся и сформированных биопленок K. schroeteri – 24 и 72 ч соответственно. Исследование роста биопленок на тефлоновых кубиках в присутствии различных концентраций норадреналина показало дозозависимый характер действия гормона. После 24 ч инкубации гормон не оказывал значимого эффекта на конечную биомассу планктонных культур, за исключением образцов с максимальной концентрацией, в которых наблюдали стимуляцию роста планктонной культуры до 122 ± 10% от контроля (рис. 1а). При этом рост биопленок снижался в присутствии норадреналина; заметное ингибирование наблюдали при 3.5 × 10–8 и 3.5 × 10–7 М: 78 ± 11 и 71 ± 13% соответственно (рис. 1б). После 72 ч инкубации какого-либо влияния на конечную биомассу планктонных культур, определяемую по оптической плотности, не наблюдали, хотя обозначалась тенденция к подавлению их роста (рис. 1в). В случае биопленок наблюдали аналогичную тенденцию: достоверное ингибирование до 78 ± 10% происходило только при 3.5 × 10–6 М норадреналина в среде (рис. 1г). Исследование метаболической активности при 3.5 × 10–6 М норадреналина в среде не показало ощутимого ингибирования, что, вероятно, указывает на влияние норадреналина скорее на синтез матрикса и формирование архитектуры биопленки, чем на способность клеток восстанавливать МТТ. Как и в случае M. luteus (Данилова и соавт., 2020), вероятные изменения метаболизма K. schroeteri в присутствии норадреналина сильнее сказываются на росте биопленок, как более характерной для микроорганизмов-комменсалов человека форме существования.
Рис. 1.
Влияние норадреналина на рост планктонных культур и биопленок K. schroeteri H01 в системе с тефлоновыми кубиками (б, г – окраска КФ, д, е – окраска МТТ): а – планктонные культуры через 24 ч инкубации; б, д – биопленки через 24 ч инкубации; в – планктонные культуры через 72 ч инкубации, г, е – биопленки через 72 ч инкубации. 1 – контроль без добавок; 2 – норадреналин, 3.5 × 10–9 М; 3 – норадреналин, 3.5 × 10–8 М; 4 – норадреналин, 3.5 × 10–7 М; 5 – норадреналин, 3.5 × 10–6 М. * p < 0.05.
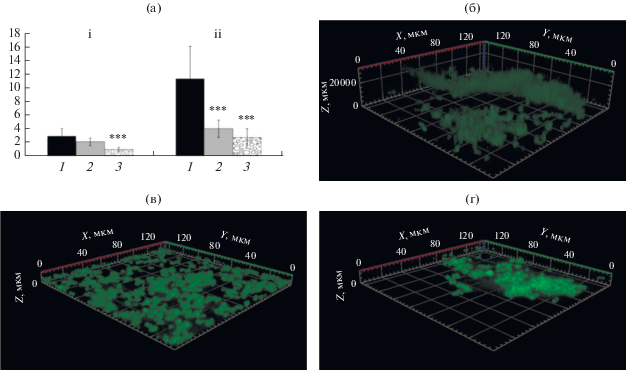
Впервые было проведено исследование био-пленок K. schroeteri с помощью КЛСМ. Измерения окрашенных SYTO9 Green образцов проводили с помощью микроскопа LSM510 и программного пакета ImageJ (плагин Comstat2) по методике, описанной ранее (Gannesen et al., 2018). Исследование структуры зрелых биопленок K. schroeteri в присутствии 3.5 × 10–9 и 3.5 × 10–6 М норадреналина показало сильный ингибирующий эффект гормона (рис. 2). Так значительно снижалась толщина биопленок (11.3 ± 4.7 мкм в контроле, 4.0 ± 1.2 мкм при 3.5 × 10–9 М норадреналина и 2.8 ± 1.2 мкм при 3.5 × 10–6 М гормона в среде, рис. 2а). Плотность биомассы биопленок при этом тоже уменьшалась, значимо – при 3.5 × × 10–6 М гормона в среде (2.93 ± 1.1 мкм3/мкм2 в контроле и 0.99 ± 0.3 мкм3/мкм2 в присутствии норадреналина). При концентрации 3.5 × 10–9 М норадреналина также наблюдали утончение биопленок до 2.1 ± 0.51 мкм, однако разброс показателей не позволял говорить о значимости эффекта. Визуализация изображений (рис. 2б–2г) демонстрирует более плоские биопленки китококков в присутствии гормона (рис. 2в–2г). Таким образом, можно предполагать, что норадреналин в модельных системах не влияет на процесс адгезии клеток к абиотическим поверхностям – тефлону и стеклу. Возможно, что в присутствии норадреналина активируются некие глобальные каскады биохимических реакций, подобные тем, которые запускаются сигнальной системой QseBC у Escherichia coli (Weigel, Demuth, 2016). У грамположительных микроорганизмов пока не обнаружено систем, подобных QseBC, однако потенциально мишенями для гормонов могут быть другие сенсоры. Также вероятно, что гормон действует сразу на несколько мишеней, но при разных концентрациях в среде, что потенциально могло бы служить объяснением дозозависимого эффекта, или один рецептор может по-разному реагировать на различные концентрации гормона, как это показано на моторной коре у человека (Fresnoza et al., 2014). Помимо этого, имеются свидетельства о мультитаргетном действии других гормонов на клетки. К примеру, прогестерон при разных концентрациях активирует различные мишени в Т-клетках, модулируя иммунный ответ при аутоиммунных заболеваниях (Tan et al., 2015). Потенциально, похожие явления возможны и в бактериальных клетках. Необходимы исследования изменений биохимического состава матрикса биопленок K. schroeteri, изменения поверхностных свойств клеток и экспрессии генов для дальнейшего углубленного изучения эффекта норадреналина.
Рис. 2.
КЛСМ биопленок K. schroeteri H01, окрашенных SYTO 9 Green после 72 ч инкубации: а – количественные характеристики биопленок; б – контроль без добавок; в – норадреналин, 3.5 × 10–9 М; г – 3.5 × 10–6 М; i – плотность биомассы биопленок, мкм3/мкм2 (1 – контроль, 2 – норадреналин 3.5 × 10–9 М, 3 – норадреналин 3.5 × 10–6 М); ii ‒ средняя толщина биопленок, мкм. *** p < 0.001.
Таким образом, впервые были получены данные о структуре биопленок Kytococcus schroeteri и эффекте норадреналина на бактерию. Получено еще одно доказательство взаимосвязи комменсальной микробиоты человека и его гормональных регуляторных систем. Несмотря на гораздо более сложные взаимодействия микроорганизмов с организмом человека и друг с другом в составе мультивидовых сообществ на коже, полученные нами результаты способствуют продвижению к лучшему пониманию взаимодействия человека и его микробиоты на примере K. schroeteri.
Список литературы
Данилова Н.Д., Соловьева Т.В., Мартьянов С.В., Журина М.В., Ганнесен А.В. Стимулирующий эффект адреналина на биопленки Micrococcus luteus C01 // Микробиология. 2020. Т. 89. С. 488–492.
Danilova N.D., Solovyeva T.V., Mart’yanov S.V., Zhurina M.V., Gannesen A.V. Stimulatory effect of epinephrine on biofilms of Micrococcus luteus C01 // Microbiology (Moscow). 2020. V. 89. P. 493–497.
Журина М.В., Ганнесен А.В., Мартьянов С.В., Тетенева Н.А., Штратникова В.Ю., Плакунов В.К. Никлозамид как перспективный антибиопленочный агент // Микробиология. 2017. Т. 86. С. 439–447.
Zhurina M.V., Gannesen A.V., Mart’yanov S.V., Teteneva N.A., Shtratnikova V.Y., Plakunov V.K. Niclosamide as a promising antibiofilm agent //Microbiology (Moscow). 2017. V. 86. P. 455–462.
Ножевникова А.Н., Бочкова Е.А., Плакунов В.К. Мультивидовые биопленки в экологии, медицине и биотехнологии // Микробиология. 2015. V. 84. P. 623–644.
Nozhevnikova A.N., Botchkova E.A., Plakunov V.K. Multi-species biofilms in ecology, medicine, and biotechnology // Microbiology (Moscow). 2015. V. 84. P. 731–750.
Becker K., Schumann P., Wüllenweber J., Schulte M., Weil H.P., Stackebrandt E., Peters G., von Eiff C. Kytococcus schroeteri sp. nov., a novel Gram-positive actinobacterium isolated from a human clinical source // Int. J. Syst. Evol. Microbiol. 2002. V. 52. P. 1609–1614.
Berridge M.V., Herst P.M., Tan A.S. Tetrazolium dyes as tools in cell biology: New insights into their cellular reduction // Biotechnol. Annu. Rev. 2005. V. 11. P. 127–152.
Borrel V., Thomas P., Catovic C., Racine P.J., Konto-Ghiorghi Y., Lefeuvre L., Duclaroir-Poc C., Zouboulis C., Feuilloley M.G. Acne and stress: impact of catecholamines on Cutibacterium acnes // Front. Med. 2019. V. 6. P. 155.
Boukerb A.M., Robert M., Teteneva N.A., Danilova N.D., Zhurina M.V., Mart’yanov S. V., Plakunov V.K., Feuilloley M.G., Gannesen A.V. Draft genome sequence of Kytococcus schroeteri strain h01, isolated from human skin // Microbiol. Resour. Announc. 2019. V. 8. Art. e01081-19.
Boutcher S.H., Maw G.J., Taylor N.A. Forehead skin temperature and thermal sensation during exercise in cool and thermoneutral environments // Aviat. Space Environ. Med. 1995. V. 66. P. 1058–1066.
Boyanova L. Stress hormone epinephrine (adrenaline) and norepinephrine (noradrenaline) effects on the anaerobic bacteria // Anaerobe. 2017. V. 44. P. 13–19.
Fournière M., Latire T., Souak D., Feuilloley M. G., Bedoux G. Staphylococcus epidermidis and Cutibacterium acnes: two major sentinels of skin microbiota and the influence of cosmetics // Microorganisms. 2020. V. 8. Art. 1752.
Fresnoza S., Stiksrud E., Klinker F., Liebetanz D., Paulus W., Kuo M.F., Nitsche M.A. Dosage-dependent effect of dopamine D2 receptor activation on motor cortex plasticity in humans // J. Neurosci. 2014. V. 34. P. 10701–10709.
Gannesen A.V., Borrel V., Lefeuvre L., Netrusov A.I., Plakunov V.K., Feuilloley M.G. Effect of two cosmetic compounds on the growth, biofilm formation activity, and surface properties of acneic strains of Cutibacterium acnes and Staphylococcus aureus // MicrobiologyOpen. 2019. V. 8. Art. e00659.
Lange-Asschenfeldt B., Marenbach D., Lang C., Patzelt A., Ulrich M., Maltusch A., Terhorst D., Stockfleth E., Sterry W., Lademann J. Distribution of bacteria in the epidermal layers and hair follicles of the human skin // Skin Pharmacol. Physiol. 2011. V. 24. P. 305–311.
Nouioui I., Carro L., García-López M., Meier-Kolthoff J.P., Woyke T., Kyrpides N.C., Pukall R., Klenk H.-P., Goodfellow M., Goker R. Genome-based taxonomic classification of the phylum Actinobacteria // Front. Microbiol. 2018. V. 9. P. 2007.
Shah A.S., Vijayvargiya P., Jung S., Wilson J.W. Postoperative hardware-related infection from Kytococcus schroeteri: its association with prosthetic material and hematological malignancies – a report of a case and review of existing literature // Case Rep. Infect. Dis. 2019. V. 2019. Art. 6936472.
Tan I.J., Peeva E., Zandman-Goddard G. Hormonal modulation of the immune system – A spotlight on the role of progestogens // Autoimmun. Rev. 2015. V. 14. P. 536–542.
Weigel W.A., Demuth D.R. Qse BC, a two-component bacterial adrenergic receptor and global regulator of virulence in Enterobacteriaceae and Pasteurellaceae // Mol. Oral Microbiol. 2016. V. 31. P. 379–397.
Дополнительные материалы отсутствуют.


