Микробиология, 2022, T. 91, № 6, стр. 763-768
Влияние фторидных соединений сурьмы на почвенную микрофлору и методы их детоксикации
И. В. Киселева a, *, А. Н. Холомейдик b, Л. Н. Щапова a, А. Е. Панасенко b
a Федеральный научный центр биоразнообразия наземной биоты
Восточной Азии ДВО РАН
690022 Владивосток, Россия
b Институт химии ДВО РАН
690022 Владивосток, Россия
* E-mail: kiseleva-iv@inbox.ru
Поступила в редакцию 25.11.2021
После доработки 28.04.2022
Принята к публикации 04.05.2022
- EDN: ELZSRE
- DOI: 10.31857/S0026365621100724
Аннотация
Установлено токсическое действие SbF3 и NaSbF4 в концентрации 50 и 100 мг/л на почвенную микрофлору. При внесении 50 мг/л в питательную среду (МПА) единично обнаруживались бактерии и микроскопические грибы. Дозировка 100 мг/л полностью подавляла рост бактерий в исследованных почвах. Микроскопические грибы более устойчивы к действию исследованных соединений. При добавлении 0.1 М раствора NaH2PO4 к растворам SbF3 и NaSbF4 наблюдалось уменьшение концентрации растворенных ионов Sb3+ в 5.7–6.9 раз, но на численность почвенных микроорганизмов такой раствор по-прежнему оказывал токсическое действие. Показано, что в отличие от реагентной очистки, метод сорбционного извлечения Sb(III) был более эффективен. Водные растворы с концентрацией сурьмы 5000 мг/л, использованные для разведения почвенной суспензии, губительно воздействовали на весь спектр микроорганизмов, развивающихся на среде МПА. После сорбционной очистки концентрация сурьмы снижалась до 201.3 мг/л, отмечался рост микроорганизмов.
В настоящее время проблема загрязнения окружающей среды различными тяжелыми металлами стоит остро в различных регионах. При этом основным источником загрязнения являются месторождения, при разработке которых металлы попадают в окружающую среду и мигрируют, главным образом, с водными потоками, представляя опасность для микроорганизмов, растений, животных и человека. За счет способности большинства тяжелых металлов образовывать нерастворимые соли и оксиды, их накопление происходит преимущественно в почве. Одним из металлов, обладающих токсическим действием по отношению к различным типам живых организмов, является сурьма. Этому элементу уделяется мало внимания в работах почвоведов, доля упоминания Sb в публикациях составляла всего 0.9% (Водяницкий, 2012).
В КНР, в провинции Хунань, где расположено одно из крупнейших в мире месторождений сурьмы Сигуаньшань (Xikuangshan), в результате его разработки наблюдается масштабное загрязнение почвы и грунтовых вод сурьмой (Wang, 2011; Fu, 2016). В России в Приморском крае в ХХ в. активно разрабатывались месторождения угля, содержащего в виде примеси сурьму. В настоящее время в Партизанском и Надеждинском районах Приморского края обнаружено загрязнение сурьмой шахтных вод, которые имеют контакт с грунтовыми водами и выходят в реки, использующиеся для водоснабжения нескольких городов и поселков.
Известно, что соединения сурьмы обладают, в зависимости от природы вещества и его концентрации, либо токсическим, либо стимулирующим действием по отношению к морским и патогенным микроорганизмам, клеточным культурам, растениям и животным (Ковалева, Земнухова, 2019). Таким образом, почвенная микрофлора может служить индикатором загрязненности почв поллютантами, в частности, сурьмой. Согласно общесанитарному показателю (влияние на самоочищающую способность почв и почвенный микробиоценоз) ПДК сурьмы в почве составляет 50 мг/кг (МУ 2.1.7.730-99, 1999).
Цель работы – оценить токсическое действие сурьмы(III) на микроорганизмы, выделенные из почв Приморского края, установить диапазон токсичности и найти физико-химические методы снижения концентрации Sb(III) до приемлемого уровня.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
При проведении исследований использовались образцы бурозема типичного (Haplic Cambisol), отобранные в районе Академгородка под дубовым лесом и серогумусовой техногенной почвы (Folic Technosol) взятые на территории бывшего военного аэродрома в районе ст. Седанка под разнотравьем (Приморский край, г. Владивосток).
Отбор почвенных образцов проводился в начале ноября 2020 г. из верхнего (0–10 см) горизонта в соответствии с ГОСТ 17.4.4.02-84 (2008). Названия почв приведены согласно российской (Шишов и соавт., 2004) и международной классификации (IUSS Working Group WRB…, 2014). Для почвы, формирующейся на территории заброшенного аэродрома, использована классификация, предложенная Прокофьевой и соавт. (2014).
Определение органического углерода проведено мокрым сжиганием по Тюрину, рН вод – потенциометрически (Аринушкина, 1970). Общую численность почвенной аммонифицирующей микрофлоры учитывали методом высева почвенной суспензии различной степени разведения на среду, содержащую мясо-пептонный агар (МПА). Эту среду применяют для выделения широкого спектра почвенных микроорганизмов (Методы почвенной микробиологии…, 1991).
В работе было исследовано влияние различных концентраций сурьмы: 1, 10, 50 и 100 мг/л при добавлении в питательную среду, а так же 5000 и 201.3 мг/л при разведении почвенной суспензии. В качестве модельных соединений были использованы растворимые соединения, способные к миграции в природных средах – фторид сурьмы (SbF3) и комплексное соединение тетрафтороантимонат натрия (NaSbF4). В качестве контрольного варианта использована среда МПА без внесения соединений сурьмы.
Для реагентной очистки растворов SbF3 и NaSbF4 использовали 0.1 М раствор дигидрофосфата натрия (NaH2PO4) в стехиометрическом количестве.
В качестве сорбентов исследовали кремнийсодержащие материалы различного состава. Используя в качестве источника кремния биогенное сырье – шелуху риса, путем пиролиза в бескислородных условиях был получен углеродсодержащий материал (образец 1) и окислительным обжигом – высокочистый биогенный аморфный кремнезем (образец 2) (Земнухова, 2005). На основе соломы риса был получен алюмосиликат натрия (образец 3), проявляющий высокие сорбционные свойства по отношению к органическим красителям (Панасенко, 2019). С использованием биогенного кремнезема из шелухи риса был получен композиционный железосодержащий материал (образец 4) (Панасенко, 2017). Для оценки возможности извлечения соединений сурьмы исследуемыми образцами были построены кривые извлечения ионов Sb3+ из водных растворов SbF3 с концентрацией металла 20–800 мг/л в статических условиях. Концентрацию сурьмы в растворах определяли методом атомно-абсорбционной спектрометрии на спектрометре SOLAAR M6 (“Thermo”, США).
Статистическая обработка результатов анализа проведена в программе Statistica.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Численность микроорганизмов в почве зависит от времени года, содержания органического вещества, плотности сложения почв, кислотности, влажности, температуры и других факторов. Исследованные почвы формируются в разных условиях. Для бурозема типичного характерны слабокислая реакция среды (рН вод 5.5) и высокое содержание органического углерода (8.0%). Серогумусовой почве свойственна нейтральная реакция среды (рН вод 6.7) и низкое содержание Сорг (3.9%). Влажность исследованных почв составляла 23–26%.
Все это обусловливает изначально различное количество микроорганизмов (млн КОЕ на 1 г почвы) в контрольных вариантах исследованных почв: 3.9 ± 0.21 в буроземе и 10.1 ± 1.1 в серогумусовой почве. Для бурозема типичного отмечен рост грибов (до 32% от общего числа микроорганизмов на среде МПА).
Выявлена небольшая разница между численностью микроорганизмов в контроле и при внесении 1 и 10 мг/л SbF3 и NaSbF4. Однако эта разница находится в пределах ошибки.
Токсическое действие обоих соединений для двух типов почв обнаружено при концентрации 50 и 100 мг/л (рис. 1). При внесении 50 мг/л в посевах единично обнаруживаются бактерии и микроскопические грибы. Дозировка 100 мг/л полностью подавляет рост бактерий в исследованных почвах, развиваются только грибы, но их численность незначительна.
Рис. 1.
Численность микроорганизмов (млн КОЕ) в зависимости от концентрации соединений Sb(III): 1 – бурозем типичный (Haplic Cambisol); 2 – серогумусовая техногенная почва (Folic Technosol).
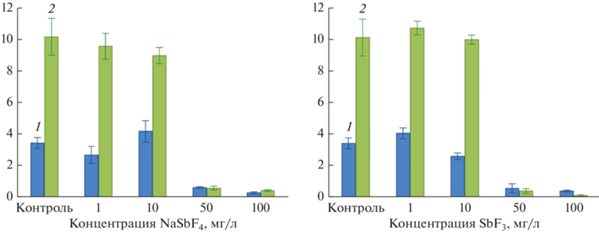
Аммонифицирующим микроорганизмам принадлежит ведущая роль в разложении содержащих азот сложных соединений. Резкое сокращение их численности может привести к серьезным экологическим последствиям. Важнейшим почвенно-микробиологическим процессом, определяющим наличие и содержание гумуса в почве, является деструкция растительного опада. В связи с этим, при попадании сурьмы в почву, может происходить снижение ее плодородия.
Известен реагентный способ очистки техногенных и природных вод, при котором воду обрабатывают растворами веществ, которые разрушают поллютанты, либо связывают их в неактивные формы. В случае сурьмы одним из способов перевести растворенные ионы Sb3+ в форму нерастворимого осадка является взаимодействие с фосфат-ионами ${\text{PO}}_{4}^{{3 - }},$ поскольку фосфат сурьмы SbPO4 – нерастворимое соединение (Bolan, 2022). При добавлении 0.1 М раствора дигидрофосфата натрия NaH2PO4 к растворам SbF3 и NaSbF4 наблюдается опалесценция, что свидетельствует об образовании частиц SbPO4 коллоидных размеров (10−7–10−9 м). По данным атомно-абсорбционной спектрометрии концентрация растворенных ионов Sb3+ в растворе при такой реагентной обработке уменьшается в 5.7–6.9 раз. Однако на численность почвенных микроорганизмов такой раствор по-прежнему оказывает токсическое действие (рис. 2). По-видимому, на микроорганизмы токсическое действие оказывают не только растворенные ионы Sb3+, но и коллоидные частицы фосфата сурьмы SbPO4.
Рис. 2.
Численность микроорганизмов (тыс. КОЕ) при концентрации соединений Sb(III) 100 мг/л и с внесением дигидрофосфата натрия: 1 – бурозем типичный (Haplic Cambisol); 2 – серогумусовая техногенная почва (Folic Technosol).
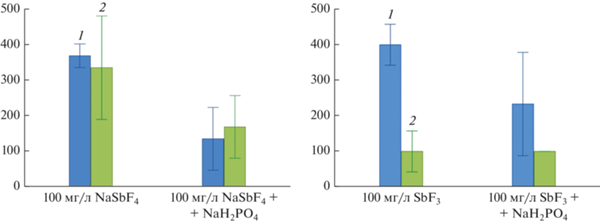
Применение сорбентов является одним из наиболее эффективных способов извлечения поллютантов из раствора. Для ионов тяжелых металлов высокими сорбционными характеристиками обладают кремнийсодержащие оксидные сорбенты – диоксид кремния, силикаты и алюмосиликаты (Yarusova, 2017). Также высокие сорбционные свойства по отношению к ионам сурьмы проявляют углеродные материалы и оксиды железа. Среди известных сорбентов для извлечения сурьмы в исследованном диапазоне концентраций большинство демонстрируют сорбционную емкость порядка 100–250 мг/г, а наилучший известный материал – бернессит показывает емкость 759 мг/г (Zhang, 2021).
В настоящей работе оценивали возможность использования для очистки водных сред от ионов сурьмы(III) четырех сорбционных материалов различной природы (табл. 1), которые проявляют высокие сорбционные свойства по отношению к другим поллютантам – органическим красителям (метиленовый синий), радионуклидам (Cs, Sr, Co) и тяжелым металлам (Pb).
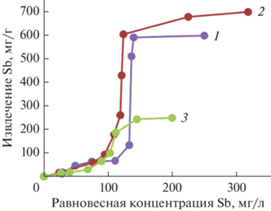
Кривые извлечения сурьмы (рис. 3) из модельных растворов SbF3 показывают, что наибольшей эффективностью обладает образец 3 – биогенный алюмосиликат натрия из соломы риса (емкость 596 мг/г, степень извлечения сурьмы из растворов – до 76%) (Холомейдик, 2021).
Рис. 3.
Изотермы извлечения сурьмы из растворов SbF3 кремнийсодержащими материалами (нумерация образцов по табл. 1).

Для исследования реальной эффективности сорбционной очистки в отношении микрофлоры почв был использован раствор c высокой концентрацией SbF3 (5000 мг/л) и такой же раствор после сорбционной очистки биогенным алюмосиликатом натрия. Концентрация сурьмы после фильтрации через сорбент составила 201.3 мг/л (степень извлечения 96–96.7%). В данном случае исследованные растворы после стерилизации использовали для разведения почвенной суспензии с последующим высевом на чистую питательную среду МПА. Установлено, что раствор с концентрацией в 5000 мг/л оказывает губительное воздействие на весь спектр микроорганизмов, развивающихся на среде МПА. После сорбционной очистки отмечен рост микроорганизмов на среде МПА до 9–11 тыс. КОЕ/г почвы.
Дополнительно были исследованы сорбционные свойства алюмосиликата натрия по извлечению сурьмы из почвенных водных вытяжек (рис. 4). Установлено, что эффективность сорбента меняется в зависимости от типа почвы. Относительно модельного раствора SbF3 в случае вытяжки из серогумусовой техногенной почвы сорбционная емкость снижается на 59%, однако для бурозема – повышается на 16%.
Рис. 4.
Изотермы извлечения сурьмы из почвенных вытяжек биогенным алюмосиликатом натрия: 1 – водный раствор SbF3; 2 – вытяжка из бурозема + SbF3; 3 – вытяжка из серогумусовой почвы + SbF3.
Таким образом, установлено токсическое действие SbF3 и NaSbF4 в концентрации 50 и 100 мг/л на почвенную микрофлору. Концентрация соединений сурьмы(III) в питательной среде в дозе 50 мг/л резко снижает численность аммонификаторов в почве, 100 мг/л – практически полностью уничтожает аммонифицирующие микроорганизмы, которым принадлежит ведущая роль в разложении содержащих азот сложных соединений. Установлено, что микроскопические грибы более устойчивы к действию исследованных соединений.
При реагентном способе очистки с использованием 0.1 М раствор дигидрофосфата натрия (NaH2PO4) отмечено токсическое действие полученного раствора на численность почвенных микроорганизмов.
Показано, что в отличие от реагентной очистки, метод сорбционного извлечения Sb(III) эффективен и позволяет извлекать из водных растворов до 96.7% растворенной сурьмы. Водные растворы с высокой концентрацией сурьмы (5000 мг/л), использованные для разведения почвенной суспензии, губительно воздействовали на весь спектр микроорганизмов, развивающихся на среде МПА. После сорбционной очистки биогенным алюмосиликатом натрия концентрация сурьмы снижалась до 201.3 мг/л, отмечался рост микроорганизмов, что позволяет говорить об эффективности использования такого метода очистки для реальных природных систем.
Дешевый и экологически чистый сорбент – биогенный алюмосиликат натрия при извлечении сурьмы из почвенных вытяжек обладает емкостью до 700 мг/г, что сопоставимо с наилучшими из известных сорбционных материалов. Также для очистки водных сред от сурьмы представляет интерес железосодержащий композиционный материал, обладающий магнитными свойствами.
Список литературы
Аринушкина Е.В. Руководство по химическому анализу почв. М.: МГУ, 1970. 487 с.
Водяницкий Ю.Н. Нормативы содержания тяжелых металлов и металлоидов в почвах // Почвоведение. 2012. № 3. С. 368–375.
Vodyanitskii Y.N. Standards for the contents of heavy metals and metalloids in soils // Euras. Soil Sci. 2012. V. 45. P. 321–328. https://doi.org/10.1134/S1064229312030131
ГОСТ 17.4.4.02-84. Охрана природы. Почвы. Методы отбора и подготовки проб для химического, бактериологического, гельминтологического анализа. Введ. 01.01.1986 г. М.: Стандартинформ, 2008. 8 с.
Земнухова Л.А., Федорищева Г.А., Егоров А.Г., Сергиенко В.И. Исследования условий получения, состава примесей и свойств аморфного диоксида кремния из отходов производства риса // Журн. прикладной химии. 2005. Т. 78. С. 324–328.
Ковалева Е.В., Земнухова Л.А. Экотоксикологические свойства комплексных фторидных соединений сурьмы(III) // Вестн. Томского гос. ун-та. Химия. 2019. № 13. С. 28–41. https://doi.org/10.17223/24135542/13/4
Методы почвенной микробиологии и биохимии / Под ред. Звягинцева Д.Г. М.: Изд-во МГУ, 1991. 303 с.
Панасенко А.Е., Борисова П.Д., Арефьева О.Д., Земнухова Л.А. Алюмосиликаты из соломы риса: получение и сорбционные свойства // Химия растительного сырья. 2019. № 3. С. 291–298.
Панасенко А.Е., Ткаченко И.А., Квач А.А., Земнухова Л.А. Магнитные свойства композиционных материалов на основе аморфного кремнезема растительного и минерального происхождения // Журн. неорганической химии. 2017. Т. 62. С. 972–976.
Гигиеническая оценка качества почвы населенных мест: Методические указания. МУ 2.1.7.730-99. М.: Федеральный центр госсанэпиднадзора Минздрава России. 1999. 38 с.
Прокофьева Т.В., Герасимова М.И., Безуглова О.С., Бахматова К.А., Гольева А.А., Горбов С.Н., Жарикова Е.А., Матинян Н.Н., Наквасина Е.Н., Сивцева Н.Е. Введение почв и почвоподобных образований городских территорий в классификацию почв России // Почвоведение. 2014. Т. 47. № 10. С. 1155–1164.
Prokof’eva T.V., Gerasimova M.I., Bezuglova O.S., Bakhmatova K.A., Gol’eva A.A., Gorbov S.N., Zharikova E.A., Matinyan N.N., Nakvasina E.N., Sivtseva N.E. Inclusion of soils and soil-like bodies of urban territories into the Russian soil classification system // Euras. Soil Sci. 2014. V. 47. P. 959–967. https://doi.org/10.1134/S1064229314100093
Холомейдик А.Н., Панасенко А.Е. Извлечение ионов Sb3+ кремнийсодержащими материалами из шелухи и соломы риса // Химия и химическое образование: 8-й международный симпозиум, 04–06 октября 2021 г.: сборник науч. трудов. Владивосток: Изд-во Дальневост. фед. ун-та, 2021. 188 с. https://doi.org/10.24866/7444-4121-0.
Шишов Л.Л., Тонконогов В.Д., Лебедева И.И., Герасимова М.И. Классификация и диагностика почв России. Смоленск: Ойкумена, 2004. 342 с.
Bolan N., Kumar M., Singh E., Kumar A., Singh L., Kumar S., Keerthanan S., Hoang S.A., El-Naggar A., Vithanage M., Sarkar B., Wijesekara H., Diyabalanage S., Sooriyakumar P., Vinu A., Wang H., Kirkham M.B., Shaheen S.M., Rinklebe J., Siddique K.H.M. Antimony contamination and its risk management in complex environmental settings: a review // Environ. Int.2022. V. 158. Art. 106908. https://doi.org/10.1016/j.envint.2021.106908
Fu Z., Wu F., Mo C., Deng Q., Meng W., Giesy J.P. Comparison of arsenic and antimony biogeochemical behavior in water, soil and tailings from Xikuangshan, China // Sci. Total Environ. 2016. V. 539. P. 97–104. https://doi.org/10.1016/j.scitotenv.2015.08.146
IUSS Working Group WRB, World Reference Base for Soil Resources, International Soil Classification System for Naming Soils and Creating Legends for Soil Maps, World Soil Resources Reports No. 106. Food and Agriculture Organization, Rome, 2014.
Wang X., He M., Xi J., Lu X. Antimony distribution and mobility in rivers around the world’s largest antimony mine of Xikuangshan, Hunan Province, China // Microchem. J. 2011. V. 97. P. 4–11. https://doi.org/10.1016/j.microc.2010.05.011
Yarusova S.B., Gordienko P.S., Krishna R., Azarova Yu.A., Suponina A.P., Perfilev A.V., Sharma Y.C. Sorption characteristics of economically viable silicate sorbents for sequestration of lead ions from aqueous solutions // Resource-Efficient Technol. 2017. V. 3. P. 213–221. https://doi.org/10.1016/j.reffit.2017.05.002
Zhang X., Xie N., Guo Y., Niu D., Sun H. Yang Y. Insights into adsorptive removal of antimony contaminants: Functional materials, evaluation and prospective // J. Hazard. Mater. 2021. V. 418. Art. 126345. https://doi.org/10.1016/j.jhazmat.2021.126345
Дополнительные материалы отсутствуют.


