Микология и фитопатология, 2019, T. 53, № 1, стр. 26-35
Морфологические особенности штаммов Amorphotheca resinae при росте в авиационном топливе и на питательных средах
А. А. Кривушина 1, *, Л. Н. Чекунова 2, В. Л. Мокеева 2
1 Всероссийский научно-исследовательский институт авиационных материалов
105005 Москва, Россия
2 Московский государственный университет имени М.В. Ломоносова
119991 Москва, Россия
* E-mail: kopengagen8@mail.ru
Поступила в редакцию 01.09.2017
После доработки 01.12.2017
Принята к публикации 20.12.2017
Аннотация
Из образцов авиационного топлива выделены культуры вида Amorphotheca resinae, известного как “керосиновый гриб”. Изучены морфологические особенности пяти штаммов А. resinae при росте на питательной среде Чапека и агаризованном сусле. Показано, что признаки конидиального спороношения, описанные для форм “керосинового гриба” А. resinae f. avellaneum и А. resinae f. resinae, являются нестабильными и встречаются в культуре одного и того же штамма. Рассмотрены морфологические особенности штаммов А. resinae при росте в авиационном топливе. Показано, что у штаммов А. resinae при развитии в топливе образуются точно такие же конидиальные структуры, как и при росте на питательных средах, что свидетельствует о высокой степени приспособленности гриба к данной специфической среде.
О проблеме поражения авиационного топлива мицелиальными грибами и другими микроорганизмами известно уже давно. В результате развития микромицетов происходит засорение топливных систем, следствием чего может быть выход двигателей из строя. Случаи засорения топливных фильтров неоднократно происходили при выполнении полетов таких типов самолетов, как Ил-76, Ту-154, Ту-134, М-17 и др. (Semenov et al., 2008). Причиной аварии может стать также образование грибами кислот и ферментов, что ведет к усилению коррозии металлов, разрушению неметаллических материалов и к нарушению герметичности баков (Koval, Sidorenko, 1989; Ferrari et al., 1998; Hamme et al., 2003; Rauch et al., 2006). Среди грибов, повреждающих топливо, наиболее известен Amorphotheca resinae Parbery, который чаще всего можно встретить в научной литературе под названием его несовершенной стадии. За весь период его изучения их было несколько: Hormodendrum resinae Lindau, Cladosporium resinae (Lindau) G.A. de Vries и Hormoconis resinae (Lindau) Arx et G.A. de Vries.
История вида начинается в 1851 г., когда ученый Бонорден выделил род Hormodendrum с 4 видами, которые на настоящий момент относятся к роду Penicillium. До наших дней сохранились лишь описания плохого качества, и ничего неизвестно о типовых образцах. Поэтому нельзя идентифицировать гриб, описанный автором. В 1904 г. Линдау выделил из смолы хвойных деревьев два гриба. Первый гриб имел синнемы, второй – свободные конидиеносцы. Второй гриб был назван Линдау как Hormodendrum resinae. На самом деле ученый выделил две анаморфы одного и того же гриба – Sorocybe resinae (Fr.) Fr. Однако это стало известно лишь спустя много лет. Анаморфа S. resinae имеет относительное сходство с анаморфой Amorphotheca resinae, в частности по строению спороношений. Однако, в отличие от “керосинового гриба”, у Sorocybe resinae конидии более темные, а боковые стенки конидий заметно утолщены по сравнению с полюсными (Crous et al., 2007; Seifert еt аl., 2007). Эти различия ранее не были отмечены учеными, что в итоге привело к ошибкам. Например, долгое время считали, что повышенное содержание гриба в почве связано с хвойными деревьями, так как его часто выделяли со смолы (Sinadskiy, 1969). По-видимому, в подобных сообщениях речь шла об анаморфе S. resinae. В 1952 г. Вриез описал новый вид Cladosporium avellaneum, выделенный из косметических средств. Позже Вриез изучил описания Линдау и заключил, что Hormodendrum resinae и Cladosporium avellaneum – это один и тот же вид. Гриб был переименован в Cladosporium resinae, а эпитет “avellaneum” стал относиться к названию одной из форм “керосинового гриба”. Таким образом, названия Cladosporium resinae и Hormodendrum resinae широко использовались в обиходе до 1973 г. (Seifert еt аl., 2007). В 1969 г. Парбери описал аскомицет с клейстотециями Amorphotheca resinae – телеоморфу “керосинового гриба” (Parbery, 1971b). Парбери не учел, что название Hormodendrum resinae относится к анаморфе гриба Sorocybe resinae (Seifert еt аl., 2007). В 1973 г. Аркс и Вриез описали род Hormoconis на основе вида Hormodendrum resinaе. В намерения ученых входило объединение всех имеющихся названий анаморфы “керосинового гриба”. По их мнению, название Cladosporium resinae не подходило, поскольку “керосиновый гриб” отличается от видов рода Cladosporium отсутствием рубчиков на конидиях (Crous et al., 2007; Seifert еt аl., 2007). Таким образом, в связи со всеми вышеперечисленными фактами, название Hormodendrum resinae некорректно использовать для анаморфы “керосинового гриба”. Современное название анаморфы Amorphotheca resinae – это Hormoconis resinae, несмотря на то, что оно основано на ошибочном Hormodendrum resinaе. Название Cladosporium resinae широко использовалось в течение многих лет. И сейчас его можно встретить в прикладной научной литературе.
Вид обнаружен в пробах авиатоплива в Австралии, в большом количестве проб топлива в Бразилии и в Калифорнии. Об обнаружении Amorphotheca resinae есть сообщения из Англии, Дании, Индии, Сирии, Нигерии, Японии, Новой Зеландии, Кубы и др. Очевидно, расширение авиалиний может способствовать распространению гриба по всему земному шару (Koval, Sidorenko, 1989). Некоторые ученые предположили, что именно этот гриб стал причиной ряда авиакатастроф (Pomortseva et al., 1977; Andreyuk et al., 1980; Koval, Sidorenko, 1989; McVea, Solly, 1991).
В научно-технической и научно-популярной литературе данный вид можно встретить под названием “креозотовый гриб”, так как ранее его часто обнаруживали на поврежденной древесине, пропитанной креозотом. Вред, причиняемый им, считали не слишком ощутимым. Когда было установлено, что гриб вызывает деструкцию авиационных топлив, началось его всестороннее изучение, и за способность расти на бензине, керосине и другом горючем, а также на керосиновых фракциях нефти он был переименован в “керосиновый”. Это название прочно укрепилось за A. resinae. В природе гриб обитает в различных биогеоценозах и известен как компонент почвенной микобиоты (Sinadskiy, 1969). A. resinae неоднократно выделяли из загрязненных нефтью почв и других субстратов, содержащих углеводороды (San-Blas et al., 1996; Crous et al., 2007).
Целью данной работы было выделить культуры “керосинового гриба” A. resinae из образцов пораженного авиационного топлива, а также изучить морфологические особенности штаммов данного вида при росте в авиационном топливе и на искусственных питательных средах.
МАТЕРИАЛЫ И МЕТОДЫ
В работе были использованы 9 образцов авиационного топлива марки ТС-1 объемом около 500 мл каждая. Первые четыре извлечены непосредственно из кессон-баков эксплуатирующихся самолетов, совершивших аварийные посадки по причине забивки фильтров. Это образцы ”Китай” (К), “Краснодар” (Kr) и “Ульяновск” (Ul), которые содержали топливо, воду из отстойной зоны баков и темноокрашенные слизистые сгустки на границе раздела фаз. Четвертый образец “Иран” (Ir) содержал топливо, а позже, после нескольких месяцев хранения образца в лаборатории, в нем образовался небольшой мицелиальный сгусток. Другие пять образцов топлива прошли экспозицию в закрытых чашках Петри с добавлением минеральной среды на экспериментальных площадках в городах Батуми и Сочи (Polyakova et al., 2013; Polyakova et al., 2016). Образец “Батуми-1” (Bat-1) находился на экспозиции 18 месяцев, образец “Батуми-2” (Bat-2) – 24 месяца. Образцы “Сочи-1” (S-1), “Сочи-2” (S-2) и “Сочи-3” (S-3) были на экспозиции 13, 15 и 25 месяцев соответственно. Чашки ежемесячно открывали на 1 час, топливо и минеральную среду добавляли по мере испарения. За указанные периоды в образцах топлива образовались хлопьевидные образования и небольшие сгустки.
Для выделения грибов из образцов топлива использовали стандартные методы, описанные в нашей предыдущей работе (Krivushina et al., 2016).
Для выявления морфологических особенностей использовали питательные среды Чапека с концентрацией сахарозы 3%, агаризованное сусло и топливо ТС-1, штаммы выращивали при 25°С. Микроморфологию изучали на световом и электронном сканирующем микроскопах. Препараты для сканирующей микроскопии готовили из фрагментов среды с мицелием, которые фиксировали 1 ч в глутаральдегиде (2.5%), далее промывали три раза по 15 мин в фосфатном буфере, обезвоживали в серии спиртов (30, 50, 70, 80 и 96%) и помещали в ацетон. Образцы высушивали при критической точке, напыляли платино-палладиевой смесью (ионный распылитель Goko IB-3) и исследовали на сканирующих электронных микроскопах CamScan S2 и Jeol JSM-6380.
РЕЗУЛЬТАТЫ
Из четырех образцов пораженного топлива, взятых из баков самолетов, было выделено 18 видов микромицетов, относящихся к 8 родам (Krivushina et al., 2016). Во всех четырех образцах топлива был обнаружен “керосиновый гриб” A. resinae. Выделение большинства остальных видов грибов носило единичный характер. В образце “Краснодар” A. resinae значительно преобладал по частоте встречаемости на чашках Петри и по количеству колоний в них, в образце “Ульяновск” A. resinae оказался единственным выделенным видом. Образец “Иран” изначально представлял собой только слой топлива без видимых загрязнений. Но после нескольких месяцев хранения образца на дне емкости образовался небольшой мицелиальный сгусток диаметром несколько миллиметров, который, как позже выяснилось, принадлежал A. resinae. В четвертом образце “Китай”, помимо A. resinae, на чашках преобладали колонии еще одного вида – Monascus floridanus. Если о способности Amorphotheca resinae усваивать углеводороды авиационного топлива известно уже давно, то данных о росте в топливе Monascus floridanus найдено не было. В наших исследованиях было впервые показано, что выделенный штамм M. floridanus способен расти в авиационном топливе и на различных углеводородах наравне с Amorphotheca resinae (Krivushina, 2012; Krivushina et al., 2012).
Из пяти образцов топлива, прошедших экспозицию на экспериментальных площадках, было выделено 12 видов микромицетов, относящихся к 7 родам анаморфных аскомицетов (Krivushina et al., 2016). В двух образцах “Батуми” по частоте встречаемости на чашках Петри преобладал A. resinae, в образцах топлива “Сочи” микромицеты выделялись единично, а штаммы A. resinae не были обнаружены вовсе.
Далее у пяти штаммов A. resinae (Bat-1, Ir-12, К-68, Кr-42, Ul-1), выделенных из разных образцов топлива, были изучены их макро- и микроморфологические особенности при росте на среде Чапека, агаризованном сусле и в авиационном топливе ТС-1, результаты представлены в табл. 1–3.
Таблица 1.
Макроморфологические особенности изучаемых штаммов Amorphotheca resinae при росте на питательных средах
| Штамм | Цвет поверхности колонии | Характер поверхности колонии | Реверс колонии, цвет | Скорость роста на 10 день роста при 25°С | |||||
|---|---|---|---|---|---|---|---|---|---|
| Среда Чапека | Сусло-агар | Среда Чапека | Сусло-агар | Среда Чапека | Сусло-агар | Среда Чапека | Сусло-агар | ||
| Основной цвет | Диаметр центральной темной зоны | ||||||||
| Bat-1 | Оранжевато-ореховые, ближе к краю бесцветные | 2.5–3.0 | Орехово-коричневые, ближе к краю светлые | Тонкие, прижатые | Широкорастущие, плотные, “песчаные”, обильный белый воздушный мицелий | Темно-коричневый | Темно-коричневый | 3.5–4.0 | 4.0–4.5 |
| Ir-12 | 2.5–3.0 | Широкорастущие, плотные, “песчаные” | 3.5–4.0 | 4.5–5.0 | |||||
| K-68 | 1.2–1.5 | 3.0–3.5 | 4.0–4.5 | ||||||
| Kr-42 | 2.2–2.5 | 3.2–3.5 | 4.0–4.5 | ||||||
| Ul-1 | 2.5–3.0 | 3.5–4.0 | 4.5–5.0 | ||||||
Таблица 2.
Микроморфологические особенности изучаемых штаммов Amorphotheca resinae при росте на питательных средах (10-е сутки роста при 25°С)
| Штамм A. resinae | Наличие полового спороношения | Строение конидиальных головок | Характеристика рамоконидий | Характеристика конидий | ||||
|---|---|---|---|---|---|---|---|---|
| Строение | Форма, размер | Поверхность | Образование | Строение, форма, размер | Поверхность | |||
| Bat-1 | Не найдено | Конидиеносцы чаще метельчато или древовидно разветвленные, реже прямые, неразветвленные | Одноклетные, редко двухклетные | Цилиндрические, 8–20 мкм дл., 3–5 мкм шир. | Гладкие или слегка шероховатые | На рамоконидиях и конидиеносцах, в цепочке 1–2 штуки | Одноклетные, от эллипсоидных до яйцевидных, 3–6 × 2–3 мкм | Гладкие |
| Ir-12 | На рамоконидиях и конидиеносцах, в цепочке 1–3 штуки | |||||||
| K-68 | ||||||||
| Kr-42 | На рамоконидиях и конидиеносцах, в цепочке 1–2 штуки | |||||||
| Ul-1 | На рамоконидиях и конидиеносцах, в цепочке 1–3 штуки | |||||||
Таблица 3.
Морфологические особенности изучаемых штаммов Amorphotheca resinae при росте в топливе (20-е сутки роста при 25°С)
| Штамм A. resinae | Наличие полового спороношения | Внешняя характеристика мицелия | Характеристика рамоконидий | Характеристика конидий | Хламидоспоры | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| Цвет | Высота мицелиальной “пробки”, мм | Строение | Форма, размер | Поверхность | Образование | Строение, форма, размер | Поверхность | |||
| Bat-1 | Не найдено | Темно-коричневый | 5–9 | Одноклетные, редко двухклетные | Цилиндрические, 8–20 мкм дл., 3–5 мкм шир. | Гладкие или слегка шероховатые | На рамоконидиях и конидиеносцах | Одноклетные, от эллипсоидных до яйцевидных, 3–6 × 2–3 мкм | Гладкие | Апикальные и интеркалярные, 5–6 мкм диам. |
| Ir-12 | 7–10 | |||||||||
| K-68 | 5–9 | |||||||||
| Kr-42 | 7–10 | |||||||||
| Ul-1 | 8–12 | |||||||||
Как видно из табл. 1, при росте на питательных средах такие внешние признаки, как скорость роста колоний, цвет и характер их поверхности, окраска реверсивной стороны у всех пяти изученных штаммов A. resinae были приблизительно одинаковы. Отличия касались, в основном, лишь окраски центральной части колонии у данных грибов на среде Чапека (рис. 1). При росте на данной среде колонии изученных штаммов ближе к краю становились бесцветными, центральная часть оставалась более темной. У разных штаммов размеры центральной области и интенсивность ее окраски варьировали. Кроме того, для штамма A. resinae Bat-1 при росте на агаризованном сусле отмечен обильный воздушный мицелий белого цвета в виде радиальных линий, идущих от центра колоний к краю, что не встречено у других штаммов. Однако данные признаки не являются существенными для установления морфологических различий между изученными штаммами.
Рис. 1.
Внешний вид колоний штаммов Аmorphotheca resinae на среде Чапека (левая колонка) и на агаризованном сусле (правая колонка) после 10 суток роста при 25°С: а, б – штамм Bat-1; в, г – штамм Ir-12; д, е – штамм K-68; ж, з – штамм Kr-42; и, к – штамм Ul-1.

Согласно полученным данным (табл. 2) изученные штаммы A. resinae также схожи по микроморфологическим особенностям. Все грибы активно спорулируют уже с первых дней роста. Такие основные признаки как строение, форма, размер, характер поверхности рамоконидий и конидий полностью идентичны у изученных культур (рис. 2). Также штаммы схожи по строению конидиальных головок, небольшие отличия можно выявить лишь по числу конидий в цепочках.
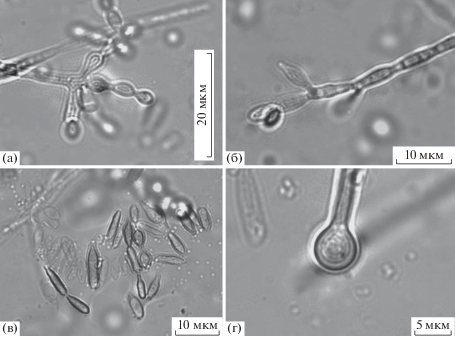
Рис. 2.
Конидиальное спороношение Аmorphotheca resinae на примере штамма Bat-1: а, б, в – ветвление конидиеносцев; г, д – рамоконидии и конидии.

При выращивании всех исследуемых штаммов A. resinae в пробирках с топливом и минеральной средой в большинстве случаев наблюдается небольшая задержка роста на начальных этапах развития, что соответствует литературным данным (Bilay, Koval, 1980). Первые признаки развития появляются на 7–10-е сутки, а на 18–21-е сутки образуются крупные мицелиальные сгустки на границе раздела водной и топливной фаз. Вначале сгустки светлоокрашенные, со временем они начинают темнеть и становятся темно-коричневыми (рис. 3). Через 20–30 суток, достигнув определенного размера, мицелиальные сгустки прекращают свой рост. Внешне они напоминают темную пробку между слоем топлива и минеральной среды. Диаметр такой мицелиальной пробки соотносится с диаметром пробирки, а высота колеблется от 5 до 12 мм в зависимости от активности штамма (табл. 3). При наклоне пробирки мицелиальная пробка не смещается, плотно зафиксирована между стеклянными стенками пробирки и препятствует перемешиванию слоев топлива и водно-минеральной среды. На этом примере наглядно видно, как может происходить закупорка трубчатых деталей топливных систем при развитии A. resinae, что является частой причиной сбоя техники.
Рис. 3.
Внешний вид мицелиального сгустка штамма Аmorphotheca resinae Ir-12 после одного месяца роста в пробирке с топливом и минеральной средой: 1 – слой топлива, 2 – мицелий, 3 – водно-минеральный слой.

Исследование фрагментов мицелиальных сгустков с помощью световой (рис. 4) и сканирующей электронной (рис. 5) микроскопии показало, что у штаммов A. resinae № К-68, Bat-1, Кr-42, Ul-1, Ir-12 при развитии в топливе образуются точно такие же конидиальные структуры, как и при росте на искусственных питательных средах. Определить количество конидий в цепочке при росте гриба в топливе не представляется возможным, поскольку в жидкой среде цепочки конидий очень быстро распадаются. Как видно из табл. 3, все остальные основные морфологические признаки у выделенных штаммов полностью совпадают.
ОБСУЖДЕНИЕ
Из литературы известно, что существуют четыре формы конидиальной стадии A. resinae. Описаны они были в то время, когда эпитет “Cladosporium resinae” активно использовался для обозначения анаморфы “керосинового гриба”, соответственно, его формы имеют названия Cladosporium resinae f. avellaneum, C. resinae f. resinae, C. resinae f. albidum и C. resinae f. sterile (Sheridan et al., 1972; Sheridan, Troughton, 1972; Levkina, Rebrikova, 1976). Согласно литературным данным, формы отличаются между собой, в основном, по внешним морфологическим признакам и частично по строению конидиального аппарата.
В своей работе, помимо сравнения изучаемых штаммов между собой, мы решили рассмотреть вопрос о принадлежности изучаемых штаммов к одной из форм на основании макро- и микроморфологических признаков.
Для форм “керосинового гриба” были установлены различия в первую очередь по цвету и характеру поверхности колоний (Levkina, Rebrikova, 1976). Согласно описаниям колонии f. avellaneum светло-коричневые, при старении с оранжевым оттенком, часто с белым краем, прижатые и плотные. Колонии f. resinae темно-коричневые с оливково-зеленым оттенком, рыхлые, пушистые. Для f. albidum характерен белый цвет колоний, у f. sterile колонии пигментированные, но не спороносящие (Sheridan et al., 1972). Кроме того, известно, что существуют и промежуточные варианты между всеми формами по внешним морфологическим признакам. Эти вариации, наряду с физиологическими различиями по способности усваивать углеводороды топлива, создают трудности для определения гриба до формы (Sheridan, Troughton, 1972). Как правило, из топлив выделяли f. avellaneum, но чаще в литературе нет ссылок на форму. Обычно идентификация заканчивается на уровне вида (Levkina, Rebrikova, 1976). Штаммы, выделенные нами, по внешнему виду колоний более соответствуют форме f. avellaneum, хотя этот признак довольно нестабильный.
Известно, что у f. avellaneum и f. resinae имеется разница в строении конидиальных головок. F. avellaneum характеризуется прямыми, простыми, неразветвленными, но компактными конидиеносцами, f. resinae – метельчато- или древовидно-разветвленными конидиеносцами (Levkina, Rebrikova, 1976). Попытка решить вопрос о принадлежности изучаемых штаммов к одной из форм на основании строения конидиального аппарата привела к обнаружению в культурах пяти изучаемых штаммов вариаций конидиальных головок, характерных для обеих форм (табл. 3). Это согласуется с данными литературы, в которой авторы отмечают довольно частую встречаемость конидиального аппарата, промежуточного между f. avellaneum и f. resinae. (Sheridan et al., 1972). Все остальные микроморфологические признаки, представленные в табл. 2, соответствуют описаниям в имеющихся определителях (Ellis, 1971; Domsch et al., 2007; Lugauskas et al., 1987), причем они характерны как для f. avellaneum, так и для f. resinae (Sheridan, Troughton, 1972; Domsch et al., 2007; Crous et al., 2007).
Таким образом, признаки форм “керосинового гриба” довольно нестабильны. Это касается и внешнего вида колоний, и строения конидиального аппарата. В связи с этим, подобно ряду авторов, занимающихся изучением данного вида, мы не относим выделенные штаммы Аmorphotheca resinae к какой-либо конкретной форме, а считаем выделение данных форм в целом нецелесообразным.
В отношении морфологических особенностей изученных грибов при росте в топливе, также не выявлены различия между штаммами в строении конидиального аппарата. Кроме того, показано, что при развитии в топливе у A. resinae образуются точно такие же конидиальные структуры, как и при росте на искусственных питательных средах. Это в очередной раз подтверждает тот факт, что среда, содержащая углеводороды авиационного топлива, является благоприятной для развития A. resinae. Быстрые темпы развития мицелиальной биомассы при росте в топливе, образование хорошо развитых конидиальных структур, а также частая встречаемость “керосинового гриба” в образцах авиационного топлива свидетельствуют о том, что A. resinae до настоящего времени является преобладающим видом в данной специфической среде и может стать причиной микробиологического поражения топлив и выхода из строя топливных систем.
Работа выполнена в рамках Государственного задания, части 2 п. 01 10 (тема № АААА-А16-116021660084-1 “Биологическое разнообразие и экология грибов и лишайников как основа рационального природопользования”) с использованием приборной базы Центра коллективного пользования научным оборудованием “Лаборатория электронной микроскопии биологического факультета МГУ (Electron microscopy laboratory of Moscow State University Biology Faculty)”. Работа является частью Соглашения о научно-техническом сотрудничестве между федеральным государственным бюджетным образовательным учреждением высшего образования “Московский государственный университет имени М.В. Ломоносова” и федеральным государственным унитарным предприятием “Всероссийский научно-исследовательский институт авиационных материалов” от 28.04.2015 г.
Список литературы
Andreyuk E.I., Bilay V.I., Koval E.Z. Microbial corrosion and its agents. Naukova dumka, Kiev, 1980 (in Russ.).
Bilay V.I. The Fusaria. Naukova dumka, Kiev, 1977 (in Russ.).
Bilay V.I., Koval E.Z. The growth of fungi on oil hydrocarbons. Naukova dumka, Kiev, 1980 (in Russ.).
Booth C. Fusarium: Laboratory guide to the identification of the major species. Commonwealth Mycological Institute, Kew, Surrey, 1977.
Crous P.W., Braun U., Schubert K., Groenewald J.Z. Delimiting Cladosporium from morphologically similar genera. Stud. Mycol. 2007. V. 58. P. 33–56.
Domsch K.H., Gams W., Anderson T.H. Compendium of soil fungi. 2nd ed. Lubrecht and Cramer Ltd, Eching, 2007.
Dudka I.A., Wasser S.P., Elanskaya I.A. Methods of experimental mycology. Naukova dumka, Kiev, 1982 (in Russ.).
Ellis M.V. Dematiaceous Hyphomycetes. Kew, Surrey, 1971.
Ferrari M.D., Neirotti E., Albornoz C. Occurrence of heterotrophic bacteria and fungi in an aviation fuel handling system and its relationship with fuel fouling. Rev. Argentina Microbiol. 1998. V. 30. P. 105–114
Gams W. Phialophora and some similar morphologically little-differentiated anamorphs of divergent ascomycetes. Stud. Mycol. 2000. V. 45. P. 187–199.
Gams W., Holubova-Jechova V. Chloridium and some other dematiaceous Hyphomycetes growing on decaying wood. Stud. Mycol. 1976. V. 13. P. 59–71.
Hamme J.D.V., Singh A., Ward O.P. Recent advances in petroleum microbiology. Microbiol. Molec. Biol. Rev. 2003. V. 67(4). P. 503–549.
Hoog G.S. de, Guarro J., Gene J., Figueras M.J. Atlas of cli-nical fungi. CBS, Utrecht, 2000.
Index Fungorum. http://www.indexfungorum.org. 2017. Accessed 22.03.2017.
Koval E.Z., Sidorenko L.P. Mycodestructors of industrial materials. Naukova dumka, Kiev, 1989 (in Russ.).
Krivushina A.A. Micromycetes in aviation fuel. Abstract of Cand. Biol. Thesis. Moscow, 2012 (in Russ.).
Krivushina A.A., Chekunova L.N., Mokeeva V.L., Polyakova A.V. Study of micromycetes isolated from exploiting plane fuel tanks. Mikologiya i fitopatologiya. 2016. V. 50 (2). P. 108–114 (in Russ.).
Krivushina A.A., Chekunova L.N., Polyakova A.V. New “kerosene” fungus Monascus floridanus. In: Sovremennaya mikologiya v Rossii. T 3. Materialy III Syezda mikologov Rossii. Moskva, 2012. P. 221 (in Russ.).
Levkina L.M., Rebrikova N.L. Physiological properties of Cladosporium resinae (Lindau) de Vries. Mikologiya i fitopatologiya. 1976. V. 10 (5). P. 374–380 (in Russ.).
Lugauskas A.Y., Mikulskene A.I., Shlyauzhene D.Yu. Catalogue of micromycetes – biodestructors of polymer materials. Nauka, Moscow, 1987 (in Russ.).
McVea G.G., Solly R.K. Control of fuel microorganisms with magnetic devices: laboratory investigation with Hormoconis resinae. Aircraft Materials Technical Memorandum. 1991. V. 408. P. 1–11.
Polyakova A.V., Krivushina A.A., Goryashnik J.S., Buharev G.M. Microbiological resistance tests in natural conditions of different climatic zones. Trudy VIAM. 2016. V. 4. P. 12.
Polyakova A.V., Krivushina A.A., Goryashnik J.S., Yako-venko T.V. Microbiological resistance tests in warm and humid climates. Trudy VIAM. 2013. V. 7. P. 6.
Pomortseva N.V., Nette I.T., Liber L.I. Formation of vitamin B6 by fungus Cladosporium resinae. Prikladnaya biokhimiya i mikrobiologiya. 1977. V. 13 (5). P. 718–721 (in Russ.).
Raper K.B., Fennell D.I. The genus Aspergillus. The Williams and Wilkins Company, Baltimore, 1965.
Raper K.B., Thom C., Fennell D.I. A manual of the Penicillia. Hafner Publishing Company, N.Y.; London, 1968.
Rauch M.E., Graef H.W., Rozenzhak S.M., Jones S.E., Bleckmann C.A., Kruger R.L., Naik R.R. Characterization of microbial contamination in United States air force aviation fuel tanks. J. Industr. Microbiol. Biotechnol. 2006. V. 33 (1). P. 29–36.
Seifert K.A., Hughes S.J., Boulay H., Louis-Seize G. Taxonomy, nomenclature and phylogeny of three cladosporium-like hyphomycetes, Sorocybe resinae, Seifertia azaleae and the Hormoconis anamorph of Amorphoteca resinae. Stud. Mycol. 2007. V. 58. P. 235–245.
Semenov S.A., Gumargaliyeva K.Z., Zaikov G.E. Biodeterioration of materials and technology product. Gorenie, destruktsiya i stabilizatsiya polimerov. Nauchnye osnovy i tekhnologii. SPb., 2008. P. 73–99 (in Russ.).
Sheridan J.E., Tan Y.L., Nelson J. Studies on the “kerosene fungus” Cladosporium resinae (Lindau) de Vries. Part III. Morphology, taxonomy and physiology. Tuatara. 1972. V. 19 (3). P. 130–165.
Sheridan J.E., Troughton J.H. Conidiophores and conidia of the kerosene fungus Cladosporium resinae in the light and scanning electron microscopes. New Zealand J. Bot. 1972. V. 11. P. 145–152.
Sinadskiy Yu.V. The first international symposium on biodeterioration. Mikologiya i fitopatologiya. 1969. V. 3. P. 394–400 (in Russ.).
Watanabe T. Pictorial Atlas of soil and seed fungi: morphologies of cultured fungi and key to species. Lewis Publishers, Boca Raton etc., 1994.
Андреюк Е.И., Билай В.И., Коваль Э.З., Козлова И.А. (Andreyuk et al.) Микробная коррозия и ее возбудители. Киев: Наукова думка, 1980. 288 с.
Билай В.И. (Bilay) Фузарии. Киев: Наукова думка, 1977. 443 с.
Билай В.И., Коваль Э.З. (Bilay, Koval) Рост грибов на углеводородах нефти. Киев: Наукова думка, 1980. 340 с.
Дудка И.А., Вассер С.П., Эланская И.А. (Dudka et al.) Методы экспериментальной микологии. Киев: Наукова думка, 1982. 550 с.
Коваль Э.З., Сидоренко Л.П. (Koval, Sidorenko) Микодеструкторы промышленных материалов. Киев: Наукова думка, 1989. 187 с.
Кривушина А.А. (Krivushina) Микромицеты в авиационном топливе: автореф. дис. … канд. биол. наук. М., 2012. 24 с.
Кривушина А.А., Чекунова Л.Н., Полякова А.В. (Krivushina et al.) Новый “керосиновый” гриб Monascus floridanus // Современная микология в России. Том 3. Материалы III съезда микологов России. М.: Национальная академия микологии, 2012. С. 221.
Кривушина А.А., Чекунова Л.Н., Мокеева В.Л., Полякова А.В. (Krivushina et al.) Изучение микромицетов, обнаруженных в топливных баках эксплуатирующихся самолетов // Микология и фитопатология. 2016. Т. 50. Вып. 2. С. 108–114.
Левкина Л.М., Ребрикова Н.Л. (Levkina, Rebrikova) Физиологические особенности Cladosporium resinae (Lindau) de Vries // Микология и фитопатология. Т. 10. Вып. 5. 1976. С. 374–380.
Лугаускас А.Ю., Микульскене А.И., Шляужене Д.Ю. (Lugauskas et al.) Каталог микромицетов – биодеструкторов полимерных материалов. М.: Наука, 1987. С. 258–259.
Полякова А.В., Кривушина А.А., Горяшник Ю.С., Бухарев Г.М. (Polyakova et al.) Испытания на микробиологическую стойкость в натурных условиях различных климатических зон // Труды ВИАМ. 2016. № 4. С. 12.
Полякова А.В., Кривушина А.А., Горяшник Ю.С., Яковенко Т.В. (Polyakova et al.) Испытания на микробиологическую стойкость в условиях теплого и влажного климата // Труды ВИАМ. 2013. № 7. С. 6.
Поморцева Н.В., Нетте И.Т., Либер Л.И. (Pomortseva et al.) Образование витамина В6 грибом Cladosporium resinae // Прикладная биохимия и микробиология. 1977. Т. 13. № 5. С. 718–721.
Семенов С.А., Гумаргалиева К.З., Заиков Г.Е. (Semenov et al.) Биоповреждения материалов и изделий техники // Горение, деструкция и стабилизация полимеров. СПб.: Научные основы и технологии, 2008. С. 73–99.
Синадский Ю.В. (Sinadskiy) Первый международный симпозиум по биологическим повреждениям // Микология и фитопатология. 1969. Т. 3. С. 397–400.
Дополнительные материалы отсутствуют.
Инструменты
Микология и фитопатология