Российские нанотехнологии, 2021, T. 16, № 5, стр. 688-693
БИОМАРКЕР ДЛЯ ИДЕНТИФИКАЦИИ РЫБНЫХ ПРОДУКТОВ В ОСТАТКАХ НА ПОВЕРХНОСТИ АРХЕОЛОГИЧЕСКОЙ КЕРАМИКИ
В. М. Пожидаев 1, *, Е. С. Азаров 2, Н. П. Бабиченко 1, П. К. Кашкаров 1, Е. Б. Яцишина 1
1 Национальный исследовательский центр “Курчатовский институт”
Москва, Россия
2 Исторический музей
Москва, Россия
* E-mail: pojidaev2006@yandex.ru
Поступила в редакцию 09.07.2020
После доработки 11.08.2020
Принята к публикации 18.08.2020
Аннотация
Фрагменты керамики – одна из самых распространенных находок при археологических раскопках. Определение характера использования керамических сосудов является важным для понимания повседневной жизни древних обществ. Идентификация остатков пищи на поверхности глиняных сосудов дает ценную информацию о способах их использования и пищевых пристрастиях древних людей. С помощью метода газовой хроматографии/масс-спектрометрии исследованы продукты окисления растительных масел и животных жиров и показано, что в процессе окислительной деструкции кратной связи жирных кислот образуются дикарбоновые кислоты, которые являются биомаркерами исходных жиров в остатках на древней керамике. Одним из основных продуктов окисления рыбьего жира является дикарбоновая янтарная кислота, которая может служить биомаркером рыбных остатков на древней керамике. Для уточнения атрибуции древних глиняных сосудов исследованы 63 образца органических остатков с поверхности фрагментов керамики из археологических памятников. В остатках на фрагментах 26 древних сосудов обнаружена янтарная кислота, что послужило доказательством их использования для приготовления пищи из рыбных продуктов.
ВВЕДЕНИЕ
Керамические изделия имели очень большое значение в древнем хозяйстве. Различные предметы из глины сопровождают человека не только в течение всей его жизни, но и присутствуют в качестве погребального инвентаря или дара при устройстве погребений. Фрагменты керамики – одна из самых распространенных находок при раскопках археологических памятников. Керамика является важным носителем информации: по ней можно определить размеры посуды, состав обожженной глины, установить технологию гончарного производства и традиции определенных обществ в декорировании изделий из глины.
Определение характера использования керамических сосудов является важным для понимания повседневной жизни, торговли и погребальных обычаев древних обществ. Остатки пищи часто обнаруживаются на поверхности древних глиняных сосудов. Идентификация этих остатков методами аналитической химии помогает определить назначение сосудов и дает ценную информацию о способах их использования и пищевых пристрастиях древних людей [1–6].
МАТЕРИАЛЫ И МЕТОДЫ
Реагенты. Все использованные растворители и реактивы имели квалификацию “х. ч.” или “для ВЭЖХ”.
Подготовка образцов. Окисление жиров и масел. К навеске около 0.05 г масла или жира добавляли 3 мл метилового спирта и 100 мкл 30%-ного раствора перекиси водорода. Реакционную смесь нагревали с обратным холодильником на песчаной бане (при 80°С). Через 1, 3 и 5 ч реакционную смесь охлаждали до комнатной температуры, отбирали 0.5 мл для получения метиловых эфиров жирных кислот.
Получение метиловых эфиров жирных кислот (МЭЖК). К 0.5 мл реакционной смеси добавляли 0.5 мл 2%-ного раствора серной кислоты в метаноле и нагревали с обратным холодильником в течение трех часов. По окончании нагревания охлаждали до комнатной температуры, добавляли 5 мл диэтилового эфира и 3 мл воды. Реакционную смесь встряхивали в течение 5 мин. Слои разделяли, отделяли верхний эфирный слой. Эфир удаляли до сухого остатка и растворяли в 0.5 мл н-гексана.
Извлечение и дериватизация остатков органических веществ из фрагментов керамики. К навеске около 200 мг порошка образца, полученного механическим соскабливанием с поверхности керамики, добавляли 0.5 мл 2%-ного раствора серной кислоты в метаноле и нагревали с обратным холодильником в течение трех часов. По окончании нагревания реакционную смесь охлаждали до комнатной температуры, добавляли 5 мл диэтилового эфира, 3 мл воды и встряхивали в течение 5 мин. Слои разделяли, отделяли верхний эфирный слой. Эфир удаляли током азота до сухого остатка и растворяли в 100 мкл гексана.
Аппаратура и вспомогательное оборудование. Анализ проводили методом газовой хроматографии–масс-спектрометрии (ГХ/МС) на газовом хроматографе НР-6890 с масс-спектрометрическим детектором MSD 5975 фирмы Agilent Technologies. Условия хроматографирования: колонка капиллярная НР-5ms длиной 30 м и внутренним диаметром 0.25 мм, толщина пленки неподвижной фазы 0.25 мкм. Начальная температура колонки 80°С (выдержка 4 мин); программирование температуры от 80 до 280°С со скоростью 4°С/мин. Выдержка при конечной температуре 10 мин. Газ-носитель – гелий, 1 мл/мин, деление потока 1:10. Температура испарителя 280°С, линии переноса детектора 280°С. Объем пробы 1 мкл. Детектирование проводили методом ионизации электронным ударом в режиме сканирования по полному ионному току в диапазоне 50–900 а.е.м. Скорость сканирования – 1.76 скан/с, энергия ионизации 70 эВ, температура квадруполя и источника ионов – 150 и 230°С.
Идентификацию соединений осуществляли с использованием масс-спектров базы данных NIST/EPA/NIH mass spectral library 2014.
Анализ МЭЖК проводили на газовом хроматографе фирмы Bruker модели 430GС с пламенно-ионизационным детектором на кварцевой капиллярной колонке SelectTM Biodisel for FAME длиной 30 м и внутренним диаметром 0.32 мм, толщина пленки неподвижной фазы 0.25 мкм. Температурная программа колонки: начальная температура – 140°C, выдержка 4 мин, повышение температуры до 250°C со скоростью 4°C/мин и выдержка в изотермическом режиме в течение 10 мин при 250°C. Температура инжектора – 260°C, детектора – 260°C. Скорость потока газа-носителя (азота) 20 мл/мин, деление потока 1: 10. Объем пробы 2 мкл. Идентификацию МЭЖК проводили с использованием стандартной смеси МЭЖК SP-37 (Supelco 37 Component FAME Mix), содержащей в своем составе метиловые эфиры 37 жирных кислот (ЖК) разного строения.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Исследование органических остатков на поверхности древних керамических сосудов в основном проводят после экстрагирования липидных компонентов с поверхности артефактов различными растворителями [1–6]. В качестве растворителей используют хлороформ, метиленхлорид, гексан, петролейный эфир, метанол и их смеси. Наиболее часто используется смесь растворителей, предложенная в [7]: хлороформ–метанол (2: 1). Липиды, извлеченные по методу Фолча, достаточно полно отражают изначальный состав остатков жиров в исследуемых керамических сосудах [7].
При длительном захоронении в земле жиры подвергаются деградации. В литературе предложено несколько схем механизмов окислительной деградации жиров, но пока на этот счет нет единого мнения. Основной путь деградации включает в себя образование низкомолекулярных компонентов в результате свободно-радикальных реакций окисления двойной связи ненасыщенных ЖК липидов. Первичным результатом химических изменений при деградации остатков жиров в качестве основных продуктов образуются гидрокси- и дигидроксипроизводные соответствующих ненасыщенных ЖК, которые в дальнейшем распадаются на более стабильные дикарбоновые кислоты (ДК). Образование ДК происходит в процессе разрыва углерод-углеродной двойной связи [8–13].
В [9–11] при исследовании состава остатков на археологических керамических изделиях методом ГХ/МС обнаружено значительно меньшее содержание ДК и гидроксикислот, которые можно было ожидать исходя из стехиометрических соотношений. На этом основании можно предположить, что продукты окисления вымываются с поверхности археологической керамики во время захоронения путем выщелачивания подземными водами или химически связываются в полимерные продукты в результате реакции поликонденсации образующихся продуктов окисления. Последующей щелочной обработкой остатков керамики после экстракции растворителями было выделено дополнительное количество продуктов окисления: дикарбоновых кислот C7–C12 со значительным преобладанием азелаиновой (ДК-9) кислоты, а также 9- и 10-гидроксиоктадекановых и двух изомеров 9,10-дигидроксиоктадекановой кислот. По-видимому, основным путем сохранения продуктов окислительной деградации липидов является связывание их в полимерную матрицу. При экстракции органическими растворителями извлекается лишь часть органических остатков с поверхности образца. При обработке керамики спиртовой щелочью полимерная матрица расщепляется на исходные мономеры [11–13], что приводит к выделению дополнительного количества продуктов окисления.
Дикарбоновые кислоты образуются при полной деструкции кратной связи, ближайшей к карбоксильной группе. Образование конкретной ДК зависит от положения кратной связи в молекуле исходной ЖК. Продукты окислительной деструкции ненасыщенных ЖК, сопровождающейся разрывом углерод-углеродной двойной связи, приведены в табл. 1.
Таблица 1.
Продукты окислительной деструкции ненасыщенных жирных кислот, животных жиров и растительных масел, сопровождающейся разрывом углерод-углеродной двойной связи
| Ненасыщенная жирная кислота | Формула (положение кратных связей) | Дикарбоновая кислота |
|---|---|---|
| Миристолеиновая | С14:1 (9) | Нонандиовая С9 (азелаиновая) |
| Пальмитолеиновая | С16:1 (9) | Азелаиновая С9 |
| Олеиновая | С18:1 (9) | Азелаиновая С9 |
| Линолевая | С18:2 (9, 12) | Азелаиновая С9 |
| Линолевая конъюгированная | С18:2 (9, 11) | Азелаиновая С9 |
| α-Линоленовая | С18:2 (9, 12, 15) | Азелаиновая С9 |
| γ-Линоленовая | С18:2 (6, 9, 12) | Гександиовая С6 |
| Арахидоновая | С20:4 (5, 8, 11, 14) | Пентадиовая С5 (глутаровая) |
| Эйкозапентаеновая | С20:5 (5, 8, 11, 14, 17) | Глутаровая С5 |
| Докозапентаеновая | С22:5 (7, 10, 13, 16, 19) | Гептандиовая С7 (пимелиновая) |
| Докозагексаеновая | С22:6 (4, 7, 10, 13, 16, 19) | Бутандиовая С4 (янтарная) |
Положение кратной связи у девятого атома углерода характерно для многих ненасыщенных кислот, входящих в состав растительных и животных жиров, поэтому азелаиновая кислота преобладает во всех жировых остатках с поверхностей исследуемых глиняных черепков.
Дикарбоновые кислоты достаточно стабильны к окислительной деградации при длительных захоронениях и могут служить биомаркерами исходных жиров в остатках на древней керамике. Образование азелаиновой кислоты не является специфическим фактором, отражающим присутствие какой-либо индивидуальной ЖК в остатках. Согласно данным табл. 1 можно отметить, что образование специфических ДК возможно только при полной окислительной деструкции полиненасыщенных жирных кислот (ПНЖК), присутствие которых характерно исключительно для рыбных продуктов.
Для подтверждения гипотезы образования ДК проведено исследование окисления некоторых растительных масел и животных жиров. Продукты окисления переводили в МЭЖК и анализировали методом ГХ. Результаты исследования процесса окисления животных жиров и растительных масел представлены в табл. 2.
Таблица 2.
Результаты исследования процесса окисления животных жиров и растительных масел
| Масло/жир | Вре- мя, ч | ДК-4 | 14:0 | ДК-9 | 16:0 | 16:1 | 18:0 | 18:1 | 18:2 | 20:5 | 22:6 | 9-окси | 10-окси | Эритро- | Трео- | P/S |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Коровье масло | 0 | – | 8.7 | – | 28.9 | 1.6 | 11.6 | 24.4 | 3.7 | – | – | – | – | – | – | 2.5 |
| 3 | – | 8.8 | 0.8 | 28.8 | 1.4 | 11.7 | 17.0 | 2.3 | – | – | 2.2 | 2.3 | 1.3 | 1.4 | 2.5 | |
| 5 | – | 8.8 | 3.6 | 28.9 | 1.2 | 11.7 | 11.6 | 1.1 | – | – | 2.9 | 3.0 | 0.3 | 0.3 | 2.5 | |
| Оливковое масло | 0 | – | – | – | 14.6 | 1.1 | 2.8 | 72.8 | 7.9 | – | – | – | – | – | – | 5.2 |
| 3 | – | – | 2.5 | 14.7 | 1.0 | 2.9 | 49.8 | 4.9 | – | – | 6.4 | 6.3 | 3.5 | 3.6 | 5.1 | |
| 5 | – | – | 12.6 | 14.7 | 0.9 | 2.9 | 35.1 | 2.3 | – | – | 7.5 | 7.6 | 0.8 | 0.9 | 5.1 | |
| Подсолнеч-ное масло | 0 | – | – | – | 7.8 | 0.1 | 3.0 | 25.7 | 63.1 | – | – | – | – | – | – | 2.6 |
| 3 | – | – | 8.7 | 7.9 | 0.1 | 3.1 | 17.2 | 38.2 | – | – | 7.4 | 7.5 | 3.9 | 4.0 | 2.5 | |
| 5 | – | – | 14.2 | 7.8 | – | 3.1 | 11.9 | 18.6 | – | – | 9.2 | 9.1 | 1.2 | 1.3 | 2.5 | |
| Рыбий жир | 0 | – | 11.3 | – | 21.9 | 10.0 | 4.2 | 15.3 | 2.6 | 9.1 | 12.7 | – | – | – | – | 5.2 |
| 3 | 0.8 | 11.5 | 0.6 | 22.1 | 9.0 | 4.2 | 10.7 | 1.6 | 3.6 | 2.5 | 2.9 | 3.1 | 0.8 | 0.9 | 5.2 | |
| 5 | 1.4 | 11.6 | 3.4 | 22.3 | 8.6 | 4.3 | 7.4 | 0.8 | – | – | 2.0 | 2.1 | 0.5 | 0.6 | 5.2 |
Из результатов, приведенных в табл. 2, видно, что при окислении жиров и масел содержание ненасыщенных кислот в триацилглицеридах уменьшается. Это сопровождается образованием ДК. Конечным продуктом полного окисления исследуемых жиров и масел является азелаиновая кислота. Содержание ДК пропорционально уменьшению содержания большинства ненасыщенных ЖК животных жиров и растительных масел.
Остатки рыбных продуктов редко обнаруживаются в органических остатках на древней керамике. В состав ацилглицеридов рыбьего жира входят ПНЖК – эйкозапентаеновая и докозагексаеновая, которые могли бы выступить в роли биомаркеров рыбных продуктов. Содержание докозагексаеновой кислоты в рыбьем жире может достигать 15%. Однако ПНЖК значительно сильнее подвержены окислительной деградации в процессе длительного захоронения, чем основные ненасыщенные кислоты жиров и масел. Поэтому в остатках из керамических сосудов полиненасыщенные кислоты никогда не обнаруживаются. В настоящее время факт их наличия методом ГХ/МС устанавливается в основном за счет выявления промежуточных производных соответствующих ненасыщенных ЖК [14]. Однако такие соединения также не являются стабильными.
При полной окислительной деструкции докозагексаеновой кислоты, преобладающей в составе ПНЖК рыбьего жира, образуется янтарная кислота, которая более устойчива к деградации при длительных захоронениях и поэтому могла бы служить биомаркером остатков рыбных пищевых продуктов. На практике ДК не обнаруживается и в органических остатках древних глиняных сосудов. Причиной этого является хорошая растворимость янтарной кислоты в воде – 6.8/100 г (для сравнения растворимость азелаиновой кислоты – 0.24/100 г) [15]. В результате чего она вымывается из органических остатков с поверхности артефактов.
Благодаря более сильной кислотности (относительно угольной кислоты) янтарная кислота способна реагировать с карбонатами щелочноземельных металлов (Ca, Mg), присутствующих в почвенных породах. Соли янтарной кислоты (сукцинаты кальция и магния) хуже растворимы в воде, чем сама кислота [15]. Образование сукцинатов металлов препятствует вымыванию янтарной кислоты грунтовыми водами и тем самым способствует ее сохранности в органических остатках на поверхности археологической керамики.
Таким образом, возможны два основных пути сохранения продуктов окислительной деградации липидов: связывание гидрокси- и дикарбоновых кислот в полимерную матрицу и образование солей щелочноземельных металлов с некоторыми ДК (С4–С5). Для экстракции жировых остатков с поверхности глиняных сосудов и их фрагментов чаще всего используют органические растворители и спиртовую щелочь. Сукцинаты щелочноземельных металлов не растворимы в органических растворителях и не реагируют с растворами спиртовой щелочи, по этой причине не извлекаются с поверхности керамики и не обнаруживаются в остатках.
Для извлечения жировых остатков с поверхности древней керамики использовали 2%-ный раствор серной кислоты в метаноле. При таком способе обработки образцов керамики практически одновременно протекают четыре процесса: извлечение органических остатков, разрушение полимерной матрицы, кислотный гидролиз ацил-глицеридов и этерификация ЖК метиловым спиртом. Серная кислота реагирует с сукцинатами щелочноземельных металлов с образованием свободной янтарной кислоты, которая этерифицируется метиловым спиртом и таким образом обнаруживается методом газовой хроматографии. Благодаря использованию этого способа извлечения жировых остатков с поверхности археологической керамики янтарная кислота может служить биомаркером наличия остатков рыбных продуктов в исследуемых древних сосудах.
Для идентификации возможного наличия остатков рыбных продуктов были исследованы 63 фрагмента керамики от 56 сосудов из раскопок восьми многослойных археологических памятников экспедициями Исторического музея в разное время на территории Рязанской и Ярославской областей. Большинство из исследуемых образцов принадлежит к бронзовому веку (конец III–II тыс. до до н.э.) – 43 образца. Остальные образцы относятся как к более раннему периоду неолита (6 образцов, VI–IV тыс. до н.э.), так и к более позднему раннему железному веку (10 образцов) и средневековью (4 образца).
Хроматограмма органических остатков с поверхности одного из исследуемых фрагментов керамики приведена на рис. 1.
Рис. 1.
Хроматограмма органических остатков одного из исследуемых фрагментов керамики. Отнесение пиков: 1 – янтарная (ДК-4), 2 – глутаровая (ДК-5), 4 – адипиновая (ДК-6), 5 – пимелиновая (ДК-7), 6 – субериновая (ДК-8), 9 – азелаиновая (ДК-9), 10 – миристиновая (С14:0), 11 – пальмитиновая (С16:0), 12 – стеариновая (С18:0) кислоты; 3, 7, 8 – эфиры фталевой кислоты (современные антропогенные загрязнители).
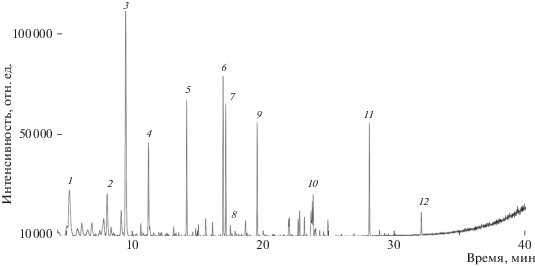
В жирно-кислотных профилях остатков с поверхности исследованных фрагментов керамики преобладали насыщенные ЖК – С16:0 (пальмитиновая) и С18:0 (стеариновая), в значительно меньших количествах обнаружены С12:0 (лауриновая), С14:0 (миристиновая), а также ЖК с нечетным числом атомов углерода – С15:0 (пентадекановая), С17:0 (маргариновая). Обнаружение кислот С15:0 и С17:0 характерно для жвачных животных [14]. Такие кислоты образуются в пищеварительном тракте животных с многокамерным желудком под воздействием бактерий [16, 17]. Значение С16:0/С18:0 (P/S) в жировых остатках с поверхности исследуемых фрагментов керамики находятся в диапазоне 0.5–4.5.
Ненасыщенные ЖК подвержены окислительной деградации в процессе длительного захоронения. Насыщенные кислоты более устойчивы к этому процессу. Относительное содержание насыщенных кислот (пальмитиновой и стеариновой, пальмитиновой и миристиновой) практически не изменяется со временем захоронения. Поэтому для идентификации жиров в органических остатках археологических образцов рядом исследователей было предложено использовать соотношение содержания насыщенных ЖК [16–18]. Наиболее широко для этого используется соотношение содержания пальмитиновой и стеариновой кислот (коэффициент P/S). В [18] было отмечено, что величина этого коэффициента менее 2.3 характерна для продуктов животного происхождения. Для растительной пищи и рыбных продуктов величина P/S, как правило, больше 2.3. В остатках на поверхности 26 фрагментов исследуемой керамики величина P/S больше 2.3, что позволяет сделать вывод о возможном использовании растительных и/или рыбных продуктов в этих сосудах. Достоверная идентификация растительной пищи по величине соотношения содержания пальмитиновой и стеариновой кислот возможна только при отсутствии других критериев, которые характеризуют животные жиры: наличие лауриновой и миристиновой кислот, а также ЖК с нечетным числом атомов углерода. Миристиновая кислота, а также кислоты с нечетным числом атомов углерода (С15:0, С17:0) обнаружены в жировых остатках всех исследуемых фрагментов керамики. Это позволяет утверждать, что ни один из исследуемых глиняных сосудов не использовался для приготовления только растительной пищи.
В остатках на фрагментах керамики обнаружены дикарбоновые кислоты: нонандиовая (азелаиновая, С9), октандиовая (С8), гептандиовая (С7), гександиовая (С6), в том числе в 26 образцах – бутандиовая (янтарная, С4). Как отмечалось ранее, янтарная кислота может образоваться при окислительной деструкции докозагексаеновой ЖК, которая присутствует исключительно в рыбных продуктах. Таким образом, обнаружение янтарной кислоты в органических остатках на древней керамике может служить доказательством использования этих глиняных сосудов для приготовления пищевых продуктов из рыбы. Рыболовство являлось одним из традиционных способов добывания пищи в древности, особенно учитывая расположения практически всех археологических памятников по берегам различных водоемов. Помимо изучения пищевых пристрастий выявление рыбных продуктов в органических остатках позволяет оценить значение рыболовства в экономике конкретных древних обществ.
ЗАКЛЮЧЕНИЕ
Методом ГХ/МС исследованы продукты окисления растительных масел и животных жиров. Показано, что в процессе окислительной деструкции кратной связи ненасыщенных жирных кислот образуются дикарбоновые кислоты. Одним из продуктов окисления рыбьего жира, содержащего докозагексаеновую кислоту, является янтарная кислота, которая может служить биомаркером рыбных остатков на древней керамике.
Для уточнения атрибуции древних глиняных сосудов были исследованы 63 фрагмента керамики из археологических памятников разного времени. В остатках на 26 керамических фрагментах была обнаружена янтарная кислота, что послужило доказательством использования этих глиняных сосудов для приготовления пищи из рыбных продуктов.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (грант № 17-29-04100 офи-м).
Список литературы
Evershed R.P., Dudd S.N., Copley M.S. et al. // Chemistry of Archaeological Animal Fats. Acc. Chem. Res. 2002. V. 35. P. 660.
Evershed R.P. // Archaeometry. 2008. V. 50. № 6. P. 895. https://doi.org/10.1111/j.1475-4754.2008.00446.x
Evershed R.P., Heron C., Charters S., Goad L.J. // Proceedings of the British Academy. 1992. № 77. P. 187.
Пожидаев В.М., Сергеева Я.Э., Слушная И.С. и др. // Бутлеров. сооб. 2017. Т. 52. № 12. С. 73.
Пожидаев В.М., Сергеева Я.Э., Офицеров Е.Н. и др. // Бутлеров. сооб. 2018. Т. 56. № 11. С. 47.
Пожидаев В.М., Сергеева Я.Э., Камаев А.В. // Журн. аналит. химии. 2017. Т. 72. № 6. С. 589. https://doi.org/10.7868/S0044450217060135
Folch J., Lees M., Sloane-Stanley G. // J. Biol. Chem. 1957. V. 226. P. 497.
Mayyas A., Douglas K., Hoffmann T. et al. // Mediterr. Archaeol. Ar. 2013. V. 13. № 2. P. 189.
Giorgi G., Salvini L., Pecci A. // J. Archaeol. Sci. 2010. V. 37. P. 1453. https://doi.org/10.1016/j.jas.2010.01.005
Regert M., Bland H.A., Dudd S.N. et al. // Proc. R. Soc. Lond. B. 1998. V. 265. P. 2027.
Regert M., Dudd S.N., van Bergen P.F. et al. // Proc. Br. Archaeol. Rep. Soc. 2001. V. 939. P. 78.
Correa-Ascencio M., Evershed R.P. // Analyst. 2014. V. 6. № 5. P. 1330. https://doi.org/10.1039/c3ay41678j
Evershed R.P., Dudd S.N., Copley M.S. et al. // Acc. Chem. Res. 2002. V. 35. № 8. P. 660. https://doi.org/10.1021/ar000200f
Cramp L.J.E., Evershed R.P. // Treatise on Geochemistry: Archaeology and Anthropology. 2014. V. 14. P. 319.
Справочник химика. Т. 2. Основные свойства неорганических и органических соединений / гл. ред. Никольский Б.П. М.; Л.: Химия, 1964. 1168 с.
Evershed R.P., Mottram H.R., Dudd S.N. et al. // Naturwissenschaften. 1997. V. 84. № 9. P. 402. https://doi.org/10.1007/s001140050417
Mottram H.R., Dudd S.N., Lawrence G.J. et al. // J. Chromatogr. 1999. V. 833. № 2. P. 209. https://doi.org/10.1016/S0021-9673(98)01041-3
Papakosta V., Pesonen P. 11th Nordic Conference on the Application of Scientific Methods in Archaeology, Helsinki, Finland, October 20th–23rd 2015. P. 32.
Дополнительные материалы отсутствуют.
Инструменты
Российские нанотехнологии


