Российские нанотехнологии, 2022, T. 17, № 3, стр. 385-393
Изучение электропроводящих гидрогелей на основе ксантана и пэдот псс с помощью спектроскопии комбинационного рассеяния света
Д. С. Большин 1, 2, *, П. К. Кашкаров 1, 2
1 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
2 Национальный исследовательский центр “Курчатовский институт”
Москва, Россия
* E-mail: ds.boljshin@physics.msu.ru
Поступила в редакцию 27.10.2021
После доработки 12.01.2022
Принята к публикации 20.01.2022
Аннотация
Изучены структурные особенности поли(3,4-этилендиокситиофен) полистирен сульфоната (ПЭДОТ ПСС) в синтезированном гидрогеле на основе ксантана. Выявлено, что ПЭДОТ ПСС образует устойчивую структуру с полисахаридом в большей степени, чем со структурообразующим поливиниловым спиртом. Предложена техника сравнения степени окисления ПЭДОТ ПСС по спектрам комбинационного рассеяния света, позволяющая при дальнейших исследованиях подобных материалов идентифицировать и качественно оценивать влияние процесса структурных изменений цепи ПЭДОТ на электропроводность гидрогелей.
ВВЕДЕНИЕ
В настоящее время электропроводящие гидрогели вызывают существенный интерес у научного сообщества. Их успешно применяют в медицине – в технологиях изготовления контактных линз, перевязочного материала для ран, средств адресной доставки лекарств и материала для тканевой инженерии [1, 2]. Также данные материалы весьма перспективны для применения в различных развивающихся областях, к которым относятся:
– электроды имплантируемых биотопливных элементов и биосенсоров [3];
– мягкая робототехника [4];
– электробиоинтерфейсы для имплантируемых и носимых устройств [4, 5];
– нейропротезирование и инвазивные нейроинтерфейсы [6, 7];
– среда для реализации вычислений с использованием биомолекул или клеток [8];
– гибридные материалы, содержащие живые клетки [9, 10].
Для придания электропроводности полимерным гелям в их состав добавляют как неорганические наноструктуры, такие как углеродные наноматериалы, наночастицы (НЧ) металлов и их оксидов, так и полимеры, среди которых наиболее активно обсуждаются полианилин [11] и поли(3,4-этилендиокситиофен) полистирен сульфонат (ПЭДОТ ПСС) [12]. ПЭДОТ ПСС широко используется в различных приложениях в медицине и биотехнологии, на данный момент он отличается наибольшей электропроводностью и биосовместимостью, что делает его подходящим для различных имплантируемых устройств, включая электроды инвазивных нейроинтерфейсов [13–15]. В средах с высокой ионной силой, таких как физиологические растворы, гидрогели, в частности каррагинановый, проявляют ионообменные свойства [16, 17]. В то же время гидрогели на основе полисахаридов, таких как ксантан и каррагинан, обладают рядом перспективных механических свойств, например они достаточно близки к свойствам некоторых тканей организма человека, могут также выступать в роли носителей различных НЧ [3, 18, 19]. Контролируя состав и процесс синтеза гидрогелей, можно добиться желаемой пористости геля или способности коллапсировать в ответ на изменение pH или ионной силы, окружающей гель среды. Эти свойства позволяют использовать гидрогели для контролируемого выделения биологически активных веществ [20, 21]. Возможно создавать электропроводящие гидрогели на основе ксантана, способные к самовосстановлению [11].
В [5] показано, что в геле, состоящем из йотта-каррагинана, поливинилового спирта (ПВС) и ПЭДОТ ПСС, наблюдаются емкостные эффекты при набухании в жидкости. Это важное с прикладной точки зрения свойство материала, нуждающееся в изучении. Также отдельного изучения требуют процессы, которые могут происходить во время синтеза подобных гидрогелей, например химические взаимодействия электропроводящего полимера с другими компонентами геля, влияние составляющих геля на процесс транспорта заряда в полимере [15], неравномерное распределение электропроводящего полимера по гидрогелю [5] и др.
Цель настоящей работы – исследование структуры и конформации ПЭДОТ ПСС в ряде синтезированных гелей с помощью спектроскопии комбинационного рассеяния света (КРС). Данный метод особенно успешно применяется для определения фазовой однородности веществ, а в совокупности с другими методами может дать достаточно полное представление как о химическом составе, так и о структуре изучаемого материала.
МАТЕРИАЛЫ И МЕТОДЫ
Получение гидрогелей. Основной вариант гидрогеля включает в себя ПВС, ксантан, ПЭДОТ ПСС и наночастицы магнетита. Методика получения гидрогеля разработана на основе публикаций [3, 5, 18]. На первой стадии в разных колбах готовили растворы ксантана (SpecialIngredients, Англия) и ПВС (Авилон-Компанихим, Россия) по 0.75 г на 30 мл дистиллированной воды при температуре 70°С в течение трех часов на магнитных мешалках. Частота перемешивания 400–540 об./мин. Полученные растворы смешивали с добавлением 1.3% раствора ПЭДОТ ПСС (Sigma-Aldrich, Китай), так чтобы объемное отношение растворов ПВС, ксантана и ПЭДОТ ПСС было 5:5:3. Полученную смесь перемешивали на магнитной мешалке в течение 40 мин при частоте 230–260 об./мин и температуре 40°С. В процессе перемешивания добавляли полученные химическим осаждением сульфата железа НЧ магнетита со средним размером 60 нм. Масса НЧ составляла 0.83% от суммарной массы компонентов образца, перед добавлением суспензию НЧ обрабатывали в ультразвуковой ванне в течение 20 мин. Полученную смесь замораживали на сутки, а потом на сутки выставляли оттаивать в сушильный шкаф. По результатам четырех таких циклов получался сухой образец гидрогеля.
Остальные образцы гидрогелей, изучаемые в работе, получены по такой же методике, но с исключением некоторых компонент из синтеза. В результате получены гидрогели:
– полный: ПВС–ксантан–ПЭДОТ ПСС–НЧ;
– без НЧ: ПВС–ксантан–ПЭДОТ ПСС;
– без ксантана и НЧ: ПВС–ПЭДОТ ПСС.
Набухаемость гидрогелей. В работе определяли предельную способность набухания для ксантановых гелей. Образцы, помещенные в воду или физиологический раствор, периодически взвешивали в течение часа. Далее приведем только предельные значения отношения массы поглощенной жидкости к начальной массе образца.
Подготовка образцов для измерения спектров КРС. Подготовленные для КРС-спектроскопии образцы описаны в табл. 1. Для получения спектров гидрогелей в набухшем состоянии образцы находились более суток в соответствующих средах. NaCl в физиологическом растворе имел пропорцию, соответствующую составу крови, т.е. 3.3 г/л. Раствор трех солей имел в составе NaCl, KCl и NaHCO3 в пропорциях 5, 1 и 4 г/л соответственно. ПЭДОТ ПСС и суспензию магнетита высушивали в течение 4 ч в сушильном шкафу при 40°С на стеклянной подложке.
Таблица 1.
Описание бразцов для измерения спектров КРС
| Образец | Состав | Состояние |
|---|---|---|
| 1 | ПВС–ксантан–ПЭДОТ ПСС–НЧ | Сухой |
| 2 | ПВС–ксантан–ПЭДОТ ПСС–НЧ | Набухший в дистиллированной воде |
| 3 | ПВС–ксантан–ПЭДОТ ПСС–НЧ | Набухший в физиологическом растворе NaCl |
| 4 | ПВС–ксантан–ПЭДОТ ПСС | Сухой |
| 5 | ПВС–ПЭДОТ ПСС | Сухой |
| 6 | ПВС–ПЭДОТ ПСС | Набухший в растворе трех солей |
| 7 | ПЭДОТ ПСС | Сухой |
| 8 | НЧ | Сухой |
| 9 | ПВС | Сухой порошок, исходный продукт |
| 10 | Ксантан | Сухой порошок, исходный продукт |
Измерения спектров КРС. Спектры КРС получены на многофункциональной системе для атомно-силовых и КРС-исследований NTEGRA Spectra (НТ-МДТ, Россия). При измерении образцы находились на стеклянной подложке в воздушной среде при нормальных условиях. Возбуждающее излучение от He–Ne-лазера с длиной волны 632.8 нм фокусировалось на образце объективом со 100-кратным увеличением и с числовой апертурой NA = 0.95. Рассеянное излучение регистрировалось охлаждаемой ПЗС-камерой Andor. Спектральное разрешение при указанной длине волны возбуждающего излучения – 0.08 нм (<2 см–1). Калибровку монохроматора осуществляли по эталонному образцу полистирола.
Обработка полученных результатов. Анализ структуры образцов проводили посредством декомпозиции спектров и идентификации полученных линий. Поэтому обработке измеренных спектров в данной работе было уделено особое внимание, в частности удаляли шумы, линии интерференции и низкочастотный фон.
Высокочастотные шумы сглаживали методом Савицкого–Голея. Для уверенности в том, что для сглаживания были выбраны правильные параметры и при сглаживании не удалялась часть полезного спектра, например, не обрезали пики более чем на величину шума, отдельно проводили анализ удаленных шумов. В них проводили поиск выбросов и тенденций при использовании скользящего среднего, однако такой анализ осложнялся неоднородностью распределения внутри диапазона одного измерения. Поэтому разработали интервальный метод тестирования шумов на гетероскедастичность, который предполагает, что наилучшие параметры сглаживания соответствуют наиболее широкой области однородности отфильтрованных шумов. Для каждого набора параметров сглаживания брали отрезок отфильтрованных шумов, для которого рассчитывали p-значимость теста Уайта мультипликативным методом Лагранжа [22–24] на гетероскедастичность. Далее отрезок смещали или изменяли длину, шаг дискретности – 1/100 диапазона спектра. Таким образом, перебирая все возможные интервалы для всех возможных параметров сглаживания, можно подтвердить выбор определенного набора, для которого отрезок гетероскедастичности имеет бóльшую длину.
Интерференционные шумы (гребенка) и часть низкочастотного фона (широкие холмы) исключали из спектров двумя подтверждающими друг друга алгоритмами. Базовую линию сглаживали методом Савицкого–Голея с полиномами от первой до третьей степени и с шириной окна от 3 до 1001 точек. Из всех полученных результатов сглаживания составляли единую матрицу. Фон и интерференцию извлекали как первую и вторую компоненты методом главных компонент [25]. Результаты, полученные методом независимых компонент [26], совпадали с предыдущими, повышая достоверность результата. Полученные компоненты вычитали из спектров. Остатки низкочастотного фона удаляли методом “катящегося колеса” (rolling circle filter).
Для разложения составных пиков спектра на отдельные компоненты использовали линию, являющуюся упрощенной комбинацией гауссова и лоренцева пика, определяемую формулой
(1)
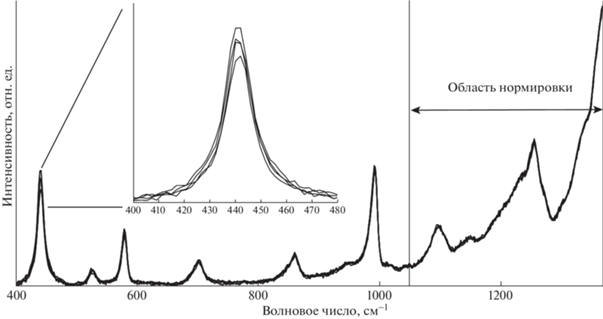
$\begin{gathered} f(k,A,{{k}_{0}},\sigma ,\gamma ) = \gamma A{{e}^{{ - \frac{{{{{(k - {{k}_{0}})}}^{2}}}}{{{{\sigma }^{2}}}}}}} + \\ + \;(1 - \gamma )\frac{{A{{\sigma }^{2}}}}{{({{{(k - {{k}_{0}})}}^{2}} + {{\sigma }^{2}})}}, \\ \end{gathered} $Для начальных приближений и последующего анализа в работе была собрана база расшифровок линий спектров ПЭДОТ в различных состояниях, ПЭДОТ ПСС и его производных [27–38]. Пример расшифровки полученных спектров приведен на рис. 1.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В полученных спектрах гидрогелей наибольшей интенсивностью КРС обладает ПЭДОТ ПСС, это также делает невозможным выделение в спектрах гидрогелей (образцы 1–7) линий других компонент (образцы 8–10). Подчеркнем, что извлечение из спектров количественной информации весьма затруднительно, поскольку полимер состоит из спектроскопически неэквивалентных сегментов, разных по степени окисления [27]. Более того, учитывая эксперименты с олигомерами ПЭДОТ [28] и то, что его сегменты могут быть конформационно неоднородными [38], вычисления осложняются резонансом возбуждающего излучения с молекулами или частями молекул определенной эффективной длины. Несмотря на это, благодаря анализу спектров КРС удается выявить качественные изменения, происходящие с ПЭДОТ в гидрогелях в различных состояниях. Кроме того, численные результаты позволяют ранжировать объекты исследования по определенному признаку.
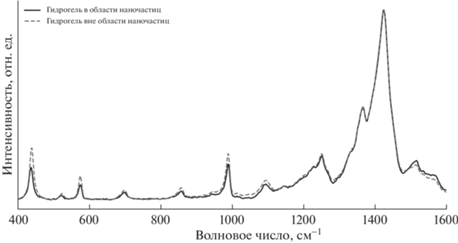
Гомогенность гидрогеля. Для ПЭДОТ ПСС и гидрогелей спектры снимали в нескольких точках, чтобы исследовать неоднородность синтезируемых гидрогелей. Высушенный на стеклянной подложке ПЭДОТ ПСС продемонстрировал ожидаемую высокую гомогенность, в то время как для некоторых гелей удалость отследить локальные различия. В областях спектров от 1050 до 1370 см–1 в основном проявляются колебания С–С-связей внутри и между тиофеновыми кольцами ПЭДОТ, обозначаемые в литературе Сα–Сα' и Сβ–Сβ. Поэтому при изучении гомогенности образцов эта область была выбрана для нормировки. Для образца 4 наблюдаются изменения в 16% высоты максимума линий на 438 и 577 см–1, отвечающих за планарные деформации С–О–С диоксиэтиленового кольца (рис. 2). Подобные изменения могут характеризовать степень планарности ПЭДОТ ПСС в гидрогелях по отношению к чистому ПЭДОТ ПСС. Более того, в сравнении с образцом 4 большей однородностью по осевой ориентации цепей полимера обладает образец 5, так как для него аналогичные изменения не превышают 10%. Не стоит исключать фактор формы начального геля перед высушиванием, а также скорость сушки, все это, предположительно, может давать больший разброс по осевой ориентации ПЭДОТ.
Набухаемость гидрогелей. В дистиллированной воде гидрогель ПВС–ксантан–ПЭДОТ ПСС абсорбирует и удерживает объем жидкости, по массе в 30–50 раз превышающий массу сухого геля. Добавление низкомолекулярной соли в физиологических пропорциях вызывает частичное сжатие геля. Для того чтобы различать коллапс, при котором происходит максимальное сжатие с выталкиванием всего растворителя из объема гидрогеля, и случай частичного сжатия геля, последний называется в литературе контракцией. В присутствии низкомолекулярной соли в физиологическом растворе контракция геля вызывается уменьшением разности осмотического давления противоионов внутри и вне геля [39]. В этом случае масса удерживаемой жидкости была в 15 раз больше массы сухого геля. При наличии НЧ в геле масса абсорбированной дистиллированной воды может в 70 раз превышать массу сухого геля. Причину такого увеличения абсорбционных свойств геля обсудим далее.
Деформация межцикловых связей. В спектрах ксантановых гидрогелей можно обнаружить искажение полимерной цепи ПЭДОТ. Во-первых, максимум локального пика (1258 см–1) смещается в сторону меньших волновых чисел примерно на 8 см–1 с перераспределением интенсивности на его левое плечо. Во-вторых, наблюдается изменение интенсивности линии при 1095 см–1, соответствующей искажению С–С-связей, которые скорее относятся к Сα–Сα', чем к Сβ–Сβ. Линия около 1039 см–1 в данном случае не рассматривается, так как ее может искажать вклад ПСС [40]. В [27] смещение линии 1258 см–1 эмпирически связывают с увеличением степени легирования, при этом игнорируя смещение этой линии в другую сторону в политиофене. К тому же легирование ПЭДОТ может сопровождаться его конформационными изменениями, а именно, “выпрямлением” цепи. В левое плечо максимума при 1250–1258 см–1 также может вносить вклад Cβ–H-изгиб, что подтверждается расчетами и экспериментами [27, 31, 37], и, как будет показано далее, у ПЭДОТ ПСС в гелях степень восстановления выше. Поэтому изменения в спектре до 1258 см–1 следует считать просто индикатором изменения положения цепи ПЭДОТ.
КРС-спектры гидрогелей раскладывали на отдельные компоненты области широкого пика от 1000 до 1600 см–1 (рис. 1). В диапазоне 1000–1270 были определены шесть компонент. Две из них в районе 1254 и 1267 см–1 более всего соответствуют колебаниям недеформированных Сα–Сα'-связей ПЭДОТ в нейтральном состоянии. На рис. 3 видна строгая корреляция высот первой (1095 см–1) и третьей (1186 см–1) компонент, нормированных на суммарную интенсивность линий 1254 и 1267 см–1 для разных образцов. Первая соответствует деформации межцикловых Сα–Сα'-связей, вторая – изгибам Cβ–H с небольшим вкладом смещенных Сα–Сα'. Можно проследить, как состояние и структура гидрогелей влияют на деформацию полимера. Расширение полимерной матрицы гидрогеля и отсутствие в матрице ксантана приводят к уменьшению деформации межцикловых связей.
Рис. 3.
Распределение максимумов линий 1095 и 1186 см–1, нормированных на суммарную интенсивность недеформированных Сα–Сα'-связей, для образцов 1–7.

Положение ПЭДОТ ПСС в гидрогеле. Пик при 522 см–1 можно отнести к непланарным деформациям диоксиэтиленового кольца, так как в [33] этот пик наблюдается в ИК-спектрах как колебание вне плоскости диоксиэтиленового кольца. А в спектрах из работы [31] этот пик растет со степенью окисления до некоторой предельной величины. Здесь можно предположить, что ограничивающим фактором для него являются именно конформационные изменения ПЭДОТ. В области от 400 до 800 см–1 соотношение линий, отвечающих за колебания связей С–О–С и С–S–C, и спектры для ксантановых гелей (образцов 1–4) идентичны. Следовательно, осевое положение цепей ПЭДОТ не изменяется даже при расширении ПВC-ксантановой матрицы во время набухания. При этом, как показано выше, деформация межцикловых связей ослабевает с расширением матрицы гидрогеля. Все это позволяет сделать заключение, что ПЭДОТ ПСС как бы «намотан» на ксантан. Причем именно на ксантан, так как в набухшем гидрогеле без ксантана (образец 6) искажение наименьшее, поскольку ПЭДОТ ПСС сильнее всего “выпрямляется” набухающей матрицей гидрогеля. В этом геле ПЭДОТ ПСС находится в более восстановленном состоянии, что будет показано далее, и должен был бы “свернуться” [38], но он фиксируется ПВС-матрицей, вероятно, за счет гидрофильных взаимодействий. Дополнительным фактом в пользу выдвигаемой гипотезы является то, что дисахариды основной цепи ксантана совместно с О-ацетиловыми остатками создают физические комплексы с двухвалентными катионами в основном тяжелых металлов. Также известно, что Ca2+ стабилизирует ксантановые спирали [21].
Согласно [5, 18] для полученных гидрогелей структурообразующим элементом является скорее ПВС, чем полисахарид. Полисахарид относительно равномерно распределяется по матрице ПВС и повышает ее стабильность. В [5] показано возникновение емкостных свойств гидрогеля при набухании в жидкости. Предлагаемая в настоящей работе схема взаимодействия ПЭДОТ ПСС и ксантана позволяет предположить три варианта ячеек, возникающих в объеме геля в процессе набухания и выступающих в роли микроконденсаторов:
– полисахарид|ПЭДОТ|ПВС|вода|ПЭДОТ|полисахарид;
– полисахарид|ПЭДОТ|вода|ПВС|вода|ПЭДОТ| полисахарид;
– полисахарид|ПЭДОТ|вода|ПЭДОТ|полисахарид.
Степень окисления ПЭДОТ ПСС. При разложении КРС-спектров гидрогелей в диапазоне 1300–1600 см–1 определены семь компонент. Центры четырех линий, относящихся к асимметричным колебаниям Сα=Сβ, были определены аппроксимацией исходных спектров при 1495.6, 1514.8, 1534, 1564.6 см–1. Здесь третья линия относится к ПЭДОТ в состоянии биполярона, а вторая и четвертая – к колебаниям нейтрального ПЭДОТ в центре и на концах цепи [28]. Центры трех линий симметричных колебаний в этой области определены при 1398.5 1425.3 и 1452.4 см–1. Первая из этих линий была введена искусственно, чтобы отражать промежуточное состояние ПЭДОТ ПСС. В [31] у чистого ПЭДОТ в процессе окисления максимум широкого пика сначала смещается к 1410 от 1425 см–1, а потом к 1450 см–1, это объясняется появлением промежуточного состояния полярона ПЭДОТ. Вторая и третья линии относятся к восстановленному и окисленному состоянию ПЭДОТ ПСС соответственно. Обозначим интенсивность спектральной линии как $I_{{x,n}}^{y}$, где x – симметричное или асимметричное колебание (s, a), n – номер линии симметричных или несимметричных колебаний, y – окисленная, восстановленная или промежуточная (o, r, i) формы ПЭДОТ ПСС. По результату декомпозиции спектров рассчитываются значения $I_{{s,1}}^{i}$, $I_{{s,2}}^{r}$, $I_{{s,3}}^{o}$, $I_{{a,1}}^{r}$, $I_{{a,2}}^{r}$, $I_{{a,3}}^{o}$, $I_{{a,4}}^{r}$. Качественно сравнить степень окисления/восстановления ПЭДОТ ПСС в полученных гидрогелях можно через показатель, который рассчитывается как отношение сумм интенсивностей линий окисленного ПЭДОТ ПСС к восстановленному. Рассчитывается показатель отдельно для трех случаев:
– для линий симметричных колебаний
– для линий асимметричных колебаний
– для суммы линий симметричных и асимметричных колебаний
Результат представлен на рис. 4.
Рис. 4.
Рассчитанные величины, характеризующие степени окисления/восстановления ПЭДОТ ПСС в различных образцах.
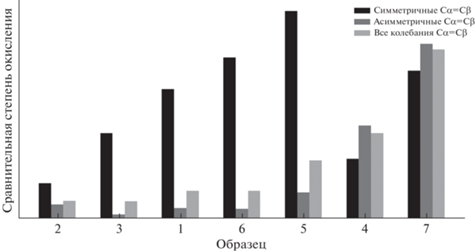
В гелях (образцы 1–6) ПЭДОТ ПСС находится в более восстановленном состоянии, чем сам по себе (образец 7). Причем этот эффект усиливается, если в состав геля входят НЧ или гель помещен в среду. При сравнении образцов 1–3, 5, 6, для которых не так очевидно соотношение суммарной интенсивности Сα=Сβ-колебаний, следует обратить внимание на соотношение антисимметричных колебаний. Полученный результат соответствует физическим ожиданиям, например ионы натрия образуют соль с ПСС, а высоколегированный ПЭДОТ имеет тенденцию возвращаться к своему нейтральному состоянию [31], к тому же полимерная матрица предотвращает конформационное изменение, которое могло бы препятствовать процессу восстановления [33, 38]. Также видно, что в геле без ксантана (образец 5) состояние ПЭДОТ ПСС более восстановленное, чем у ксантанового геля (образец 4), однако в набухшем геле (образец 6) дальнейшее восстановление ПЭДОТ ПСС в присутствии более концентрированного раствора ионов натрия не доходит до уровня геля с ксантаном в физиологическом растворе (образец 3). Такое поведение ПЭДОТ ПСС можно объяснить конкуренцией полисахарида за катионы натрия с ПСС, как в физиологических растворах, и способностью образовывать физические комплексы в сухом геле [21]. Пока остается неизвестным вклад процесса изменения структуры ксантана, к примеру, для каррагинана известна более высокая степень спирализации молекулы в физиологических растворах, что сопровождается меньшей набухаемостью гелей [18]. Данные свойства требуют дальнейших исследований, так как позволяют говорить о перспективности использования подобных гидрогелей для ионных интерфейсов [4].
Влияние наночастиц. КРС-линии магнетита, как упоминалось ранее, отсутствуют в спектрах гидрогеля, однако в некоторых точках измерения образца 1 возникает специфичный низкочастотный фон, который скорее всего связан с попаданием НЧ магнетита в область облучения. При неизменной форме спектра в области колебаний С–С- и С=С-связей интенсивность линий диоксиэтиленового кольца и серы упала более чем в 1.5 раза (рис. 5). Такое поведение может быть объяснено аналогично наблюдаемому в исследовании резонансному КРС ПЭДОТ на золотых НЧ [41]. Причиной может быть ориентация ПЭДОТ ПСС вокруг наночастиц перпендикулярно их поверхности. Если в этом случае плотность упаковки ПЭДОТ ПСС на поверхности НЧ позволяет проникать молекулам растворителя между цепями ПЭДОТ ПСС, то это может объяснить увеличение количества удерживаемой гидрогелем воды.
ЗАКЛЮЧЕНИЕ
При анализе спектров КРС выдвинуто предположение, что в синтезированных гелях ПЭДОТ ПСС оплетает ксантановый остов полимерной матрицы, что делает его более устойчивым к вымыванию из гидрогелей и предотвращает его конформационное изменение. Если такая структура подтвердится другими методами, то это позволит принять описанную в работе схему возникновения электрической емкости геля и исключить фактор конформационного изменения при электрофизических исследованиях гидрогелей. Также это позволит говорить о проводящих гидрогелях как о более перспективном материале в качестве электрических конденсаторов, чем о просто пленках ПЭДОТ ПСС [42], где конформационные изменения ограничивают электрическую емкость.
Предложенная техника сравнения степени окисления ПЭДОТ ПСС по спектрам КРС дает возможность при дальнейших исследованиях материалов с этим полимером идентифицировать и качественно оценивать влияние на проводимость процесса структурных изменений цепи ПЭДОТ.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (грант № 20-32-90221, “Аспиранты”). Отдельные измерения были выполнены с использованием оборудования ЦКП ИРЭА НИЦ “Курчатовский институт”.
Список литературы
Aswathy S.H., Narendrakumar U., Manjubala I. // Heliyon. 2020. V. 6. № 4. P. e03719. https://doi.org/10.1016/j.heliyon.2020.e03719
Caló E., Khutoryanskiy V.V. // Eur. Polym. J. 2015. V. 65. P. 252. https://doi.org/10.1016/j.eurpolymj.2014.11.024
Antipova C., Parunova Y., Vishnevskaya M. et al. // 12th Int. Conf. Dev. eSystems Eng. 2019. P. 513. https://doi.org/10.1109/DeSE.2019.00099
Yang C., Suo Z. // Nat. Rev. Mater. 2018. V. 3. № 6. P. 125. https://doi.org/10.1038/s41578-018-0018-7
Gotovtsev P.M., Badranova G.U., Zubavichus Y.V. et al. // Heliyon. 2019. V. 5. P. 02498. https://doi.org/10.1016/J.HELIYON.2019.E02498
Hong G., Yang X., Zhou T., Lieber C.M. // Curr. Opin. Neurobiol. 2018. V. 50. P. 33. https://doi.org/10.1016/j.conb.2017.11.007
Madhusudanan P., Raju G., Shankarappa S. // Roy. Soc. Int. 2020. V. 17. № 162. P. 20190505. https://doi.org/10.1098/rsif.2019.0505
Gotovtsev P.M., Kirillova D.A., Vasilov R.G. // Nanotechnologies in Russia. 2020. V. 15. P. 3. https://doi.org/10.1134/S1995078020010036
Gotovtsev P. // Appl. Sci. 2020. V. 10. P. 3990. https://doi.org/10.3390/APP10113990
Smith R.S.H., Bader C., Sharma S. et al. // Adv. Funct. Mater. 2020. V. 30. № 1907401. https://doi.org/10.1002/adfm.201907401
Hua D., Gao S., Zhang M. et al. // Carbohydr. Polym. 2020. V. 247. P. 116743. https://doi.org/10.1016/J.CARBPOL.2020.116743
Qiongyao P., Jingsi C., Tao W. et al. // InfoMat. 2020. V. 2. P. 843. https://doi.org/10.1002/inf2.12113
Musk E. // J. Med. Internet Res. 2019. V. 21. P. 16194. https://doi.org/10.2196/16194
Lu B., Yuk H., Lin S. et al. // Nat. Commun. 2019. V. 101. № 10. P. 1. https://doi.org/10.1038/s41467-019-09003-5
Xi F., Wanyi N., Hsinhan T. et al. // Adv. Sci. 2019. V. 6. P. 1900813. https://doi.org/10.1002/ADVS.201900813
Hermansson A.M., Eriksson E., Jordansson E. // Carbohydr. Polym. 1991. V. 16. № 3. P. 297. https://doi.org/10.1016/0144-8617(91)90115-S
Adhimoorthy P., Jittrakorn U., ChihTsai H. et al. // Chem. Eng. J. 2020. V. 391. P. 123585. https://doi.org/10.1016/J.CEJ.2019.123585
Badranova G.U., Gotovtsev P.M., Zubavichu Y.V. et al. // J. Mol. Liq. 2016. V. 223. P. 16. https://doi.org/10.1016/j.molliq.2016.07.135
Bueno V.B., Bentini R., Catalani L.C., Petri D.F.S. // Carbohydr. Polym. 2013. V. 92. P. 1091. https://doi.org/10.1016/J.CARBPOL.2012.10.062
Croitoru C., Roata I.C., Pascu A., Stanciu E.M. // Polymers. 2020. V. 12. P. 1544. https://doi.org/10.3390/polym12071544
Petri D.F.S. // J. Appl. Polym. Sci. 2015. V. 132. P. 42035. https://doi.org/10.1002/APP.42035
Breusch T.S., Pagan A.R. // Rev. Econ. Stud. 1980. V. 47. P. 239. https://doi.org/10.2307/2297111
White H.A. // Econometrica 1980. V. 48. P. 817.
Greene W.H. Econometric Analysis. New Jersey: Prentice Hall. 2002. 215 p.
Pearson K. // Philos. Mag. 1901. V. 2. P. 559.
Hyvärinen A., Karhunen J., Oja E. Independent component analysis. NY: Wiley, 2001. 475 p.
Łapkowski M., Proń A. // Synth. Met. 2000. V. 110. P. 79. https://doi.org/10.1016/S0379-6779(99)00271-4
Tran-Van F., Garreau S., Louarn G. et al. // J. Mater. Chem. 2001. V. 11. P. 1378. https://doi.org/10.1039/b100033k
Tamburri E., Orlanducci S., Toschi F. et al. // Synth. Met. 2009. V. 159. P. 406. https://doi.org/10.1016/j.synthmet.2008.10.014
Fernando E., Matsumoto A., Zoetebier B. et al. // Org. Electron. 2014. V. 15. P. 1062. https://doi.org/10.1016/j.orgel.2014.02.022
Garreau S., Louarn G., Buisson J.P. et al. // Macromol. 1999. V. 32. P. 6807. https://doi.org/10.1021/ma9905674
Garreau S., Louarn G., Lefrant S. et al. // Synth. Met. 1999. V. 101. P. 312. https://doi.org/10.1016/S0379-6779(98)01146-1
Chiu W.W., Travaš-Sejdić J., Cooney R.P., Bowma-ker G.A. // Synth. Met. 2005. V. 155. P. 80. https://doi.org/10.1016/j.synthmet.2005.06.012
Almeida P.V., Izumi C.M.S., Dos Santos H.F., Sant’Ana A.C. // Quim. Nova. 2019. V. 42. P. 1073. https://doi.org/10.21577/0100-4042.20170417
Chiu W.W., Travaš-Sejdić J., Cooney R.P., Bowma-ker G.A. // J. Raman Spectrosc. 2006. V. 37. P. 1354. https://doi.org/10.1002/jrs.1545
Duvail J.L., Rétho P., Garreau S. et al. // Synth. Met. 2002. V. 131. P. 123. https://doi.org/10.1016/S0379-6779(02)00195-9
Louarn G., Buisson J.P., Lefrant S., Fichou D. // J. Phys. Chem. 1995. V. 99. P. 11399. https://doi.org/10.1021/j100029a016
Ouyang J., Xu Q., Chu C. et al. // Polymers. (Guildf). 2004. V. 45. P. 8443. https://doi.org/10.1016/j.polymer.2004.10.001
Philippova O.E. // Polym. Sci. Ser. C+. 2000. V. 42. № 2. P. 208.
Stavytska-Barba M., Kelle A.M. // J. Phys. Chem. 2010. V. 114. P. 6822. https://doi.org/10.1021/jp100135x
Moraes B.R., Campos N.S., Izumi C.M.S. // Vib. Spectrosc. 2018. V. 96. P. 137. https://doi.org/10.1016/j.vibspec.2018.04.006
Zhao Q., Jamal R., Zhang L. et al. // Nanoscale Res. Lett. 2014. V. 9. P. 1. https://doi.org/10.1186/1556-276X-9-557
Дополнительные материалы отсутствуют.
Инструменты
Российские нанотехнологии