Неорганические материалы, 2019, T. 55, № 11, стр. 1183-1189
Синтез нитридов в процессе магниетермического восстановления оксидных соединений тантала и ниобия
В. М. Орлов 1, *, Р. Н. Осауленко 2, В. Я. Кузнецов 1
1 Институт химии и технологии редких элементов и минерального сырья им. И.В. Тананаева ФИЦ КНЦ
Российской академии наук
184209 Мурманская обл., Апатиты, Академгородок, 26а, Россия
2 Петрозаводский государственный университет
185910 Республика Карелия, Петрозаводск, пр. Ленина, 33, Россия
* E-mail: orlov@chemy.kolasc.net
Поступила в редакцию 06.03.2019
После доработки 18.04.2019
Принята к публикации 15.05.2019
Аннотация
Исследована возможность получения нитридов тантала и ниобия при восстановлении Та2O5, Nb2O5, Mg4Та2O9 и Mg4Nb2O9 парами магния. Процесс вели в две стадии: восстановление оксидов при остаточном давлении аргона в реакторе 5 кПа и температуре 820°С в течение 4 ч; азотирование продуктов восстановления в атмосфере азота при 820 и 900°С в течение 1–12 ч. Фазовый состав полученных после выщелачивания оксида магния порошков исследовали на дифрактометрах ДРФ-2 и ДРОН-4, удельную поверхность определяли методом БЭТ на приборе Micromeritics TriStar II 3020. При использовании в качестве прекурсора Та2O5 получен продукт, содержащий θ-TaN, ε-TaN и Ta2N. При использовании в качестве прекурсора Nb2О5 образуются нитриды NbN с гранецентрированной кубической и гексагональной плотноупакованной решетками, Nb2N и Nb4N3. Продукты восстановления Mg4Та2O9 и Mg4Nb2O9 не азотируются. Дано объяснение полученным результатам.
ВВЕДЕНИЕ
Нитриды переходных металлов, в частности тантала и ниобия, рассматриваются как перспективные функциональные материалы [1, 2]. При этом для многих областей применения большое значение имеет удельная поверхность материала [3, 4]. Одним из методов получения нитридов является аммонолиз мелкодисперсных порошков металлов или их оксидов [5]. Использование для этих целей мезопористых порошков тантала и ниобия, получаемых восстановлением их оксидных соединений парами магния, позволяет получать соединения этих металлов с азотом уже после 1–2-часовой обработки в токе аммиака при температуре 600–700°С [6, 7]. Однако при аммонолизе порошков с большой удельной поверхностью, в которых преобладают поры размером менее 5–10 нм, уже при температуре 500–600°С происходит многократное уменьшение поверхности. Кроме того, в результате присутствия на поверхности частиц слоя естественного оксида основную массу порошков с большой удельной поверхностью составляет аморфный оксид [8]. Поэтому на первой стадии аммонолиза образуются оксинитриды тантала и ниобия. И если далее образование фазы нитрида при аммонолизе порошка ниобия с удельной поверхностью 123 м2/г наблюдалось уже после выдержки при температуре 700°С [7], то при аммонолизе порошка тантала с удельной поверхностью 56 м2/г даже после трехчасовой выдержки при температуре 870°С продуктом реакции был оксинитрид [6].
Поскольку уменьшение поверхности при аммонолизе мезопористых порошков происходило за счет исчезновения пор менее 10 нм, представляло интерес исследовать возможность азотирования металла непосредственно в процессе восстановления. В этом случае прослойки оксида магния, разделяющие частицы металла и определяющие структуру порошка [9], должны способствовать сохранению пористости частиц и соответственно поверхности полученного нитрида. Кроме того, продукты реакции не должны содержать оксинитриды.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве исходных материалов использовали пентаоксиды тантала и ниобия, а также танталат магния (ТМ) Mg4Та2O9 и ниобат магния (НМ) Mg4Nb2O9. ТМ и НМ синтезировали спеканием смеси исходных оксидов при температуре 1300°С. Процесс азотирования вели в реакторе, аналогичном использовавшемуся при восстановлении оксидных соединений парами магния [10]. Контейнеры с оксидными соединениями располагали над контейнером с магнием. Азот высокой чистоты подавали в реактор непосредственно из баллона без дополнительной очистки.
Предварительные эксперименты при температуре в реакторе 900°С показали, что в атмосфере азота восстановление оксидных соединений и соответственно образования нитридов тантала и ниобия не происходит. Это, скорее всего, объясняется тем, что магний, взаимодействуя с азотом, образует нитрид Mg3N2. Следует отметить, что энтальпия образования Mg3N2 составляет –461 кДж/моль, а ТаN и NbN всего –272 и –234 кДж/моль соответственно [11], т.е. реакция азотирования магния является приоритетной. Температура разложения нитрида магния 1500°С. Вследствие этого при заполнении азотом в реакторе отсутствуют пары магния и восстановления оксидов не происходит. Поэтому в дальнейшем процесс осуществляли в 2 этапа. Вначале вели восстановление при температуре 820°С и остаточном давлении аргона в реакторе 5 кПа в течение 4 ч. После этого реактор заполняли азотом и, поддерживая его избыточное давление на уровне 30–100 кПа, осуществляли выдержку при температуре 820 или 900°С в течение 1–12 ч. Полученную реакционную массу (РМ) выщелачивали 15%-ным раствором азотной кислоты. Порошок промывали дистиллированной водой до нейтральной реакции и сушили при температуре 70°С.
Фазовый состав продуктов реакции определяли на дифрактометре ДРФ-2 с CuKα-излучением и графитовым монохроматором. Идентификацию фаз осуществляли по базе дифрактометрических данных PDF-2 ICPDS-ICCD 2002. Для уточнения параметров кристаллической структуры использовали автоматизированный рентгеновский дифрактометр ДРОН-4, метод Ритвельда и базу данных структур неорганических кристаллов ICSD, Карлсруе, 2013. На приборе Micromeritics TriStar II 3020 измеряли удельную поверхность адсорбционным статическим методом БЭТ и параметры пористости методом BJH. Содержание азота и кислорода определяли методом газо-адсорбционной хроматографии в сочетании с импульсным нагревом на анализаторе К-671.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В табл. 1 и 2 приведены удельная поверхность (S), содержание азота (СN) и фазовый состав продуктов, полученных азотированием пентаоксидов тантала и ниобия в ходе двухстадийного эксперимента в зависимости от температуры азотирования и длительности выдержки. Ориентировочное содержание фаз определено по соотношению высоты соответствующих рефлексов на рентгенограммах. Содержание азота в продуктах, рассчитанное на основе приведенного фазового состава, хорошо коррелирует с данными анализа. Температура и длительность выдержки РМ в атмосфере азота практически не оказали влияния на содержание азота в полученных порошках и их удельную поверхность. Удельная поверхность соответствовала поверхности порошков тантала и ниобия, получаемых восстановлением парами магния в аналогичных условиях без стадии азотирования. Изменение объема и поверхности пор разных размеров в зависимости от длительности азотирования продуктов восстановления пентаоксида тантала приведено на рис. 1. Данные свидетельствуют о том, что с увеличением длительности выдержки при температуре 820°С с 3 до 12 ч объем пор увеличился с 0.057 до 0.105 см3/г. Доля поверхности, обеспечиваемая порами размером более 10 нм, выросла с 40 до 48%. В этих же условиях при использовании в качестве прекурсора пентаоксида ниобия объем пор, наоборот, уменьшился с 0.089 до 0.075 см3/г, а их средний диаметр изменился с 13.6 до 11.6 нм. При использовании в качестве прекурсора ТМ или НМ параметры пористости с изменением температуры и длительности выдержки стадии азотирования оставались практически неизменными.
Таблица 1.
Характеристики азотированных продуктов, полученных после восстановления Та2О5
| Опыт | Условия азотирования |
Характеристики продуктов | ||||||
|---|---|---|---|---|---|---|---|---|
| t, °С | τ, ч | S, м2/г | СN, % | Содержание фаз, % | ||||
| TaN | ТаN0.83 | Ta2N | Та | |||||
| 1 | 820 | 1 | 16 | 6.8 | 40 | 35 | 20 | 5 |
| 2 | 3 | 16 | 6.4 | 45 | 30 | 15 | 10 | |
| 3 | 6 | 22 | 6 | 35 | 45 | 20 | – | |
| 4 | 12 | 25 | 5.5 | 30 | 35 | 30 | – | |
| 5 | 900 | 1 | 17 | 4.9 | 25 | 20 | 45 | 10 |
| 6 | 3 | 17 | 6.5 | 40 | 40 | 20 | – | |
| 7 | 6 | 25 | 6 | 17 | 62 | 22 | – | |
| 8 | 12 | 27 | 5.5 | 25 | 50 | 25 | – | |
Таблица 2.
Характеристики азотированных продуктов, полученных после восстановления Nb2О5
| Опыт | Условия азотирования |
Характеристики продуктов | ||||||
|---|---|---|---|---|---|---|---|---|
| t, °С | τ, ч | S, м2/г | СN, % | Содержание фаз, % | ||||
| NbN (куб.) | NbN (гекс.) | Nb2N | Nb | |||||
| 1 | 820 | 1 | 25 | 10.4 | 45 | 25 | 20 | 10 |
| 2 | 3 | 25 | 10.1 | 50 | 30 | 10 | 10 | |
| 3 | 6 | 27 | 10.2 | 40 | 45 | – | 5 | |
| 4 | 12 | 24 | 11.5 | 50 | 50 | – | – | |
| 5 | 900 | 3 | 28 | 10.3 | 30 | 50 | 10 | 10 |
| 6 | 6 | 20 | 11 | 60 | 10 | 30 | – | |
| 7 | 12 | 27 | 10.5 | 40 | 55 | 5 | – | |
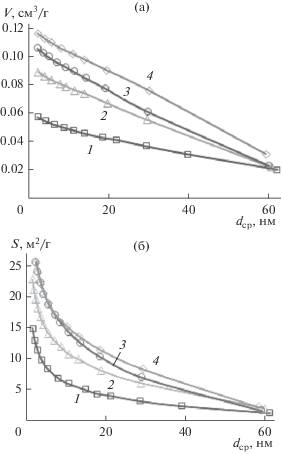
Рис. 1.
Зависимости суммарного объема (а) и поверхности пор (б) от их среднего диаметра в азотированных продуктах после восстановления Та2О5 при температуре 820°С и выдержке 3 (1), 6 (2), 12 ч (3); 900°С, 12 ч (4).
Рентгенограммы образцов 6 и 7 (табл. 1), полученных азотированием РМ после восстановления Та2О5, приведены на рис. 2. Уточненный методом Ритвельда фазовый состав и параметры кристаллической структуры нитридов приведены в табл. 3. В соответствии с уточненными данными, в процессе азотирования образуется нитрид тантала TaN с двумя типами кристаллической решетки. Фаза θ‑TaN с гексагональной решеткой (ICSD № 76455) характеризуется пр. гр. $P\overline {\text{6}} m{\text{2}}{\text{.}}$ Гексагональная фаза ε-TaN (ICSD № 1396) с пр. гр. $P\overline {\text{6}} {\text{2}}m$ отличается от фазы θ-TaN симметрией расположения атомов азота в элементарной ячейке и примерно в 1.8 раза бóльшими периодами по осям а и b. Базис элементарной ячейки ε-TaN состоит из 6 атомов, 3 из которых тантал и 3 азот. На элементарную ячейку θ-TaN приходится 2 атома (1 Ta и 1 N).
Рис. 2.
Рентгенограммы азотированных продуктов после восстановления Та2О5 (образцы 6 и 7 из табл. 1): температура 900°С, выдержка 3 (1), 6 ч (2).
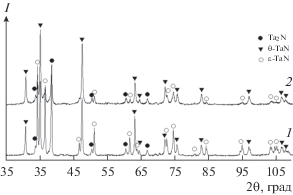
Таблица 3.
Фазовый состав и параметры структуры продуктов восстановления-азотирования Ta2О5
| Фаза | № ICSD | Пр. гр. | Периоды элементарной ячейки, Å | Содержание, % | |||
|---|---|---|---|---|---|---|---|
| a | c | ||||||
| ICSD | эксп. | ICSD | эксп. | ||||
| Азотирование 820°С, 3 ч (образец 2, табл. 1) | |||||||
| θ-TaN | 76 455 | $P\bar {6}m2$ | 2.931 | 2.9338(3) | 2.879 | 2.8806(1) | 40 |
| ε-TaN | 1396 | $P\bar {6}2m$ | 5.196(4) | 5.1891(2) | 2.911(2) | 2.9058(6) | 36 |
| Ta2N | 76 015 | $P\bar {3}m1$ | 3.0476 | 3.0479(2) | 4.9187 | 4.9193(5) | 16 |
| Ta | 151 407 | $Im{\bar {3}}m$ | 3.2959(3) | 3.3080(3) | c = a | 8 | |
| Азотирование 900°С, 3 ч (образец 6, табл. 1) | |||||||
| θ-TaN | 76 455 | $P\bar {6}m2$ | 2.931 | 2.9306(6) | 2.879 | 2.8795(1) | 39 |
| ε-TaN | 1396 | $P\bar {6}2m$ | 5.196(4) | 5.1885(8) | 2.911(2) | 2.9060(7) | 42 |
| Ta2N | 76015 | $P\bar {3}m1$ | 3.0476 | 3.0481(2) | 4.9187 | 4.9263(5) | 19 |
| Азотирование 900°С, 6 ч (образец 7, табл. 1) | |||||||
| θ-TaN | 76 455 | $P\overline {\text{6}} m{\text{2}}$ | 2.931 | 2.9323(7) | 2.879 | 2.8792(4) | 57 |
| ε-TaN | 1396 | $P\overline {\text{6}} {\text{2}}m$ | 5.196(4) | 5.1901(4) | 2.911(2) | 2.9072(6) | 18 |
| Ta2N | 76 015 | $P\overline {\text{3}} m{\text{1}}$ | 3.0476 | 3.0495(6) | 4.9187 | 4.9297(3) | 25 |
На рис. 3 приведены рентгенограммы, а в табл. 4 уточненные методом Ритвельда фазовый состав и параметры кристаллической структуры образцов 2 и 5 (табл. 2), полученных азотированием продуктов восстановления Nb2O5. Вне зависимости от температуры азотирования в образцах одновременно присутствуют нитриды NbN как с гранецентрированной кубической (ГЦК), так и с гексагональной плотноупакованной (ГПУ) решетками. Поскольку ГЦК-фаза характерна для нитрида состава NbN0.88–NbN1.00, а ГПУ-фаза для состава NbN1.00–NbN1.06 [11], возможно, их одновременное существование объясняется разной степенью азотирования частиц ниобия. С повышением температуры азотирования количество более богатой по азоту ГПУ-фазы увеличилось. Несмотря на то что в образцах, полученных азотированием РМ после восстановления пентаоксидов, по данным анализа, содержалось 3–5 мас. % кислорода, рентгенофазовый анализ не выявил присутствия оксидных фаз. Это означает, что высокое содержание кислорода обусловлено только присутствием на поверхности частиц порошка пленки естественного оксида.
Рис. 3.
Рентгенограммы азотированных продуктов после восстановления Nb2О5 (образцы 2 и 5 из табл. 2): выдержка 3 ч, температура 820 (1), 900°С (2).
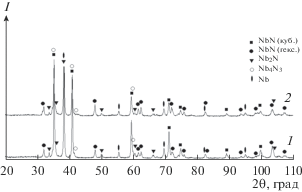
Таблица 4.
Фазовый состав и параметры структуры продуктов восстановления-азотирования Nb2О5
| Фаза | № ICSD | Пр. гр. | Периоды элементарной ячейки, Å | Содержание, % | |||
|---|---|---|---|---|---|---|---|
| a | c | ||||||
| ICSD | эксп. | ICSD | эксп. | ||||
| Азотирование 820°С, 3 ч (образец 2, табл. 2) | |||||||
| NbN (куб.) | 604392 | $Fm\bar {3}m$ | 4.3913(2) | 4.3878(4) | c = a | 49 | |
| NbN (гекс.) | 76384 | ${{P{{6}_{3}}} \mathord{\left/ {\vphantom {{P{{6}_{3}}} {mmc}}} \right. \kern-0em} {mmc}}$ | 2.968 | 2.9672(4) | 5.549 | 5.5495(3) | 20 |
| Nb2N | 31165 | ${{P{{6}_{3}}} \mathord{\left/ {\vphantom {{P{{6}_{3}}} {mmc}}} \right. \kern-0em} {mmc}}$ | 3.064 | 3.0519(2) | 4.971 | 4.9965(5) | 10 |
| Nb4N3 | 76389 | ${{I4} \mathord{\left/ {\vphantom {{I4} {mmm}}} \right. \kern-0em} {mmm}}$ | 4.382 | 4.3852(4) | 8.632 | 8.6490(1) | 11 |
| Nb | 645059 | $Im{\kern 1pt} \bar {3}m$ | 3.3063 | 3.3021(9) | c = a | 10 | |
| Азотирование 900°С, 3 ч (образец 5, табл. 2) | |||||||
| NbN (куб.) | 604392 | $Fm\bar {3}m$ | 4.3913(2) | 4.3894(9) | c = a | 41 | |
| NbN (гекс.) | 76384 | ${{P{{6}_{3}}} \mathord{\left/ {\vphantom {{P{{6}_{3}}} {mmc}}} \right. \kern-0em} {mmc}}$ | 2.968 | 2.9668(1) | 5.549 | 5.5522(4) | 38 |
| Nb2N | 31165 | ${{P{{6}_{3}}} \mathord{\left/ {\vphantom {{P{{6}_{3}}} {mmc}}} \right. \kern-0em} {mmc}}$ | 3.064 | 3.0526(3) | 4.971 | 4.9939(5) | 7 |
| Nb4N3 | 76389 | ${{I4} \mathord{\left/ {\vphantom {{I4} {mmm}}} \right. \kern-0em} {mmm}}$ | 4.382 | 4.3783(1) | 8.632 | 8.6401(3) | 9 |
| Nb | 645059 | $Im\bar {3}m$ | 3.3063 | 3.3020(6) | c = a | 5 | |
При использовании в качестве прекурсора ТМ и НМ содержание азота в продуктах, полученных их восстановлением с последующим азотированием, значительно ниже (табл. 5), чем в продуктах с использованием в качестве прекурсора пентаоксидов. Оно, так же как и величина удельной поверхности, практически не зависело от условий процесса. На рентгенограммах (рис. 4), несмотря на то что общее содержание азота в порошках выше предела растворимости, рефлексы, соответствующие нитридным фазам, не наблюдаются. Присутствие рентгеноаморфной фазы обусловлено большим количеством естественного аморфного оксида на поверхности частиц порошка [12]. Удельная поверхность азотированных порошков соответствует поверхности порошков тантала и ниобия, получаемых восстановлением этих прекурсоров в аналогичных условиях [10, 13]. Параметры элементарной ячейки порошков тантала и ниобия до (1) и после азотирования (2), рассчитанные на основании рентгенограмм (рис. 4), приведены в табл. 6. Восстановление в обоих случаях шло при температуре 820°С и остаточном давлении аргона в реакторе 5 кПа в течение 4 ч. Последующее азотирование РМ проводили при 900°С в течение 3 ч. Период элементарной ячейки порошков, полученных восстановлением с последующим азотированием (образцы 2), даже несколько меньше, чем у порошков без азотирования. Следовательно, внедрения азота в кристаллическую решетку металла не происходило. Вероятно, в порошках, полученных при использовании в качестве прекурсора ТМ и НМ, азот сорбирован большой удельной поверхностью.
Таблица 5.
Характеристики азотированных продуктов, полученных после восстановления ТМ и НМ
| Условия азотирования |
Характеристики продуктов | ||||||
|---|---|---|---|---|---|---|---|
| из ТМ | из НМ | ||||||
| t, °С | τ, ч | S, м2/г | СN, % | Фазовый состав | S, м2/г | СN, % | Фазовый состав |
| 820 | 6 | 70 | 0.95 | Та и РАФ | 132 | 1.5 | Nb и РАФ |
| 12 | 69 | 0.76 | 158 | 1.2 | |||
| 900 | 3 | 71 | 1.1 | 140 | 1.9 | ||
| 6 | 68 | 1.1 | 128 | 1.8 | |||
| 12 | 68 | 1.0 | 151 | 1.9 | |||
Рис. 4.
Рентгенограммы продуктов после восстановления (1) и азотирования (2) танталата (а) и ниобата магния (б).
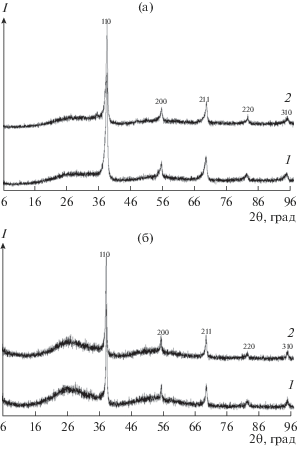
Таблица 6.
Параметры элементарной ячейки порошков, полученных магниетермическим восстановлением ТМ и НМ (I) и после дополнительного азотирования (II)
| Фаза | № ICDD | Пр. гр. | Период элементарной ячейки, Å | ||
|---|---|---|---|---|---|
| ICDD | I | II | |||
| Ta | 4-788 | $Im{\bar {3}}m$ | 3.305 | 3.3110 | 3.3051 |
| Nb | 34-370 | $Im{\bar {3}}m$ | 3.303 | 3.3072 | 3.3051 |
Возникает вопрос, почему при взаимодействии с азотом продуктов реакции восстановления пентаоксидов азотирование порошка металла происходит, но до определенных пределов, а при использовании в качестве прекурсора танталатов и ниобатов нитриды вообще не образуются? Продукты восстановления оксидных соединений тантала и ниобия представляют собой порошки губчатой структуры, состоящие из наноразмерных частиц металла [8, 13]. При восстановлении пентаоксидов в наших условиях расчетный размер частиц, исходя из величины удельной поверхности, тантала всего около 15 нм, а ниобия 30 нм. Это означает, что кинетических ограничений, связанных с диффузией азота в металле, быть не должно. Из данных табл. 1 и 2 видно, что уже после часовой выдержки РМ в атмосфере азота его содержание в продуктах достигает максимального значения. Следовательно, причиной недостаточно полного азотирования или его отсутствия является затрудненная диффузия молекул азота к поверхности металлических частиц. Частица порошка восстановленного оксидного соединения представляет собой слоистую структуру, состоящую из наноразмерных частиц металла и оксида магния [8, 9, 14]. Чтобы газ мог диффундировать внутрь восстановленной частицы, между металлом и оксидом магния должен быть зазор. Порошки, полученные восстановлением танталатов и ниобатов, характеризуются меньшим размером пор, следовательно, более тонкими прослойками оксида магния. Сравнение результатов азотирования РМ, полученной восстановлением пентаоксидов и сложных оксидов, показывает, что величина зазора зависит от толщины прослоек оксида магния. Нитриды при выдержке РМ, полученной восстановлением сложных оксидов, в атмосфере азота не образуются, потому что величина зазора между металлом и оксидом магния недостаточна для проникновения молекул азота в зону контакта с металлом. В случае азотирования РМ, полученной в результате восстановления пентаоксидов, начальный зазор между металлом и оксидом магния достаточен для проникновения азота к поверхности частиц металла, образовавшихся в объеме восстановленной частицы. В дальнейшем вследствие поглощения азота объем металлических частиц увеличивается, каналы поступления азота в наиболее мелких порах перекрываются. Азотирование на этих участках прекращается. В результате содержание азота не увеличивается и практически не меняется фазовый состав продуктов (табл. 1, 2).
ЗАКЛЮЧЕНИЕ
Выполненное исследование показало, что провести одновременное восстановление и азотирование оксидных соединений тантала и ниобия не представляется возможным, т. к. образование нитрида магния препятствует испарению последнего. Восстановление оксидов и, соответственно, синтез нитридов не происходят. Процесс вели в две стадии: восстановление при остаточном давлении аргона в реакторе 5 кПа и температуре 820°С; выдержка продуктов реакции в атмосфере азота при 820 и 900°С. В этом режиме при восстановлении Та2О5 фазовый состав представлен нитридами θ-TaN (ICSD № 76455, пр. гр. $P\overline {\text{6}} m{\text{2}}$), ε-TaN (ICSD № 1396, пр. гр. $P\overline {\text{6}} {\text{2}}m$) и Ta2N (ICSD № 76015, пр. гр. $P\overline {\text{3}} m{\text{1}}$). При использовании в качестве прекурсора Nb2О5 образуется нитрид NbN как с ГЦК- (ICSD № 604392, пр. гр. $Fm\bar {3}m$), так и с ГПУ-решетками (ICSD № 76384, пр. гр. ${{P{{6}_{3}}} \mathord{\left/ {\vphantom {{P{{6}_{3}}} {mmc}}} \right. \kern-0em} {mmc}}$), Nb2N (ICSD № 31165, пр. гр. ${{P{{6}_{3}}} \mathord{\left/ {\vphantom {{P{{6}_{3}}} {mmc}}} \right. \kern-0em} {mmc}}$) и Nb4N3 (ICSD № 76389, пр. гр. ${{I4} \mathord{\left/ {\vphantom {{I4} {mmm}}} \right. \kern-0em} {mmm}}$). Содержание азота и фазовый состав продуктов с увеличением времени выдержки практически не меняются. Порошки характеризуются мезопористой структурой с удельной поверхностью на уровне 20–28 м2/г. При использовании в качестве прекурсора Mg4Та2O9 или Mg4Nb2O9 в полученных продуктах нитриды не наблюдались.
Анализ результатов показывает, что размер зазора между частицами металла и прослойками оксида магния в слоистой структуре восстановленной частицы, обеспечивающего доступ молекул азота к поверхности реагирования, определяется размером пор, т.е. толщиной пластинок оксида магния, разделяющих частицы металла. В порошках, полученных восстановлением пентаоксидов тантала и ниобия, доля поверхности, определяемая порами размером менее 10 нм, на уровне 20 и 50% соответственно. В порошках, полученных восстановлением Mg4Та2O9 и Mg4Nb2O9, она увеличивается до 80 и 95% [8, 15].
Список литературы
Тот Л. Карбиды и нитриды переходных металлов: Пер. с англ. / Под реда. Гельда П.В. М.: Мир, 1974. 296 с.
Ningthoujam R.S., Gajbhiye N.S. Synthesis, Electron Transport Properties of Transition Metal Nitrides and Applications // Progress Mater. Sci. 2015. V. 70. № 5. P. 50–154.
Maeda K., Terashima H., Kase K., Domen K. Nanoparticulate Precursor Route to Fine Particles of TaON and ZrO2–TaON Solid Solution and Their Photocatalytic Activity for Hydrogen Evolution under Visible Light // Appl. Catal. A: General. 2009. V. 357. № 2. P. 206–212.
Wang X.-J., Krumeich F., Worle M. et al. Niobium(V) Oxynitride: Synthesis, Characterization, and Feasibility as Anode Material for Rechargeable Lithium-Ion Batteries // Chem. Eur. J. 2012. V. 18. № 19. P. 5970–5978.
Lu D., Kondo J. N., Hara M. et al. Systematical Investigation on Characteristics of a Photocatalyst: Tantalum Oxynitrides // Microscopy. 2014. V. 63. № 4. P. 313–324.
Орлов В.М., Кузнецов В.Я., Осауленко Р.Н. Аммонолиз магниетермических порошков тантала // Журн. неорган. химии. 2017. Т. 62. № 1. С. 38–43.
Орлов В.М., Осауленко Р.Н. Свойства нитридов, получаемых аммонолизом магниетермических порошков ниобия // Неорган. материалы. 2018. Т. 54. № 7. С. 675–680.
Орлов В.М., Крыжанов М.В., Князева А.И. Порошки тантала с мезопористой структурой // Физикохимия поверхности и защита материалов. 2016. Т. 52. № 5. С. 500–504.
Müller R., Bobeth M., Brumm H. et al. Kinetics of Nanoscale Structure Development During Mg-Vapour Reduction of Tantalum Oxide // Int. J. Mater. Res. 2007. V. 98. № 11. P. 1138–1145.
Орлов В.М., Крыжанов М.В. Получение нанопорошков тантала магниетермическим восстановлением танталатов // Металлы. 2015. № 4. С. 93–97.
Самсонов Г.В., Кулик О.П., Полищук В.С. Получение и методы анализа нитридов. Киев: Наукова думка, 1978. 318 с.
Орлов В.М., Осауленко Р.Н., Крыжанов М.В., Лобов Д.В. Рентгенографическое исследование магниетермических танталовых порошков // Неорган. материалы. 2017. Т. 53. № 4. С. 386–391.
Орлов В.М., Крыжанов М.В., Калинников В.Т. Восстановление оксидных соединений ниобия парами магния // ДАН. 2015. Т. 465. № 2. С. 182–185.
Gille G., Schnitter Ch., Brumm H. et al. Nanosize structures composed of valve metals and valve metal suboxides and process for producing them: Pat. WO 2009/021820. 2009.
Орлов В.М., Крыжанов М.В., Князева А.И. Осауленко Р.Н. Порошки ниобия с мезопористой структурой // Физикохимия поверхности и защита материалов. 2018. Т. 54. № 5. С. 444–449.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы


