Неорганические материалы, 2019, T. 55, № 12, стр. 1342-1350
Физико-химический и методологический подходы к разработке комплексных схем получения высокочистых веществ
В. А. Федоров 1, *, Н. А. Потолоков 1, Т. К. Менщикова 1, М. Н. Бреховских 1
1 Институт общей и неорганической химии им. Н.С. Курнакова Российской академии наук
119991 Москва, Ленинский пр., 31, Россия
* E-mail: fedorov@igic.ras.ru
Поступила в редакцию 10.04.2019
После доработки 30.05.2019
Принята к публикации 19.06.2019
Аннотация
Обобщены результаты исследований по разработке физико-химического и научно-методологического подходов к получению высокочистых веществ с использованием комплексных технологических схем. В основу положены идентификация и химические превращения примесей в процессах извлечения из исходного сырья, синтеза и глубокой очистки веществ различными методами. Разработан научно-методологический подход к выбору и обоснованию комплексных схем получения соединений особой чистоты с суммарным содержанием микропримесей 1 × 10–4–1 × 10–5 мас. % (марки 6N и 7N) из традиционного и нетрадиционного сырья. Получены партии высокочистых мышьяк- и галлийсодержащих веществ и проведены их испытания в технологии перспективных материалов микроэлектроники и оптики.
ВВЕДЕНИЕ
Высокочистые вещества находят все возрастающее применение в различных приоритетных направлениях науки и техники, в таких как микро- и наноэлектроника, оптика, лазерная техника, гелиоэнергетика. Необходимы вещества с суммарным содержанием микропримесей 1 × 10–4–1 × × 10–5 мас. %.
Достижения такого качества возможны на основе исследований глубокой очистки веществ традиционными (ректификация, адсорбция, экстракция, микрофильтрация) и нетрадиционными (кристаллизация, мембранное газоразделение) методами [1]. Наш многолетний опыт работы и достижения других авторов [2] свидетельствуют о том, что применение только одного высокоэффективного метода не обеспечивает получение веществ требуемой чистоты. Особый интерес представляют разработки комплексных схем, включающих в себя направленный синтез исходного вещества и комбинацию процессов, каждый из которых обладает определенной селективностью по отношению к конкретным классам микропримесей. Реализация такого подхода дает возможность достигнуть максимальной степени очистки и высокого выхода вещества. Так, перспективным является применение ректификации в сочетании с другими процессами, например, кристаллизацией, адсорбцией, химико-термической обработки (ХТО) для глубокой очистки соединений мышьяка, кремния, металлоорганических соединений (МОС) [2, 3]. Однако эти работы скорее относятся к решению практических вопросов очистки конкретных веществ и не рассматривают общие проблемы по всему циклу: от синтеза (извлечения) до технологии конечных высокочистых продуктов.
Целью настоящей работы является обобщение физико-химического и научно-методологического подходов к разработке комплексных технологических схем получения некоторых классов высокочистых веществ из различного сырья.
На этапе исследований решались следующие научно-технические задачи:
– комплексный анализ исходного сырья, определение агрегатной и химической формы примесей;
– идентификация химических форм примесей и их превращение в процессах глубокой очистки веществ;
– разработка физико-химических основ (статика, кинетика, динамика) и проверка эффективности потенциально пригодных методов очистки;
– выбор и обоснование комплексных технологических схем получения высокочистых веществ квалификаций 6N и 7N с учетом генетических особенностей исходного сырья;
– получение экспериментальных партий особо чистых веществ и их испытания в технологии полупроводниковых и оптических материалов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Объектами исследования служили промышленные образцы элементного мышьяка и его триоксида различной квалификации, извлекаемые из сульфидных руд (As2S3, FeAsS) и галлийсодержащие вещества из нетрадиционного сырья – вторичных отходов цветной металлургии и полупроводниковых материалов АIIIBV. AsCl3 синтезировали из элементов; AsН3 был получен гидролизом Mg3As2. Первостепенное внимание уделено переработке технических соединений мышьяка в высокочистые продукты (элементный мышьяк, трихлорид мышьяка, арсин) из люизита, запасы которого (более 10 000 т) могут служить основным альтернативным промышленным источником из-за отсутствия в нашей стране рудных месторождений мышьяка.
Синтез и глубокую очистку веществ осуществляли в аппаратуре из особо чистого кварца. Методики процессов ректификации AsCl3, адсорбции микропримесей в паровой фазе, экстракции, кристаллизации мышьяка из расплава представлены в [3].
Качество веществ контролировали с помощью химико-спектрального, газохроматографического, масс-спектрометрического и хромато-масс-спектрометрического анализов [3].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
С применением различных методов проведено физико-химическое исследование исходного сырья, подлежащего переработке в продукты квалификации “ос. ч.”.
Микро- и макросостав отходов. Установлено, что исходное сырье содержит, как правило, вторую фазу (до 30 мас. %) и значительное количество примесей (более 3%). В качестве примера в табл. 1 приведена характеристика качества технического мышьяка различного происхождения. Все образцы близки по своим физико-химическим свойствам, отличаются по примесному составу, однако пригодны для переработки в высокочистые продукты.
Таблица 1.
Характеристика качества технического мышьяка, полученного из различного сырья
| Примесь | Содержание примеси, мас. % | ||
|---|---|---|---|
| гидролиз люизита с разложением реакционных масс | из отходов цветной металлургии | на основе традиционного сырья (As2S3) | |
| Fe | 4 × 10–3 | 4 × 10–2 | 5 × 10–4 |
| Al | 2 × 10–4 | 2.8 × 10–2 | 1 × 10–4 |
| Mn | 5 × 10–5 | 2.5 × 10–3 | 3 × 10–5 |
| Cr | 6 × 10–4 | 4 × 10–4 | 8 × 10–5 |
| Na, K | 2 × 10–1 | 3 × 10–2 | >1 × 10–2 |
| Si | 2 × 10–4 | 6 × 10–3 | 2 × 10–3 |
| Zn | 5 × 10–3 | 4 × 10–3 | 2 × 10–4 |
| Ca | 4 × 10–3 | 4 × 10–3 | 2 × 10–4 |
| Ni | 4 × 10–4 | 3 × 10–4 | 7 × 10–5 |
| Ti | 1 × 10–3 | 1 × 10–4 | – |
| Pb | 6 × 10–3 | 3 × 10–2 | 4 × 10–4 |
| Cd | 8 × 10–5 | – | – |
| S, Se, Te | >2 × 10–2 | 4 × 10–4 | 9 × 10–4 |
| C | 2.9 | 3.1 | >10–2 |
Галлий технический после извлечения из отходов GaAs и GaP путем вакуум-термической обработки (ВТО) и особенно после жидкофазной эпитаксии (ЖФЭ) содержит 2–15 мас. % примесей в виде второй фазы, которую удаляли фильтрацией [4]. Типичное содержание примесей в галлии после извлечения методом ВТО из отходов GaAs газофазной эпитаксии GaAs (группы 1, 2), GaP (группы 3, 4) и ЖФЭ (группа 5) представлено в табл. 2. Видно, что концентрация примесей находится в пределах от 2.3 × 10–1 до 1.2 × 10–1 мас. % и максимальна для галлия, выделенного из отходов после ЖФЭ. Содержание основного компонента составляет более 99.7 мас. %.
Таблица 2.
Содержание примесей в галлии после очистки фильтрацией
| Примесь | Содержание примесей, мас. % | ||
|---|---|---|---|
| группы 1, 2 | группы 3, 4 | группa 5 | |
| Ni | 3 × 10–4 | 1 × 10–4 | 1 × 10–4 |
| Zn | 1 × 10–3 | 1 × 10–4 | 5 × 10–2 |
| Cu | 6 × 10–2 | 6 × 10–2 | 5 × 10–3 |
| Al | 1 × 10–3 | 1 × 10–4 | 1 × 10–2 |
| Pb | 2 × 10–4 | 2 × 10–4 | 1 × 10–4 |
| Fe | 8 × 10–4 | 8 × 10–4 | 1 × 10–4 |
| Si | 1 × 10–3 | 1 × 10–3 | 1 × 10–3 |
| Sn | 1 × 10–2 | 1 × 10–3 | 5 × 10–1 |
| Mn | 5 × 10–4 | 5 × 10–4 | 1 × 10–4 |
| Cr | 3 × 10–3 | 1 × 10–4 | 1 × 10–4 |
| In | 1 – 5* | 1 × 10–3 | 1 × 10–1 |
| Te | 1 × 10–4 | 1 × 10–4 | 5 × 10–3 |
| Ag | 3 × 10–2 | 3 × 10–2 | 1 × 10–4 |
| Ca | 4 × 10–4 | 1 × 10–4 | 1 × 10–4 |
| As | 1 × 10–3 | <1 × 10–5 | 1 × 10–3 |
| Ge | 1 × 10–2 | 1 × 10–2 | 1 × 10–2 |
| S | 1 × 10–4 | 1 × 10–4 | 1 × 10–4 |
| P | <1 × 10–5 | 1 × 10–4 | <1 × 10–5 |
| Суммарное содержание | 1.2 × 10–1* | 8 × 10–2 | 2.3 × 10–1 |
Идентификация и химические превращения примесей. Знания химических форм примесей необходимы для обоснования методов и комплексных схем глубокой очистки веществ.
Методологический подход к решению этой группы задач проиллюстрируем на наиболее ярком в научном плане и имеющем важное практическое значение примере – на получении высокочистого мышьяка и его соединений из различного сырья. Установлено, что в AsCl3 различного способа получения примеси присутствуют в виде хлоридов, оксихлоридов, ацетилхлоридов, причем ряд примесей находится в нескольких химических формах (табл. 3). В синтезированном из элементов в среде AsCl3 (HCl), S, Si и Se находятся в основном в виде оксихлоридов, что объясняется их склонностью к гидролизу.
Таблица 3.
Основные химические формы примесей в AsCl3
| Примесь | Химическая форма примеси в AsCl3, синтезированном | |
|---|---|---|
| из элементов (t = 150°С) | из As2S3 | |
| Mg, Mn, Pb, Fe, Sn, Ni, Al, Cr, Cu, Zn, Co, Ti | MnClm | MnClm |
| Кремний | SiCl4, Si2Cl6, (Si2OCl6) | Si2OCl6 (SiCl4, Si2Cl6) |
| Сера | S2Cl2 (SO2, SO2Cl2, SOCl2) | SOCl2, SO2Cl2 (S2Cl2) |
| Селен | SeCl4 | SeOCl2(SeCl4) |
| Вода и гидроксиды | H2O, As(OH)nCl3 – n, AsOCl | |
| Органические соединения | CHCl3, C2H5Cl, CCl4, 1,1-C2H4Cl2, C2Cl6, 1,2-C2H4Cl2, 1,1,1,2-C2H2Cl4, 1,1,2,2- C2H2Cl4, C2HCl5 | |
| As-органические соединения | Отсутствуют | CH3AsCl2, C2H5AsCl2, (CH3)2AsCl, C2H5OAsCl2 |
Принципиальным моментом является возможное превращение химических форм примесей в процессах синтеза и глубокой очистки AsCl3.
Так, в AsCl3 различного способа получения сера находится в виде Sэл, S2Cl2, SO2Cl2, SO2. Наиболее стабильной формой S является сульфурилхлорид. Селен в виде SеOCl2 находится в зависимости от содержания HCl и H2O в динамическом равновесии с другими формами. Наиболее стабильной формой является SeOCl2, а переход его в AsCl3 при синтезе из мышьяка (с примесью As2О3) значителен. В процессах получения AsCl3 протекают обратимые реакции (см. табл. 3):
(1)
${\text{AsC}}{{{\text{l}}}_{3}} + {{{\text{H}}}_{{\text{2}}}}{\text{O}} = {\text{As}}\left( {{\text{OH}}} \right){\text{C}}{{{\text{l}}}_{2}} + {\text{HCl}},$(2)
${\text{As}}\left( {{\text{OH}}} \right){\text{C}}{{{\text{l}}}_{2}} = {\text{AsOCl}} + {\text{HCl}}.$В области концентраций H2O в AsCl3 менее 3 × × 10–2 моль/л при 20°С гидролиз протекает по первой ступени, при содержании H2O более 3 × × 10–2 моль/л наблюдается замещение хлора по схеме: AsCl3 + nH2O = As(OH)3–n + nHCl, где n = 2, 3.
Химические формы примесей в арсине, полученном из технического мышьяка по схеме ${\text{A}}{{{\text{s}}}_{2}}{{{\text{S}}}_{3}} \to {\text{A}}{{{\text{s}}}_{{{\text{техн}}}}} \to {\text{M}}{{{\text{g}}}_{3}}{\text{A}}{{{\text{s}}}_{2}} \to {\text{As}}{{{\text{H}}}_{3}}$ составляют:
– углеводороды (метан, этан, этилен и др.), суммарное содержание которых достигает 1 × 10–1–1 × × 10–2 мас. %. Химическая форма нахождения стабильна;
– гидриды серы, селена, теллура (1 × 10–2 мас. %); эти примеси лабильны;
– фосфины и стибин (1 × 10–2%); стабильны при ректификации.
Специфической примесью в арсине является вода (0.5%), очистка от которой ректификацией затрудняется из-за образования аэрозолей. AsH3 c более низким содержанием примесей получают электрохимическим способом из люизита [5].
Результаты по идентификации и превращению химических форм примесей служат основой для разработки методов глубокой очистки веществ.
Физико-химические основы процессов глубокой очистки веществ. Излучено поведение примесей в процессах глубокой очистки мышьяк- и галлийсодержащих веществ методами ректификации, адсорбции в паровой фазе, экстракции, ХТО, направленной кристаллизации.
На рис. 1 схематично показано поведение примесей в процессах глубокой очистки AsCl3 ректификацией. Видно, что происходит эффективная очистка AsCl3 от примесей хлоридов металлов, теллура, органических веществ, влаги. Исключение составляют халькогены (S2Cl2, SeOCl2) и кремний (Si2OCl6). Таким образом, ректификация обеспечивает эффективную очистку AsCl3 от большинства примесей и может служить основным методом получения AsCl3 особой чистоты.
Рис. 1.
Поведение примесей в процессах очистки AsCl3 экстракцией 12N HCl (1), ректификацией (2), адсорбцией в паровой фазе на угле БАУ (3).
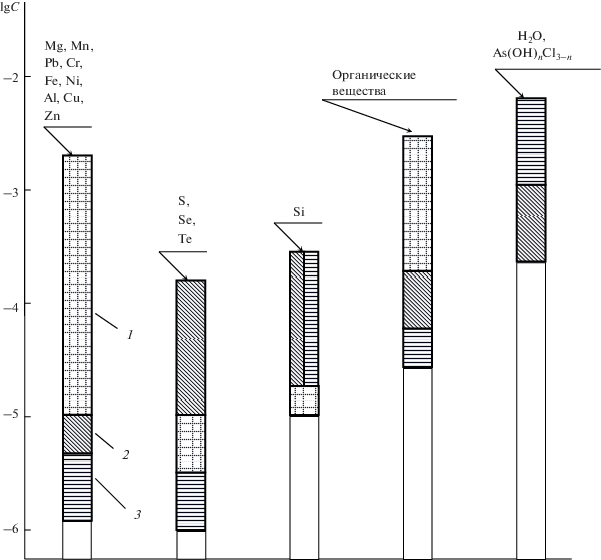
Для глубокой очистки AsCl3 от микропримесей нами предложен адсорбционный метод в паровой фазе на активированном угле БАУ. Данные, приведенные на рис. 1, характеризуют селективность поглощения углем БАУ в паровой фазе (138°С) примесей серы, селена, теллура, органических веществ и хлоридов металлов. Очистка же от соединений кремния, As-органических веществ, воды и гидроксохлоридов незначительна.
Экспериментальные данные по ХТО AsCl3 до 800–900°С показывают, что МОС подвергаются пиролизу при высоких температурах с образованием элементного мышьяка с примесью углерода. AsCl3, синтезированный из элементов при пониженных температурах, подвергать ХТО нецелесообразно из-за отсутствия в нем МОС.
Из данных рис. 1 видно, что экстракция эффективна для удаления примесей большинства металлов, кремния, халькогенов и менее эффективна для очистки AsCl3 от органических и кислородсодержащих веществ. Применение экстракционного метода с использованием 12N HCl перспективно на предварительных стадиях получения особо чистого AsCl3 при значительном содержании примесей в исходном сырье (до 10–2 мас. %).
Глубокая очистка галлия. С учетом специфических особенностей технического галлия из отходов полупроводниковых материалов (табл. 2) изучена эффективность его очистки различными методами. Основные результаты сводятся к следующему:
– гидрохимическая обработка (ГХО) отходов кислотами снижает примеси щелочных и щелочноземельных элементов до 10–5–10–6 мас. %;
– ВТО уменьшает концентрацию Cd, As, P, Te, S и Se до 5 × 10–5 мас. % по сравнению с начальным n × 10–4%;
– электрохимическое рафинирование (ЭХР) с высокой эффективностью позволяет удалять примеси Sn, In, Cr, Fe, Ni, Mn, Ag до 4 × 10–5–5 × 10–6%;
– направленная кристаллизация по Чохральскому (НКЧ) и горизонтальная направленная кристаллизация (ГНК) эффективны для удаления примесей из галлия – глубина очистки достигает ≤1 × 10–6%. Однако эффективность НКЧ резко падает при высоких начальных концентрациях примесей;
– разработан модифицированный метод направленной кристаллизации с вращением контейнера (НКВК), определены условия эффективного отделения примесей при их высоком начальном содержании [4].
Изложенные выше результаты исследований по разработке физико-химических основ глубокой очистки мышьяк- и галлийсодержащих веществ свидетельствуют о невозможности получения в отдельных случаях продуктов квалификации “ос. ч.” с применением лишь одного высокоэффективного метода. Однако такое качество не удовлетворяет современным техническим требованиям микроэлектроники. Необходима комбинация методов в рамках единой комплексной схемы.
Комплексные технологические схемы получения высокочистых веществ. В основу разработки комплексных схем нами положен принцип постадийного удаления различных классов примесей. При технической организации процессов учитывали генетические особенности перерабатываемого сырья, главным из которых является возможная лабильность химических форм микропримесей. Таким образом, весь процесс получения высокочистого вещества включает четыре основных стадии:
– направленный синтез;
– стабилизацию химических форм примесей;
– высокоэффективные, многоступенчатые процессы разделения;
– финишную очистку.
На основе предельных возможностей методов очистки на рис. 2, 3 представлены комплексные технологические схемы получения высокочистых AsCl3 и галлия, на рис. 4, 5 – номограммы поведения примесей.
Рис. 2.
Технологическая схема получения высокочистого мышьяка из отходов цветной металлургии и продуктов детоксикации люизита по схеме “гидролиз-электролиз”.
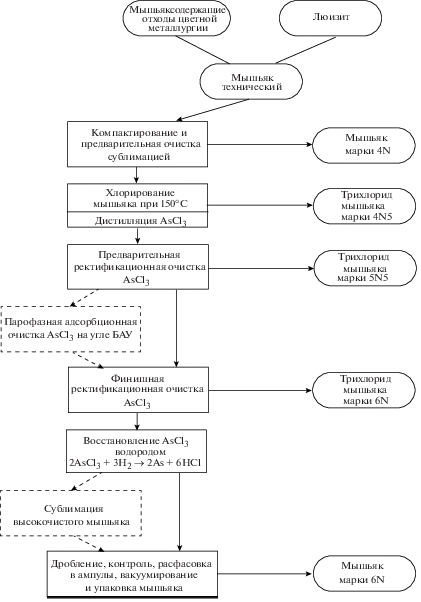
Рис. 3.
Комплексная технологическая схема получения высокочистого галлия из отходов производства полупроводниковых материалов.
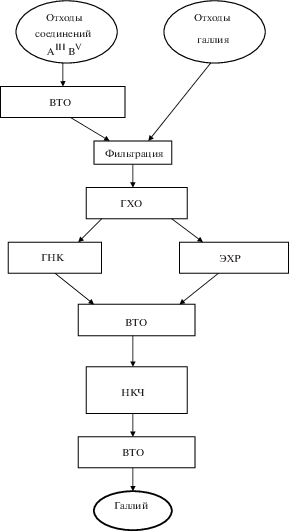
Рис. 4.
Номограмма поведения примесей при очистке AsCl3: 1 – органические вещества, 2 – Н2О, 3 – Si, 4 – S, 5 –труднолетучие хлориды, 6 – Se, 7 – Te.
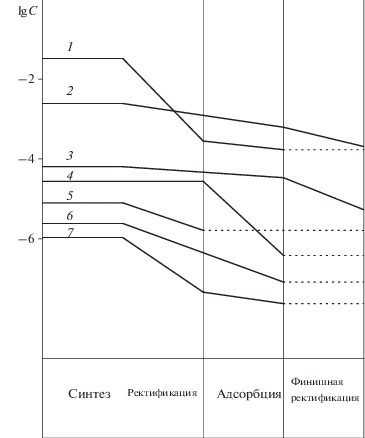
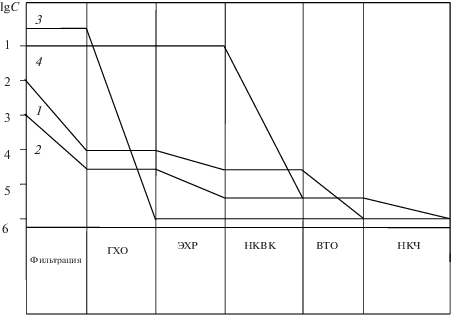
Рис. 5.
Номограмма поведения примесей при очистке технического галлия: 1 – As, P, Te, Cd, S, Se; 2 – Si, Cr, Fe, Ni; 3 – Na, K, Ca, Al, Zn, Mg; 4 – Sn, In, Cu, Fe, Mn, Ag, Au, Pb, Co.
В процессе очистки AsCl3 (рис. 2) стабилизация химических форм примесей халькогенов, кремния, кислородсодержащих веществ и ацетилхлоридов достигается на стадиях синтеза AsCl3 и предварительной ректификации. В тех случаях, когда в исходном сырье содержатся значительные количества халькогенов, необходима дополнительная адсорбционная очистка.
Все схемы переработки различных видов технического мышьяка позволяют получить продукт практически одинаковой чистоты (6N). Наибольшей простотой характеризуется схема очистки AsCl3, синтезированного из элементов при пониженной температуре, тогда используется лишь один высокоэффективный метод – ректификация. AsCl3 после очистки характеризуется низким содержанием микропримесей (мас. %): Mn, Mg, Pb, Cu, Fe, Ni, Al, Cr, Zn < 2 × 10–6; Sb и Sn(сумма) <5 × 10–6; S < 5 × 10–6; Sе < 5 × 10–6; Те < 1 × 10–8; органические вещества <5 × 10–5; МОС мышьяка <1 × 10–4. Восстановление AsCl3 “ос. ч.” водородом обеспечивает получение элементного мышьяка марки 6N. Последующая очистка направленной кристаллизацией [6] позволяет получить продукт уникального качества – 99.99999 мас. % (7N).
В процессе глубокой очистки технического галлия из различных видов отходов по комплексной схеме (рис. 3) на стадии предварительной фильтрации имеет место отделение от второй фазы; резко снижается концентрация As, P, Te, Cd, S, Se. Высокая степень удаления щелочных и щелочноземельных элементов, Zn и Al, оксидных и гидроксидных включений достигается ГХО. При начальном содержании Sn, Ag ниже 0.05 мас. % и маломасштабном производстве предпочтительнее использовать НКВК. Применение ЭХР целесообразно при больших объемах производства с высоким содержанием примесей. Финишной стадией является НКЧ, обеспечивающая снижение содержания примесей до 2 × 10–6 мас. %.
Содержание примесей в образцах высокочистого галлия, полученного из различных видов отходов по предложенной схеме (рис. 5), приводит практически к одинаковым результатам. Очищенный галлий отвечает квалификации 99.9999 мас. % (6N), не уступая по качеству материалу из традиционного сырья.
Комплексная схема получения высокочистого арсина включает постадийное удаление из него различных классов примесей. Первой стадией этого процесса является синтез AsH3 гидролизом Mg3As2 в нейтральной среде, при этом не образуются гидриды элементов VI группы. От углеводородов, фосфина, стибина AsH3 селективно очищается низкотемпературной ректификацией. Эффективность различных методов глубокой очистки AsH3 изложена в [7]. Таким образом, производимый для эпитаксиальных технологий соединений АIIIBV арсин имеет чистоту 99.9999 мас. %. Использование в качестве исходного сырья технического AsH3 – продукта от детоксикации люизита – обеспечивает чистоту не хуже 99.99995%. Термическим разложением при 750–850°С выделен высокочистый мышьяк с низким содержанием примесей. Заключительной операцией получения высокочистого мышьяка, является, как правило, вакуумная сублимация или кристаллизация из расплава для перевода образующегося As в компактный образец, устойчивый к окислению.
Важно отметить, что применение высокочистых мышьяксодержащих соединений (AsCl3, элементный мышьяк, AsH3) и галлия квалификаций 6N и 7N обеспечивает изготовление в производственных условиях полупроводниковых материалов АIIIBV и широкого класса уникальных изделий микроэлектроники и оптики с высокими характеристиками.
ЗАКЛЮЧЕНИЕ
Развиты научно-технические основы получения высокочистых мышьяк- и галлийсодержащих веществ квалификации 99.9999 (6N) и 99.99999 мас. % (7N) из различного исходного сырья – традиционного и нетрадиционного.
Обоснован физико-химический и научно-методологический подходы к разработке комплексных технологических схем получения высокочистых веществ, основой которых является комплексный анализ исходного сырья, идентификация химических форм примесей и их превращения в процессах синтеза (извлечения) и глубокой очистки веществ с учетом генетических особенностей исходного сырья.
Получены партии AsCl3, элементного мышьяка, AsH3 и Ga квалификаций 6N и 7N, высокое качество которых подтверждено результатами испытаний при изготовлении перспективных материалов микроэлектроники и оптики.
Развитые научно-технические основы получения мышьяка и галлия высокого качества дают возможность повышать степень их чистоты и совершенствовать технологию производства по экологическим и экономическим показателям.
Список литературы
Чурбанов М.Ф., Пашинкин А.С., Федоров В.А. Актуальные задачи химии высокочистых веществ // Неорган. материалы. 2009. Т. 45. № 9. С. 1029–1034.
Нисельсон Л.А., Ярошевский А.Г., Гасанов и др. Глубокая очистка мышьяка // Высокочистые вещества. 1997. № 4. С. 69–74.
Fedorov V.A., Churbanov M.F. High pure Arsenic and its Compaunds for Optical and Semiconducting Materials // Inorg. Mater. 2016. V. 52. № 13. P. 1339–1360.
Козлов С.А., Потолоков Н.А., Федоров В.А. и др. Получение высокочистого галлия из отходов производства полупроводниковых материалов // Неорган. материалы. 2003. Т. 39. № 12. С. 5–16.
Турыгин В.В., Томилов А.П., Федоров В.А. Получение летучих неорганических гидридов электрохимическим методом // Высокочистые вещества. М.: Научный мир, 2018. С. 632–661.
Федоров В.А., Гасанов А.А., Потолоков Н.А. и др. Глубокая очистка мышьяка методом кристаллизации // Неорган. материалы. 2018. Т. 54. № 10. С. 1085–1091.
Федоров В.А., Потолоков Н.А., Менщикова Т.К., Бреховских М.Н. Гидридный метод получения высокочистого мышьяка // Неорган. материалы. 2018. Т. 54. № 10. С. 1092–1098.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы


