Неорганические материалы, 2019, T. 55, № 12, стр. 1267-1273
Синтез α-Si3N4 в режиме горения с участием легкоплавких солевых добавок
В. В. Закоржевский 1, *, Н. И. Мухина 1
1 Институт структурной макрокинетики и проблем материаловедения им. А.Г. Мержанова
Российской академии наук
142432 Московская обл., Черноголовка, ул. Академика Осипьяна, 8, Россия
* E-mail: zakvl@ism.ac.ru
Поступила в редакцию 21.11.2018
После доработки 08.04.2019
Принята к публикации 06.06.2019
Аннотация
Изучено влияние легкоплавких солевых добавок на морфологический и фазовый состав нитрида кремния полученного в режиме горения. Показано влияние добавок на механизм структурообразования. На основе расчетов равновесных составов для условий синтеза предложены механизмы влияния добавок на процесс структурообразования. Показано влияние температуры синтеза и добавок на фазовый состав продуктов синтеза. Определены условия получения порошков альфа фазы нитрида кремния с равноосной формой частиц.
ВВЕДЕНИЕ
Керамические материалы из нитрида кремния нашли широкое применение для производства конструкционной и функциональной керамики, работающей в экстремальных условиях высоких температур и механических нагрузок. Во многом прочностные свойства керамики зависят от характеристик исходных порошков нитрида кремния. В зависимости от способа получения керамического материала используются порошки с разным химическим и морфологическим составом. Важными параметрами, влияющими на свойства керамики, являются размер и форма частиц. Для получения керамики методом горячего прессования используются порошки с высокой удельной поверхностью (10–15 м2/г) и равноосной формой частиц. Для получения заготовок Si3N4 методом шликерного литья предпочтительно использовать более крупные порошки с удельной поверхностью 5–7 м2/г, чтобы увеличить степень наполнения шликера. Чтобы предусмотреть усадку керамики в трех плоскостях при спекании также необходимо использовать порошки с равноосной формой частиц. Однако при производстве длинномерных заготовок методом шликерного литья желательно использовать порошок Si3N4 с удлиненной или волокнистой формой частиц. При впрыске шликера с такими частицами в форму они ориентируются в одну сторону. При спекании формируется микроструктура преимущественно с однонаправленным расположением зерен β-Si3N4. Такая структура керамики дает повышенные прочностные характеристики на изгиб. Таким образом, форма частиц так же важна, как химический и фазовый состав.
В основном, порошок нитрида кремния получают печным способом [1–3] и методом синтеза и разложения диимида кремния [4]. Процесс синтеза управляем и позволяет получить порошок нитрида кремния с заданным химическим и фазовым составом. Однако для получения частиц равноосной формы выполняются операции измельчения и классификации продуктов синтеза.
При получении α-Si3N4 в режиме горения для реализации низкотемпературного синтеза в состав шихты вводятся газифицирующиеся добавки, такие как NH4Cl, NH4F. Частицы нитрида кремния, полученные таким способом, представлены нитевидными кристаллами и имеют тонковолокнистую микроструктуру. Такая микроструктура формируется за счет реализации газофазного механизма структурообразования, в котором участвуют газообразные продукты разложения – NH4Cl и NH4F [5]. При получении α-Si3N4 с использованием субмикронного порошка кремния без добавок NH4Cl, NH4F также реализуется газофазный механизм структурообразования, в котором участвуют оксид и субоксид кремния. При этом образуются частицы удлиненной формы [6]. Для получения порошков нитрида кремния с равноосной формой частиц также требуются длительное измельчение и классификация. Поскольку частицы нитрида кремния удлиненной формы образуются в результате газофазных реакций, для получения частиц равноосной формы необходимо создать условия синтеза, которые препятствуют реализации газофазного механизма структурообразования. Влияние пленкообразующих, т.е. негазифицирующихся, солевых добавок на процесс структурообразования при самораспространяющемся высокотемпературном синтезе (СВС) Si3N4 не изучено. В работах по синтезу нитрида кремния методом СВС-аз, при котором в качестве побочного продукта образуются NaF или NaCl, не описано влияние галогенидов натрия на фазовый состав и микроструктуру нитрида кремния [7].
В представленной работе исследовано влияние добавок легкоплавких солей на микроструктуру и фазовый состав нитрида кремния.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для экспериментов использовали базовый состав шихты Si + Si3N4. В качестве добавок были использованы бескислородные водорастворимые легкоплавкие соли. Характеристики исходных компонентов шихты представлены в табл. 1.
Таблица 1.
Характеристика исходных компонентов шихты
| Компонент | tпл, °С | tкип, °С | d50, мкм | Sуд, м2/г | α-фаза, мас. % | Кислород, мас. % |
|---|---|---|---|---|---|---|
| Si | 1419 | 2–2.5 | 5–6 | 0.8 | ||
| Si3N4 | 1900 (возг.) | 1900 (возг.) | 3–4 | 97 | 1.4 | |
| NaF | 992 | 1704 | 200 | |||
| NaCl | 801 | 1465 | 200 | |||
| Na2SiF6 | 570 (разл.) | 200 |
Синтез проводили при содержании кремния в шихте 23–28 мас. % для разных экспериментов. Содержание солей в шихте – 1 и 3 мас. %. Смешивание компонентов шихты проводили в шаровой мельнице в течение 1 ч. Начальное давление азота 6.0 МПа. Масса шихты 3.0 кг. Эксперименты проводили в промышленном СВС-реакторе объемом 30 л.
Синтезированные образцы нитрида кремния, полученные с участием фтористого натрия, измельчали керамическими шарами в воде в течение 1 ч для разрушения конгломератов и удаления фтористого натрия. Частицы нитрида кремния отделяли от раствора NaF с помощью вакуум-фильтра, промывали дистиллированной водой. После сушки нитрид кремния дезагломерировали на струйной мельнице.
Морфологию продуктов синтеза изучали с помощью сканирующего электронного микроскопа LEO 1450 фирмы Carl Zeiss SMT AG Company. Размер частиц определяли на лазерном анализаторе частиц MicroSizer 201. Фазовый состав продуктов синтеза определяли с помощью дифрактометра ДРОН 3М. Массовое содержание α-фазы определяли по методике, описанной в [8]. Температуры горения измеряли с помощью термопары ВР5-ВР20.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Влияние фтористого натрия. При изучении влияния фтористого натрия на микроструктуру полученного Si3N4 и параметры синтеза установлено, что при введении 1 мас. % NaF в состав шихты продукт синтеза формируется в виде конгломератов, которые состоят из частиц равноосной формы размером 0.5–3 мкм (рис. 1). При снижении содержания кремния в шихте с 28 до 24 мас. % температура горения снижается от 1849 до 1713°С. Содержание мелких частиц возрастает, а диапазон размеров частиц составляет 0.3–3 мкм (рис. 2). Несмотря на уменьшение размера частиц, удельная поверхность для всех образцов составила 3.4 м2/г, видимо, из-за консолидации частиц Si3N4 с помощью фтористого натрия. Содержание α-фазы для 28% Si снизилось с 97 до 96 мас. %, а для 24 мас. % Si возросло до 98 мас. %. При увеличении солевой добавки до 3 мас. % температура горения составила 1773°С. Содержание α-фазы в продукте синтеза значительно уменьшилось – с 97 до 91 мас. %, видимо, из-за увеличения количества NaF в шихте. Продукт синтеза состоял из конгломератов, образованных в основном равноосными частицами размером 0.5–3 мкм с преобладанием частиц размером более 1 мкм. Также присутствуют удлиненные частицы, которые имеют огранку, присущую β-фазе Si3N4 (рис. 3). Удельная поверхность составила 2.6 м2/г. РФА не показал наличия NaF в продукте синтеза, поскольку основные пики NaF совпадают с пиками α-Si3N4 и их нельзя выделить. Однако элементный анализ, проведенный с помощью энерго-дисперсионного анализатора, показал наличие в образцах Si3N4 атомов фтора и натрия в количестве 0.7–1.3 мас. %. Наличие NaF зафиксировано в точке измерения температуры, на глубине 40 мм, так и в приповерхностном, более холодном, слое спека. В центральной области спека, на глубине 60 мм от поверхности, сформировалась микроструктура с игольчатой формой частиц (рис. 4). Поскольку при СВС нитрида кремния по сечению спека наблюдается градиент температур, то температура горения в центральной области превысила 1773°С, что привело к формированию игольчатых частиц β-Si3N4. Содержание α-фазы составило 51 мас. %. Анализ не показал наличия NaF. Видимо, газификация фтористого натрия способствует фазовому α → β-переходу.
Рис. 4.
Микроструктура центральной части спека Si3N4 при содержании в шихте 26 мас. % Si и 3 мас. % NaF.

Расчет равновесного состава с участием фтористого натрия показал образование Si3N4 , Siж, Naг, SiF, а также Na2SiO3 в виде жидкости. Силикат натрия, видимо, образуется в виде пленки на поверхности частиц кремния при взаимодействии NaF с оксидной пленкой кремния по реакции Si + SiO2 + NaF = Na2SiO3 + SiF. Поскольку силикат натрия имеет более высокую температуру плавления (1089°С) и кипения, чем фтористый натрий, пленка Na2SiO3 препятствует реализации газофазного механизма синтеза.
Основные параметры и характеристика продуктов синтеза представлены в табл. 2.
Таблица 2.
Основные параметры и характеристика продуктов синтеза с добавкой фтористого натрия
| Si, мас. % | NaF, мас. % | tгор, °С (расчет) | tгор, °С | Скорость горения, мм/с | α-фаза, мас. % | Sуд, м2/г | Размер частиц, мкм |
|---|---|---|---|---|---|---|---|
| 28 | 1 | 1864 | 1849 | 0.38 | 96 | 3.4 | 0.5–3.0 |
| 26 | 1 | 1800 | 1784 | 0.31 | 98 | 3.4 | 0.5–3.0 |
| 24 | 1 | 1723 | 1713 | 0.24 | 98 | 3.4 | 0.3–3.0 |
| 26 | 3 | 1792 | 1773 | 0.33 | 91 | 2.0 | 0.5–3.0 |
Влияние гексафторсиликата натрия. В отличие от фтористого натрия, который плавится при температуре 992°С, гексафторсиликат натрия разлагается при температуре 570°С с образованием фтористого натрия и газообразного SiF4. В итоге, при разложении 1 мас. % Na2SiF6 в шихте остается 0.45 мас. % NaF. При содержании 26 мас. % кремния в шихте температура синтеза составила 1808°С, содержание α-фазы незначительно снизилось по сравнению с исходной шихтой – с 97 до 93 мас. %. Изучение микроструктуры показало, что продукт синтеза состоит преимущественно из частиц равноосной формы размером 0.5–3 мкм, также присутствуют частицы игольчатой формы, присущие β-Si3N4 (рис. 5). При снижении доли кремния в шихте до 23 мас. % температура горения составила 1634°С. Содержание α-фазы возросло с 97 до 98 мас. %. Конгломераты Si3N4 состоят из равноосных частиц размером 0.3–3 мкм (рис. 6). Удельная поверхность возросла с 3.2 до 3.6 м2/г. Микроструктура нитрида кремния, полученного из шихты, содержащей 26 мас. % кремния и 3 мас. % Na2SiF6, в основном представлена частицами равноосной формы размером 0.5–3 мкм с преобладанием частиц размером более 1 мкм, также присутствуют частицы удлиненной формы (рис. 7). Частичное образование β-фазы связано с высокой температурой горения (1750°С) и относительно высоким содержанием солевой добавки. РФА показал снижение содержания α-фазы в продукте синтеза по сравнению с исходной шихтой – с 97 до 95 мас. %. Удельная поверхность уменьшилась до 2.3 м2/г. Элементный анализ, проведенный с помощью энерго-дисперсионного анализатора, показал наличие натрия в количестве 0.66 мас. %. Основные параметры и характеристика продуктов синтеза представлены в табл. 3.
Таблица 3.
Основные параметры и характеристика продуктов синтеза с добавкой гексафторсиликата натрия
| Si, мас. % | Na2SiF6, мас. % | tгор, °С (расчет) | tгор, °С | Скорость горения, мм/с | α-фаза, мас. % | Sуд, м2/г | Размер частиц, мкм |
|---|---|---|---|---|---|---|---|
| 26 | 1 | 1860 | 1808 | 0.29 | 93 | 3.2 | 0.5–3.0 |
| 23 | 1 | 1690 | 1634 | 0.17 | 98 | 3.6 | 0.3–3.0 |
| 26 | 3 | 1799 | 1750 | 0.19 | 95 | 2.3 | 0.5–3.0 |
Влияние хлористого натрия. При введении в состав шихты 1 мас. % хлористого натрия температура горения составила 1677 и 1615°С для 26 и 24 мас. % Si соответственно. Микроструктура представлена частицами равноосной и удлиненной формы (рис. 8). При снижении температуры горения содержание частиц удлиненной формы возрастает (рис. 9). Содержание α-фазы возросло на 2 мас. % по сравнению с шихтой. При введении 3 мас. % NaCl в шихту температура горения составила 1802°С для 26 мас. % Si. Содержание α‑фазы не изменилось по сравнению с шихтой. Микроструктура также представлена частицами равноосной и удлиненной формы (рис. 10). Удельная поверхность Si3N4 при использовании хлористого натрия в количестве 1–3 мас. % и в интервале температур горения 1615–1802°С для всех образцов находилась в диапазоне 3.7–4.2 м2/г. Размеры и форма частиц не изменились. РФА показал наличие NaCl во всех образцах Si3N4. Установлено, что фаза NaCl присутствует только в поверхностном слое спека. Видимо, в процессе горения шихты NaCl испаряется в центральной, более горячей, области волны горения и конденсируется в приповерхностном, более холодном, слое спека.
Образование нитевидных кристаллов Si3N4 свидетельствует о реализации газофазного механизма структурообразования [9]. Расчет равновесного состава с участием хлористого натрия помимо нитрида кремния показал наличие Naг, SiCl, SiO, Siж, которые, видимо, способствуют частичной реализации газофазного механизма структурообразования. Из-за низкой температура кипения NaCl возможна реакция NaClг + Siж = SiCl + Naг, которая обеспечивает синтез Si3N4 по реакции SiCl + Naг + N2 = = Si3N4 + NaCl в газовой фазе с образованием частиц игольчатой формы. При этом NaCl конденсируется в приповерхностном слое спека. Основные параметры и характеристика продуктов синтеза представлены в табл. 4.
Таблица 4.
Основные параметры и характеристика продуктов синтеза с добавкой хлористого натрия
| Si, мас. % | NaCl, мас. % | tгор, °С (расчет) | tгор, °С | Скорость горения, мм/с | α-фаза, мас. % | Sуд, м2/г | Размер частиц, мкм |
|---|---|---|---|---|---|---|---|
| 26 | 1 | 1773 | 1677 | 0.22 | 97 | 3.7 | 0.5–3.0 |
| 24 | 1 | 1726 | 1615 | 0.15 | 99 | 4.2 | 0.3–3.0 |
| 26 | 3 | 1808 | 1785 | 0.24 | 97 | 3.7 | 0.5–3.0 |
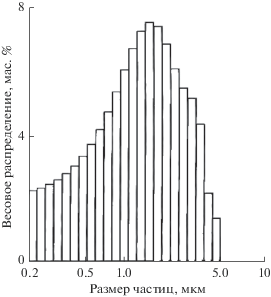
После измельчения и дезагломерации образцов нитрида кремния, синтезированных с участием фтористого натрия, получен порошок нитрида кремния с равноосной формой частиц, полидисперсным распределением (рис. 11, 12). Средний диаметр частиц составил 1.2–1.5 мкм, удельная поверхность 5–6 м2/г.
ЗАКЛЮЧЕНИЕ
При использовании солевых добавок NaF и Na2SiF6 формируются частицы Si3N4 равноосной формы. Увеличение содержания солей в шихте приводит к снижению содержания α-фазы. Размер частиц Si3N4 уменьшается при снижении температуры синтеза. При увеличении содержания добавки от 1 до 3 мас. % увеличивается доля частиц с размером более 1 мкм. Наиболее мелкие частицы нитрида кремния формируются при содержании 1 мас. % добавки в шихте. Размер частиц Si3N4, полученного с солевыми легкоплавкими добавками, соизмерим с размером частиц исходного порошка кремния. Образование частиц равноосной формы происходит вследствие низкой температуры плавления и высокой температуры кипения NaF, а также из-за образования жидкого силиката натрия на поверхности частиц кремния. Пленка жидких NaF и Na2SiO3 на поверхности капли кремния препятствует реализации синтеза в газовой фазе, а процесс азотирования в этом случае протекает в диффузионном режиме в объеме капли жидкого кремния.
При использовании добавки NaCl формируются частицы Si3N4 равноосной и игольчатой формы. При снижении температуры горения содержание частиц игольчатой формы возрастает. Образованию игольчатых частиц, видимо, способствует низкая температура кипения NaCl, которая стимулирует реализацию газофазного механизма структурообразования по реакции NaClг + + Siж = SiCl + Naг, SiCl + Naг + N2 = Si3N4 + NaCl. Увеличение содержания NaCl в шихте до 3 мас. % не приводит к снижению содержания α-фазы.
Список литературы
Atkinson A., Moulson A.J., Roberts E.W. Nitridation of High Purity Silicon // J. Am. Ceram. Soc. 1976. V. 59. № 3. P. 285–289.
Zhang S.C., Cannon W.R. Preparation of Silicon Nitride from Silica // J. Am. Ceram. Soc. 1984. V. 67. № 10. P. 691–695.
Ekelund M., Forslund B., Zheng J. Control of Particle Size in Si3N4 Powders Prepared by High-Pressure Carbothermal Nitridation // J. Mater. Sci. 1996. V. 21. № 21. P. 5749.
Yamada T. Preparation and Evaluation of Sinterable Silicon Nitride Powder by Imide Decomposition Method // Am. Ceram. Soc. Bull. 1993. V. 72. № 5. P. 99–106.
Zakorzhevsky V.V., Borovinskaya I.P. Some Regularities of α-Si3N4 Synthesis in a Commercial SHS Reactor // Int. J. SHS. 2000. V. 9. № 2. P. 171–191.
Закоржевский В.В., Боровинская И.П. Синтез нитрида кремния в режиме горения с использованием ультрадисперсных порошков кремния // Порошковая металлургия. 2009. № 7/8. С. 3–9.
Амосов А.П., Бичуров Г.В. Азидная технология самораспространяющегося высокотемпературного синтеза микро- и нанопорошков нитридов. М.: Машиностроение-1, 2007. 526 с.
Per-Olov Käll. Quantitative Phase Analysis of Si3N4-based Materials // Chem. Scr. 1988. V. 28. P. 439–446.
Гиваргизов Е.И. Рост нитевидных и пластинчатых кристаллов из пара. М.: Наука, 1977. 304 с.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы