Неорганические материалы, 2019, T. 55, № 2, стр. 117-122
Реакционная способность поверхности монокристаллического кремния в процессах молекулярного наслаивания
Ю. К. Ежовский *
Санкт-Петербургский государственный технологический институт (технический университет)
190013 Санкт-Петербург, Московский пр., 26, Россия
* E-mail: ezhovski1@mail.ru
Поступила в редакцию 05.03.2018
Аннотация
На основе макромолекулярной концепции строения твердых тел по индуктивным постоянным проведена количественная оценка реакционной способности гидроксильных групп поверхности монокристаллических матриц на примере кремния. Показано влияние толщины оксидного слоя на поверхности матрицы на реакционную способность силанольных групп в процессах молекулярного наслаивания.
ВВЕДЕНИЕ
Развитие химической нанотехнологии, использующей матричный синтез низкоразмерных систем, во многом определяется возможностью оптимального выбора реагентов и условий поверхностных реакций. В таких процессах, как молекулярное наслаивание (МН) [1, 2], или атомно-слоевое осаждение – ALD-технология [3–5], при взаимодействии функциональных групп поверхности с низкомолекулярным реагентом газовой фазы образуются поверхностные соединения, являющиеся структурными единицами синтезируемого материала, например тонкой пленки. Эти гетерогенные процессы носят циклический характер: каждая последующая реакция проводится только после полного протекания предыдущей, удаления избытка реагента и продуктов реакции. При предельном (монослойном) заполнении поверхности в каждом цикле реализуется слоевой механизм формирования и толщина слоев определяется только числом циклических реакций. Процесс носит саморегулирующийся характер и позволяет контролировать состав и толщину с точностью до монослоя. Перспективность этих методов для создания наносистем электроники очевидна, что продемонстрировано в ряде работ, например [4–6], а их дальнейшее развитие и использование во многом определяются возможностью количественной оценки характеристик поверхностных процессов.
Целью данной работы явилась разработка подхода, позволяющего провести количественную оценку реакционной способности гидроксильных функциональных групп поверхности монокристаллических матриц на примере кремния.
ТЕОРЕТИЧЕСКИЙ АНАЛИЗ
Реакционная способность поверхности твердых тел определяется целым рядом факторов, основными из которых являются состав, структура, наличие дефектов и др. [7, 8], и наиболее эффективно проявляется в таких процессах, как каталитическая и сорбционная активность, оценку которой проводят, как правило, по кислотно-основным характеристикам, что требует определенного набора индикаторов.
В процессах молекулярного наслаивания, как уже отмечалось, используются поверхностные реакции, основанные на хемосорбции низкомолекулярного реагента функциональными группами поверхности, например гидроксильными. Оценку их реакционной способности можно провести на основе количественного подхода, использующего индуктивный эффект [9], что дает возможность определять направление и стехиометрию поверхностных реакций, осуществлять корректировку температурных условий, состава реакционной среды и т.д.
Согласно остовной концепции строения твердых тел [2], любое твердое вещество можно представить как совокупность химически инертного остова (X) и реакционно-способных функциональных групп поверхности (Y) (например, –ОН). Тогда эффективную электроотрицательность остова как заместителя в поверхностном соединении можно охарактеризовать индуктивной (индукционной) константой σi. Наиболее распространенная концепция индуктивного эффекта – внутримолекулярная поляризация, передаваемая по цепочке связей, и любой случай проявления индуктивного эффекта может быть описан уравнением [9]
где А – любая коррелируемая величина; α – коэффициент пропорциональности, отражающий чувствительность реакционного центра (Y) к воздействию заместителя (Х).Высокой чувствительностью к электронным эффектам обладает ядерный магнитный резонанс, являющийся одним из наиболее корректных методов для определения индуктивных констант, однако требования к самим объектам исследования ограничивают его использование. Определить величину σi можно также по сдвигам частот валентных колебаний связи Si–H, которая очень чувствительна к эффектам заместителей, сдвиг ее частот практически исключает влияние стерических факторов [9]. В этом случае индуктивное влияние поверхностной группировки атомов (или даже всего остова твердого тела) можно охарактеризовать значением константы σs, и уравнение (1) примет вид
(2)
${{\nu }_{i}} = {{\nu }_{0}} + \alpha \left( {\Sigma {{\sigma }_{i}} + {{\sigma }_{s}}} \right),$Синтезировать поверхностные соединения, содержащие Si–H-связь, можно на гидроксилированной поверхности твердых веществ (X–ОН) при ее обработке парами хлор- или алкоксисиланов (ClnR3 – nSiH или (OR)nR3 – nSiH) по реакции
В результате математической обработки экспериментальных данных, полученных для серии поверхностных соединений на дисперсных оксидах [10], и значений констант Тафта ($\Sigma \sigma _{i}^{*}$) для известных заместителей [11] были определены коэффициенты соотношения (2) и получено выражение
Следует отметить, что $\sigma _{s}^{*}$ также будет определяться по шкале индуктивных констант Тафта, наличие информации по которым для большого числа низкомолекулярных заместителей значительно упрощает расчетную часть методики и делает предлагаемый подход в достаточной степени универсальным.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Эксперименты по хемосорбции силанов и анализ спектральных характеристик полученных продуктов проводились на образцах кремния КЭФ-5.0 с ориентациями (111) и (100). Значения индуктивной константы рассчитывались по результатам ИК-спектроскопии многократного нарушенного полного внутреннего отражения (МНПВО) на кремниевых элементах с параметрами: угол падения луча θ = 45°, число отражений n = 28. Элементы после шлифовки и полировки протравливались в полирующем травителе СР-4 в течение 5–7 мин, а непосредственно перед экспериментом обрабатывались в 5%-ном растворе HF. Толщина остаточного оксидного слоя, по эллипсометрическим оценкам, не превышала 1.5 нм. Регистрация спектров осуществлялась непосредственно в вакуумной кювете-реакторе, обеспечивающей обработку поверхности образцов в вакууме (до 10–3 Па) или контролируемой газовой среде в диапазоне температур 20–600°С. Спектры каждого образца снимались на ИК-спектрометре с фурье-анализатором как в режиме накопления, так и многократно с разверткой при различных скоростях сканирования и масштабах регистрации частот с последующим усреднением значений в результате их компьютерной обработки. Отклонение отдельных измерений от среднестатистических значений в области частот 2100–3800 см–1 не превышало 2 см–1.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Изучение процесса гидроксилирования свежепротравленного кремния и с последующей сорбцией диметилхлорсилана (ДМХС) показало, что форма спектра в области частот 3700–3750 см–1 аналогична ИК-спектрам дегидратированной поверхности узкопористых силикагелей. При этом наблюдалось образование тетраметилдисилоксана, который полностью десорбировался при повышении температуры до 473 K. Эти данные позволили установить, что силанольные группы поверхности кремния в реакции с ДМХС не участвуют, в то время как на поверхности силикагеля (ШСК-250) в аналогичных условиях образовывались термоустойчивые поверхностные соединения ≡Si–O–Si(СH3)2H с ν(SiH) = 2152 см–1 [10]. По-видимому, это связано как с низкой электрофильностью ДМХС, так и с отличием в электронном строении поверхностных атомов кремния и кремнезема. Поскольку на поверхности даже свежепротравленного в растворе HF кремния, по нашим оценкам из эллипсометрических измерений, имеется сверхтонкая (1.0–1.5 нм) пленка оксида, при обработке парами воды вполне вероятно образование, наряду с силанольными группами, координационно-связанного гидратного покрова, который и приводит к образованию тетраметилдисилоксана.
Энергия активации реакций электрофильного замещения протона силанольных групп зависит от протоноакцепторных свойств атакующего реагента, поэтому можно выбрать замещенный силан, способный вступать в реакцию с относительно малоактивными гидроксильными группами поверхности кремния. Для выявления сходства и отличий с ДМХС был выбран триэтоксисилан (ТЭС), взаимодействие которого с поверхностью кремния изучалось при различных условиях: от комнатной температуры до 673 К. На рис. 1 представлены спектры МНПВО для образцов, прошедших различные термохимические обработки, позволившие в итоге синтезировать устойчивые поверхностные соединения, содержащие Si–H-связь, и определить не только индуктивный эффект матрицы, но и стехиометрию поверхностной реакции.
Рис. 1.
ИК-спектры МНПВО поверхности кремния: 1 – после гидратации при 473 К и последующей обработки парами ТЭС при 300 К; 2, 3 – после термостатирования в течение 30 мин в вакууме при 373 и 473 К соответственно; 4 – после гидратации в парах воды при 473 К.
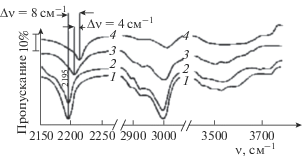
При обработке вакуумированных в течение 1 ч при 473 К образцов кремния парами воды при той же температуре и после охлаждения обработанного парами ТЭС при комнатной температуре в спектре 1 (рис. 1) наблюдалась полоса поглощения Si–H-связи и характерный набор полос поглощения С–Н-связей этокси-групп. Значение ν(SiH) в спектре 1 (рис. 1) совпадало с частотой валентных колебаний связи Si–H ТЭС (ν = 2195 см–1). Это указывало на отсутствие каких либо химических реакций в системе. После термостатирования в течение 30 мин при 373 К (спектр 2, рис. 1) наблюдалась деформация низкочастотной области полосы поглощения Si–H-связей, что вызвано образованием на поверхности кремния адсорбированного алкоксизамещенного дисилоксана, образующегося в результате реакции, аналогичной реакции с ДМХС. Только после термостатирования при 473 K в течение 1 ч в спектре образца наблюдалось снижение интенсивности полос поглощения связей Si–H и С–Н. При этом форма полосы поглощения Si–H связей становилась симметричной, а сама полоса смещалась в коротковолновую часть спектра (спекр 3, рис. 1), что вызвано термодесорбцией избытка реагента и образующегося дисилоксана. Смещение ν(Si–H) свидетельствовало о замене одной или нескольких алкоксигрупп на более электроотрицательные заместители. Указанные изменения и термоустойчивость полученного продукта при 473 К свидетельствовали о его химической связи с поверхностью, которая может образоваться только при реакции между силанольными группами и этокси-группами сорбированного силана по схеме
(4)
$\begin{gathered} {{( \equiv {\text{Si}}--{\text{OH}})}_{m}} + {{\left( {{\text{O}}{{{\text{С }}}_{2}}{{{\text{Н }}}_{5}}} \right)}_{3}}{\text{SiН }} \to \\ \to {{( \equiv {\text{Si}}--{\text{O}}--)}_{m}}{\text{Si}}{{\left( {{\text{O}}{{{\text{С }}}_{2}}{{{\text{Н }}}_{5}}} \right)}_{{3--m}}}{\text{H}} + m{{{\text{С }}}_{2}}{{{\text{Н }}}_{5}}{\text{OН }}. \\ \end{gathered} $Не вступившие в реакцию алкокси-группы можно заменить на гидроксильные при обработке поверхности образца парами воды. Действительно, как видно из сопоставления спектров 2 и 3 (рис. 1), при гидратации наблюдалось снижение интенсивности полосы поглощения связей С–Н и заметное увеличение поглощения в области валентных колебаний ОН-групп (ν = 3600–3700 см–1). При этом ν(Si–H) смещалась на 4 см–1 в коротковолновую часть спектра. Наблюдаемые изменения в спектрах 3 и 4 (рис. 1) происходили в результате реакции
(5)
$\begin{gathered} {{( \equiv {\text{Si}}--{\text{O}})}_{m}}{\text{Si}}{{\left( {{\text{O}}{{{\text{С }}}_{2}}{{{\text{Н }}}_{5}}} \right)}_{{3--m}}}{\text{H}} + \left( {3--m} \right){{{\text{H}}}_{2}}{\text{O}} \to \\ \to {{( \equiv {\text{Si}}--{\text{O}})}_{m}}{\text{Si}}{{\left( {{\text{OН }}} \right)}_{{3--m}}}{\text{H}} + \left( {3--m} \right){{{\text{С }}}_{2}}{{{\text{Н }}}_{5}}{\text{OH}}. \\ \end{gathered} $Для определения стехиометрии реакций (4) и (5) (численного значения коэффициента m) можно воспользоваться установленной зависимостью (3). Преобразовав это уравнение и заменив (3–m) алкокси-групп (σi(OC2H5) = 1.366) [11] на эквивалентное количество ОН-групп (σi(OH) = 1.550) [11], сдвиг частот валентных колебаний Si–H-связи можно определить как: Δν(SiH) = a(3–m)OH[σi(OH) – – σi(OC2H5)], откуда
Следовательно, строение поверхностных соединений, образующихся в ходе реакции (4), соответствует формуле (≡Si–O)2Si(OС2Н5)H. Воспользовавшись также уравнением (3) и подставив в него значение ν(SiH) = 2203 см–1 (спектр 3, рис. 1) для этого соединения, можно оценить индуктивный эффект кремнекислородных групп на поверхности монокристаллического кремния КЭФ-5.0 или эффективную электроотрицательность всего кремниевого остова по шкале индуктивных констант Тафта:
Значение аналогичного параметра для кремнийкислородных групп на поверхности силикагеля (ШСК-250) при 473 K существенно выше ($\sigma _{s}^{*}$ = = 4.57) [10]. Сопоставление этих величин позволяет установить, что силанольные группы поверхности кремния обладают значительно меньшей протонодонорной способностью, чем аналогичные группы поверхности силикагеля. Это вызвано ингибирующим действием кристаллического остова, обладающего достаточной концентрацией носителей заряда, снижающей индуктивный эффект. Отсутствие заметного влияния типа ориентации кремниевой матрицы обусловлено, по-видимому, более значимым воздействием поверхностного оксидного слоя, аморфная структура которого экранирует кристаллическое поле матрицы.
Анализ полученных результатов для силикагеля и кремния позволил предположить, что на реальной поверхности кремниевых матриц ОН-группы будут обладать протонодонорной способностью, определяемой предысторией образца, а именно – толщиной оксидного слоя, образовавшегося после предварительных обработок. Поэтому было проведено изучение влияния толщины слоя SiO2 на спектральные характеристики хемосорбированного силана на кремнии.
Слои SiO2 заданной толщины на поверхности элементов МНПВО синтезировались методом молекулярного наслаивания при попеременной обработке поверхности парами SiCl4 и H2O. Их толщина определялась эллипсометрическим методом по измерению поляризационных углов Δ и Ψ и рассчитывалась в приближении однослойной модели Друде–Тронстона [12]. Параметры Δ и Ψ регистрировались на эллипсометре по схеме PQSA [13] с фиксированным компенсатором. В качестве источника линейно поляризованного света использовался лазер ЛГ-75 с длиной волны излучения 632.8 нм. Для повышения точности измерений осуществлялась магнитная модуляция светового луча. Погрешность в определении этих параметров не превышала ±0.1′. Расчет толщины слоев проводился с использованием показателей преломления, определенных по методу Холмса [13].
На рис. 2 представлены ИК-спектры МНПВО образцов кремния с синтезированным слоем SiO2, обработанных парами ДМХС при 473 К. Сопоставление спектров 1–4 показало, что с увеличением количества циклов обработки (N) парами SiCl4 и H2O, а соответственно, и толщины SiO2 наблюдалось увеличение интенсивности поглощения в области частот валентных колебаний связей Si–H (ν(SiH) = 2135–2150 см–1) и C–H (ν(СH) = 2900–3000см–1), а также заметное смещение полосы ν(SiH) в коротковолновую часть спектра. Это однозначно указывает на увеличение концентрации силанольных групп, вступающих в реакцию, причем до N ≈ 15 их количество возрастало пропорционально N (рис. 3) и в дальнейшем изменялось незначительно.
Рис. 2.
ИК-спектры МНПВО поверхности (111) образцов Si, подвергнутых циклической обработке парами тетрахлорида кремния и воды при 473 К с последующей обработкой ДМХС при той же температуре: 1 – число циклов обработки N = 4, 2 – N = 10, 3 – N = = 20, 4 – N = 30, 5 – N = 40, 6 – спектр образца после травления и обработки ТЭС.
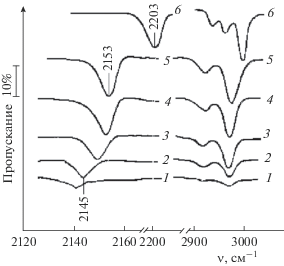
Рис. 3.
Зависимости относительной интенсивности полос поглощения Si–H-связи (1) и толщины SiO2, полученного без использования триэтиламина (ТЭА) (2) и с его использованием (2 '), от числа циклов (N) молекулярного наслаивания.
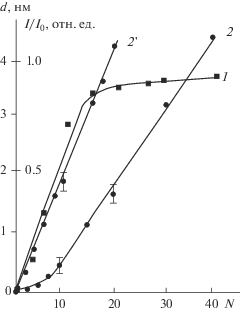
Как было установлено, на свежепротравленной поверхности кремния силанольные группы вообще не вступали в реакцию с ДМХС, но с ТЭС реагировали с образованием поверхностных соединений. Для сравнения на рис. 2 представлен фрагмент спектра (спектр 6) свежепротравленного кремниевого элемента МНПВО, обработанного парами ТЭС. С увеличением толщины оксида индуктивный эффект кремниевой матрицы ослабевал и возрастало влияние поверхностного оксидного слоя, а вместе с ним и активность силанольных групп. Вероятно, по этим же причинам на начальных этапах синтеза (N < 10) наблюдалось замедленное формирование оксидного слоя (кривая 2 на рис. 3).
Полученные данные позволили установить количественную взаимосвязь между толщиной оксидного слоя на кремнии и индуктивным эффектом матрицы и, следовательно, активностью гидроксильных групп (рис. 4). Наибольшие изменения $\sigma _{s}^{*}$ наблюдались до толщины dс ≈ 3–4 нм, когда индукционное влияние кремниевого остова практически соответствовало остову силикагеля ШСК-250. При этом наблюдалась активная хемосорбция ДМХС. Следует учесть, что даже свежепротравленная в водных травителях поверхность кремния содержит тонкий оксидный слой (по нашим оценкам, около 1 нм), и рассчитанная по экспериментальным значениям ν(SiH) величина $\sigma _{s}^{*}$ = 2.9 характеризует именно такую поверхность.
Оценка индуктивной константы, проведенная по частоте валентных колебаний групп Si–H, образующихся непосредственно в процессе травления кремния плавиковой кислотой (ν(SiH) = 2096 см–1), дало значение $\sigma _{s}^{*}$ = 1.63. Эта величина характеризует поверхность кремния, практически лишенную оксидного слоя, и указывает на низкую активность силанольной группы, непосредственно связанной с кремниевым остовом. Присутствие в данном случае на поверхности фтор-групп может несколько повышать значение $\sigma _{s}^{*},$ однако экстраполяция зависимости $\sigma _{s}^{*}$ = f(d) к значению $\sigma _{s}^{*}$ = 1.63 (рис. 4) дает достаточно реальную толщину собственного оксида (d ≈ 1 нм), хорошо совпадающую с эллипсометрическими оценками.
ЗАКЛЮЧЕНИЕ
Сопоставление индукционных констант Тафта для хлор- и этокси-групп (2.880 и 1.366 соответственно [11]) и полученное значение для кремния КЭФ-5.0 ($\sigma _{s}^{*}$ = 2.9) показали, что реакция гидроксильных групп поверхности этой матрицы с соединениями, содержащими этокси-группы, предпочтительнее, так как в этом случае идет обмен на заместитель с большей эффективной электроотрицательностью. Поэтому для полного протекания поверхностных реакций следует либо выбрать реагент с $\sigma _{i}^{*}$ < $\sigma _{s}^{*},$ либо использовать дополнительную активацию гидроксилов, которая может осуществляться как повышением температуры (или другим активирующим воздействием), так и применением химических реагентов – протоноакцепторов. Например, использование ТЭА как катализатора обмена позволило ликвидировать латентный период в формировании слоев оксида кремния [14], вызванный частичным заполнением поверхности при N < 10, и активировать рост слоев SiO2 (кривая 2 ' на рис. 3) – прирост толщины за один цикл обработки был близок к расчетному значению для монослоя.
Список литературы
Алесковский В.Б. Химическая сборка материалов // Вестн. АН СССР. 1975. № 6. С. 48–54.
Алесковский В.Б. О природе твердых химических соединений // Журн. прикл. химии. 1982. Т. 55. № 4. С. 725–730.
Suntola T. Atomic Layer Epitaxy // Mater. Sci. Rep. 1989. V. 4. № 7. P. 261–312.
Seidel T., Londergan A., Winkler L. Progress and Opportunities in Atomic Layer Deposition // Solid State Technol. 2003. № 5. P. 67–71.
Miikkulainen V., Leskela M., Ritala M., Puurunen R.L. Crystallinity of Inorganic Films Grown by Atomic Layer Deposition: Overview and General Trends // J. Appl. Phys. 2013. V. 113. № 2. P. 021301–021402.
Yong Shin Kim, Sun Jin Yun. Nanolaminated Al2O3–TiO2 Thin Films Grown by Atomic Layer Deposition // J. Crys. Growth. 2005. V. 274. P. 585–593.
Фахльман Б.Д. Химия новых материалов и нанотехнологии / Под ред. Третьякова Ю.Д. и Гудилина Е.А. М.: Интеллект, 2011. 463 с.
Владимиров Г.Г. Физика поверхности твердых тел. Санкт-Петербург: Лань, 2016. 348 с.
Гаммет Л. Основы физической органической химии. М.: Мир, 1972. 341 с.
Ежовский Ю.К. Количественный подход в химической нанотехнологии поверхности твердых тел // Хим. физика. 2006. Т. 25. № 5. С. 72–90.
Справочник химика. М.; Л.: Химия, 1971. Т. 3. 1005 с.
Аззам Р., Башара Н. Эллипсометрия и поляризованный свет. М.: Мир, 1981. 583 с.
Громов В.К. Введение в эллипсометрию. Л.: Изд. ЛГУ, 1986. 192 с.
Ежовский Ю.К. Получение наноструктурных пленок оксида и нитрида кремния с использованием нанотехнологии // Неорган. материалы. 2013. Т. 49. № 9. С. 971–975.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы



