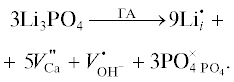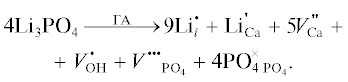Неорганические материалы, 2019, T. 55, № 7, стр. 760-768
Структура и термическая стабильность керамики из литийзамещенного гидроксиапатита
В. В. Смирнов 1, *, С. М. Баринов 1, С. В. Смирнов 1, А. И. Крылов 1, О. С. Антонова 1, М. А. Гольдберг 1, Т. О. Оболкина 1, А. А. Коновалов 1, А. В. Леонов 2
1 Институт металлургии и материаловедения им. А.А. Байкова Российской академии наук
119334 Москва, Ленинский пр., 49, Россия
2 Московский государственный университет им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
* E-mail: smirnov2007@mail.ru
Поступила в редакцию 14.08.2018
После доработки 14.02.2019
Принята к публикации 18.02.2019
Аннотация
Изучено влияние введения катионов лития на фазовый состав, параметры кристаллической решетки и размеры областей когерентного рассеяния гидроксиапатита в зависимости от температуры термообработки (900, 1200 и 1400°С). Показано, что катионы лития способствуют переходу апатита в литийзамещенные формы трикальцийфосфата при высоких степенях замещения (20 мол. %) при температуре термообработки 1200 и 1400°С. При степенях замещения 1, 5 и 10 мол. % введение лития не приводит к дестабилизации структуры апатита даже при температуре 1400°С.
ВВЕДЕНИЕ
Гидроксиапатит (ГА, Са5(РО4)3(ОН)) является одним из наиболее перспективных соединений для использования в регенеративно-восстановительной хирургии для замещения поврежденных участков костной ткани. Это связано с близостью ГА к минеральному составу естественной костной ткани. ГА-материалы предназначены в основном для создания прочных нерезорбируемых имплантатов, которые должны обладать высокими механическими свойствами [1]. Актуальными являются исследования, направленные на разработку ГА-материалов с регулируемыми свойствами, например за счет модификации ионами металлов [2, 3]. Перспективным является создание литийзамещенных форм (Li-ГА). Это связано с влиянием лития на биологические свойства ГА: он повышает скорость остеогенной дифференцировки мезенхимальных стволовых клеток [4]; ускоряет деградацию ГА благодаря активации клеток, участвующих в процессе ремоделирования костной ткани [5]; активирует β-катенин (сигнальный медиатор), что способствует заживлению переломов [6]. Введение лития способствует спеканию ГА-керамики и, как следствие, увеличению прочности керамических материалов на основе ГА, обусловленному уменьшением пористости образцов.
Исследования свойств апатитов, содержащих ионы лития, ограничены, особенно в области влияния катионов лития на параметры кристаллической решетки и устойчивость фазового состава при термообработке ГА-материалов в широком температурном диапазоне. Например, проведены исследования фазового состава и структуры керамики до 1250°С при содержании лития менее 1% [7], показавшие, что при 1050°С происходит трансформация ГА в β-трикальцийфосфат (β-ТКФ), а при 1250°С образуется в основном α-ТКФ. Исследования при большей степени замещения (10 и 20 ат. %) [8] выявили полный переход ГА в Са10Li(PO4)7 при термической обработке при 900°С. Исследования по получению Li-ГА (0, 1, 5, 10, 20, 40% оксида лития) описаны в [9]. Определены фазовый состав и параметры кристаллической решетки. Однако температура термообработки была невысокой, лишь 100°С, что не позволило выявить влияние лития на фазовый состав, термическую стабильность и параметры кристаллической решетки материалов с высокой степенью закристаллизованности.
В настоящей работе исследовано влияние степени замещения ионов кальция на катионы лития в количестве 0, 1, 5, 10 и 20 мол. % на изменение параметров кристаллической решетки и фазового состава в зависимости от температуры термообработки 900, 1200 и 1400°С. Выбор температур обусловлен особенностями технологии ГА-керамики, которую получают спеканием при температурах 1200–1300°С.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Расчетные составы синтезируемых соединений приведены в табл. 1. Синтез проводили методом осаждения из водных растворов. Для этого в раствор, содержащий нитраты кальция и лития, при перемешивании добавляли растворы гидрофосфата аммония. Осаждение проводили при pH 9.3–9.7. Содержание компонентов рассчитывали в соответствии с реакцией
(1)
$\begin{gathered} ({\text{1}}0--x){\text{Ca}}{{\left( {{\text{N}}{{{\text{O}}}_{{\text{3}}}}} \right)}_{{\text{2}}}} + {\text{6}}{{\left( {{\text{N}}{{{\text{H}}}_{{\text{4}}}}} \right)}_{{\text{2}}}}{\text{HP}}{{{\text{O}}}_{{\text{4}}}} + \\ + \,\,{\text{2}}x{\text{LiN}}{{{\text{O}}}_{{\text{3}}}} \to {\text{С }}{{{\text{а }}}_{{{\text{1}}0--х }}}{\text{L}}{{{\text{i}}}_{{{\text{2}}x}}}{{\left( {{\text{P}}{{{\text{O}}}_{{\text{4}}}}} \right)}_{{\text{6}}}}{{\left( {{\text{OH}}} \right)}_{{\text{2}}}}, \\ \end{gathered} $Таблица 1.
Состав материалов
| Обозначение | Степень замещения, мол. % | Расчетная формула соединения |
|---|---|---|
| 0Li-ГА | 0 | Ca10(PO4)6(ОН)2 |
| 1Li-ГА | 1 | Ca9.9Li0.2(PO4)6(OH)2 |
| 5Li-ГА | 5 | Ca9.5Li(PO4)6(OH)2 |
| 10Li-ГА | 10 | Ca9Li2(PO4)6(OH)2 |
| 20Li-ГА | 20 | Ca8Li4(PO4)6(OH)2 |
После синтеза осадок подвергали старению в течение 21 сут для увеличения степени закристаллизованности апатитовой фазы [10]. Затем проводили операцию фильтрования. Полученные порошки прокаливали при 900, 1200 и 1400°C.
Материалы исследовали методом рентгенографического анализа (дифрактометр Shimadzu XRD 6000) с использованием базы данных JCPDS PCPDFWIN. Для расчета параметров элементарной ячейки использовался метод Ритвельда с привлечением программы FullProf Suite. Проводили Фурье-ИК-спектроскопию (Termonicolet Avatar 330FT-IR). Анализ пористости образцов выполняли с использованием гидростатического взвешивания в соответствии с ГОСТ 2409-95. Для этого образцы размером 30 × 4 × 4 мм прессовали в стальной пресс-форме при удельном давлении 100 МПа и термообрабатывали в диапазоне температур 900–1400°С.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
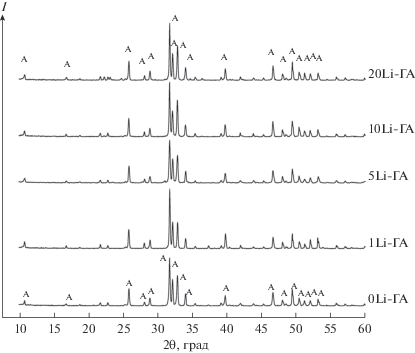
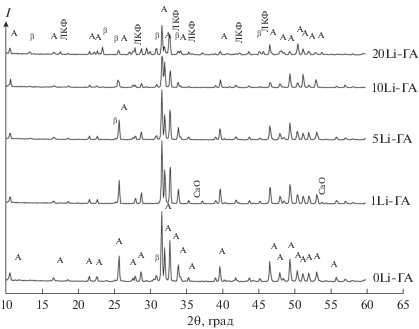
В материалах 0 Li-ГА после термообработки при 900°С образуется одна фаза – ГА. При дальнейшем подъеме температуры до 1200°С наблюдается образование небольшого количества β-ТКФ. Эти результаты согласуются с данными работы [11], где показано, что ГА частично переходит в β-ТКФ после термообработки в диапазоне 900–1200°С. Дальнейший подъем температуры до 1400°С приводит к формированию до 30% α-ТКФ. Для всех замещенных форм Li-ГА после термообработки при 900°С присутствует одна фаза – апатитовая (рис. 1), при этом содержание лития не влияет на степень кристалличности (интенсивность пиков на дифрактограммах). После термообработки при 1200°С для образцов с замещением 5–10 мол. % выявлено образование небольшого количества β-ТКФ (рис. 2). При этом с увеличением количества лития интенсивность пиков на дифрактограммах снижается, что связано с уменьшением степени закристаллизованности основной фазы. Для материалов 20Li-ГА происходит резкое изменение состава – апатит частично распадается на две фазы: β-ТКФ (20%) и литий-кальциевый фосфат LiCaPO4 (ЛКФ). После термообработки при 1400°С образуется литийзамещенная форма Ca10Li(PO4)7 (Li-ТКФ) начиная с состава 5Li-ГА (в количестве 15%) (рис. 3). Дальнейшее увеличение содержания лития приводит к повышению количества Li-ТКФ и снижению содержания ГА (табл. 2). При этом содержание α-ТКФ снижается с 27% (0Li-ГА) до 3% (1Li-ГА) и равно нулю для материалов с бóльшим содержанием лития (5Li-ГА, 10Li-ГА, 20Li-ГА). Определение Li-ТКФ (JCPDS 45-550) для материалов 5Li-ГА, 10Li-ГА, 20Li-ГА затруднено из-за близости их рефлексов к β-ТКФ (JCPDS 9-169).
Рис. 3.
Дифрактограммы порошков после термообработки при 1400°С (А – ГА, α – α-ТКФ, Li-ТКФ – Ca10Li(PO4)7).
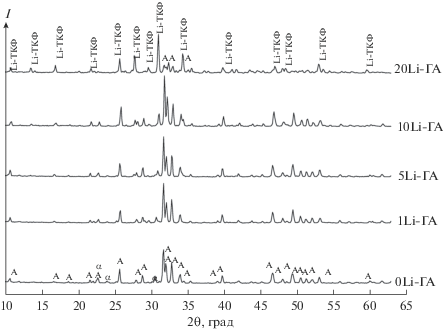
Таблица 2.
Фазовый состав материалов
| Образец | Фазовый состав | Количество, % | ||
|---|---|---|---|---|
| 900°C | 1200°C | 1400°C | ||
| 0Li-ГА | Ca10(PO4)6(OH)2 | 100 | 90 | 73 |
| α-Ca3(PO4)2 | – | – | 27 | |
| β-Ca3(PO4)2 | – | 10 | – | |
| 1Li-ГА | Ca10(PO4)6(OH)2 | 100 | 100 | 97 |
| α-Ca3(PO4)2 | – | – | 3 | |
| 5Li-ГА | Ca10(PO4)6(OH)2 | 100 | 91 | 85 |
| β-Ca3(PO4)2 | – | 9 | – | |
| Ca10Li(PO4)7 | 15 | |||
| 10Li-ГА | Ca10(PO4)6(OH)2 | 100 | 90 | 78 |
| β-Ca3(PO4)2 | – | 10 | – | |
| Ca10Li(PO4)7 | – | 22 | ||
| 20Li-ГА | Ca10(PO4)6(OH)2 | 100 | 53 | 24 |
| β-Ca3(PO4)2 | – | 20 | – | |
| LiCaPO4 | – | 27 | – | |
| Ca10Li(PO4)7 | – | – | 76 | |
При этом было проведено подробное исследование основных пиков, которое показало, что рефлексы, принадлежащие Li-ТКФ, были смещены в сторону больших углов в среднем на 0.2° по сравнению с β-ТКФ. Это было интерпретировано в соответствии с картотекой JCPDS как образование нового соединения, содержащего литий, – Ca10Li(PO4)7, т.к. известно, что при замещении катиона с большим радиусом (Са2+) на меньший (Li+) происходит уменьшение параметров кристаллической решетки [12, 13].
Необходимо также отметить, что при термообработке при 1200°С кроме ГА наблюдается образование двух фаз: β-ТКФ (Ca3PO4) и ЛКФ (LiCaPO4) с отношением Са/Li = 50/50, а при температуре 1400°С кроме ГА образуется только одно соединение – Ca10Li(PO4)7 с отношением Са/Li = 10/1. Данный эффект можно объяснить перераспределением катионов лития между фазами. При низких температурах термообработки (1200°С) образуется смесь фаз с различным содержанием лития, что может являться следствием неоднородности распределения компонентов, заложенной на стадии синтеза материалов. При повышении температуры (1400°С) процессы диффузии протекают более активно, в результате происходит перераспределение вводимого катиона между фазами и формирование одного литийзамещенного соединения с небольшим содержанием лития.
Кроме того, при высоких температурах для LiCaPO4 наблюдается потеря лития [14], в результате могут образовываться соединения со структурой витлокита, к которым относится Ca10Li(PO4)7.
РФА выявил смещение пиков в сторону меньших значений 2θ для материала 1Li-ГА, термообработанного при на 900°С, по сравнению с чистым ГА. Это свидетельствует об увеличении параметров решетки (табл. 3). Данный эффект можно объяснить размещением катионов лития в междоузлиях с образованием твердого раствора внедрения и вакансий в катионной подрешетке. Это наиболее вероятно, учитывая существенно меньший радиус катиона Li по сравнению с катионом Са (Са2+ – 1.04 Å, Li+ – 0.68 Å).
Таблица 3.
Параметры элементарной ячейки и размеры ОКР
| Образец | a, Å (±0.002) | c, Å (±0.002) | ОКР, нм | a, Å (±0.002) | c, Å (±0.002) | ОКР, нм | a, Å (±0.002) | c, Å (±0.002) | ОКР, нм |
|---|---|---|---|---|---|---|---|---|---|
| 900°С | 1200°С | 1400°С | |||||||
| 0Li-ГА | 9.420 | 6.886 | 58 | 9.423 | 6.884 | 121 | 9.427 | 6.910 | 111 |
| 1Li-ГА | 9.424 | 6.889 | 58 | 9.414 | 6.881 | 123 | 9.423 | 6.887 | 83 |
| 5Li-ГА | 9.427 | 6.879 | 51 | 9.419 | 6.882 | 117 | 9.417 | 6.892 | 109 |
| 10Li-ГА | 9.425 | 6.881 | 59 | 9.407 | 6.893 | 91 | 9.383 | 6.869 | 71 |
| 20Li-ГА | 9.425 | 6.881 | 59 | Преобладает новая витлокитоподобная фаза | Преобладает новая витлокитоподобная фаза | ||||
Необходимо также учитывать, что формирование ГА-структуры проходило постепенно в течение 21 сут старения в маточном растворе [10].
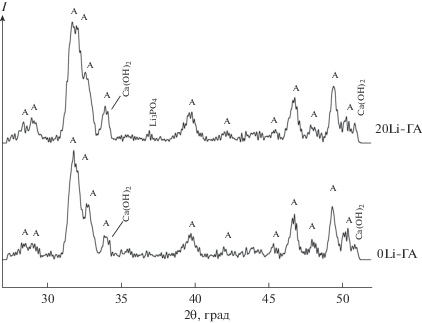
В процессе старения происходят реакции между компонентами с образованием промежуточных соединений с их последующим взаимодействием между собой и формированием структуры ГА. Известно, что фосфат лития Li3PO4 имеет низкую растворимость (–lgПР = 8.5 [15]), поэтому в процессе реакции (1) сначала наиболее вероятно его осаждение, затем происходит формирование более растворимого осажденного гидроксиапатита (ОГА) (–lgПР = ∼5.5 в щелочной среде, рН 8.0–8.5 [16]). В ходе дальнейшего выдерживания осадка в маточном растворе происходит его кристаллизация с прохождением реакции между ОГА и фосфатом лития с образованием более закристаллизованных замещенных форм ГА по сравнению с исходным ОГА. Такое взаимодействие возможно, учитывая, что свежеосажденные порошки имеют высокую дисперсность и химическую активность. Это подтверждается исследованиями фазового состава порошковых материалов после их старения в маточном растворе (рис. 4), которые показали присутствие в ГА незначительного количества непрореагироваших до конца соединений – гидроксида кальция и фосфата лития. При этом образование фосфата лития наблюдалось в порошках с наибольшим содержанием замещающего катиона.
Таким образом, можно сделать вывод, что окончательное формирование структуры ГА и реакция между компонентами проходят при последующих высокотемпературных обработках. С учетом вышесказанного можно записать реакцию дефектообразования при вхождении в междоузлия катионов лития с формированием твердого раствора внедрения и образованием катионных вакансий и вакансий в анионной подрешетке по ОН-группе
При дальнейшем увеличении количества ионов лития (5, 10 и 20 мол. %) параметры кристаллической решетки изменяются незначительно. Это можно объяснить проявлением другого механизма вхождения ионов лития в кристаллическую решетку ГА – формированием твердых растворов замещения с образованием вакансий по кислороду:
(3)
${\text{L}}{{{\text{i}}}_{{\text{3}}}}{\text{P}}{{{\text{O}}}_{{\text{4}}}}\xrightarrow{{{\text{Г А }}}}3{\text{Li}}_{{{\text{Ca}}}}^{'} + {{V}^{{\centerdot \centerdot \centerdot }}}_{{{\text{P}}{{{\text{O}}}_{4}}}} + {\text{PO}}{{_{4}^{ \times }}_{{\,{\text{P}}{{{\text{O}}}_{4}}}}}.$Приведенная реакция также обусловлена соотношением (кальций + литий)/фосфор, которое больше, чем кальций/фосфор в стехиометрическом ГА. При этом количество избыточного лития возрастает с увеличением его концентрации (табл. 1). Таким образом, образующийся избыток катионов лития встраивается в катионную подрешетку кальция с образованием вакансий в анионной подрешетке по РО4-группам.
Просуммировав уравнения реакций (1) и (2), получим реакцию образования твердых растворов для материалов с высокой (5–20 мол. %) концентрацией катионов лития (реакция (3)). При этом образуются вакансии как по катиону, так и по аниону
Таким образом, при низкой концентрации катионов лития происходит преимущественно образование твердых растворов внедрения и, как следствие, увеличение параметров кристаллической решетки. При увеличении содержания катионов лития в ГА происходит образование твердых растворов внедрения и замещения, параметры кристаллической решетки при этом практически не изменяются.
Для материалов со степенью замещения 1, 5 и 10 мол. %, термообработанных при 1200 и 1400°С, наблюдается тенденция к снижению параметра а кристаллической решетки. Параметр с изменяется незначительно – уменьшается или увеличивается. Как отмечается в работе [17], изменения параметров кристаллической решетки, когда один из параметров уменьшается, а второй может увеличиваться, типичны при образовании твердых растворов замещения. Для материалов со степенью замещения 20 мол. % начинает преимущественно образовываться литийсодержащий ТКФ. Это можно объяснить термической нестабильностью литийзамещенного ГА вследствие образования многочисленных дефектов структуры. Это наглядно проявляется для материала 20Li-ГА (табл. 1), когда возрастающее количество вакансий, особенно по ОН-группам, способствует переходу ГА в ТКФ (реакция (4)).
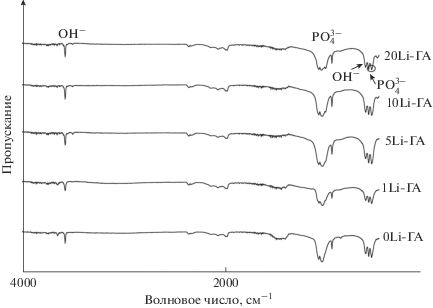
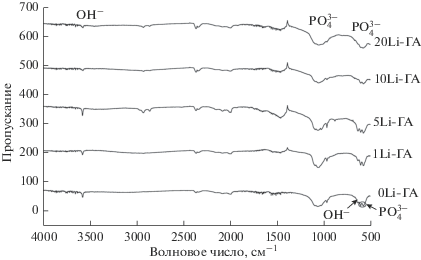
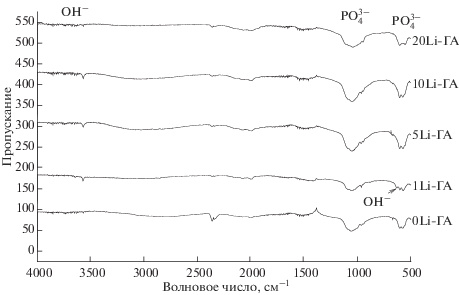
Данные ИК-спектроскопии показали, что образцы, термообработанные на 900°С, имели спектры, характерные для ГА, практически не отличающиеся друг от друга (рис. 5) [18]. Изменения в спектрах наблюдаются после термообработки образцов при более высокой температуре 1200°С. Для материалов со степенью замещения 1–5 мол. % сохраняются типичные колебания с характерными полосами поглощения для фосфат-групп (573, 600 и в диапазоне 960–1188 см–1) и ОН-групп (631, 3571 см–1) (рис. 6). При увеличении концентрации лития до 10 и 20 мол. % полоса 631 см–1 исчезает, а полоса при 3571 см–1 становится слабо выраженной. Это связано с потерей воды (ОН-групп) в результате трансформации апатитовой фазы в ТКФ. После термообработки при 1400°С полоса при 631 см–1 отсутствует независимо от степени замещения. Для материалов с замещениями 1, 5 и 10 мол. % полоса поглощения при 3571 см–1 слабо выражена, в то время как для образцов с 0 и 20 мол. % лития она практически отсутствует (рис. 7). Это показывает, что катионы лития стабилизируют апатитовую фазу (способствуют сохранению гидроксильных групп в структуре апатита) при высоких температурах (1400°С) при степени замещения в диапазоне 1–10 мол. %. Эти выводы согласуется с данными РФА (табл. 2).
На размер ОКР замещенных форм ГА, прокаленных при 900°С, степень замещения не оказывает заметного влияния. Значения ОКР находятся в диапазоне 47–58 нм. При 1200°С для образцов с небольшим замещением (1 мол. %) наблюдается рост ОКР апатитовой фазы. Однако при больших концентрациях лития, как правило, происходит уменьшение размеров, что связано с образованием новых фаз. При термообработке при 1400°С можно наблюдать общую тенденцию к снижению значений ОКР по сравнению с таковыми для 0Li-ГА. Объяснить данный эффект можно влиянием искажений кристаллической решетки. Известно, что снижение параметров кристаллической решетки приводит к уменьшению размера ОКР и, наоборот, повышение – к росту ОКР [12, 17]. Подобные зависимости особенно наглядно прослеживаются для Li-замещенных форм при термообработке при 1400°С, когда наблюдается тенденция к уменьшению параметров кристаллической решетки и, соответственно, уменьшение размера ОКР по сравнению с ГА.
Уменьшение значений ОКР с увеличением температуры при переходе от 1200 к 1400°С можно объяснить образованием новых соединений, которые возникают в результате частичной трансформации исходных низкотемпературных фаз в новые высокотемпературные более термодинамически устойчивые фазы. В результате, вместо одной фазы (одного кристалла) образуется несколько, что приводит к снижению размера кристаллов.
Исследования образцов после спекания показали (табл. 4), что введение катионов лития способствует получению плотной керамики. При этом для образцов 5, 10 и 20Li-ГА достигается практически беспористое состояние уже при 1100°С (табл. 4). Снижение пористости керамики объясняется действием катионов лития, которые при внедрении в ГА образуют дефекты в кристаллической решетке (реакции (2)–(4)) как по катиону, так и по аниону, что приводит к интенсификации процесса спекания по твердофазному механизму.
Таблица 4.
Открытая пористость керамических образцов
| Темпера-тура, °С | П, % | ||||
|---|---|---|---|---|---|
| 0Li-ГА | 1Li-ГА | 5Li-ГА | 10Li-ГА | 20Li-ГА | |
| 1000 | 55.0 | 53.3 | 50.7 | 20.3 | 8.8 |
| 1100 | 35.5 | 12.3 | >0.1 | >0.1 | >0.1 |
| 1200 | 15.5 | 7.8 | >0.1 | >0.1 | >0.1 |
| 1400 | >0.1 | >0.1 | >0.1 | >0.1 | >0.1 |
На рис. 8 показана микроструктура материалов, спеченных при 1100°С. Можно отметить рост зерен керамики с увеличением количества лития: для керамики 5Li-ГА размер зерен находится в диапазоне от 0.4 до 4 мкм, для 10Li-ГА – от 0.8 до 4 мкм, для 20Li-ГА – от 2 до 5 мкм. При этом структура керамики с 20 мол. % лития характеризуется более плотным срастанием зерен между собой, что делает границы зерен плохо различимыми. Таким образом, допирование литием интенсифицирует не только процесс спекания, но и рост зерна при спекании ГА-керамики.
ЗАКЛЮЧЕНИЕ
Синтезирован и исследован широкий спектр литийзамещенных порошков номинального состава ГА, подвергнутых термообработке при 900, 1200, 1400°С. Выявлено влияние катионов лития на параметры кристаллической решетки и значения ОКР. Показано, что при температуре 1200 и 1400°С катионы лития способствуют частичному переходу апатита в литийзамещенные формы ТКФ, количество которых возрастает с увеличением степени замещения. При температуре 1400°С катионы лития способствуют сохранению OH-групп в апатитовой структуре при степени замещения 1, 5 и 10%.
Показано, что ионы лития, образуя в зависимости от степени замещения твердые растворы внедрения или/и замещения в ГА, интенсифицируют процесс спекания за счет образования вакансий по катиону и аниону, что позволяет получать плотные керамические материалы ГА уже при 1100°С. Полученные результаты следует учитывать при разработке технологии литийсодержащей ГА-керамики с регулируемыми свойствами, предназначенной для применения в реконструктивно-заместительной костной хирургии.
Список литературы
Баринов С.М. Керамические и композиционные материалы на основе фосфатов кальция для медицины // Успехи химии. 2010. Т. 79. № 1. С. 15–32.
Баринов С.М., Комлев В.С. Биокерамика на основе фосфатов кальция. М.: Наука, 2005. 206 с.
Кубарев О.Л., Баринов С.М., Комлев В.С. Распределение магния при синтезе бифазных фосфатов кальция // Докл. РАН. 2008. Т. 418. № 4. С. 497–499.
Satija N.K., Sharma D., Afrin F., Tripathi R.P., Gangenahalli B. High Throughput Transcriptome Profiling of Lithium Stimulated Human Mesenchymal Stem Cells Reveals Priming Towards Osteoblastic Lineage // PLoS One. 2013. V. 8. № 1. P. e55769.
Wang Y., Yang X., Gu Z., Qin H., Li L., Liu J., Yu X. In vitro Study on the Degradation of Lithium-Doped Hydroxyapatite for Bone Tissue Engineering Scaffold // Mater. Sci. Eng. C. 2016. V. 66. P. 185–192.
Chen Y., Whetstone H.C., Lin A.C., Nadesan P., Wei Q.X., Poon R., Alman B.A. Beta-Catenin Signaling Plays a Disparate Role in Different Phases of Fracture Repair: Implications For Therapy to Improve Bone Healing // PLoS Med. 2007. V. 4. P. 1216–1229.
Drdlik D., Slama M., Hadraba H., Drdlikova K., Cihlar J. Physical, Mechanical, and Biological Properties of Electrophoretically Deposited Lithium-Doped Calcium Phosphates // Ceram. Int. 2018. V. 44. № 3. P. 2884–2891.
Kaygili O., Keser S., Ates T., Yakuphanoglu F. Synthesis and Characterization of Lithium Calcium Phosphate Ceramics // Ceram. Int. 2013. V. 39. № 7. P. 7779–7785.
Badran H., Yahia I.S., Hamdy M.S., Awwad N.S. Lithium-Doped Hydroxyapatite Nano-Composites: Synthesis, Characterization, Gamma Attenuation Coefficient and Dielectric Properties // Rad. Phys. Chem. 2017. V. 130. P. 85–91.
Гольдберг М.А., Смирнов В.В., Иевлев В.М., Баринов С.М., Куцев С.В., Шибаева Т.В., Шворнева Л.И. Влияние времени старения на свойства порошков в системе гидроксиапатит карбонат кальция // Неорган. материалы. 2012. Т. 48. № 2. С. 225–225.
Meejoo S., Maneeprakorn W., Winotai P. Phase and Thermal Stability of Nanocrystalline Hydroxyapatite Prepared via Microwave Heating // Thermochim. Acta. 2006. V. 447. № 1. P. 115–120.
Лукин Е.С. Современная оксидная керамика с регулируемой микроструктурой. Ч. III. Микроструктура и процессы рекристаллизации в керамических оксидных материалах // Огнеупоры и техническая керамика. 1996. № 7. С. 2–7.
Беляков А.В., Лукин Е.С. Физико-химические основы получения порошков твердых растворов и сложных оксидов // Тр. Моск. хим.-технол. ин-та им. Д.И. Менделеева. 1987. № 146. С. 5–17.
Zhang X., Mo F., Zhou L., Gong M. Properties-Structure Relationship Research on LiCaPO4:Eu2+ as Blue Phosphor for NUV LED Application // J. Alloys Compd. 2013. V. 575. P. 314–318.
Ефимов А.И., Белорукова Л.П., Василькова И.В., Чечев В.П. Свойства неорганических соединений. Справочник. Л.: Химия, 1983. Т. 392.
Chen Z.F., Darvell B.W., Leung V.W.H. Hydroxyapatite Solubility in Simple Inorganic Solutions // Arch. Oral Biology. 2004. V. 49. № 5. P. 359–367.
Беляков А.В., Лукин Е.С., Попова Н.А., Горожен-ко Ю.Д., Мамаева Н.Б., Андрианов Н.Т. О спекании высокодисперсных порошков // Тр. Моск. хим.-технол. ин-та им. Д.И. Менделеева. 1988. № 153. С. 104–110.
Mezahi F., Oudadesse H., Harabi A., Lucas-Girot A., Le Gal Y., Chaair H., Cathelineau G. Dissolution Kinetic and Structural Behaviour of Natural Hydroxyapatite vs. Thermal Treatment: Comparison to Synthetic Hydroxyapatite // J. Therm. Anal. Calorim. 2008. V. 95. № 1. P. 21–29.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы