Неорганические материалы, 2019, T. 55, № 7, стр. 775-781
Тепловое расширение шеелитоподобных молибдатов в виде порошков и керамики
М. Г. Токарев 1, Е. А. Потанина 1, *, А. И. Орлова 1, С. А. Хайнаков 2, М. С. Болдин 1, Е. А. Ланцев 1, Н. В. Сахаров 1, А. А. Мурашов 1, С. Гарсия-Гранда 2, А. В. Нохрин 1, В. Н. Чувильдеев 1
1 Нижегородский государственный университет им. Н.И. Лобачевского
603950 Нижний Новгород, пр. Гагарина, 23, Россия
2 Университет Овьедо
33003 Овьедо, ул. Сан Франциско, 1, Испания
* E-mail: Ekaterina.potanina@list.ru
Поступила в редакцию 23.05.2018
После доработки 10.02.2019
Принята к публикации 12.02.2019
Аннотация
Получены новые твердые растворы состава NaxSr1 – 2xNdxMoO4 (x = 0–0.5, Δx = 0.1) со структурой шеелита. Определены их кристаллографические параметры в зависимости от состава и температуры. Рассчитаны коэффициенты теплового расширения при t = 25–1000°C: αa = (12.9–14.9) × 10–6 °С–1, αc = (24.9–25.9) × 10–6 °С–1. Керамику спекали методом SPS при tmax ≈ 872–985 °C и τ ≈ 650–750 с. Относительная плотность керамики составила 97–99%.
ВВЕДЕНИЕ
Повышение экологической безопасности при обращении с радиоактивными отходами (РАО) является актуальной проблемой современной атомной индустрии. Улучшение известных и разработка новых материалов с нужными эксплуатационными характеристиками для изоляции высокоактивных отходов должны способствовать снижению риска от попадания радионуклидов в окружающую среду. В этом отношении перспективны кристаллические минералоподобные формы – реализация принципа “природоподобия”.
Среди них внимания заслуживают структурные аналоги минералов группы шеелита (CaWO4) и, в частности, молибдаты.
Молибден изучается в настоящее время как перспективный материал для оболочек ТВЭЛ, заменитель используемому цирконию [1], который имеет недостатки: 1) может активно реагировать с водой с образованием водорода при температурах выше 700°С, что чрезвычайно опасно при авариях на АЭС; 2) реагирует с перегретым диоксидом урана в ядерном топливе, что приводит к выделению дополнительного тепла и снижает температуру плавления топлива, способствуя перегреву и плавлению активной зоны АЭС [2, 3]. Замена Zr на Mo в названных конструкциях будет формировать новый тип Mo-содержащих отходов.
В [4] молибдаты со структурой повеллита, изоструктурного шеелиту, изучают для иммобилизации ядерных отходов, богатых молибденом (Mo-rich nuclear waste). Такие кристаллические формы могут также включать лантаноиды и актиноиды [5].
В природе шеелит кристаллизуется в тетрагональной сингонии (пр. гр. I41/a) и состоит из полиэдров CaО8 и WО4, соединенных через общие О-вершины [6].
Для соединений с такой структурой характерен широкий изовалентный и гетеровалентный изоморфизм. По данным [7], катионы Ca могут быть частично или полностью замещены на катионы Sr, Cu, Mn, Fe, Ba, РЗЭ (Nd, Pm, Sm, Eu), Cr, Nb, Ta, а катионы W – на Mo, Ge, V, I, Re. В литературе представлено большое число работ о соединениях со структурой шеелита, содержащих катионы: K, La–Lu [8]; Ca, Sr, Ba и РЗЭ [9]; ЩЗЭ и Pm [10, 11]; Li, Na и Np [12]; Na и U(IV) [13]; K, Rb, Cs и Nd, Pu, Am [14]; Li, Na и Pu [15]; Li, K и La, Nd, Dy, Er [16]; Li, Rb, РЗЭ [17]; Li и K, Rb, Tl, Nd [18]; Li, Tl, РЗЭ [19]; K, Cu и Ho, Gd, Tb [20, 21]; Li, Ba и Gd, Tm [22]. Во всех изученных системах представлены либо индивидуальные соединения (вольфраматы и молибдаты Ca, Sr, Ba, РЗЭ), либо твердые растворы с двумя типами катионов: 1) щелочных и щелочноземельных элементов, 2) щелочных и f-элементов (РЗЭ, урана), 3) щелочноземельных и РЗЭ.
Поведение веществ со структурой шеелита при нагревании изучено в большей степени для индивидуальных соединений. Описанные в [23, 24] коэффициенты теплового расширения при t = 25–1000°C для CaWO4, CaMoO4, SrMoO4, BaMoO4 составили: αа = 13.5 × 10–6, αс = 22.8 × × 10–6 °C–1; αа = 12.7 × 10–6, αс = 21.4 × 10–6 °C–1; αа = 11.4 × 10–6 °C–1; αа = 9.38 × 10–6 °C–1 соответственно. Изученные вольфраматы и молибдаты относят к материалам с высоким температурным коэффициентом линейного расширения (ТКЛР).
Необходимо учитывать, что порошковые образцы не являются надежной формой хранения компонентов РАО. В настоящей работе предлагается поликристаллические соединения помещать в керамические матрицы. При этом важное значение имеет метод спекания. В [25, 26] синтез керамики составов K0.5La0.5MoO4 и Li0.5Ln0.5MoO4 (Ln = Nd, Er, Gd, Y, Yb, Sm, и Ce) проводили методом одноосного холодного прессования с последующим обжигом при t = 560–720°C в течение 2 или 5 ч, достигнутая относительная плотность составила ρотн = 93–95%.
Условия процесса спекания керамики методом Spark Plasma Sintering (SPS), примененного в настоящей работе, являются широкорегулируемыми, в том числе спекание можно проводить при высоком давлении и относительно малых температуре и времени, что делает возможным получение керамик из материалов с низкими температурами разложения, легковозгоняющихся соединений, имеющих фазовые переходы при высоких температурах [27, 28].
При разработке материалов для консолидации отходов ядерных технологий в кристаллические матрицы важным является знание о формировании твердых растворов с более сложными составами, чем описанные выше, их поведении при нагревании и возможности получения из них плотной керамики.
В настоящей работе сделан шаг в таком направлении. Стояла задача получить и охарактеризовать твердые растворы молибдатов со структурой шеелита, в составе которых совместно могут присутствовать щелочные, щелочноземельные и редкоземельные элементы: Na, Sr, Nd. В них Sr, Nd являются имитаторами продуктов ядерного распада, а Nd – также имитатором минор-актиноидов.
Предстояло синтезировать твердые растворы состава NaxSr1 – 2xNdxMoO4 с x = 0–0.5, Δx = 0.1 установить концентрационные пределы их существования, оценить поведение при нагревании, получить и исследовать керамику на их основе.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез порошков. Для получения порошков использовали метод осаждения в водных системах. Исходные реагенты NaNO3, Sr(NO3)2, Nd(NO3)3 · 6H2O растворяли в воде в стехиометрических количествах и при постоянном перемешивании добавляли раствор осадителя (NH4)6Mo7O24 · · 4H2O. Наблюдали моментальное выпадение осадка. Перемешивание продолжали еще 30 мин. Образовавшуюся суспензию грели 10 ч при 90°С. Сухой остаток диспергировали в агатовой ступке в течение 20 мин и затем выдерживали при t = 500, 600, 700, 800, 900, 1000°С с τ = 15 ч на каждой стадии. Контроль фазового состава и диспергирование в агатовой ступке выполняли после каждого этапа термостатирования.
Синтез керамики. Для спекания керамики использовали метод SPS. Порошки помещали в графитовую пресс-форму с внутренним диаметром 10.8 мм и нагревали за счет пропускания миллисекундных импульсов постоянного электрического тока большой мощности (до 3 кА). Температуру измеряли с помощью пирометра Chino IR-AH, сфокусированного на поверхности графитовой пресс-формы. Спекание осуществляли в вакууме (6 Па). Величина приложенного одноосного давления составляла ~70 МПа.
Методы и установки. Элементный состав определяли с помощью энергодисперсионной рентгеновской спектроскопии (EDS) на установке JEOL JSM 6610LV (JEOL Ltd., Япония).
Фазовый состав порошков и керамики устанавливали на рентгеновском дифрактометре Shimadzu LabX XRD-6000 (CuКα-фильтрованное излучение, λ = 1.54056 Å) в интервале углов 2θ = = 10°–50°.
Высокотемпературные рентгенографические исследования выполняли на рентгеновском дифрактометре Panalytical X’Pert Pro с высокотемпературной камерой Anton Paar HTK-1200N в интервале температур 25–1000°С, в интервале углов 2θ = 15°–60°.
Спекание порошков в керамики проводили на установке DR. SINTER model SPS-625 Spark Plasma Sintering System (SPS SYNTEX INC. Ltd., Япония).
Плотность керамики измеряли методом гидростатического взвешивания в дистиллированной воде на весах Sartorius CPA 225D.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Порошковые образцы. Полученные образцы представляли собой мелкокристаллические порошки сиреневого цвета (кроме х = 0 – бесцветный).
Рассчитанные и экспериментально установленные значения x (табл. 1) различались незначительно.
Таблица 1.
Рассчитанные и экспериментально установленные элементные составы образцов NaxSr1 – 2xNdxMoO4
| х | Na, х | Sr, 1 – 2х | Nd, х |
|---|---|---|---|
| расчет | эксперимент | ||
| 0 | 0 | 1 | 0 |
| 0.1 | 0.11 | 0.78 | 0.11 |
| 0.2 | 0.20 | 0.60 | 0.20 |
| 0.3 | 0.29 | 0.42 | 0.29 |
| 0.4 | 0.41 | 0.18 | 0.41 |
| 0.5 | 0.5 | 0 | 0.5 |
Согласно данным РФА после термообработки, однофазные продукты составов NaxSr1 – 2xNdxMoO4 (x = 0–0.5) образовались при t = 800°C и сохраняли свой состав после нагревания при t = 1000°C в течение τ = 15 ч. На рис. 1 представлены рентгенограммы после всех стадий температурной обработки для образца Na0.1Sr0.8Nd0.1MoO4. Результаты для других составов были аналогичными. Дифрактограммы образцов после термостатирования при t = 800°C приведены на рис. 2.
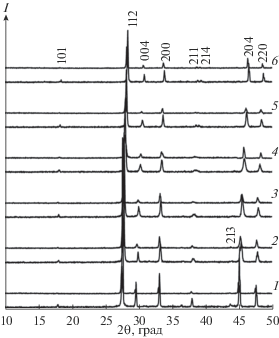
Рис. 1.
Дифрактограммы порошка Na0.1Sr0.8Nd0.1MoO4 после термообработки при 500 (1), 600 (2), 700 (3), 800 (4), 900 (5), 1000°С (6).
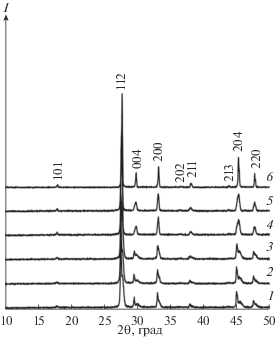
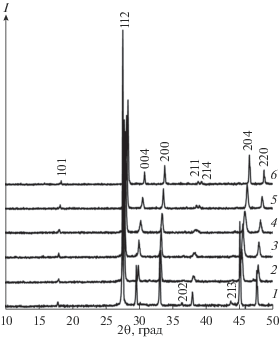
Рис. 2.
Дифрактограммы порошков NaxSr1 – 2xNdxMoO4 с x = 0 (1), 0.1 (2), 0.2 (3), 0.3 (4), 0.4 (5), 0.5 (6) после термической обработки при t = 800°С (τ = 15 ч).
Порошки кристаллизовались в структурном типе шеелита, пр.гр. I41/a (аналоги базы данных ICDD: SrMoO4 – № 08-0482, Na0.5Nd0.5MoO4 – № 25-0852).
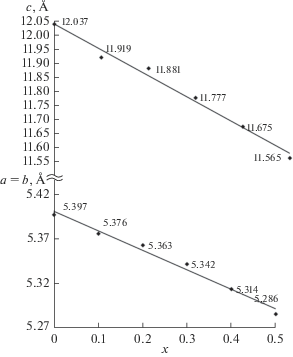
На рис. 3 в виде графических зависимостей от состава приведены параметры элементарных ячеек a и c. Зависимости имели линейный характер для всего интервала значений x, с увеличением x величины a, c уменьшались.
Таким образом, в изучаемой системе наблюдается формирование ряда твердых растворов, реализуется гетеровалентное изоморфное замещение 2Sr2+ $ \rightleftarrows $ Na+ + Nd3+.
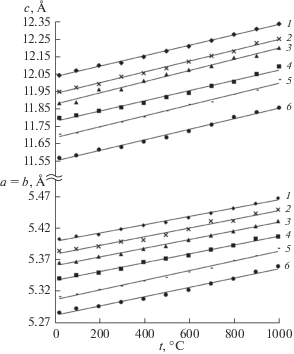
Для полученных образцов NaxSr1 – 2xNdxMoO4 с x = 0, 0.1, 0.2, 0.3, 0.4, 0.5 исследовали поведение при нагревании методом высокотемпературной рентгенографии в интервале температур от 25 до 1000°C. Зависимости рассчитанных параметров элементарной ячейки от температуры a = f(t) и c = f(t) (рис. 4) характеризуются монотонным ростом.
Рис. 4.
Зависимости параметров элементарной ячейки a и c образцов NaxSr1 – 2xNdxMoO4 с x = 0 (1), 0.1 (2), 0.2 (3), 0.3 (4), 0.4 (5), 0.5 (6) от температуры.
Значения осевых (αa и αс) и среднего (αср) ТКЛР, а также анизотропии теплового расширения (Δα) исследуемых молибдатов представлены в табл. 2.
Таблица 2.
Коэффициенты и анизотропия теплового расширения молибдатов NaxSr1 – 2xNdxMoO4
| x | α × 106, °С–1 | |||
|---|---|---|---|---|
| αa | αc | αcр | Δα | |
| 0 | 12.9 | 24.9 | 18.9 | 12.0 |
| 0.1 | 13.0 | 25.1 | 19.1 | 12.1 |
| 0.2 | 13.0 | 25.2 | 19.1 | 12.2 |
| 0.3 | 14.9 | 25.4 | 20.2 | 10.5 |
| 0.4 | 13.1 | 25.5 | 19.3 | 12.4 |
| 0.5 | 13.2 | 25.9 | 19.6 | 12.7 |
ТКЛР характеризовали изучаемые молибдаты как высокорасширяющиеся. Они близки к значениям коэффициентов для молибдата SrMoO4 [24].
Керамические образцы. Из порошков NaxSr1 – 2xNdxMoO4 с x = 0, 0.1, 0.2, 0.3, 0.4, 0.5 получили керамику методом SPS. Диаграммы спекания привели на рис. 5, режимы спекания, экспериментальные и относительные плотности – в табл. 3: tmax ≈ 872–985°C, τ ≈ 650–750 с, ρотн ≈ 97–99%.
Рис. 5.
Зависимости скорости усадки S и температуры t от времени нагрева/спекания для образцов NaxSr1 – 2xNdxMoO4 с x = 0 (а), 0.1 (б), 0.2 (в), 0.3 (г), 0.4 (д), 0.5 (е): 1 – температура спекания, 2 – скорость усадки.
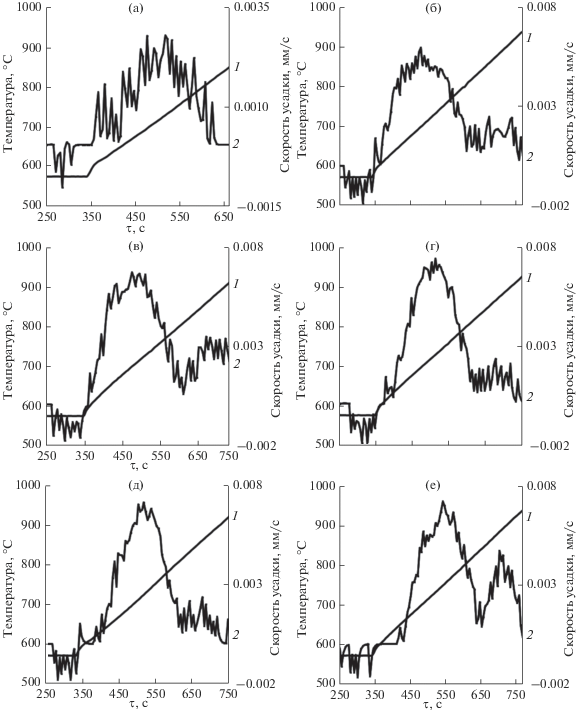
Таблица 3.
Режимы спекания и характеристики керамических образцов NaxSr1 – 2xNdxMoO4
| x | Рmax, МПа | tmax, °С | Smax × 103, мм/с | τсп, с | ρэксп, г/см3 | ρотн, % |
|---|---|---|---|---|---|---|
| 0 | 67.5 | 872 | 2.74 | 650 | 4.582 ± 0.008 | 97.08 |
| 0.1 | 67.3 | 985 | 6.99 | 750 | 4.675 ± 0.015 | 97.72 |
| 0.2 | 68.4 | 941 | 6.66 | 750 | 4.771 ± 0.009 | 99.29 |
| 0.3 | 69.1 | 942 | 7.28 | 750 | 4.783 ± 0.025 | 98.24 |
| 0.4 | 69 | 942 | 7.10 | 750 | 4.901 ± 0.009 | 98.93 |
| 0.5 | 68.5 | 942 | 7.16 | 750 | 4.987 ± 0.012 | 98.81 |
Согласно данным РФА (рис. 6), керамические образцы сохранили состав исходных порошковых.
Рис. 6.
Дифрактограммы молибдатов NaxSr1 – 2x-NdxMoO4 с x = 0 (1), 0.1 (2), 0.2 (3), 0.3 (4), 0.4 (5), 0.5 (6): нижние дифрактограммы – порошковые, верхние – керамические образцы.
Таким образом, расширены представления о семействе Мо-содержащих фаз со структурой шеелита, получены новые данные о поведении молибдатов сложного катионного состава при нагревании. Показана перспективность применения технологии SPS для спекания Мо-содержащих фаз.
ЗАКЛЮЧЕНИЕ
Образование твердых растворов NaxSr1 – 2xNdxMoO4 происходит во всем интервале х от 0 до 0.5. Параметры элементарных ячеек монотонно изменялись с изменением x. Исследование термической устойчивости показало, что полученные порошковые образцы сохраняли фазовый состав после термостатирования при t = 1000°C. Найденные коэффициенты теплового расширения для интервала температур 25–1000°C составили αa = (12.9–14.9) × 10–6°С–1, αc = (24.9–25.9) × 10–6°С–1. Получены керамические образцы с ρотн ≈ 97–99%.
Полученные результаты демонстрируют возможность применения шеелитоподобных кристаллических форм, содержащих молибден, в качестве матриц для иммобилизации компонентов РАО.
Список литературы
Borisevich V.D., Yan J., Smirnov A.Y., Bonarev A.K., Zeng S., Sulaberidze G.A., Jiang D. Cascade Design for Isotopically Modified Molybdenum as an Alternative to Zirconium Alloys // Chem. Eng. Res. Des. 2017. V. 128. P. 257–264. doi org/https://doi.org/10.1016/j.cherd.2017.10.018
Burakov B.E., Anderson E.B., Shabalev S.I., Strykanova E.E., Ushakov S.V., Trotabas M., Blanc J.-Y., Winter P., Duco J. The Behavior of Nuclear Fuel in First Days of the Chernobyl Accident // Mater. Res. Soc. Symp. Proc. 1997. P. 1297–1308. https://doi.org/10.1557/PROC-465-1297
Foreman M.R.St. An Introduction to Serious Nuclear Accident Chemistry // Cogent Chem. 2015. V. 1. № 1. P. 1–18. dx.doi.org/https://doi.org/10.1080/23312009.2015.1049111
Brinkman K., Fox K., Marra J., Reppert J., Crum J., Tang M. Single Phase Melt Processed Powellite (Ba,Ca)MoO4 for the Immobilization of Mo-Rich Nuclear Waste // J. Alloys Compd. 2013. V. 551. P. 136–142. doi org/https://doi.org/10.1016/j.jallcom.2012.09.049
Bosbach D., Rabung T., Brandt F., Fanghänel T. Trivalent Actinide Coprecipitation with Powellite (CaMoO4): Secondary Solid Solution Formation during HLW Borosilicate-Glass Dissolution // Radiochim. Acta. 2004. V. 92. P. 639–643. doi org/https://doi.org/10.1524/ract.92.9.639.54976
Morozov V.A., Mironov A.V., Lazoryak B.I., Khaiki-na E.G., Basovich O.M., Rossell M.D., Van Tendeloo G. Ag1/8Pr5/8MoO4: an Incommensurately Modulated Scheelite-Type Structure // J. Solid State Chem. 2006. V. 179. № 4. P. 1183–1191. doi org/https://doi.org/10.1016/ j.jssc.2005.12.041
Евдокимов А.А., Ефремов В.А., Трунов В.К., Клейнман И.А., Джуринский Б.Ф. Соединения редкоземельных элементов. Молибдаты. Вольфраматы. М.: Наука, 1991. 261 с.
Hanusa J. Raman Scattering and Infra-Red Spectra of Tungstates KLn(WO4)2-Family (Ln: La–Lu) // J. Mol. Struct. 1984. V. 114. P. 471–474. doi org/https://doi.org/10.1016/0022-2860(84)87189-6
Колыш А.В., Крюкова А.И., Коршунов И.А. Влияние растворимости компонентов на образование молибдатов редкоземельных элементов и 2-валентных металлов (кальция, стронция, бария) // Радиохимия. 1973. Т. 15. № 1. С. 3–7.
Колыш А.В., Крюкова А.И., Коршунов И.А. Влияние природы растворителя на образование смешанных кристаллов прометия с молибдатами щелочноземельных металлов из расплава. II. Сокристаллизация прометия с молибдатом кальция // Радиохимия. 1970. Т. 12. № 6. С. 814–818.
Колыш А.В., Крюкова А.И., Коршунов И.А. Влияние природы растворителя на образование смешанных кристаллов прометия с молибдатами щелочноземельных металлов из расплава. II. Сокристаллизация прометия с молибдатом стронция // Радиохимия. 1970. Т. 12. № 6. С. 808–814.
Pages M., Freundlich W. Phases of Scheelite Structure in the Neptunium Molybdate and Sodium or Lithium Molybdate Systems // J. Inorg. Nucl. Chem. 1972. V. 34. № 9. P. 2797–2801. doi org/https://doi.org/10.1016/0022-1902(72)80584-0
Lee M.R., Mahe P. Molybdates et Tungstates d’Uranium IV et de Sodium // C.R. Acad. Sci. Paris. 1974. V. 279. № 26. P. 1137–1170.
Tabuteau A., Pages M. Identification and Crystal Chemistry of Double Molybdates of Alkali Metals (K, Rb, Cs) and Transuranium Elements (Np, Pu, Am) // J. Inorg. Nucl. Chem. 1980. V. 42. № 3. P. 401–403. https://doi.org/10.1016/0022-1902(80)80015-7
Tabuteau A., Pages M., Freundlich W. Sur les Phases de Structure Scheelite dans les Systèms Molybdate de Plutonium-Molybdate de Lithium ou Sodium // Mater. Res. Bull. 1972. V. 7. № 7. P. 691–697. https://doi.org/10.1016/ 0025-5408(72)90058-X
Basovich O.M., Khaikina E.G., Solodovnikov S.F., Tsyrenova G.D. Phase Formation in the Systems Li2MoO4–K2MoO4–Ln2(MoO4)3 (Ln = La, Nd, Dy, Er) and Properties of Triple Molybdates LiKLn2(MoO4)4 // J. Solid State Chem. 2005. V. 178. № 5. P. 1580–1588. doi org/https://doi.org/10.1016/j.jssc.2004.12.016
Басович О.М., Хайкина Е.Г., Васильев Е.В., Фролов А.М. Фазообразование в системах Li2MoO4–Rb2MoO4–Ln2(MoO4)3 и свойства LiRbLn2(MoO4)4 // Журн. неорган. химии. 1995. Т. 40. № 12. С. 2047–2051.
Морозов В.А., Лазоряк Б.И., Смирнов В.А., Михаилин В.В., Басович О.М., Хайкина Е.Г. Кристаллические структуры и люминесцентные свойства тройных молибдатов LiMNd2(MoO4)4 (M = K, Rb, Tl) // Журн. неорган. химии. 2001. Т. 46. № 6. С. 977–982.
Басович О.М., Хайкина Е.Г. Синтез и исследование тройных молибдатов лития, таллия и редкоземельных элементов // Журн. неорган. химии. 1994. Т. 39. № 9. С. 1419–1420.
Szillat H., Müller-Buschbaum Hk. Synthese und Kristallstructur von KCuHoMo4O16 // Z. Naturforsch. 1994. V. 49. P. 350–354.
Müller-Buschbaum Hk., Gallinat St. Synthese und Röntgenstrukturanalyse von KCuGd2Mo4O16 und KCuTb2Mo4O16 // Z. Naturforsch. 1995. V. 50. P. 1794–1798.
Клевцова Р.Ф., Васильев А.Д., Глинская Л.А., Круглик А.И., Кожевникова Н.М., Корсун В.П. Кристаллоструктурное исследование тройных молибдатов состава Li3Ba2Ln3(MoO4)8, Ln = Gd, Tm // Журн. структур. химии. 1992. Т. 33. № 3. С. 126–130.
Achary S.N., Patwe S.J., Mathews M.D., Tyagi A.K. High Temperature Crystal Chemistry and Thermal Expansion of Synthetic Powellite (CaMoO4): a High Temperature X-ray Diffraction (HT-XRD) Study // J. Phys. Chem. Solids. 2006. V. 67. P. 774–781. doi org/ https://doi.org/10.1016/j.jpcs.2005.11.009
Binoy K.M., Hrudananda J., Asuvathraman R., Govindan Kutty K.V. Electrical Conductivity and Thermal Expansion Behavior of MMoO4 (M = Ca, Sr and Ba) // J. Alloys Compd. 2015. V. 640. P. 475–479. doi org/https://doi.org/10.1016/j.jallcom.2015.04.054
Pang L.-X., Zhou D., Cai C.-L., Liu W.-G. Infrared Spectroscopy and Microwave Dielectric Properties of Ultra-Low Temperature Firing (K0.5La0.5)MoO4 Ceramics // Mater. Lett. 2013. V. 92. P. 36–38. doi org/https://doi.org/10.1016/j.matlet.2012.10.082
Pang L.-X., Zhou D., Guo J., Yue Z.-X., Yao X. Microwave Dielectric Properties of (Li0.5Ln0.5)MoO4 (Ln = Nd, Er, Gd, Y, Yb, Sm, and Ce) Ceramics // J. Am. Ceram. Soc. 2015. V. 98. № 1. P. 130–135. doi org/https://doi.org/10.1111/jace.13247
Hérisson de Beauvoir T., Molinari F., Chung-Seu U.C., Michau D., Denux D., Josse M. Densification of MnSO4 Ceramics by Cool-SPS: Evidences for a Complex Sintering Mechanism and Magnetoelectric Coupling // J. Eur. Ceram. Soc. 2018. V. 38. № 11. P. 3867–3874. doi org/https://doi.org/10.1016/j.jeurceramsoc.2018.04.005
Herisson de Beauvoir T., Sangregorio A., Bertrand A., Payen C., Michau D., Chunga U.-C., Josse M. Cool-SPS Stabilization and Sintering of Thermally Fragile, Potentially Magnetoelectric, NH4FeP2O7 (CJ-3:IL04) // Ceram. Int. In Press. doi org/https://doi.org/10.1016/j.ceramint.2018.12.103
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы