Неорганические материалы, 2020, T. 56, № 10, стр. 1137-1144
Влияние механической обработки и способа введения углеродного материала на электрохимические свойства композитов Li4Ti5O12/C
И. А. Стенина 1, *, А. Н. Соболев 1, А. А. Кузьмина 2, Т. Л. Кулова 2, А. Б. Ярославцев 1
1 Институт общей и неорганической химии им. Н.С. Курнакова Российской академии наук
119991 Москва, Ленинский пр., 31, Россия
2 Институт физической химии и электрохимии им. А.Н. Фрумкина Российской академии наук
119991 Москва, Ленинский пр., 31, корп. 4, Россия
* E-mail: stenina@igic.ras.ru
Поступила в редакцию 06.03.2020
После доработки 10.04.2020
Принята к публикации 16.04.2020
Аннотация
Золь–гель-методом с последующей механической обработкой в планетарной мельнице получены анодные материалы Li4Ti5O12/C различной степени дисперсности. Углерод вводили как методом in situ, так и путем механического смешения титаната лития с сажей Timcal. Полученные материалы охарактеризованы с помощью рентгенофазового анализа, электронной микроскопии, метода низкотемпературной адсорбции азота; проведено их электрохимическое тестирование. Показано, что уменьшение размера частиц Li4Ti5O12 при увеличении интенсивности помола в планетарной мельнице более выражено для композитов с сажей Timcal. При малой скорости заряда/разряда (0.1С) электрохимическая емкость композитов, обработанных в планетарной мельнице при скоростях ≤400 об./мин, выше таковой для исходного Li4Ti5O12. При высоких плотностях тока (18С) наибольшей величиной электрохимической емкости (107 мАч/г) характеризуется композит Li4Ti5O12 с сажей Timcal, обработанный при 200 об./мин.
ВВЕДЕНИЕ
Благодаря небольшому весу, высокой плотности энергии и возможности работы при высоких скоростях заряда/разряда литий-ионные аккумуляторы (ЛИА) занимают лидирующее положение на рынке вторичных источников тока [1, 2]. Основной областью применения ЛИА являются портативные электронные устройства, электромобили, что определяет повышенные требования к их безопасности и сроку службы. В то же время электродные материалы, использующиеся в современных коммерческих ЛИА, часто не отвечают им в полной мере. Это обуславливает поиск новых материалов для ЛИА и путей улучшения свойств уже существующих [3, 4].
В последние годы в качестве перспективного анодного материала для ЛИА рассматривается титанат лития Li4Ti5O12, что, в первую очередь, определяется его безопасностью [5–7] и низкой деградацией при циклировании за счет малого (<0.2%) изменения объема элементарной ячейки Li4Ti5O12 [8]. Кроме того, интеркаляция лития в нем происходит при практически постоянном рабочем потенциале ~1.5 В [9, 10]. Это позволяет минимизировать процессы окисления электролита и образования на поверхности электрода пассивной электролитной пленки (SEI) [11]. В то же время величины электронной и ионной проводимости Li4Ti5O12 сравнительно малы, что значительно ограничивает его использование в устройствах, требующих высокой пиковой мощности [12–14].
Для улучшения электрохимических характеристик титаната лития используется ряд подходов. Так, ионную проводимость анодного материала позволяет увеличить гетеровалентное допирование [15–19], а создание композитов с высокопроводящими углеродными добавками (Li4Ti5O12/C) обеспечивает быструю доставку лития к частицам материала за счет быстрого переноса ионов Li+ и электронов по межзеренным границам [20–23]. Добавка углеродного материала возможна как в ходе синтеза титаната лития (метод in situ), так и к уже готовому Li4Ti5O12. В первом случае процесс проводят путем смешения углерода с Li4Ti5O12 (или его прекурсором) с последующим отжигом в инертной или восстановительной атмосфере [22, 24]. Использование данного способа также приводит к ограничению роста частиц титаната лития в ходе синтеза [25, 26]. При уменьшении размера частиц Li4Ti5O12 не только увеличивается площадь его контакта с электролитом, но также сокращается длина диффузионного пути ионов лития в ходе процессов внедрения/экстракции и улучшается кинетика интеркаляции лития, что, в конечном итоге, приводит к возможности сохранения высоких значений емкости электродного материала при увеличении скорости заряда/разряда [27–29]. В этой связи особое внимание уделяется как синтезу наноматериалов на основе титаната лития различными методами (гидротермальным, золь–гель) [30, 31], так и механической постобработке Li4Ti5O12, полученного твердофазным способом, с целью уменьшения размера его частиц [32]. Однако введение прекурсора углерода методом in situ приводит к некоторому усложнению процесса синтеза. Поэтому более перспективным, особенно для производства, может быть механическое смешение готовых частиц титаната лития с углеродным материалом. Это тем более привлекательно, поскольку при приготовлении электродной пасты для сборки аккумулятора используется сажа. Представляется, что механическая обработка композитов Li4Ti5O12/C в шаровой мельнице может привести не только к большей степени гомогенизации и более равномерному распределению углеродного материала, но и к уменьшению размера сростков/агломератов титаната лития и, соответственно, улучшению электрохимических свойств материала в целом.
Целью данной работы было исследование влияния способа введения углеродного материала и последующей механической обработки на электрохимические свойства композитов Li4Ti5O12/C.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Титанат лития (LTO) получали золь–гель-методом в присутствии лимонной кислоты по предложенной ранее методике [29]. Тетрабутилат титана (Alfa Aesar, 98+%), карбонат лития (Merck, >99%) растворяли в смеси этанол + азотная кислота (объемное соотношение 5 : 1). К полученному раствору добавляли раствор лимонной кислоты в минимальном количестве воды. Полученную смесь нагревали при 95°С до образования желатиноподобной массы, которую затем выдерживали при 400°С в течение 5 ч на воздухе и перетирали в агатовой ступке до однородной массы. В случае синтеза композитов LTO/5S к полученному прекурсору титаната лития добавляли 5 мас. % сахарозы (Sigma-Aldrich, >99%), перетирали и отжигали при температуре 800°С в течение 5 ч в токе аргона. Композиты LTO/5СT или LTO/10СT получали путем механического смешения титаната лития, отожженного при 800оС на воздухе, с 5 и 10 мас. % сажи Timcal.
Далее все полученные материалы подвергали механической обработке в планетарной мельнице Fritch Pulverisette 7 classic line с использованием агатовых размольных стаканов и шаров в этаноле. Помол проводили в течение 8 ч при скорости 200–600 об./мин в режиме: вращение – 3 мин, пауза – 2 мин. Скорость помола (об./мин) указана в названии образцов, например, LTO/5S_200 или LTO/10СT_0.
Для проведения рентгенофазового анализа образцов использовали дифрактометр Rigaku D/MAX 2200 (излучение CuKα). Размер частиц (d) оценивали на основании уширения линий рентгенограмм (области когерентного рассеяния (ОКР)) по формуле Дебая-Шеррера, используя в качестве стандарта LaB6:
где k – постоянная Шеррера (0.9), λ – длина волны, B –ширина линии образца при дифракционном угле θ, b – ширина линии стандарта.Микроструктуру полученных образцов изучали с помощью сканирующего электронного микроскопа (СЭМ) Carl Zeiss NVision 40.
Исследование удельной площади поверхности полученных композитов проводили методом БЭТ при –196°С с помощью анализатора Сорбтометр-М (ООО “Катакон”). Перед измерением образцы дегазировали при 200°С в течение 1 ч. Из величин удельной площади поверхности рассчитывали размеры частиц (l) исходя из предположения, что частицы имеют кубическую форму:
(2)
$l = {6 \mathord{\left/ {\vphantom {6 {\left( {\rho S} \right)}}} \right. \kern-0em} {\left( {\rho S} \right)}},$Содержание углерода в полученных композитах определяли методом CHN-анализа на элементном анализаторе EuroVektor EA3000.
Для приготовления электродной пасты смешивали полученные композиты Li4Ti5O12/C (активный материал), сажу (Timcal) и фторид поливинилидена (Aldrich), предварительно растворенный в N-метилпирролидиноне (Aldrich), в соотношении 88 : 10 : 2. Полученную электродную массу наносили на сетку из нержавеющей стали, используемую в качестве токоотвода (толщина слоя 10–15 мг/см2), затем прессовали под давлением 0.1 ГПа и сушили при 120°С в вакууме в течение 8 ч.
Для исследования электрохимических характеристик использовали трехэлектродные герметичные электрохимические ячейки с литиевым вспомогательным и литиевым электродом сравнения, в качестве сепаратора использовался нетканый полипропилен (НПО “Уфим”). Электрохимические ячейки собирали в перчаточном боксе в атмосфере сухого аргона. В качестве электролита применяли 1М LiPF6 в смеси этиленкарбоната, диэтилкарбоната и диметилкарбоната (1 : 1 : 1) (Aldrich). Электрохимическое циклирование ячеек проводили в интервале потенциалов от 1 до 3 В с помощью зарядно-разрядного стенда ЗРУ 50 мА-10 В (ООО “НТЦ Бустер”). Тестирование проводили в гальваностатическом режиме при плотностях тока 20–3200 мА/г.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На рис. 1 представлены рентгенограммы исследуемых материалов. Углеродное покрытие, полученное методом in situ, так же как и используемая для приготовления композитов сажа, являются рентгеноаморфными. Рентгенограммы исходного титаната лития, отожженного на воздухе, и композита Li4Ti5O12/5S, полученного с использованием сахарозы, представлены рефлексами шпинели Li4Ti5O12 (пр. гр. Fd3m, PDF-2 № 72-0426). Нанесение углеродного покрытия на титанат лития методом in situ закономерно приводит к получению более дисперсного материала по сравнению с Li4Ti5O12, отожженным на воздухе, что выражается в некотором уширении линий рентгенограмм. Действительно, удельная площадь поверхности Li4Ti5O12/5S (10 м2/г) оказалась почти в 3 раза больше, чем Li4Ti5O12 (3 м2/г). При этом размер ОКР для этих материалов составил 51 и 87 нм соответственно (табл. 1), что значительно меньше размеров частиц, рассчитанных из удельной площади поверхности (171 и 570 нм). Это свидетельствует о том, что полученные материалы представлены преимущественно агломератами частиц, причем в ходе помола эти агломераты частично разрушаются.
Рис. 1.
Рентгенограммы композиционных материалов LTO/5S_0 (1), LTO/5S_200 (2), LTO/5S_400 (3), LTO/5S_600 (4), LTO_200 (5), LTO/5CT_200 (6), LTO/10CT_400 (7), LTO/10CT_600 (8); приведены hkl рефлексов титаната лития, соответствующие карточке № 72-0426 (PDF-2), символами * и + обозначены рефлексы фазы рутила и материала размольного стакана.
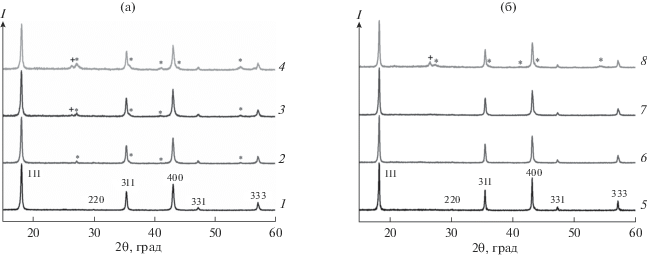
Таблица 1.
Размер частиц и площадь поверхности полученных образцов
| Образец | Площадь поверхности ±1, м2/г | Размер частиц по данным БЭТ, нм | Размер частиц (ОКР), нм |
|---|---|---|---|
| LTO_0 | 3 | 570 | 87 |
| LTO/10CT_0 | 8 | 214 | 87 |
| LTO_200 | 11 | 156 | 74 |
| LTO/5CT_200 | 13 | 132 | 75 |
| LTO/10CT_200 | 19 | 90 | 72 |
| LTO/10CT_400 | 20 | 86 | 66 |
| LTO/10CT_600 | 19 | 90 | 64 |
| LTO/5S_0 | 10 | 171 | 51 |
| LTO/5S_200 | 16 | 107 | 50 |
| LTO/5S_400 | 20 | 86 | 48 |
| LTO/5S_600 | 22 | 78 | 47 |
Механическая обработка в планетарной мельнице приводит к уширению линий рентгенограмм исследуемых образцов и появлению рефлексов диоксида титана (рутила) и материала размольного стакана. При этом в случае композиционных материалов, полученных методом in situ, последний эффект более выражен и образование рутила наблюдается уже при скорости помола 200 об./мин. Содержание примесей существенно возрастает по мере увеличения интенсивности помола.
Для композитов, полученных смешением с сажей Timcal, механическая обработка приводит к значительному уменьшению ОКР частиц – с 87 до 64 нм (табл. 1). Их удельная площадь поверхности, резко возрастая с 3 до 19 м2/г (для исходного Li4Ti5O12 и обработанного при 200 об./мин соответственно), далее с увеличением интенсивности обработки практически не меняется. В случае композиционных материалов, полученных методом in situ, механическая обработка лишь незначительно влияет на размер частиц. Так, с увеличением скорости помола от 200 до 600 об./мин величина ОКР уменьшается от 50 до 47 нм (табл. 1). При этом увеличение удельной площади поверхности, согласно данным по низкотемпературной адсорбции азота, напротив, более выражено (с 10 для исходного Li4Ti5O12/5S до 23 м2/г для материала, обработанного при скорости 600 об./мин). Таким образом, размеры ОКР титаната лития в композитах, полученных как методом in situ, так и смешением с сажей, уменьшаются с ростом интенсивности механической обработки. Аналогично с ростом скорости помола уменьшается и размер частиц полученных образцов, рассчитанный из их удельной площади поверхности (табл. 1), что связано в первую очередь с разрушением агломератов частиц.
Данные сканирующей электронной микроскопии (рис. 2а, 2б) подтверждают, что исходный композит, полученный методом in situ, и титанат лития, отожженный на воздухе, представляют собой сростки частиц с размером последних 50–200 и 200–600 нм соответственно. При механической обработке композитов со скоростью 200 об./мин сростки частиц сохраняются, однако при этом также появляются значительно более мелкие частицы с размером до 50 и 100 нм для образцов, полученных методом in situ и смешением с сажей Timcal соответственно (рис. 2в, 2г). При увеличении интенсивности помола данная тенденция сохраняется. При этом доля частиц меньшего размера увеличивается, а средний размер частиц соответственно уменьшается.
Рис. 2.
Микрофотографии полученных композитов LTO/5S (а), LTO_0 (б), LTO/5S_200 (в), LTO/10CT_200 (г), LTO/5S_400 (д), LTO/10CT_400 (е), LTO/5S_600 (ж), LTO/10CT_600 (з).

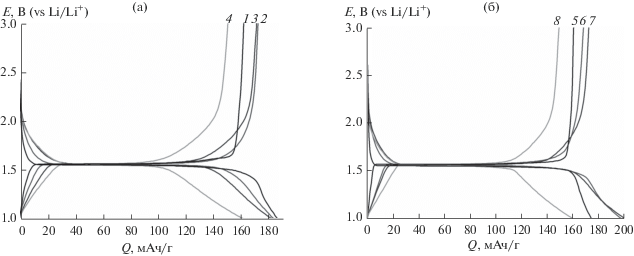
Зарядно-разрядные кривые полученных композитов (рис. 3) типичны для титаната лития: на них можно выделить участки с практически постоянным рабочим потенциалом (около 1.5 В), величина которого несколько изменяется при приближении процесса заряда (разряда) к завершению. Это обусловлено повышением вклада в данный процесс сопротивления формирующегося на поверхности слоя Li7Ti5O12/Li4Ti5O12, которое растет с ростом его толщины. В то же время можно отметить, что механическая обработка в шаровой мельнице приводит к уменьшению длины участка с постоянным потенциалом, причем этот эффект более выражен для образцов, обработанных при скорости помола 600 об./мин (рис. 3). Кроме того, несколько меняется и сам ход кривых как в начале, так и при приближении к завершению процессов заряда/разряда – они становятся более пологими. Ранее мы наблюдали схожий процесс при исследовании электрохимических свойств наноразмерного титаната лития [33], который связан с ростом взаимной растворимости фаз, сосуществующих в ходе интеркаляции/деинтеркаляции – Li4Ti5O12 и Li7Ti5O12, при уменьшении размера частиц. Кроме того, образующийся в процессе помола в качестве примеси рутил, имеющий меньшую емкость, также характеризуется более наклонной зарядно/разрядной кривой за счет большей взаимной растворимости формирующихся фаз и несколько отличным потенциалом плато [14].
Рис. 3.
Зарядно-разрядные кривые на 5-м цикле при плотности тока 20 мА/г для композиционных материалов LTO/5S_0 (1), LTO/5S_200 (2), LTO/5S_400 (3), LTO/5S_600 (4), LTO_0 (5), LTO/10CT_200 (6), LTO/10CT_400 (7), LTO/10CT_600 (8).
На рис. 4 приведены зависимости разрядной емкости полученных материалов в ходе циклирования при различной плотности тока. Разрядная емкость титаната лития, обработанного на скорости 200 об./мин, оказалась выше таковой для исходного Li4Ti5O12 при высоких скоростях циклирования (плотность тока ≥1600 мА/г) (рис. 4а). Добавление 5% сажи в ходе помола (при той же скорости) приводит к некоторому увеличению емкости и при низких плотностях тока. Среди всех образцов, подвергнутых механической обработке при 200 об./мин, наибольшей емкостью характеризуется образец, содержащий 10% сажи: 168 и 106 мАч/г при плотности тока 20 и 3200 мА/г. Дальнейшее увеличение скорости помола приводит к падению электрохимической емкости полученных композитов (рис. 3б). При этом если емкость композита, обработанного при скорости 400 об./мин, оказалась сопоставимой с исходным материалом, то для образца LTO/10CT_600 она значительно ниже во всем диапазоне плотностей тока, что в первую очередь обусловлено значительным количеством примеси электрохимически неактивных или малоактивных фаз.
Рис. 4.
Изменение обратимой разрядной емкости в ходе циклирования композитов Li4Ti5O12/C, полученных смешением с сажей (а, б) и методом in situ (в); плотность тока (мА/г) указана на рисунках.
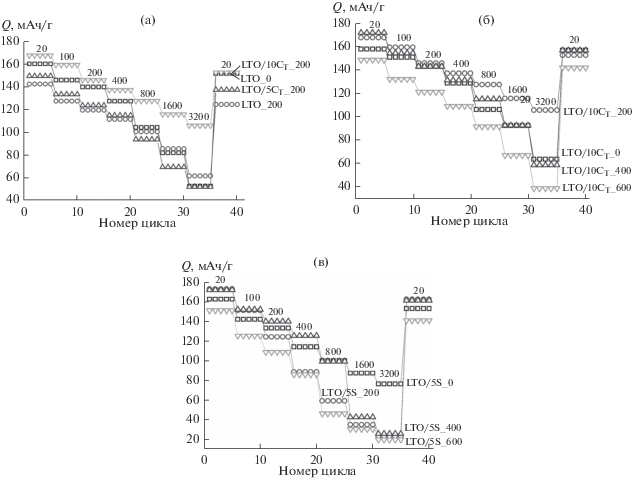
Нанесение углеродного покрытия на титанат лития методом in situ в сочетании с помолом в планетарной мельнице при малых скоростях (200 и 400 об./мин) приводит к увеличению электрохимической емкости полученных материалов при малых скоростях разряда/заряда: с 162 для исходного LTO/5S_0 до 172 мАч/г при плотности тока 20 мА/г (рис. 4в), что близко к теоретической величине (175 мАч/г). В то же время при дальнейшем повышении скорости циклирования наблюдается падение емкости композитов, что особенно выражено при плотностях тока ≥1600 мА/г. Механическая обработка в шаровой мельнице композитов LTO/5S приводит к значительному повышению дисперсности материала (удельная площадь поверхности возрастает почти в 2 раза) в первую очередь за счет разрушения агломератов его частиц. При этом какая-то часть самих частиц или их поверхности может остаться без проводящего углеродного покрытия. Это неизбежно должно приводить к падению емкости, особенно на больших скоростях заряда/разряда. Емкость материала, обработанного при скорости 600 об./мин, значительно ниже емкости исходного композита LTO/5S во всем диапазоне плотностей тока, что также определяется наличием примеси.
ЗАКЛЮЧЕНИЕ
Золь–гель-методом с последующей механической обработкой в шаровой мельнице получены анодные материалы Li4Ti5O12/C различной степени дисперсности. При этом введение углеродного материала проводили как путем нанесения углеродного покрытия методом in situ исходя из сахарозы, так и путем смешения титаната лития с сажей Timcal. По данным РФА, БЭТ и СЭМ, с ростом интенсивности помола средний размер частиц Li4Ti5O12 уменьшается. Данный эффект более выражен для композитов с сажей Timcal. В то же время можно отметить, что для получения титаната лития с меньшим размером частиц более эффективен метод нанесения углеродного покрытия in situ, нежели его механическая обработка в планетарной мельнице.
В случае композитов с сажей при увеличении скорости помола до 600 об./мин происходит образование примесных фаз, преимущественно рутила. Для композитов, полученных методом in situ, данный эффект наблюдается уже при скорости помола 200 об./мин. Создание композитов с углеродом методом in situ в сочетании с помолом в шаровой мельнице на малых скоростях (≤400 об./мин) приводит к повышению электрохимической разрядной емкости анодных материалов на их основе при малых плотностях тока (0.1С) по сравнению с исходным титанатом лития, но увеличивает их степень деградации. При высокой скорости заряда/разряда (18С) наибольшей величиной электрохимической емкости (106 мАч/г) характеризуется композит с сажей Timcal, обработанный при 200 об./мин.
Список литературы
Cebulla F., Naegler T., Pohl M. Electrical Energy Storage in Highly Renewable European Energy Systems: Capacity Requirements, Spatial Distribution, and Storage Dispatch // J. Energy Storage. 2017. V. 14. P. 211–223. https://doi.org/10.1016/j.est.2017.10.004
Zubi G., Dufo-López R., Carvalho M., Pasaoglu G. The Lithium-Ion Battery: State of the Art and Future Perspectives // Renewable Sustainable Energy Rev. 2018. V. 89. P. 292–308. https://doi.org/10.1016/j.rser.2018.03.002
Paterakis N.G., Erdinc O., Catalão J.P.S. An overview of Demand Response: Key-elements and international experience // Renewable Sustainable Energy Rev. 2017. V. 69. P. 871–891. https://doi.org/10.1016/j.rser.2016.11.167
Stenina I.A., Yaroslavtsev A.B. Nanomaterials for Lithium-Ion Batteries and Hydrogen Energy // Pure Appl. Chem. 2017. V. 89. № 8. P. 1185–1194. https://doi.org/10.1515/pac-2016-1204
Yi T.-F., Jiang L.-J., Shu J., Yue C.-B., Zhu R.-S., Qiao H.-B. Recent Development and Application of Li4Ti5O12 as Anode Material of Lithium Ion Battery // J. Phys. Chem. Solids. 2010. V. 71. P. 1236–1242. https://doi.org/10.1016/j.jpcs.2010.05.001
Han C., He Y.-B., Liu M., Li B., Yang Q.-H., Wong C.-P., Kang, F. A Review of Gassing Behavior in Li4Ti5O12-Based Lithium Ion Batteries // J. Mater. Chem. A. 2017. V. 5. P. 6368–6381. https://doi.org/10.1039/C7TA00303J
Sun X., Radovanovic P.V., Cui B. Advances in Spinel Li4Ti5O12 Anode Materials for Lithium-Ion Batteries // New J. Chem. 2015. V. 39. P. 38–63. https://doi.org/10.1039/C4NJ01390E
Ohzuku T., Ueda A., Yamamoto N. Zero-Strain Insertion Material of Li[Li1/3Ti5/3]O4 for Rechargeable Lithium Cells // J. Electrochem. Soc. 1995. V. 142. P. 1431–1435. https://doi.org/10.1149/1.2048592
Xu G., Han P., Dong S., Liu H., Cui G., Chen L. Li4Ti5O12-Based Energy Conversion and Storage Systems: Status and Prospects // Coord. Chem. Rev. 2017. V. 343. P. 139–184. https://doi.org/10.1016/j.mser.2015.10.001
Yi T.-F., Yang S.-Y., Xie Y. Recent Advances of Li4Ti5O12 as Promising Next Generation Anode Material for High Power Lithium-Ion Batteries // J. Mater. Chem. A. 2015. V. 3. P. 5750–5777. https://doi.org/10.1039/C4TA06882C
Song M.-S., Kim R.-H., Baek S.-W., Lee K.-S., Park K., Benayad A. Is Li4Ti5O12 a Solid-Electrolyte-Interphase-Free Electrode Material in Li-Ion Batteries? Reactivity between the Li4Ti5O12 Electrode and Electrolyte // J. Mater. Chem. A. 2014. V. 2. P. 631–636. https://doi.org/10.1039/C3TA12728A
Aravindan V., Lee Y.-S., Madhavi S. Research Progress on Negative Electrodes for Practical Li-Ion Batteries: Beyond Carbonaceous Anodes // Adv. Energy Mater. 2015. V. 5. № 13. Art. 1402225. https://doi.org/10.1002/aenm.201402225
Sandhya C.P., John B., Gouri C. Lithium Titanate as Anode Material for Lithium-Ion Cells: a Review // Ionics. 2014. V. 20. № 5. P. 601–620. https://doi.org/10.1007/s11581-014-1113-4
Ярославцев А.Б., Кулова Т.Л., Скундин А.М. Электродные наноматериалы для литий-ионных аккумуляторов // Успехи химии. 2015. Т. 84. № 8. С. 826–852.
Stenina I.A., Sobolev A.N., Yaroslavtsev S.A., Rusakov V.S., Kulova T.L., Skundin A.M., Yaroslavtsev A.B. Influence of Iron Doping on Structure and Electrochemical Properties of Li4Ti5O12 // Electrochim. Acta. 2016. V. 219. P. 524–530. https://doi.org/10.1016/j.electacta.2016.10.034
Kulova T.L., Kreshchenova Yu.M., Kuz’mina A.A., Skundin A.M., Stenina I.A., Yaroslavtsev A.B. New High-Capacity Anode Materials Based on Gallium-Doped Lithium Titanate // Mendeleev Commun. 2016. V. 26 № 4. P. 238–239. https://doi.org/10.1016/j.mencom.2016.05.005
Qian D., Gu Y., Chen Y., Liu H., Wang J., Zhou H. Ultra-High Specific Capacity of Cr3+-Doped Li4Ti5O12 at 1.55 V as Anode Material for Lithium-Ion Batteries // Mater. Lett. 2019. V. 238. P. 102–106. https://doi.org/10.1016/j.matlet.2018.11.163
Guo M., Wang S., Ding L.-X., Huang C., Wang H. Tantalum-Doped Lithium Titanate with Enhanced Performance for Lithium-Ion Batteries // J. Power Sources. 2015. V. 283. P. 372–380. https://doi.org/10.1016/j.jpowsour.2015.02.154
Cho H., Son H., Kim D., Lee M., Boateng S., Han H., Kim K.M., Kim S., Choi H., Song T., Lee K.H. Impact of Mg-Doping Site Control in the Performance of Li4Ti5O12 Li-Ion Battery Anode: First-Principles Predictions and Experimental Verifications // J. Phys. Chem. C. 2017. V. 121. P. 14994–15001. https://doi.org/10.1021/acs.jpcc.7b01475
Stenina I.A., Kulova T.L., Skundin A.M., Yaroslavtsev A.B. Carbon Composites as Anode Materials for Lithium-Ion Batteries // Rev. Adv. Mater. Sci. 2017. V. 49. P. 140–149.
Cheng Q., Tang S., Liang J., Zhao J., Lan Q., Liu C., Cao Y.-C. High Rate Performance of the Carbon Encapsulated Li4Ti5O12 for Lithium Ion Battery // Results Phys. 2017. V. 7. P. 810–812. https://doi.org/10.1016/j.rinp.2017.01.040
Park J.-H., Kang S.-W., Kwon T.-S., Park H.S. Spray-Drying Assisted Synthesis of a Li4Ti5O12/C Composite for High Rate Performance Lithium Ion Batteries // Ceram. Int. 2018. V. 44. P. 2683–2690. https://doi.org/10.1016/j.ceramint.2017.10.217
Mu D., Chen Y., Wu B., Huang R., Jiang Y., Li L., Wu F. Nano-Sized Li4Ti5O12/C Anode Material with Ultrafast Charge/Discharge Capability for Lithium Ion Batteries // J. Alloys Compd. 2016. V. 671. P. 157–163. https://doi.org/10.1016/j.jallcom.2016.02.095
Sha Y., Xu X., Li L., Cai R., Shao Z. Hierarchical Carbon-Coated Acanthosphere-Like Li4Ti5O12 Microspheres for High-Power Lithium-Ion Batteries // J. Power Sources. 2016. V. 314. P. 18–27. https://doi.org/10.1016/j.jpowsour.2016.02.084
Li D., Zhang X., Miao X., Liu Y., Chen S., Chen Y., Wang W., Zhang Y. Solid-State Synthesized Li4Ti5O12 for Ultrafast Lithium Ion Storage Enabled by Carbon-Coating Induced Particle Size Tailoring // J. Alloys Compd. 2019. V. 797. № 15. P. 1258–1267. https://doi.org/10.1016/j.jallcom.2019.05.164
Yao N.Y., Liu H.K., Liang X., Sun Y., Feng X.Y., Chen C.H., Xiang H.F. Li4Ti5O12 Nanosheets Embedded in Three-Dimensional Amorphous Carbon for Superior-Rate Battery Applications // J. Alloys Compd. 2019. V. 771. P. 755–761. https://doi.org/10.1016/j.jallcom.2018.08.001
Guo X., Xiang H.F., Zhou T.P., Ju X.K., Wu Y.C. Morphologies and Structures of Carbon Coated on Li4Ti5O12 and Their Effects on Lithium Storage Performance // Electrochim. Acta. 2014. V. 130. P. 470–476. https://doi.org/10.1016/j.electacta.2014.02.139
Lim J., Choi E., Mathew V., Kim D., Ahn D., Gim J., Kang S.-H., Kim J. Enhanced High-Rate Performance of Li4Ti5O12 Nanoparticles for Rechargeable Li-Ion Batteries // J. Electrochem. Soc. 2011. V. 158. № 3. P. A275–A280. https://doi.org/10.1149/1.3527983
Stenina I. A., Kulova T. L., Skundin A. M., Yaroslavtsev A.B. High Grain Boundary Density Li4Ti5O12/Anatase-TiO2 Nanocomposites as Anode Material for Li-Ion Batteries // Mater. Res. Bull. 2016. V. 75. P. 178–184. https://doi.org/10.1016/j.materresbull.2015.11.050
Zhao S., Ka O., Xian X., Sun L., Wang J. Effect of Primary Crystallite Size on the High-Rate Performance of Li4Ti5O12 Microspheres // Electrochim. Acta. 2016. V. 206. P. 17–25. https://doi.org/10.1016/j.electacta.2016.04.132
Sandhya C.P., John B., Gouri C. Surfactant-Assisted Sol-Gel Route to Lithium Titanate and Its Electrochemical Properties // J. Alloys Compd. 2016. V. 655. P. 238–243. https://doi.org/10.1016/j.jallcom.2015.09.174
Chauque S., Oliva F.Y., Visintin A., Barraco D., Leiva E.P.M., Cámara O.R. Lithium Titanate as Anode Material for Lithium Ion Batteries: Synthesis, Post-treatment and Its Electrochemical Response // J. Electroanal. Chem. 2017. V. 799. P. 142–155. https://doi.org/10.1016/j.jelechem.2017.05.052
Stenina I. A., Il’in A.B., Yaroslavtsev A.B. Synthesis and Ionic Conductivity of Li4Ti5O12 // Inorg. Mater. 2015. V. 51. P. 62–67. https://doi.org/10.1134/S0020168515010185
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы


