Неорганические материалы, 2020, T. 56, № 10, стр. 1107-1111
Получение особо чистого иодида цезия
М. В. Мастрюков 1, М. Н. Бреховских 1, *, В. М. Климова 2, П. В. Корнев 2, В. А. Федоров 1
1 Институт общей и неорганической химии им. Н.С. Курнакова Российской академии наук
119991 Москва, Ленинский пр., 31, Россия
2 АО “Государственный научно-исследовательский и проектный институт редкометаллической промышленности “Гиредмет”
111524 Москва, Электродная ул., 2, стр. 1, Россия
* E-mail: mbrekh@igic.ras.ru
Поступила в редакцию 12.03.2020
После доработки 08.05.2020
Принята к публикации 18.05.2020
Аннотация
В работе изложены результаты физико-химических исследований процесса получения особо чистого CsI квалификации 99.998 мас. % из технического продукта, синтезируемого взаимодействием карбоната цезия и иодистоводородной кислоты. Синтезированный CsI подвергается двухстадийной очистке, включающей вакуумную сушку и высокотемпературную дистилляцию. Рассчитаны кинетические константы и определена зависимость влагосодержания от температуры. Финишной стадией очистки CsI от лимитируемых примесей является высокотемпературная дистилляция. Полученные образцы охарактеризованы по содержанию примесей металлов методом масс-спектрометрии с индуктивно связанной плазмой и РФА. Результаты представлены впервые.
ВВЕДЕНИЕ
Иодид цезия используется для выращивания сцинтилляционных монокристаллов CsI:Na, CsI:Tl [1–3], а также для изготовления стекол, прозрачных в ИК-диапазоне [4, 5]. Основным методом получения монокристаллов на основе иодида цезия является метод Киропулоса [6], позволяющий получить цилиндрические слитки массой в несколько десятков килограммов. Качество сцинтилляционных детекторов, полученных из такого материала, существенно зависит от примесного состава исходного компонента. Требования, предъявляемые к чистоте CsI, обусловлены областью его применения.
Другой перспективной областью применения поликристаллического иодида цезия являются перовскитовые солнечные элементы состава CsPbI3 [7, 8] и CsSnI3 [9, 10], охарактеризованные (до 23%) [11] коэффициентом полезного действия и достаточно низкой стоимостью фотоэлементов. Неорганические галогенидные перовскиты, которые поглощают свет в солнечных элементах, обладают улучшенными оптоэлектрическими свойствами, такими как высокий коэффициент поглощения, низкая энергия связи, высокая длина пробега и подвижность носителей заряда, а также требуемый размер запрещенной зоны.
Требования, предъявляемые к чистоте CsI, обусловлены областью его применения. Следует отметить, что при получении особо чистых веществ на финишных стадиях глубокой очистки, как правило, используются физико-химические методы, позволяющие удалить лимитируемые примеси элементов, близкие по свойствам к основному веществу. Для водорастворимых веществ с сильной зависимостью растворимости от температуры на завершающих операциях, как правило, используют высокотемпературную дистилляцию или ректификацию [12]. Ионы Na+ и K+ изоморфны ионам Cs+, поэтому для окончательной очистки иодида цезия двукратная высокотемпературная дистилляция оказывается перспективной.
Промежуточной стадией подготовки материалов для глубокой очистки высокотемпературными методами является вакуумная сушка [13]. Однако процесс сушки иодида цезия недостаточно описан в литературе.
Целью работы является исследование возможности получения особо чистого иодида цезия по схеме: синтез технического продукта с последующей вакуумной сушкой и вакуумной дистилляцией.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез иодида цезия. Технический CsI получали растворением карбоната цезия в иодистоводородной кислоте по реакции
(1)
${\text{C}}{{{\text{s}}}_{2}}{\text{C}}{{{\text{O}}}_{3}} + 2{\text{HI}} \to 2{\text{CsI}} + {{{\text{H}}}_{{\text{2}}}}{\text{O}} + {\text{C}}{{{\text{O}}}_{2}}{\kern 1pt} \uparrow ~$при комнатной температуре в сосуде из ниобия, который инертен к взаимодействию с иодидом цезия при повышенной температуре. Использовали Cs2CO3 квалификации “х. ч.” и HI “ч.”. Для полного растворения карбоната цезия раствор нагревали, кипения, рН 3, поскольку сосуд из ниобия не устойчив в кислой среде. Горячий раствор фильтровали, упаривали при температуре около 393 K, подвергали кристаллизации, затем проводили вакуумную сушку в кварцевой ампуле.
Процесс сушки изучали термогравиметрическим методом в температурном интервале 293–493 К при скорости нагревания 2 К/мин. В изотермических условиях процесс сушки изучали путем выдержки порошков при различных температурах до постоянной массы.
Получение особо чистого иодида цезия. После вакуумной сушки иодид цезия помещали в кварцевую ампулу для высокотемпературной дистилляции в вакууме. Процесс перегонки осуществляли в условиях равновесия системы жидкость–пар. Температура горячей зоны составляла 1073 K, холодной зоны – 895 K, давление в ампуле поддерживалось ~10–3 Торр. Загрузку в ампулу проводили в условиях, исключающих контакт продукта с окружающей атмосферой.
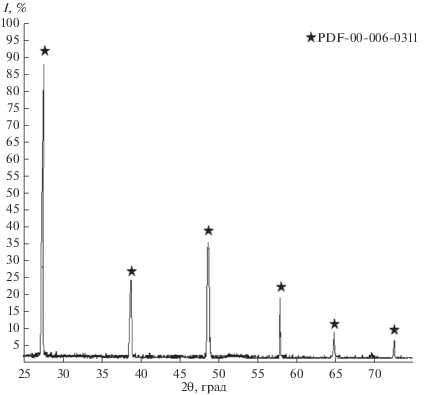
Методы исследования. Рентгенограммы образцов были получены при комнатной температуре с использованием дифрактометра Bruker D8 Advance (CuKα-излучение, Ni-фильтр и детектор LYNXEYE). Данные дифракции были собраны в диапазоне 2θ от 25° до 75° с шагом 0.01°. Идентификацию фазового состава образцов осуществляли с использованием программы Diffrac.eva и банка дифракционных данных картотеки ICDD-PDF 2.
Примесный состав определяли методом масс-спектрометрии с индуктивно связанной плазмой на спектрометре iCAP 6300 Duo (Thermo).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Для оценки кинетических параметров сушки использовалось дифференциальное уравнение с обобщенным коэффициентом диффузии
(1)
$\frac{{\partial x}}{{\partial \tau }} = {{D}_{r}}\left( {\frac{{{{\partial }^{2}}x}}{{\partial {{r}^{2}}}} + \frac{2}{r}\frac{{\partial x}}{{\partial \tau }}} \right)$с заданными граничными условиями
х(r = R) = xp; ∂x/∂r(r =0) = 0; x(r =0)= x0, где x, x0 и xр – текущее, начальное и равновесное влагосодержание соответственно; r ‒ текущая координата по радиусу; R – радиус частицы; τ – время; D – обобщенный коэффициент диффузии воды в порах [14].
Предполагалось, что влага сосредоточена на внутренней поверхности закрытых пор. Принимали, что в момент времени τ = τкр при равномерном увлажнении частиц влагосодержание x = xкр.
Аналитическое решение уравнения для среднего по радиусу влагосодержания имеет вид
(2)
$\begin{gathered} x = {{x}_{{\text{p}}}} + ({{x}_{{\text{p}}}} - {{x}_{0}}) \times \\ \times \,\,\frac{2}{\pi }\sum\limits_{n = 1}^\infty {\frac{{{{{( - 1)}}^{n}}}}{n}Si(\pi n)\exp \left( { - \frac{{{{D}_{r}}{{\pi }^{2}}}}{{{{R}^{2}}}}{{n}^{2}}\tau } \right)} . \\ \end{gathered} $Приведенный коэффициент диффузии D воды в порах выражается через обобщенный коэффициент диффузии
(3)
$D = \frac{{{{D}_{r}}{{\pi }^{2}}}}{{{{R}^{2}}}} = {{D}_{0}}\exp \left( {\frac{{\Delta H}}{{RT}}} \right),$Рис. 1.
Зависимости равновесного влагосодержания от температуры иодида цезия: 1 – расчет, 2 – эксперимент.
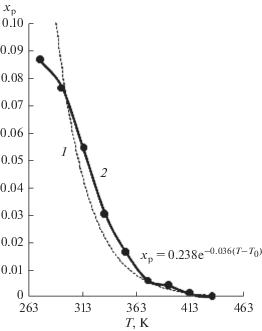
В результате обработки экспериментальных данных была построена зависимость равновесного влагосодержания от температуры иодида цезия, полученная в процессе его вакуумной сушки. Показано, что при линейном повышении температуры кривая влагосодержания описывается экспоненциальной зависимостью. С помощью уравнения (4) по методу наименьших квадратов были получены параметры равновесного влагосодержания xp и константа kp. Таким образом, теоретическое уравнение, описывающее зависимость равновесного влагосодержания иодида цезия от температуры описывается уравнением (5) (рис. 1, кривая 1).
Экспериментальные данные приведены на кривой 2. Стандартное отклонение расчетных и экспериментальных данных Sx = 0.02. С учетом дисперсии воспроизводимости по критерию Фишера для интервала значимости 0.05 установлено соответствие расчетов эксперименту.
На основании математических уравнений, описывающих процесс вакуумной сушки иодида цезия, были рассчитаны значения кинетических констант и продолжительность процесса сушки для различных температур. Данные представлены в табл. 1. Экспоненциальная зависимость D от температуры является выражением того, что диффузия происходит вследствие термически активированного движения атомов, которое всегда описывается экспонентой: ${{e}^{{ - \,\frac{q}{{kT}}}}},$ где q – энергия активации элементарного акта перемещения атома. Энергию активации можно оценить по наклону линии, описывающей зависимость в координатах lnD от Т–1. Рассчитанный коэффициент диффузии позволяет масштабировать и прогнозировать условия для промышленного производства иодида цезия.
Таблица 1.
Кинетические константы и длительность процесса сушки иодида цезия при различных температурах
| Т, К | D, м2/с | τ, с |
|---|---|---|
| 343 | 2.18 × 10–3 | 2580 |
| 363 | 5.21 × 10–3 | 1140 |
| 373 | 8.82 × 10–3 | 840 |
| 443 | 3.93 × 10–2 | 180 |
После вакуумной сушки иодида цезия была проведена высокотемпературная дистилляция в условиях равновесия системы жидкость–пар при температурах горячей зоны 1073 K и холодной зоны 895 K, давление в ампуле поддерживалось ~10–3 Торр. Данный метод очистки позволяет избавиться от большинства основных примесей, в том числе щелочных металлов, которые могут переходить в основную фракцию в виде летучих иодидов.
Полученные образцы CsI охарактеризованы методом РФА (рис. 2), результаты которого подтверждает химическую чистоту полученного образца CsI.
После очистки образцы иодида цезия были проанализированы на спектрометре с индуктивно связанной плазмой. В табл. 2 приведены данные по содержанию основных примесей в исходном карбонате цезия и в полученном иодиде цезия после комплексной очистки вакуумной сушкой и высокотемпературной дистилляцией. Трудноудаляемые примеси, которые находятся в форме оксидов или иодидов металлов, концентрируются в кубовом остатке в дистилляционной ампуле. Таким образом, полученные образцы отвечают квалификации “ос. ч.” с содержанием основного компонента 99.998 мас. %. Переход примесей из конструкционного материала не наблюдался.
Таблица 2.
Результаты определения примесного состава образцов иодида цезия
| Примесь | Содержание примесей в Cs2CO3, ppm |
Содержание примесей в CsI после дистилляции, ppm |
|---|---|---|
| Al | 8 | 0.1 |
| Cl | 10 | 3 |
| Br | 12 | 0.1 |
| Ca | 15 | <0.01 |
| F | 10 | <0.01 |
| Fe | 1 | 0.07 |
| K | 100 | 10 |
| Li | 90 | 0.01 |
| Mg | 5 | 0.1 |
| Na | 20 | 4 |
| Pb | 1 | <0.2 |
| Rb | 1000 | 0.8 |
| Ti | 20 | 0.6 |
| Sr | 10 | 0.4 |
ЗАКЛЮЧЕНИЕ
Изучен процесс получения иодида цезия квалификации “ос. ч.” (99.998 мас. % основного компонента) и оптимизированы режимы его синтеза. Рассчитаны кинетические константы вакуумной сушки, с помощью которых построена зависимость влагосодержания от температуры, что позволило скорректировать режимы вакуумной сушки и очистки методом высокотемпературной дистилляции. Полученные образцы охарактеризованы методом масс-спектрометрии с индуктивно связанной плазмой и РФА. Показано, что комбинация вакуумной сушки и высокотемпературной дистилляции позволяет получить иодид цезия высокой чистоты с содержанием примесей металлов <10–3%.
Список литературы
Schotanus P., Kamermans R. Scintillation Characteristics of Pure and Tl-Doped CsI Crystals // IEEE Trans. Nucl. Sci. 1990. V. 37. № 2. P. 177–182.https://doi.org/10.1109/23.106614
Mengesha W., Taulbee T.D., Rooney B.D., Valentine J.D. Light Yield Nonproportionality of CsI (Tl), CsI (Na), and YAP // IEEE Trans. Nucl. Sci. 1998. V. 45. № 3. P. 456–461. https://doi.org/10.1109/23.682426
Collar J.I., Fields N.E., Hai M., Hossbach T.W., Orrell J.L., Overman C.T., Perumpilly G., Scholz B. Coherent Neutrino-Nucleus Scattering Detection with a CsI [Na] Scintillator at the SNS Spallation Source // Nucl. Instrum. Methods Phys. Res., Sect. A. 2015. V. 773. P. 56–65. https://doi.org/10.1016/j.nima.2014.11.037
Yang Z., Lucas P. Tellurium-Based Far-Infrared Transmitting Glasses // J. Am. Ceram. Soc. 2009. V. 92. № 12. P. 2920–2923. https://doi.org/10.1111/j.1551-2916.2009.03323.x
Xu Y., Yang G., Wang W., Zeng H., Zhang X., Chen G. Formation and Properties of the Novel GeSe2–In2Se3–CsI Chalcohalide Glasses // J. Am. Ceram. Soc. 2008. V. 91. № 3. P. 902–905. https://doi.org/10.1111/j.1551-2916.2007.02194.x
Zaslavsky B.G. Distinctive Features of Automated Pulling of Large Scintillation Alkali Iodides Single Crystals without Oxygen-Containing Impurities // J. Cryst. Growth. 2000. V. 218. № 2–4. P. 277–281. https://doi.org/10.1016/S0022-0248(00)00525-X
Luo P., Xia W., Zhou S., Sun L., Cheng J., Xu C., Lu Y. Solvent Engineering for Ambient-Air-Processed, Phase-Stable CsPbI3 in Perovskite Solar Cells // J. Phys. Chem. Lett. 2016. V. 7. № 18. P. 3603–3608. https://doi.org/10.1021/acs.jpclett.6b01576
Ahmad W., Khan J., Niu G., Tang J. Inorganic CsPbI3 Perovskite-Based Solar Cells: A Choice for a Tandem Device // Solar RRL. 2017. V. 1. № 7. P. 1700048. https://doi.org/10.1002/solr.201700048
Chen Z., Wang J.J., Ren Y., Yu C., Shum K. Schottky solar cells based on CsSnI3 thin-films // Appl. Phys. Lett. 2012. V. 101. № 9. P. 093901. https://doi.org/10.1063/1.4748888
Shum K., Chen Z., Qureshi J., Yu C., Wang J. J., Pfenninger W., Vockic N., Midgley J., Kenney J.T. Synthesis and Characterization of CsSnI3 Thin Films // Appl. Phys. Lett. 2010. V. 96. № 22. P. 221903. https://doi.org/10.1063/1.3442511
Wu B., Zhou Y., Xing G., Xu Q., Garces H.F., Solanki A., Goh W.T., Padture N.P., Sum T.C. Long Minority-Carrier Diffusion Length and Low Surface-Recombination Velocity in Inorganic Lead-Free CsSnI3 Perovskite Crystal for Solar Cells // Adv. Funct. Mater. V. 27. № 7. P. 1604818. https://doi.org/10.1002/adfm.201604818
Бреховских М.Н., Мастрюков М.В., Корнев П.В., Гасанов А.А., Коваленко А.Э., Федоров В.А. Синтез и глубокая очистка дииодида олова // Неорган. материалы. 2019. Т. 55. № 9. С. 1029–1032. https://doi.org/10.1134/S0002337X1909001X
Семенов Г.В., Буданцев Е.В., Меламед Л.Э., Тропкина К.И. Математическое моделирование и экспериментальное исследование совмещенных циклов вакуумной сушки термолабильных материалов // Вестн. Междунар. академии холода. 2011. № 4. С. 5–11.
Попов П.В. Диффузия: учебно-методическое пособие по курсу Общая физика. М.: МФТИ, 2016. 94 с.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы