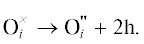Неорганические материалы, 2020, T. 56, № 10, стр. 1074-1080
Трансформация кристаллической структуры наноразмерных пленок палладия в процессе термического оксидирования
А. М. Самойлов 1, *, С. А. Ивков 1, Д. И. Пелипенко 1, М. К. Шаров 1, В. О. Цыганова 1, Б. Л. Агапов 2, Е. А. Тутов 3, Petre Badica 4
1 Воронежский государственный университет
394018 Воронеж, Университетская пл., 1, Россия
2 АО “Научно-исследовательский институт электронной техники”
394033 Воронеж, ул. Старых Большевиков, 5, Россия
3 Воронежский государственный технический университет
394026 Воронеж, Московский пр., 14, Россия
4 National Institute of Materials Physics
077125 Magurele, street Atomistilor, 405A, Romania
* E-mail: samoylov@chem.vsu.ru
Поступила в редакцию 03.05.2019
После доработки 12.05.2020
Принята к публикации 18.05.2020
Аннотация
Нанокристаллические пленки PdO изучены методами рентгеновской дифракции, растровой электронной микроскопии и локального рентгеноспектрального анализа. Установлено, что в процессе термооксидирования в атмосфере O2 нанокристаллические пленки Pd толщиной ~35 нм на подложках SiO2/Si(100) претерпевают цикл фазовых превращений с образованием PdO и его последующим разложением до исходного Pd при T > 1120 К. При этом в интервале T = 670–970 К значения параметров a и c тетрагональной решетки нанокристаллических пленок PdO монотонно увеличиваются с ростом температуры. На основании экспериментальных и литературных данных представлена модель элементарной ячейки кристаллической структуры оксида палладия(II). В рамках квазихимического подхода предложена модель, объясняющая увеличение параметров тетрагональной кристаллической решетки и p-типа проводимости нанокристаллических пленок PdO за счет образования избыточных атомов кислорода в междоузлиях.
ВВЕДЕНИЕ
Газовые сенсоры, в том числе портативные приборы индивидуального назначения, позволяют предотвратить технологические и бытовые инциденты с взрывоопасными газами, а также необходимы для систем безопасности в различных индустриальных процессах, использующих токсичные и легко воспламеняющиеся летучие вещества [1–3]. На протяжении полувека металлоксидные полупроводники находят применение в газовых сенсорах различного типа [1, 4–6]. В настоящее время функциональные свойства металлоксидных полупроводников с p-типом проводимости, таких как Cr2O3, Cu2O, PdO и др., исследованы фрагментарно, несмотря на то что эти материалы обладают большим потенциалом при их использовании в газовых сенсорах [5, 6].
Газочувствительные свойства наноструктур на основе оксида палладия(II), который характеризуется p-типом проводимости [7, 8], исследуют относительно недавно. Эксперименты показали, что сенсоры на основе наноструктур PdO различной морфологической организации обладают высокой чувствительностью, стабильностью сенсорного отклика, коротким периодом восстановления, а также хорошей воспроизводимостью сигнала датчика при детектировании в атмосферном воздухе водорода, угарного газа, паров органических соединений, оксида азота(IV) и озона [7–13].
Как известно, фазовая диаграмма системы палладий−кислород изучена недостаточно, область нестехиометрии PdO не определена, а относительно природы точечных дефектов, ответственных за p-тип проводимости, в литературе высказываются противоречивые мнения [14–16].
Целью настоящей работы является изучение характера фазовых превращений в процессе оксидирования в кислороде наноразмерных пленок Pd и трансформации кристаллической структуры веществ, образующихся в процессе оксидирования, а также уточнение гипотезы о природе точечных дефектов в PdO, ответственных за p-тип проводимости.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Использованная в настоящей работе методика формирования ультрамикродисперсных пленок металлического Pd (рис. 1а) подробно описана в предыдущих работах [7, 8, 11, 12]. Исходные пленки Pd толщиной ∼35 нм были получены методом термической сублимации палладиевой фольги с чистотой 99.99% в высоком вакууме (остаточное давление ∼10−5 Па) на подложках Si(100) с буферным слоем SiO2 толщиной d ∼ 300 нм без нагревания.
Рис. 1.
РЭМ-изображения поверхности гетероструктур до и после термооксидирования в атмосфере O2: а – гетероструктура Pd/SiO2/Si до термооксидирования; б, в – гетероструктуры PdO/SiO2/Si после оксидирования при Tox = 870 и 1070 К соответственно; г – Pd/SiO2/Si, Tox = 1148 К.

Исходные гетероструктуры Pd/SiO2/Si(100) отжигали в атмосфере сухого кислорода при давлении p(O2) ∼ 1.1 × 105 Па в проточном режиме с расходом 5 дм3/ч [9, 12, 14]. В течение 2 ч гетероструктуры Pd/SiO2/Si(100) выдерживали при температуре Tox = 510, 570, 670, 770, 870, 1070, 1120 и 1145 К и далее охлаждали до комнатной температуры в токе кислорода.
Изменение морфологии поверхности гетероструктур Pd/SiO2/Si(100) в процессе термооксидирования в атмосфере O2 изучали методом растровой электронной микроскопии (РЭМ) с использованием прибора JEOL JCM 6380 LV при кратности увеличения от ×2000 до ×150 000.
Фазовый состав и кристаллическую структуру пленок PdO, синтезированных в результате термооксидирования гетероструктур Pd/SiO2/Si(100), характеризовали методом рентгеновской дифрактометрии на приборах ДРОН-4-07 и Philips PANanalitical X’Pert с использованием CuKα- и CoKα-излучения. Дифрактограммы записывали с вращением образцов, а профили рентгеновских рефлексов строили по точкам при движении счетчика ступенями с шагом 0.01°. Четко фиксируемый рефлекс 400 подложки Si(100) служил внутренним эталоном для предотвращения случайных погрешностей.
Прецизионное определение периода кубической кристаллической решетки пленок Pd, а также параметров тетрагональной решетки PdO проводили путем экстраполяции угла дифракции к 2θ = 180° при помощи функции Нельсона–Райли. Индицирование рентгеновских рефлексов подложки Si(100), а также пленок Pd и PdO проводили на основе международной базы кристаллографических данных [17].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В предыдущих работах методами рентгенофазового анализа (РФА) и дифракции быстрых электронов были определены граничные условия процесса синтеза поликристаллических однофазных пленок PdO для последующего изучения их сенсорных свойств [8, 11, 12]. Было установлено, что оксидированием в O2 в интервале температур Tox = 770−970 К можно синтезировать гомогенные нанокристаллические пленки PdO. Однако на дифрактограммах пленок, полученных при Tox = 1070 К, были обнаружены три слабых рефлекса, которые нельзя отнести к кристаллической структуре PdO [8]. С одинаковой вероятностью и погрешностью эти пики соответствовали либо фазе Pd3.5O4 [17], либо силициду палладия Pd2Si [18].
В настоящей работе экспериментально установлен характер количественных изменений параметров тетрагональной кристаллической решетки пленок PdO, синтезированных в тех же условиях [8, 11, 12]. Единственное различие заключается в использовании подложек Si(100) с буферным слоем SiO2 толщиной 300 нм в целях предотвращения вероятного взаимодействия Pd и Si с образованием силицидов палладия.
Рентгенограммы исходных гетероструктур Pd/SiO2/Si(100), а также образцов, полученных их оксидированием в атмосфере O2 в интервале Tox = = 510−1145 K, показаны на рис. 2. Вследствие малой толщины пленок Pd и PdO значения интенсивностей рентгеновских рефлексов представлены в логарифмической шкале, поскольку интенсивность пика Si 400 практически на три порядка величины превышает интенсивность пиков Pd и PdO (рис. 2). Согласно полученным рентгеновским данным, формирование однородных поликристаллических пленок PdO в результате оксидирования исходных слоев Pd на подложках Si(100) с буферным слоем SiO2 толщиной ∼300 нм реализуется в интервале температур Tox = = 570−1070 K (рис. 2). Этот факт противоречит опубликованным ранее данным [8], полученным при исследовании пленок PdO на подложках Si(100) с более тонким слоем SiO2. Очевидно, что буферный слой SiO2 толщиной 300 нм воспрепятствовал взаимодействию Pd и Si с образованием силицида Pd2Si.
Рис. 2.
Штрих-диаграммы гетероструктур до и после термооксидирования в атмосфере O2: а – Pd/SiO2/Si, оксидирование при Tox = 510 К; б – (Pd + PdO)/SiO2/Si, Tox = 570 К; в – PdO/SiO2/Si, Tox = 870 К; г – PdO/SiO2/Si, Tox = 1070 К; д – (Pd + PdO)/SiO2/Si, Tox = 1120 К; е – Pd/SiO2/Si, Tox = 1148 К (излучение CuKα).
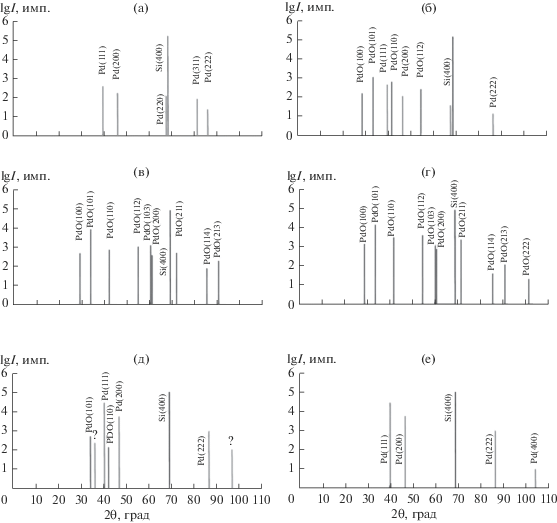
Как показано на рис. 2б–2г, с ростом температуры оксидирования наблюдается увеличение интенсивности рентгеновских пиков PdO, а также фиксируются рефлексы на дальних углах дифракции 2θ > 75°. Это свидетельствует о повышении степени структурного совершенства нанокристаллических пленок PdO. На рис. 2д видно, что при Tox = 1120 К образуются гетерогенные пленки, состоящие из трех фаз: PdO, Pd и, возможно, Pd2O. На дифрактограммах зафиксировано наличие рефлексов 101 и 110 PdO, интенсивность которых заметно ниже, чем у однофазных образцов PdO, полученных оксидированием при Tox = 1070 К. Присутствие металлического Pd установлено по интенсивным пикам 111, 200 и 222. Кроме того, обнаружены два пика относительно небольшой интенсивности, которые можно приписать оксиду Pd2O, образование которого было установлено ранее в результате оксидирования Pd при низком парциальном давлении O2 [19].
Как показано в табл. 1, процесс термооксидирования исходных нанокристаллических ультрамикродисперсных пленок Pd сопровождается фазовыми переходами от Pd к PdO (Tox ≥ 570 К) и от PdO через гетерогенные образцы (вероятно, PdO + Pd + Pd2O) к металлическому Pd при Tox > > 1120 К.
Таблица 1.
Фазовые превращения нанокристаллических пленок палладия в процессе оксидирования в атмосфере O2 в интервале температур Tox = 510−1145 К
| Tox, К | Фазовое состояние образцов | Фазовый состав пленок |
|---|---|---|
| 295−510 | Однофазные | Pd |
| 570 | Гетерогенные | Pd + PdO |
| 670−1070 | Однофазные | PdO |
| 1120 | Гетерогенные | Pd + PdO + Pd2O* |
| 1145 | Однофазные | Pd |
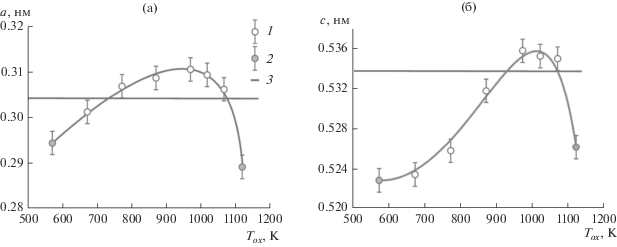
На основании полученных данных РФА рассчитаны значения параметров a и c тетрагональной кристаллической решетки нанокристаллических пленок PdO для различных Tox (рис. 3). Зависимости a = f(Tox) и c = f(Tox) для нанокристаллических пленок PdO характеризуются сходным поведением: значения обоих параметров монотонно возрастают с ростом температуры до Tox = 970 К. Для интервала температур Tox = 770–1070 K значения постоянной решетки a выше, чем эталонное значение ASTM (рис. 3а). Интервал температур оксидирования, при котором значения параметра c выше эталонных значений ASTM [21], существенно ýже: от Tox = 870 К до Tox = 1070 K (рис. 3б). PdO, содержащийся в гетерогенных пленках, полученных при Tox = 1120 K (рис. 2д), характеризуется минимальными значениями параметров тетрагональной решетки. Эти данные свидетельствуют о том, что термическое разложение пленок PdO при Tox ≥ 1120 К сопровождается резким уменьшением значений a и c, что можно объяснить удалением атомов O из кристаллической структуры PdO.
Рис. 3.
Зависимости параметров a и c тетрагональной решетки нанокристаллических пленок PdO от температуры оксидирования: 1 − однофазные пленки PdO, 2 − гетерофазные пленки PdO + Pd; 3 − данные [21].
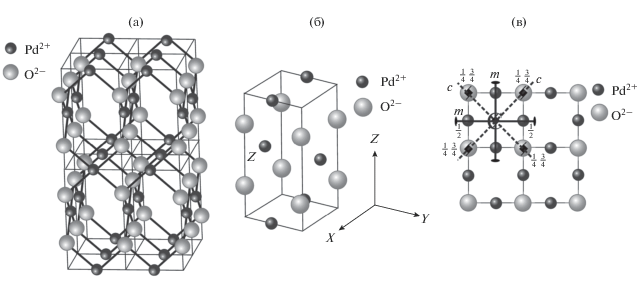
На основании полученных экспериментальных результатов и литературных данных [20–22] в настоящей работе предложен вариант элементарной ячейки кристаллической структуры оксида палладия(II), который полностью соответствует набору элементов симметрии пр. гр. ${{P{{4}_{2}}} \mathord{\left/ {\vphantom {{P{{4}_{2}}} {mmc}}} \right. \kern-0em} {mmc}},$ символу Пирсона tP4, позициям Уайкоффа атомов Pd и O, а также их кратности (рис. 4).
Рис. 4.
Кристаллическая структура (а), элементарная ячейка (б) и проекция четырех элементарных ячеек на плоскость XOY (в) с указанием элементов симметрии, характерных для пр. гр. ${{P{{4}_{2}}} \mathord{\left/ {\vphantom {{P{{4}_{2}}} {mmc}}} \right. \kern-0em} {mmc}}.$
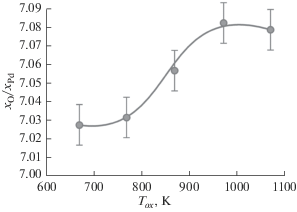
Методом локального рентгеноспектрального анализа изучен интегральный количественный состав гетероструктур PdO/SiO2/Si(100). Несмотря на наличие систематической погрешности эксперимента, имеет смысл сопоставить значения мольной доли атомов кислорода xO в гетероструктурах PdO/SiO2/Si(100) в зависимости от условий термооксидирования. На рис. 5 представлена температурная зависимость отношения мольных долей атомов кислорода и палладия ${{{{x}_{{\text{O}}}}} \mathord{\left/ {\vphantom {{{{x}_{{\text{O}}}}} {{{x}_{{{\text{Pd}}}}}}}} \right. \kern-0em} {{{x}_{{{\text{Pd}}}}}}}$ в гетероструктурах PdO/SiO2/Si(100). Установлено, что отношение ${{{{x}_{{\text{O}}}}} \mathord{\left/ {\vphantom {{{{x}_{{\text{O}}}}} {{{x}_{{{\text{Pd}}}}}}}} \right. \kern-0em} {{{x}_{{{\text{Pd}}}}}}}$ увеличивается с ростом температуры оксидирования в интервале Tox = 670−970 К, а при дальнейшем повышении температуры до Tox = = 1070 К наблюдается незначительно снижение величины ${{{{x}_{{\text{O}}}}} \mathord{\left/ {\vphantom {{{{x}_{{\text{O}}}}} {{{x}_{{{\text{Pd}}}}}}}} \right. \kern-0em} {{{x}_{{{\text{Pd}}}}}}}{\kern 1pt} .$
Рис. 5.
Зависимость отношения мольных долей атомов кислорода и палладия в гетероструктурах PdO/SiO2/Si(100) от температуры оксидирования.
Полученные экспериментальные данные позволяют предположить, что основной причиной увеличения параметров a и c решетки нанокристаллических пленок PdO (рис. 3) при оксидировании в атмосфере O2 в интервале температур Tox = 670−970 К является встраивание атомов O в кристаллическую структуру PdO. Это подтверждает увеличение содержания атомов O в гетероструктурах PdO/SiO2/Si(100) (рис. 5). Буферный слой SiO2 толщиной ∼300 нм является преградой для диффузии атомов O к поверхности раздела SiO2/Si подложки и не может быть подвержен дальнейшему оксидированию, поскольку SiO2 характеризуется практически нулевой шириной области гомогенности. Единственным объяснением увеличения концентрации атомов O (рис. 5) в гетероструктурах PdO/SiO2/Si(100) следует признать только насыщение атомами кислорода структуры PdO. Встраивание атомов O в структуру PdO может осуществляться по семейству кристаллографических плоскостей {001} и {002}, сформированных атомами Pd, которые способны образовать дополнительные связи с атомами O, в результате чего увеличивается координационное число от 4 до 6 и изменяется координационный многогранник от квадрата до октаэдра (рис. 4). Следствием такого встраивания атомов O по плоскостям {001} и {002} является увеличение параметра a кристаллической решетки PdO. Уменьшение значений параметров a и c тетрагональной решетки пленок PdO при Tox > 1070 К (рис. 3) может быть обусловлено ретроградным характером линии солидус, ограничивающей область гомогенности оксида палладия(II) справа. Термическое разложение пленок PdO, подтвержденное результатами РФА при Tox ≥ 1120 К (рис. 2д, 2е), протекает по перитектической реакции с образованием Pd и O2.
Предложенная модель позволяет объяснить не только трансформацию решетки PdO в процессе оксидирования, но и p-тип проводимости пленок PdO. В рамках квазихимического подхода [23] оксидирование Pd в атмосфере O2 можно представить в виде следующих реакций:
образование оксида палладия(II) при взаимодействии Pd и O2
(1)
${\text{Pd}} + \frac{1}{2}{{{\text{O}}}_{{\text{2}}}} \to {\text{Pd}}_{{{\text{Pd}}}}^{ \times } + {\text{O}}_{{\text{O}}}^{ \times }{\text{ ,}}$образование атомов кислорода в междоузлиях ${\text{O}}_{i}^{ \times }{\text{ }}$ при взаимодействии PdO с O2 при высокой температуре
(2)
${\text{Pd}}_{{{\text{Pd}}}}^{ \times } + {\text{O}}_{{\text{O}}}^{ \times } + \frac{1}{2}{{{\text{O}}}_{{\text{2}}}}^{{{\text{(}}G{\text{)}}}} \to {\text{Pd}}_{{{\text{Pd}}}}^{ \times } + {\text{O}}_{{\text{O}}}^{ \times } + {\text{O}}_{i}^{ \times }{\text{,}}$ионизация нейтральных атомов O в междоузлиях с образованием дырок
ЗАКЛЮЧЕНИЕ
Методами РФА и РЭМ установлено, что в процессе оксидирования в атмосфере O2 нанокристаллические пленки Pd претерпевают цикл фазовых превращений с образованием PdO и его последующим разложением до металлического Pd при T ≥ 1120 К.
Методом РФА установлено, что термооксидирование в атмосфере O2 в интервале Tox = 670–970 К приводит к монотонному увеличению параметров a и c тетрагональной решетки нанокристаллических пленок PdO с ростом температуры.
Увеличение параметров тетрагональной кристаллической решетки нанокристаллических пленок PdO объяснено в рамках квазихимического подхода за счет образования избыточных атомов кислорода в междоузлиях по кристаллографическим плоскостям {001} и {002}.
Список литературы
Yamazoe N. Toward Innovations of Gas Sensor Technology // Sens. Actuators, B. 2005. V. 108. P. 2–14.
Fine G.F., Cavanagh L.M., Afonja A., Binions R. Metal Oxide Semiconductor Gas Sensors in Environmental Monitoring // Sensors. 2010. V. 10. P. 5469–5502.
Hulanicki A., Geab S., Ingman F. Chemical Sensors Definitions and Classification // Pure and Appl. Chem. 1991. V. 63. № 9. P. 1247–1250.
Marikutsa A.V., Rumyantseva M.N., Gaskov A.M., Samoylov A.M. Nanocrystalline Tin Dioxide: Basics in Relation with Gas Sensing Phenomena. Part I. Physical and Chemical Properties and Sensor Signal Formation // Inorg. Mater. 2015. V. 51. № 13. P. 1329–1347.
Korotcenkov G., Brinzari V., Cho B.K. In2O3- and SnO2-Based Thin Film Ozone Sensors: Fundamentals // J. Sens. 2016. Article ID 3816094. 31 p. https://doi.org/10.1155/2016/3816094
Hyo-Joong Kim, Jong-Heun Lee. Highly Sensitive and Selective Gas Sensors Using p-type Oxide Semiconductors: Overview // Sens. Actuators, B. 2014. V. 192. P. 607–627.
Samoylov A.M., Ryabtsev S.V., Popov V.N., Badica P. Palladium(II) Oxide Nanostructures as Promising Materials for Gas Sensors // Novel Nanomaterials Synthesis and Applications / Ed. George Kyzas. L.: IntechOpen Publishing House, 2018. P. 211–229.
Ryabtsev S.V., Ievlev V.M., Samoylov A.M., Kuschev S.B., Soldatenko S.A. Microstructure and Electrical Properties of Palladium Oxide Thin Films for Oxidizing Gases Detection // Thin Solid Films. 2017. V. 636. P. 751–759.
Chiang Yu-Ju, Pan Fu-Ming. PdO Nanoflake Thin Films for CO Gas Sensing at Low Temperatures // J. Phys. Chem. C. 2013. V. 117. P. 15593–15601.
Yangong Zheng, Qiao Qiao, Jing Wang, Xiaogan Li, Jiawen Jian. Gas Sensing Behavior of Palladium Oxide for Carbon Monoxide at Low Working Temperature // Sens. Actuators, B. 2015. V. 212. P. 256–263.
Рябцев С.В., Шапошник А.В., Самойлов А.М., Синельников А.А., Солдатенко С.А., Кущев С.Б., Иевлев В.М. Тонкие пленки оксида палладия для газовых сенсоров // Докл. Академии наук. Cер. Физ. химия. 2016. Т. 470. № 5. С. 550–553.
Ievlev V.M., Ryabtsev S.V., Shaposhnik A.V., Samoylov A.M., Kuschev S.B., Sinelnikov A.A. Ultrathin Films of Palladium Oxide for Oxidizing Gases Detecting // Proc. Eng. 2016. V. 168. P. 1106–1109.
Kushchev S.B., Ryabtsev S.V., Soldatenko S.A., Sinel’nikov A.A., Dontsov A.I., Maksimenko A.A., Turaeva T.L. On the Synthesis of PdO–RuO2 Solid-Solution Thin Films by Thermal Oxidation and Investigation of Their Gas-Sensing Properties // J. Surf. Invest.: X-ray, Synchrotron Neutron Tech. 2019. V. 13. P. 87–91.
Ievlev V.M., Ryabtsev S.V., Samoylov A.M., Shaposhnik A.V., Kuschev S.B., Sinelnikov A.A. Thin and Ultrathin Films of Palladium Oxide for Oxidizing Gases Detection // Sens. Actuators, B. 2018. V. 255. № 2. P. 1335–1342.
García-Serrano O., Andraca-Adame A., Baca-Arroyo R., Peña-Sierra R., Romero-Paredes G.R. Thermal Oxidation of Ultra Thin Palladium (Pd) Foils at Room Conditions // Proc. Electrical Engineering Computing Science and Automatic Control (CCE) 8th Int. Conf. Merida. 2011. P. 456−460.
ASTM JCPDS – International Centre for Diffraction Data. © 1987–2009. JCPDS-ICDD. Newtown Square, PA 19073. USA.
Meyer H.-J., Müller-Buschbaum Hk. Ein Beitrag zur Chemie von Verbindungen des Bautyps MxPd3O4 // Z. Naturforsch. 1979. V. 84B. S. 1661–1662.
Suryana R., Nakatsuka O., Zaima S. Formation of Palladium Silicide Thin Layers on Si (110) Substrates // Jpn. J. Appl. Phys. 2011. V. 50. P. 05EA09-1–05EA09-5.
Kumar J., Saxena R. Formation of NaCl- and Cu2O-Type Oxides of Platinum and Palladium on Carbon and Alumina Support Films // J. Less-Common Met. 1989. V. 147. P. 59–71.
Иевлев В.М., Кущев С.Б., Синельников А.А., Солдатенко С.А., Рябцев С.В., Босых М.А., Самойлов А.М. Структура гетеросистем пленка SnO2–островковый конденсат металла (Ag, Au, Pd) // Неорган. материалы. 2016. Т. 52. № 7. С. 757–764.
Grier D., McCarthy G. JCPDS-ICDD, 1991. Card no. 43-1024.
Aroyo M.I., Perez-Mato J.M., Orobengoa D., Tasci E., de la Flor G., Kirov A. Crystallography Online: Bilbao Crystallographic Server // Bulg. Chem. Commun. 2011. V. 43. № 2. P. 183–197.
Kröger F.A. The Chemistry of Imperfect Crystals. Amsterdam: North-Holland, 1964. 650 p.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы