Неорганические материалы, 2020, T. 56, № 11, стр. 1237-1242
Физико-химические свойства мышьяксодержащих веществ – продуктов детоксикации люизита
Т. К. Менщикова 1, *, А. И. Варгунин 1, М. Н. Бреховских 1, В. А. Федоров 1, О. Е. Мыслицкий 1
1 Институт общей и неорганической химии им. Н.С. Курнакова Российской академии наук
119991 Москва, Ленинский пр., 31, Россия
* E-mail: fedorov@igic.ras.ru
Поступила в редакцию 16.05.2020
После доработки 07.07.2020
Принята к публикации 10.07.2020
Аннотация
Изложены результаты исследований физико-химических свойств мышьяксодержащих веществ – продуктов детоксикации (уничтожения) люизита. Основное внимание уделено изучению свойств арсенита натрия гидролизного, который является перспективным альтернативным промышленным источником производства высокочистого мышьяка и его соединений. Приведены данные по макро- и микросоставу сырья, зависимости плотности и давления насыщенного пара раствора Н3AsO4 от температуры. Экспериментальные данные можно использовать при переработке нетрадиционного сырья в особо чистые мышьяксодержащие соединения.
ВВЕДЕНИЕ
Высокочистый мышьяк и его соединения (AsCl3, As2O3, AsH3) являются основными компонентами для изготовления и производства широкого круга современных материалов и изделий на их основе для микро-, наноэлектроники, оптики, гелиоэнергетики, лазерной техники, волоконной оптики [1]. В РФ отсутствует производство высокочистого мышьяка, поэтому поиск новой альтернативной сырьевой базы приобретает важное практическое значение.
В последние 10–15 лет принципиально показано, что такими источниками могут быть:
– продукты детоксикации люизита в виде арсенита натрия гидролизного (АНГ), которых накоплено более 12 тыс. тонн;
– отходы производства цветной металлургии;
– отходы от любых полупроводниковых материалов АIIIBV.
АНГ получают путем щелочного гидролиза люизита, упаривания образующихся реакционных масс и дальнейшего их разложения и извлечения мышьяка в элементном виде или AsH3. Промежуточные вещества (AsCl3, AsH3) затем подвергают глубокой очистке, восстановлению или термическому разложению с получением элементного мышьяка особой чистоты квалификаций 6N и 7N. Технология характеризуется большим количеством образующихся токсичных As-содержащих отходов.
Значительные достижения достигнуты в утилизации отходов цветной металлургии в ценные продукты различной реактивной квалификации [2]. Так, основные компоненты АНГ разделяют химическими способами, выделяют мышьяк в виде As2O3, который подвергают комбинированной очистке с получением продукта “ос. ч.” или элементного мышьяка [3, 4]. Показано, что для разработки технологии и организации промышленного выпуска As-содержащих веществ на новой сырьевой базе (АНГ) [5] требуется проведение дополнительных физико-химических, технологических, экологических исследований, включая изучение гетерогенных равновесий в системах основное вещество–примесь, а также аппаратурные решения, выбор рациональных технологических схем [6]. Это позволит оценить и сопоставить реально достигнутый уровень процессов их очистки и корректно сравнить эффективность различных методов.
Целью работы являются изучение физико-химических свойств основных As-содержащих соединений – продуктов детоксикации люизита (АНГ), а также определение зависимостей плотности и давления насыщенного пара H3AsO4 в широком интервале температур, которые могли бы быть использованы в процессах получения особо чистых продуктов – AsH3 и элементного мышьяка.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использованы “сухие” продукты детоксикации люизита после его щелочного гидролиза и последующей сушки. Мышьяк элементный и арсин были выделены из АНГ электрохимическим способом путем растворения его в воде, электролиза в растворе с образованием Н3AsO4 и NaOH с выходом AsH3 по веществу до 90 мас. % [7]. Технический As2O3 был выделен из АНГ путем комбинации химических процессов и финишной очистки сублимационно-десублимационным методом до уровня 99.9–99.99 мас. %. Одновременно этот продукт является исходным сырьем для получения более чистого материала с применением вакуум-термической очистки в сочетании с процессами сорбции [4].
Плотность As-содержащих растворов изучали пикнометрическим методом [8], зависимость давления насыщенного пара – динамическим методом [9] с использованием двух вакуумметров: V.D. Нeijden и образцового ГОСТ-6121-60, температуру измеряли термометром wvt ГОСТ 165-590-71.
Качество мышьяксодержащих веществ контролировали с помощью химико-спектрального, газохроматографического, масс-спектрометрического и хромато-масс-спектрометрического методов анализа [1].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
С применением различных методов проведено физико-химическое исследование исходного сырья (АНГ), подлежащего переработке в продукцию квалификации “ос. ч.”.
Макро- и микросостав АНГ. Подтверждено, что АНГ [6] – сложная система, основными компонентами которой являются (мас. %):
– арсениты и арсенаты натрия 25–40%;
– хлорид натрия 40–50%;
– нерастворимые в воде вещества органической и неорганической природы 0.5–10%;
– примеси элементов ≥0.1%;
– углеводороды (СН4, С2Н6, С2Н4, С3Н8, С4Н6).
Значительные количества АНГ (более 12 тыс. тонн), высокое содержание в нем мышьяка и необходимость утилизации позволяют считать его уникальным альтернативным сырьем для производства мышьяксодержащих материалов [1].
В табл. 1 в качестве типичного примера приведено содержание примесей элементов в водном растворе исходного АНГ. Как и следовало ожидать, в нем присутствует значительное количество примесей, особенно Ca, Cr, Ni, Рb, халькогенов, Zn, концентрация которых сопоставима с качеством технического мышьяка и его оксида(III), выделяемых из отходов производства цветных металлов.
Таблица 1.
Содержание примесей в исходном АНГ и мышьяке “ос. ч.”, полученном по различным схемам
| Примесь | Содержание, мас. % | ||
|---|---|---|---|
| АНГ (104) | As (106) | ||
| хлоридный | гидридный | ||
| Al | 2.0 | 1.0 | <1.0 |
| Ca | 4.0 | 1.0 | 1.0 |
| Cu | 7.0 | 0.5 | 0.1 |
| Cr | 6.0 | 1.0 | 0.1 |
| Fe | 2.0 | 1.0 | 1.0 |
| Mg | 3.2 | 5.0 | 1.0 |
| Mn | 50.0 | 0.1 | <0.1 |
| Ni | 4.0 | 0.1 | <0.1 |
| Pb | 6 × 10 | 0.1 | 0.1 |
| S | >2 × 102 | 3.0 | 1.0 |
| Sb | 1.5 × 101 | 1.0 | 1.0 |
| Se | 15.0 | 1.0 | 1.0 |
| Bi | 8.0 | 0.1 | 0.1 |
| Si | 2.0 | 5.0 | 1.0 |
| Zn | 5.0 | 1.0 | 0.1 |
| Sn | 60 | 1.0 | 1.0 |
| Te | >2 × 102 | 5.0 | 1.0 |
Для выяснения возможности переработки АНГ в особо чистые мышьяксодержащие вещества были проведены серии экспериментов по технологическим схемам, пригодным для глубокой очистки As из природных источников по хлоридному и гидридному методам.
Хлоридная схема включает в себя извлечение элементного высокодисперсного мышьяка или As2O3, последующий синтез AsCl3, его очистку комбинированным методом и восстановление водородом “ос. ч.” [1]. Процесс отработан для продуктов квалификации 6N.
Гидридная схема характеризуется электрохимическим синтезом арсина, его глубокой очисткой ректификацией и термическим разложением [7]. При этом AsH3 “ос. ч.” является ключевым продуктом в технологии As и в процессах выращивания структур MOCVD-методом. Сравнение этих схем свидетельствует о том, что наиболее перспективным является гидридный метод, однако для его промышленного применения необходимо решить ряд аппаратурных и экологических проблем.
Для электрохимического синтеза арсина исходный АНГ предварительно растворяли в Н2О и насыщали хлороводородной кислотой, затем отгоняли воду с хлороводородом совместно с As2O3. В процессе электролиза в реакторе происходит накопление H3AsO4, а хлор и натрий удаляются из раствора. Степень извлечения мышьяка из АНГ в форме H3AsO4 составляет до 90%. Синтезировали образцы технического арсина с выходом по мышьяку до 90%, по току – 12% [10]. По результатам физико-химических исследований системы H3AsO4–H2O эти показатели можно повысить.
Как следует из данных табл. 1, As из очищенного ректификацией AsH3 по своему качеству превосходит продукт, полученный по хлоридной схеме, и отвечает квалификации 6N (суммарное содержание контролируемых примесей менее 3 × × 10–5 мас. %). Он обеспечивает выращивание высококачественных эпитаксиальных структур MOCVD-методом.
Для оптимизации электрохимического синтеза AsH3 важно знать физико-химические свойства системы H3РO4–H2O, в частности, удельную плотность и давление насыщенного пара в широком интервале температур (20–80°С).
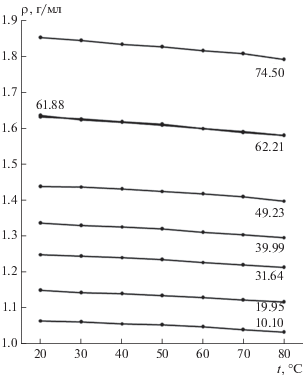
Удельная плотность. Определена плотность H3AsO4, синтезированной из элементного мышьяка “ос. ч.” и Н2О (ГОСТ 177-88) по методике [8]. Пикнометр откалиброван на дистиллированной Н2О, отклонение составляло ±0.002 г/мл, построены зависимости ρ (удельная плотность) от температуры для каждой изученной концентрации. Результаты 3–5 параллельных экспериментов приведены в табл. 2 и на рис. 1.
Таблица 2.
Удельная плотность H3AsO4 при различных температурах
| t°, C | ρ, г/мл | |||||||
|---|---|---|---|---|---|---|---|---|
| 10.10* | 19.95* | 31.64* | 39.99* | 49.23* | 61.88* | 62.21* | 74.50* | |
| 20 | 1.067 | 1.1510 | 1.2501 | 1.3367 | 1.4380 | 1.6348 | 1.6311 | 1.8499 |
| 30 | 1.064 | 1.1447 | 1.2451 | 1.3304 | 1.4373 | 1.6229 | 1.6257 | 1.8416 |
| 40 | 1.0589 | 1.1413 | 1.2421 | 1.3268 | 1.4310 | 1.6155 | 1.6165 | 1.8313 |
| 50 | 1.0555 | 1.1363 | 1.2356 | 1.3206 | 1.4252 | 1.6076 | 1.6099 | 1.8240 |
| 60 | 1.0497 | 1.1311 | 1.2285 | 1.3109 | 1.4173 | 1.5989 | 1.5985 | 1.8134 |
| 70 | 1.0425 | 1.1246 | 1.2208 | 1.3054 | 1.4092 | 1.5908 | 1.5880 | 1.8056 |
| 80 | 1.0351 | 1.1187 | 1.2147 | 1.2970 | 1.3982 | 1.5791 | 1.5793 | 1.7894 |
Эти данные можно рассматривать как справочные.
На рис. 1 показана зависимость удельной плотности от температуры для различных концентраций.
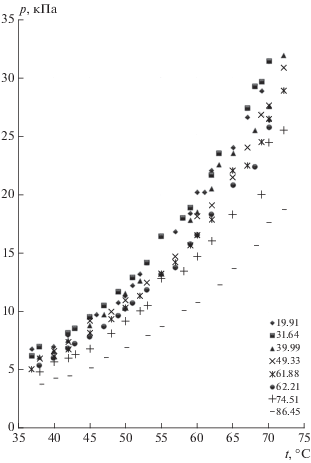
Давление насыщенного пара H3AsO4. Эксперименты по изучению давления насыщенного пара H3AsO4 выполнены динамическим методом [7] в широком интервале температур (20–85 К) и концентраций растворов кислоты. В качестве примеров на рис. 2 приведена зависимость р (кПа)–t(°C) для интервала 35–75°C. Согласно уравнению Клаузиуса–Клайперона, зависимость р = f(Т), выражается уравнением
(1)
${{{\text{d}}р} \mathord{\left/ {\vphantom {{{\text{d}}р} {{\text{d}}Т}}} \right. \kern-0em} {{\text{d}}Т}} = {{\Delta H} \mathord{\left/ {\vphantom {{\Delta H} T}} \right. \kern-0em} T}({{V}_{{\text{п}}}}--{{V}_{{\text{ж}}}}) = {{\Delta H} \mathord{\left/ {\vphantom {{\Delta H} {\Delta V}}} \right. \kern-0em} {\Delta V}},$(2)
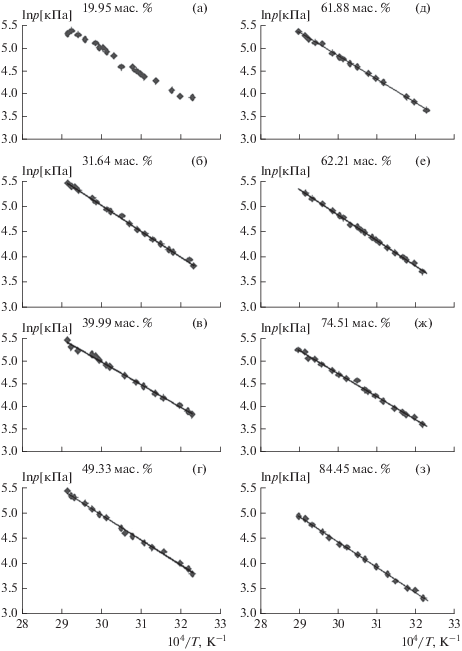
${{{\text{d}}р} \mathord{\left/ {\vphantom {{{\text{d}}р} {{\text{d}}Т}}} \right. \kern-0em} {{\text{d}}Т}} = {{--\Delta H} \mathord{\left/ {\vphantom {{--\Delta H} {R{{T}^{2}}}}} \right. \kern-0em} {R{{T}^{2}}}} + В,$На рис. 3 показаны линейные зависимости lnp от 10–4/T для изученных концентраций растворов мышьяковой кислоты. По тангенсу наклона прямых линий определены теплоты испарения H3AsO4 для различных концентраций (табл. 3).
Таблица 3.
Теплоты испарения для изученных концентраций растворов мышьяковой кислоты
| С, мас. % | ∆H, Дж/моль |
|---|---|
| 19.95 | 41 570 |
| 31.64 | 41 570 |
| 39.99 | 41 570 |
| 49.33 | 42 780 |
| 61.88 | 42 510 |
| 62.21 | 43 750 |
| 74.51 | 42 790 |
| 86.45 | 42 020 |
Средняя теплота испарения равна 42 200.0 Дж/моль. Из экспериментальных данных определен коэффициент В уравнения
(3)
${\text{ln}}p = {{--\Delta H} \mathord{\left/ {\vphantom {{--\Delta H} {RT}}} \right. \kern-0em} {RT}} + B.$Полученные результаты по изучению физико-химических свойств продуктов детоксикации люизита – АНГ – позволили оптимизировать процесс электрохимического синтеза арсина с выходом по мышьяку 95%.
ЗАКЛЮЧЕНИЕ
Изучены физико-химические свойства мышьяксодержащих соединений – основных продуктов детоксикации люизита, в частности АНГ.
Подтверждено, что АНГ представляет собой сложную многокомпонентную смесь. Определен элементный макро- и микросостав АНГ.
Показана перспектива получения наиболее чистого арсина с минимальным содержанием микропримесей 99.9999 и 99.99999 мас. % по сравнению с другими методами переработки люизита.
Определены плотность растворов и давление насыщенного пара H3AsO4 в широком интервале концентраций кислоты. Полученные результаты позволили оптимизировать процесс электрохимического синтеза АНГ с выходом по мышьяку до 95%.
Список литературы
Федоров В.А., Чурбанов М.Ф. Получение высокочистого мышьяка. Высокочистые вещества. Коллектив авторов. М.: Научный мир, 2018. С. 566–592.
Копылов Н.И., Каминский Ю.Д. Мышьяк. Новосибирск: Сибирское университетское изд-во, 2004. С. 363.
Демахин А.Г., Мащенко С.В., Федоров В.А. Оптимизация экономических и экологических задач при переработке сырья, полученного из реакционных люизита, в оксид мышьяка марки “технический” // Изв. вузов. Химия и хим. технология. 2016. Т. 59. Вып. 11. С. 117–123.
Демахин А.Г., Акчурин С.В., Федоров В.А. Применение арсенита натрия гидролизного для получения чистой мышьяксодержащей продукции // Изв. Сарат. ун-та. Нов. Сер. Химия, Биохимия, Экология. 2019. Т.29. Вып. 3. С. 11–17.
Умяров Г.А., Кузнецов Б.А., Кротович И.Н., Холстов В.И., Соловьев В.А. Методы уничтожения и утилизации запасов люизита и иприта // Рос. хим. журн. (Журн. Рос. хим. о-ва им. Д.И. Менделеева). 1993. Т. XXXVII. № 3. С. 25–28.
Федоров В.А., Ефремов А.А., Жуков Э.Г., Кузнецов Б.А., Потепалов В.П., Казанский Л.Н., Тарасевич Ю.В., Холстов В.И. Получение мышьяка особой чистоты из продуктов детоксикации люизита // Рос. хим. журн. (Журн. Рос. хим. о-ва им. Д.И. Менделеева). 1995. Т. 39. № 4. С. 46–55.
Федоров В.А., Потолоков Н.А., Менщикова Т.К., Бреховских М.Н. Гидридный метод получения высокочистого мышьяка // Неорган. материалы. 2018. Т. 54. № 10. С. 1092–1098. https://doi.org/10.1134/S0002337X18100068
Московская Т.Э. Определение плотности методом пикнометрии: Методические рекомендации. Иркутск: Изд-во Иркутского гос. ун-та, 2003. С. 1–7.
Фролов В.И., Винокуров В.А., Носов В.П. Определение температурной зависимости давления насыщенных паров и теплоты испарения индивидуальных жидкостей: Методические указания к лабораторному практикуму по курсу “Физическая химия”. Раздел “Фазовое равновесие”. М.: РГУ нефти и газа им. И.М. Губкина, 2014. 27 с.
Плаченов Т.Г., Колосенцев С.Д. Порометрия. Л.: Химия, 1988. 176 с.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы