Неорганические материалы, 2020, T. 56, № 12, стр. 1371-1379
Возможности реакционного спекания при получении прочной макропористой керамики на основе замещенных фосфатов кальция
Н. К. Орлов 1, 3, *, А. К. Киселева 1, П. А. Милькин 1, П. В. Евдокимов 1, 2, В. И. Путляев 1, 2, J. Günster 3
1 Факультет наук о материалах Московского государственного университета им. М.В. Ломоносова
119234 Москва, Ленинские горы, 1, стр. 73, Россия
2 Химический факультет Московского государственного университета им. М.В. Ломоносова
119234 Москва, Ленинские горы, 1, стр. 3, Россия
3 Federal Institute for Materials Research and Testing (BAM)
12203 Berlin, Unter den Eichen 44-46, Germany
* E-mail: nicolasorlov174@gmail.com
Поступила в редакцию 27.03.2020
После доработки 06.08.2020
Принята к публикации 10.08.2020
Аннотация
Синтезированы двойные и тройные фосфаты кальция и щелочных металлов (калия, натрия) различными способами. Впервые применен метод реакционного спекания для получения керамики на основе смешанных фосфатов кальция и щелочных металлов, а также исследован характер уплотнения многофазных материалов на основе смешанных фосфатов при спекании данным методом. Приведена микроструктура шлифов спеченных образцов различного фазового состава, определена плотность керамики, полученной из реакционных смесей различного состава. Дана оценка влияния реакционного спекания на характер пористости керамики. Методами стереолитографической печати и реакционного спекания получены макропористые керамические имплантаты на основе смешанных фосфатов кальция. Прочность на сжатие составила 0.78 ± 0.21 МПа для двухфазных образцов и 1.02 ± 0.13 МПа для трехфазных.
ВВЕДЕНИЕ
Накопление данных о функционировании имплантатов после вживления их в организм привело к тому, что на данный момент оптимальной формой имплантата считается высокопористый каркас (от 70 до 90% пор). Это обусловлено такими требованиями, предъявляемыми к костным имплантатам, как биорезорбируемость, остеокондуктивность, биосовместимость и т.д. [1–4]. Тем не менее, сам керамический каркас должен быть максимально прочным, а значит, и максимально плотным.
Увеличение плотности керамики на основе замещенных фосфатов кальция является достаточно нетривиальной задачей, что связано с тем, что в фосфатах кальция, где часть кальция замещена ионами других металлов (в частности, калием и/или натрием) [5–7], скорость диффузии катионов достаточно высока. В то же время скорость диффузии фосфатных анионов остается низкой ввиду их значительного размера и большого заряда [8, 9]. Первый фактор, который, казалось бы, должен способствовать лучшему спеканию материалов, в реальности приводит к обратному эффекту: в результате интенсивной диффузии катионов активируются процессы собирательной рекристаллизации, приводящие к формированию крупнозеренной структуры с малоподвижными порами в объеме зерен.
Таким образом, проблему получения плотной и прочной фосфатной керамики можно рассмотреть сквозь призму низкой подвижности фосфатного аниона в структуре фосфатов [9]. В данный момент существует несколько методов увеличения диффузионной подвижности при спекании. Такая проблема достаточно часто встречается при спекании соединений с ковалентным типом связи (SiC, Si3N4 и т.д.) [10, 11]. В случае ковалентных кремнийсодержащих керамик решение заключается в создании дополнительного градиента химического потенциала за счет химической реакции, протекающей прямо в процессе спекания, благодаря чему диффузионный поток атомов увеличивается, что можно трактовать как дополнительный вклад в массоперенос. Вполне логично применить подобное решение при спекании фосфатных материалов, особенно замещенных фосфатов, поскольку там проблема преобладания скорости рекристаллизации над скоростью уплотнения проявляется не менее остро.
Следует отметить, что в литературе не представлена информация о реакционном спекании кальцийфосфатной керамики и тем более керамики на основе замещенных фосфатов кальция. В основном в работах, посвященных консолидации материалов за счет протекания химических реакций, изучаются кальцийфосфатные цементы с целью образования целевого вещества в процессе низкотемпературной химической реакции уже после помещения смеси в место костного дефекта.
Цель настоящей работы – исследование возможности получения прочных (не менее 1 МПа на сжатие) макропористых керамических материалов на основе замещенных фосфатов кальция методом реакционного спекания.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для определения возможности использования реакционного спекания при получении плотной керамики на основе смешанных фосфатов кальция и щелочных металлов был выбран модельный состав CaK0.6Na0.4PO4. Он интересен тем, что имеет только один фазовый переход при температуре 667°С с минимальным отрицательным объемным эффектом (что было установлено в работе [12] методами дилатометрии и измерения зависимости проводимости от температуры). С точки зрения получения керамики это крайне удачный набор факторов. Кроме того, в данном соединении присутствуют все ионы, составляющие обычно кальцийфосфатную керамику, что позволяет оценить влияние каждого из них на процесс спекания. С точки зрения костных имплантатов, в составе присутствуют ионы калия и натрия, увеличивающие их резорбируемость.
Синтез тройного фосфата CaK0.6Na0.4PO4 проводился с использованием в качестве промежуточных соединений брушита СаНРО4 · 2Н2О и пирофосфата кальция Са2Р2О7.
Брушит был получен осаждением из водного раствора. Для этого к 400 мл 0.6 М раствора (NH4)2HPO4 (“х. ч.”) при непрерывном перемешивании на магнитной мешалке приливали 400 мл 0.6 М раствора Ca(NO3)2 (раствор готовили из Ca(NO3)2 · 4H2O (“ч.”)), суспензию оставляли перемешиваться при комнатной температуре в течение получаса:
(1)
$\begin{gathered} {\text{Ca}}{{\left( {{\text{N}}{{{\text{O}}}_{{\text{3}}}}} \right)}_{{\text{2}}}} + {{\left( {{\text{N}}{{{\text{H}}}_{4}}} \right)}_{2}}{\text{HP}}{{{\text{O}}}_{4}} + 2{{{\text{H}}}_{{\text{2}}}}{\text{O}} \to \\ \to \,\,{\text{CaHP}}{{{\text{O}}}_{4}} \cdot 2{{{\text{H}}}_{{\text{2}}}}{\text{O}}{\kern 1pt} \downarrow + \,\,2{\text{N}}{{{\text{H}}}_{{\text{4}}}}{\text{N}}{{{\text{O}}}_{3}}. \\ \end{gathered} $Полученный осадок несколько раз декантировали, затем фильтровали на вакуумном фильтре, промывая дистиллированной водой, и оставляли в сушильном шкафу при температуре 100°С на сутки.
Пирофосфат кальция был получен твердофазным методом путем обжига брушита при 800°С в течение 5 ч с последующим повторением обжига до установления фазового равновесия в образце:
(2)
$2{\text{CaHP}}{{{\text{O}}}_{4}}\cdot{\text{ }}2{{{\text{H}}}_{{\text{2}}}}{\text{O}} \to {\text{C}}{{{\text{a}}}_{{\text{2}}}}{{{\text{P}}}_{{\text{2}}}}{{{\text{O}}}_{7}} + 3{{{\text{H}}}_{{\text{2}}}}{\text{O}}.$Тройной фосфат кальция, калия и натрия получали согласно следующим реакциям:
(3)
$\begin{gathered} 0.15{\text{Ca}}{{{\text{K}}}_{{\text{4}}}}{{\left( {{\text{P}}{{{\text{O}}}_{{\text{4}}}}} \right)}_{2}} + 0.15{\text{C}}{{{\text{a}}}_{{\text{3}}}}{{\left( {{\text{P}}{{{\text{O}}}_{{\text{4}}}}} \right)}_{2}} + \\ + \,\,0.4{\text{CaNaP}}{{{\text{O}}}_{4}} \to {\text{Ca}}{{{\text{K}}}_{{{\text{0}}{\text{.6}}}}}{\text{N}}{{{\text{a}}}_{{{\text{0}}{\text{.4}}}}}{\text{P}}{{{\text{O}}}_{4}}, \\ \end{gathered} $(4)
$\begin{gathered} 0.1{\text{CaN}}{{{\text{a}}}_{4}}{{\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)}_{2}} + 0.2{\text{C}}{{{\text{a}}}_{{\text{3}}}}{{\left( {{\text{P}}{{{\text{O}}}_{{\text{4}}}}} \right)}_{2}} + \\ + \,\,0.6{\text{CaKP}}{{{\text{O}}}_{4}} \to {\text{Ca}}{{{\text{K}}}_{{{\text{0}}{\text{.6}}}}}{\text{N}}{{{\text{a}}}_{{{\text{0}}{\text{.4}}}}}{\text{P}}{{{\text{O}}}_{4}}, \\ \end{gathered} $(5)
$\begin{gathered} 0.3{\text{Ca}}{{{\text{K}}}_{{\text{2}}}}{{{\text{P}}}_{{\text{2}}}}{{{\text{O}}}_{7}} + 0.3{\text{CaC}}{{{\text{O}}}_{3}} + 0.4{\text{CaNaP}}{{{\text{O}}}_{4}} \to \\ \to \,\,{\text{Ca}}{{{\text{K}}}_{{{\text{0}}{\text{.6}}}}}{\text{N}}{{{\text{a}}}_{{{\text{0}}{\text{.4}}}}}{\text{P}}{{{\text{O}}}_{4}} + 0.3{\text{C}}{{{\text{O}}}_{2}}{\kern 1pt} \uparrow , \\ \end{gathered} $(6)
$\begin{gathered} 0.5{\text{C}}{{{\text{a}}}_{{\text{2}}}}{{{\text{P}}}_{{\text{2}}}}{{{\text{O}}}_{7}} + 0.3{{{\text{K}}}_{{\text{2}}}}{\text{C}}{{{\text{O}}}_{3}} + 0.2{\text{N}}{{{\text{a}}}_{{\text{2}}}}{\text{C}}{{{\text{O}}}_{3}} \to \\ \to \,\,{\text{Ca}}{{{\text{K}}}_{{{\text{0}}{\text{.6}}}}}{\text{N}}{{{\text{a}}}_{{{\text{0}}{\text{.4}}}}}{\text{P}}{{{\text{O}}}_{{\text{4}}}} + 0.5{\text{C}}{{{\text{O}}}_{2}}{\kern 1pt} \uparrow , \\ \end{gathered} $(7)
$\begin{gathered} 0.5{\text{C}}{{{\text{a}}}_{{\text{2}}}}{{{\text{P}}}_{{\text{2}}}}{{{\text{O}}}_{7}} + 0.6{\text{KN}}{{{\text{O}}}_{3}} + 0.4{\text{NaN}}{{{\text{O}}}_{3}} \to \\ \to \,\,{\text{Ca}}{{{\text{K}}}_{{{\text{0}}{\text{.6}}}}}{\text{N}}{{{\text{a}}}_{{{\text{0}}{\text{.4}}}}}{\text{P}}{{{\text{O}}}_{{\text{4}}}} + {\text{N}}{{{\text{O}}}_{2}}{\kern 1pt} \uparrow + 0.25{{{\text{O}}}_{2}}{\kern 1pt} \uparrow . \\ \end{gathered} $Такой выбор реакций обусловлен, во-первых, данными о фазовых отношениях в системах CaO–Na2O–P2O5 и CaO–K2O–P2O5 (реакции (3)–(5)), во-вторых, реакция (6) является (в варианте смеси пирофосфата кальция и карбоната щелочного металла) наиболее часто используемым вариантом получения ренанитов калия/натрия (CaMPO4) [13, 14], что обусловлено, в частности, невозможностью получения этих соединений растворными методами; в-третьих, реакция (7) аналогична реакции (6) с той лишь разницей, что в ней использовались нитратные соли щелочных металлов с целью понижения температуры синтеза и, возможно, спекания.
Синтез осуществлялся путем смешивания исходных реагентов и их гомогенизации с помощью шаровой мельницы планетарного типа Рulverisette (Fritsch, Германия) в барабанах с набором шаров для помола из стабилизированного оксида циркония в течение 10 мин при скорости 700 об./мин. В качестве среды помола использовался ацетон ((CH3)2CO, “х. ч.”). Гомогенизированную смесь сушили на воздухе. Полученные порошки прессовали в таблетки, на которых исследовали протекание химических реакций и уплотнение при спекании методом дилатометрии.
Фазовый состав образцов был выбран исходя из фигуративных точек двухфазной области (в дальнейшем будем обозначать данную точку как Т2) β-Ca3(PO4)2 + А (идеализированный состав Са5Na2(PO4)4, родственный нагельшмидтиту {Са4}[СаNa2◻(PO4)4 со сверхструктурой 2 × 3) и трехфазной области (в дальнейшем будем обозначать данную точку как Т3) β-Ca3(PO4)2 + А + + Х (апатитоподобная фаза с общей формулой Ca6 – yKxCa2 + yK2 –y(PO4)6◻2). Подобный выбор диктовался соображениями резорбируемости и биосовместимости потенциальных имплантатов. Небольшое количество калия обеспечивает отсутствие цитотоксической реакции, наличие β-Са3(РО4)2 (трикальцийфосфат, ТКФ) способствует лучшей спекаемости керамики, а присутствие катионов натрия повышает резорбируемость материалов.
В качестве реакционной смеси для получения многофазной керамики была выбрана смесь CaNa4(PO4)2 + Ca3(PO4)2 + CaKPO4, которая привела к наилучшим результатам при получении CaK0.6Na0.4PO4 (плотность выше 80%).
Синхронный термический анализ (термогравиметрия совместно с дифференциальным термическим анализом) проводился с помощью термоанализатора STA 409 PC Luxx (Netzsch, Германия). Измерения осуществляли на воздухе в интервале температур от комнатной до 1250°С со скоростью нагрева 10°С/мин. Навески образцов составляли ≤20 мг. Для проведения эксперимента использовали алундовые тигли.
Качественный рентгенофазовый анализ полученных образцов проводили на дифрактометре Rigaku D/Max-2500 с вращающимся анодом (Япония). Качественный анализ полученных рентгенограмм проводили с помощью программы WinXPOW при использовании базы данных ICDD PDF-2.
Линейную усадку прессованных образцов измеряли в горизонтальном дилатометре DIL 402 C (Netzsch, Германия). Режим спекания состоял из нагрева образца до t = 1200°C со скоростью 5°C/мин на воздухе и дальнейшей выдержки при данной температуре в течение 12 ч.
Микроструктуру образцов исследовали на растровом электронном микроскопе FIB-системы NVision 40 (Carl Zeiss, Германия). Для исследования на образцы был нанесен слой хрома (напылительная установка Quorum Technologies, QT-150T ES, Великобритания).
Для печати макропористых образцов композитов полимер/порошок с заданной геометрией порового пространства (типа “Кельвин”) из суспензии порошка в смеси мономеров и фотоинициатора использовали трехмерный стереолитографический DLP-принтер Ember (Autodesk, США). Толщина единичного слоя при печати трехмерного объекта составляла 50–100 мкм. Для определения необходимого времени (дозы излучения), достаточного для полимеризации текущего слоя и сцепления его с предыдущим, изучали глубину полимеризации суспензии в зависимости от дозы излучения и исходя из этого выбирали оптимальное время экспозиции единичного слоя. Послойное разбиение и загрузку модели для печати на принтер проводили с использованием программы Print Studio (Autodesk, США).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
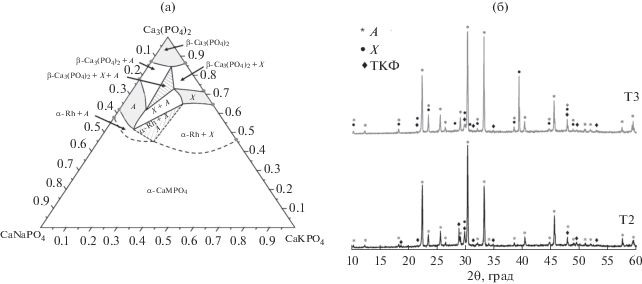
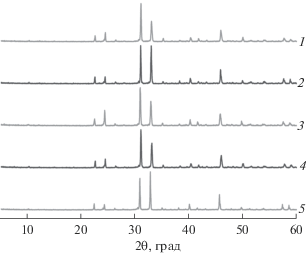
Результаты рентгенофазового анализа синтезированных образцов CaK0.6Na0.4PO4 показали, что во всех реакциях получался смешанный фосфат кальция, калия и натрия (рис. 1), что говорит о возможности использования всех вариантов синтеза для реакционного спекания и получения керамики на основе CaK0.6Na0.4PO4.
Рис. 1.
Рентгенограммы керамик CaK0.6Na0.4PO4, полученных из различных реакционных смесей: CaK4(PO4)2 + Ca3(PO4)2 + CaNaPO4 (1), CaNa4(PO4)2 + Ca3(PO4)2 + CaKPO4 (2), Ca2P2O7 + + KNO3 + NaNO3 (3), Ca2P2O7 + K2CO3 + Na2CO3 (4), 5 – CaK0.6Na0.4PO4.
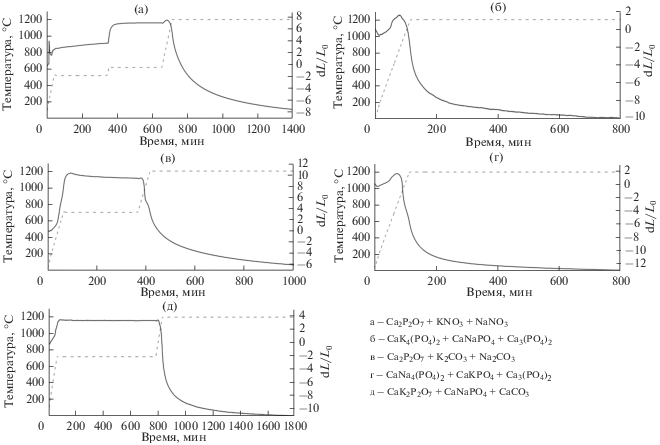
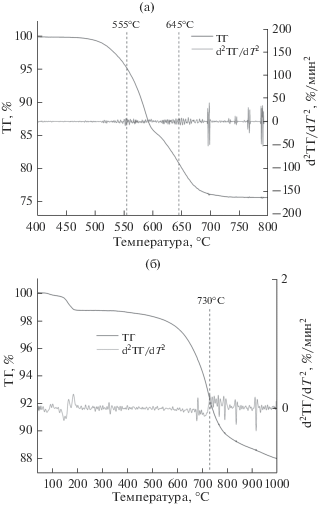
На рис. 2 представлены дилатометрические кривые спекания различных реакционных смесей. В тех случаях, где, согласно уравнению реакции, должен выделяться газообразный продукт реакции, применялся усложненный температурный режим. В частности, добавляли ступени изотермической выдержки для постепенного удаления газообразного продукта, предотвращая тем самым его резкое выделение и разрушение образца. Такие ступени выбирались путем определения максимума второй производной на графике зависимости потери массы во время реакции (ТГ) от температуры. В этой точке реакция уже проходит, но скорость выделения газообразного продукта еще не максимальна. Для нитратной смеси были определены две таких точки: 555 и 645°C соответственно. Во время спекания были установлены ступени изотермической выдержки: при 530 и 620°C. Для карбонатной смеси подобным же образом была установлена температура изотермической выдержки при 700°C (рис. 3). Таким образом была предпринята попытка смягчения последствий выделения газов в виде образования дополнительной пористости и разрушения образца.
Однако, как видно из результатов дилатометрии, примененный подход не оказал значительного влияния на итоговую усадку. Для карбонатных и нитратных смесей она оказалась на несколько процентов ниже таковой для смесей, реагирующих без выделения газообразного продукта.
В то же время наибольшую усадку показала смесь смешанного ортофосфата кальция-натрия (CaNa4(PO4)2) с калиевым ренанитом и ТКФ (реакция (4)). Данный факт еще раз подтверждает эффективность реакционного спекания натриевого ренанита, так как в случаях, когда натриевый ренанит уже присутствовал в смеси в готовом виде, спекание проходило хуже.
Микроструктура шлифов полученных керамик (рис. 4) согласуется с результатами дилатометрии. Несмотря на изотермические выдержки при низких температурах для более равномерного удаления газообразного продукта, керамика из карбонатных (рис. 4а, 4б) и нитратных (рис. 4в, 4г) смесей получилась значительно хуже. Видно, что существуют две моды в распределении размеров зерен (микронные и размером до 10 мкм); измеренная гидростатическим методом кажущаяся плотность керамики составляла 51% в случае карбонатной смеси и 42% в случае нитратной. Это говорит о невозможности применения данных реакций для получения прочных керамических материалов. Помимо этого, присутствие в микроструктуре микронных зерен, по размеру соответствующих скорее частицам исходного порошка, говорит о незавершенности спекания, что, вероятно, вызвано плохим контактом частиц из-за сильного разрыхляющего действия газообразного продукта реакции. На микрофотографиях видно, что участки с микронными частицами лишь немного припечены друг к другу, что соответствует начальной стадии спекания.
Рис. 4.
Микроструктуры шлифов керамик, полученных реакционным спеканием из смесей Ca2P2O7 + K2CO3 + Na2CO3 (а, б), Ca2P2O7 + KNO3 + NaNO3 (в, г), CaK2P2O7 + CaCO3 + CaNaPO4 (д, е), CaK4(PO4)2 + Ca3(PO4)2 + CaNaPO4 (ж, з), CaNa4(PO4)2 + Ca3(PO4)2 + CaKPO4 (и, к) (для наглядности на некоторых микрофотографиях зерна выделены пунктиром).

Другая ситуация наблюдается в случае спекания смеси CaK2P2O7 + CaCO3 + CaNaPO4. Как видно из микрофотографий (рис. 4д, 4е), в отличие от керамики из карбонатных и нитратных смесей спекание прошло более полно. Однако также заметна, хотя и в меньшей степени, значительная пористость. Кажущаяся плотность такой керамики сопоставима с образцом, содержащим карбонат кальция, и составляет 71%. Из-за значительной пористости четкое определение размеров зерен получившейся керамики затруднено, однако можно сказать, что большинство зерен имеет размер порядка 10 мкм.
Керамика из смесей CaK4(PO4)2 + Ca3(PO4)2 + + CaNaPO4 и CaNa4(PO4)2 + Ca3(PO4)2 + CaKPO4 показывает явно лучшее уплотнение (рис. 4ж, 4з и 4и, 4к). Все еще заметен большой размер зерна (более 10 мкм), однако плотность таких материалов гораздо выше – порядка 80%. Стоит также отметить, что поры располагаются преимущественно на границах зерен, что, несомненно, является положительным моментом, поскольку они могут быть удалены при дальнейшей оптимизации режима спекания.
Следующим этапом работы было изучение влияния реакционного спекания на итоговую плотность и прочность двухфазной и трехфазной керамики, составы которой принадлежат диаграмме Ca3(PO4)2–CaNaPO4–CaKPO4 (рис. 5).
Микроструктура шлифов полученной многофазной керамики на основе смеси CaNa4(PO4)2 + + Ca3(PO4)2 + CaKPO4 (рис. 6) свидетельствует о достаточно высокой плотности – 85% и достаточно большом размере зерен – около 10 мкм. На микрофотографиях видно, что поры находятся на границах зерен, что, как уже отмечалось, является положительным результатом, особенно в случае фосфатной керамики, где процессы уплотнения (удаления пор) затруднены ввиду медленной твердофазной диффузии фосфатных анионов.
Из негативных моментов следует отметить значительное количество трещин, проходящих в том числе и через объем зерна ввиду отсутствия там тормозящих пор. Это, безусловно, говорит о низкой трещиностойкости полученной керамики и, вероятно, отразится на ее прочности.
Описанные выше особенности керамики – высокая плотность, большой размер зерна и обилие трещин – объясняются несколькими факторами. Большое количество трещин может быть следствием неоптимального температурного режима спекания, в результате чего имел место чрезмерный рост зерен, вызывающий значительные напряжения при спекании. Дальнейшая оптимизация режима спекания, в том числе разработка многостадийных режимов, поможет улучшить качество получаемой керамики.
Сравнивая керамику двух различных фазовых составов друг с другом, можно отметить, что плотность двухфазного образца (Т2) несколько меньше по сравнению с трехфазным (Т3). В данном случае немаловажную роль играет тот факт, что помимо положительного влияния реакционного спекания, ускоряющего диффузию и приводящего к большему уплотнению по сравнению с обычным спеканием, в трехфазном образце присутствует апатитоподобная фаза Х, спекаемость которой гораздо лучше за счет наличия анионных вакансий, видимо, улучшающих и подвижность фосфат-анионов, чего не наблюдается при комбинации только фаз ТКФ и А (в двухфазном образце).
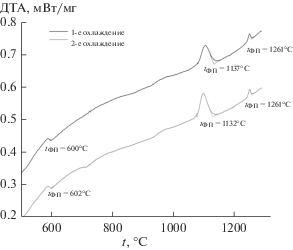
При изучении процессов спекания фосфатных материалов были также исследованы фазовые превращения для образца Т3 методом ДТА (рис. 7). Из-за особенности твердофазных превращений (малая интенсивность пиков и их “размытость” по температуре вследствие кинетической заторможенности) зафиксировать эффекты удалось только на сегментах охлаждения. Таким образом были определены три фазовых перехода: 602, 1135 и 1261°C, которые впоследствии помогут уточнить тройную диаграмму системы Ca3(PO4)2–CaNaPO4–CaKPO4.
После изучения процессов спекания на модельных таблетированных образцах подобными же приемами были изготовлены макропористые образцы со специальной геометрией порового пространства и определена их прочность. Для этого методом стереолитографической 3D-печати были сформированы макропористые образцы со структурой Кельвина. Данная структура является одной из оптимальных с точки зрения проницаемости (остеокондуктивности), прочности и невысокой относительной жесткости. Пористость такой структуры достигает 70% [18]. Это одновременно делает ее более резорбируемой и остекондуктивной при сохранении своих прочностных характеристик.
После выжигания полимера (в соответствии с разработанной ранее программой [19]) и спекания были исследованы прочностные свойства полученной керамики. В результате проведенных испытаний на сжатие было определено, что среднее значение прочности составило 0.78 ± 0.21 МПа для двухфазного образца Т2 и 1.02 ± 0.13 МПа для трехфазного Т3.
ЗАКЛЮЧЕНИЕ
Синтезирован тройной фосфат кальция, калия и натрия CaK0.6Na0.4PO4 из различных смесей. Определено, что оптимальной с точки зрения плотности и размера зерен керамики для реакционного спекания является реакция ортофосфата натрия с ТКФ и калиевым ренанитом (CaNa4(PO4)2 + + Ca3(PO4)2 + CaKPO4).
Плотность получаемой при этоим керамики на основе CaK0.6Na0.4PO4 достигает 80% при размере зерна порядка 10 мкм.
Исследовано реакционное спекание многофазных материалов на основе фосфатов кальция. Установлено, что средний размер зерна таких керамических материалов составляет 10 мкм при относительной плотности 85%.
Получены макропористые керамические имплантаты и определены значения их прочности на сжатие: 0.78 ± 0.21 МПа для двухфазного образца и 1.02 ± 0.13 МПа для трехфазного.
Список литературы
Jarcho M. Calcium Phosphate Ceramics as Hard Tissue Prosthetics // Clin. Orthop. Relat. Res. 1981. V. 157. P. 259–278.
Jarcho M., Bolen C.H., Thomas M.B., Bobick J., Kay J.F., Doremus R.H. Hydroxylapatite Synthesis and Characterisation in Dense Polycrystalline // J. Mater. Sci. 1976. V. 11. P. 2027–2035. https://doi.org/10.1007/PL00020328
Gross K.A., Berndt C.C. Biomedical Application of Apatites // Rev. Mineral. Geochem. 2002. V. 48. № 1. P. 631–672. https://doi.org/10.2138/rmg.2002.48.17
Berger G., Gildenhaar R., Ploska U. Rapid Resorbable, Glassy Crystalline Materials on the Basis of Calcium Alkali Orthophosphates // Biomaterials. 1995. V. 16. № 16. P. 1241–1248. https://doi.org/10.1016/0142-9612(95)98131-W
Evdokimov P.V., Putlyaev V.I., Ivanov V.K., Garshev A.P., Shatalova T.B., Orlov N.K., Klimashina E.S., Safronova T.V. Phase Equilibria in the Tricalcium Phosphate-Mixed Calcium Sodium (Potassium) Phosphate Systems // Russ. J. Inorg. Chem. 2014. V. 59. P. 1219–1227. https://doi.org/10.7868/S0044457X14110087
Ievlev V.M., Putlyaev V.I., Safronova T.V., Evdokimov P.V. Additive Technologies for Making Highly Permeable Inorganic Materials with Tailored Morphological Architectonics for Medicine // Inorg. Mater. 2015. V. 51. P. 1297–1315. https://doi.org/10.1134/S0020168515130038
Ando J. Phase Diagrams of Ca3(PO4)2–Mg3(PO4)2 and Ca3(PO4)2–CaNaPO4 // Bull. Chem. Soc. Jpn. 1958. V. 31. P. 201–205.
Suk-Joong L. Kang. Sintering: Densification, Grain Growth and Microstructure. L.: Butterworth, 2004. 280 p.
Champion E. Sintering of Calcium Phosphate Bioceramics // Acta Biomater. 2013. V. 9. P. 5855–5875.
Dey A., Chakrabarti O. Investigation on Synthesis of Cordierite Bonded Porous SiC Ceramics with Emphasis on Bond Phase Formation // Mater. Chem. Phys. 2019.V. 222. P. 275–285.
Guo W.-M., Wu L.-X., Ma T., You Y., Lin H.-T. Rapid Fabrication of Si3N4 Ceramic by Reaction-Bonding and Pressureless Sintering // J. Eur. Ceram. Soc. 2016. V. 36. № 16. P. 3919–3924.
Niu J.L., Zhang Z.X., Jiang D.Z. Investigation of Phase Evolution During the Formation of Calcium Potassium Sodium Orthophosphate // Mater. Chem. Phys. 2002. V. 78. № 2. P. 308–312.
Orlov N.K., Evdokimov P.V., Milkin P.A., Garshev A.V., Putlayev V.I., Grebenev V.V., Günster J. Phase Equilibria in CaNaPO4–CaKPO4 System and Their Influence on Formation of Bioceramics Based on Mixed Ca–K–Na Phosphates // J. Eur. Ceram. Soc. 2019. V. 39. № 16. P. 5410–5422. https://doi.org/10.1016/j.jeurceramsoc.2019.07.044
Niu J.L., Zhang Z.X., Jiang D.Z., Yang S.H. et al. Preperation, Structure and Solubility of Ca2KNa(PO4)2 // J. Mater. Sci. 2001. V. 36. № 15. P. 3805–3808.
Орлов Н.К., Путляев В.И., Евдокимов П.В., Сафронова Т.В., Гаршев А.В., Милькин П.А. Разработка композитной биокерамики на основе фазовых равновесий в системе Ca3(PO4)2–CaNaPO4–CaKPO4 // Неорган. материалы. 2019. Т. 55. № 5. С. 554–561. https://doi.org/10.1134/S0002337X19050154
Znamierowska T. Uklad Ca3(PO4)2–CaKPO4–CaNaPO4. Czesc I // Zesz. Nauk. Politech. 1982. Sl. 709. P. 33–43.
Znamierowska T. Uklad Ca3(PO4)2–CaKPO4–CaNaPO4. Czesc II // Zesz. Nauk. Politech. 1982. Sl. 709. P. 45–56.
Тихонов А.А., Евдокимов П.В., Путляев В.И., Сафронова Т.В., Филиппов Я.Ю. О выборе архитектуры остеокондуктивных биокерамических имплантатов // Неорган. материалы. 2018. Т. 54. № 8. С. 43–48. https://doi.org/10.31044/1684-579X-2018-0-8-43-48
Путляев В.И., Евдокимов П.В., Сафронова Т.В., Климашина Е.С., Орлов Н.К. Формирование остеокондуктивной кальцийфосфатной биокерамики Ca3 – xM2x(PO4)2 (M = Na, K) методом стереолитографической 3D-печати // Неорган. материалы. 2017. Т. 53. № 5. С. 534–541. https://doi.org/10.7868/S0002337X17050165
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы