Неорганические материалы, 2020, T. 56, № 12, стр. 1279-1284
Синтез МАХ-фазы Ti3SiC2 при горении системы TiO2–Mg–Si–C
В. И. Вершинников 1, *, Д. Ю. Ковалёв 1
1 Институт структурной макрокинетики и проблем материаловедения им. А.Г. Мержанова, Российской академии наук
142432 Московская обл., Черноголовка, ул. Академика Осипьяна, 8, Россия
* E-mail: vervi@ism.ac.ru
Поступила в редакцию 24.02.2020
После доработки 14.07.2020
Принята к публикации 17.07.2020
Аннотация
Разработаны технологические принципы получения МАХ-фазы Ti3SiC2 методом самораспространяющегося высокотемпературного синтеза (СВС) с восстановительной стадией с использованием оксида титана. Исследована зависимость состава, структуры, дисперсности порошка Ti3SiC2 от условий синтеза: состава шихты, соотношения реагирующих компонентов. Установлено, что введение дополнительного количества магния в шихту (от 10 до 20 мас. %) приводит к уменьшению содержания в порошке Ti3SiC2 силицидов TiSi2 + Ti5Si3 (от 8 до 5 мас. %), причем наименьшее содержание карбида титана соответствует 10%-ному избытку магния в шихте. Установлено, что увеличение на 10% содержания кремния в шихте приводит к уменьшению содержания силицидов TiSi2 + Ti5Si3 и карбида титана в порошке Ti3SiC2. Обнаружено влияние добавки хлорида натрия и перхлората магния в шихте на содержание силицидов TiSi2, Ti5Si3 и TiC в порошке Ti3SiC2. Определены оптимальные условия синтеза порошка, содержащего 89.1 мас. % Ti3SiC2. Полученные методом СВС с восстановительной стадией порошки представляют собой агломераты, состоящие из слоистых частиц размером 130–770 нм.
ВВЕДЕНИЕ
МАХ-фазы имеют слоистую кристаллическую структуру, что приводит к наноламинатному строению зерен с толщиной слоев до нескольких десятков нанометров. Материалы на основе МАХ-фаз сочетают свойства керамики и металлов. Подобно керамике, они имеют низкую плотность, обладают высокими модулями упругости, жаростойкостью и жаропрочностью. Аналогично металлам, они электро- и теплопроводны, имеют высокую трещиностойкость и термостойкость. Наиболее изученными МАХ-фазами, представляющими практический интерес, являются фазы на основе титана, одна из которых Ti3SiC2.
В 1967 г. в работах Новотного и др. [1] впервые была синтезирована тройная фаза – силикокарбид Ti3SiC2. При изучении свойств материала, сделанного на его основе, были выявлены уникальные свойства: сверхнизкий коэффициент трения, высокая термическая и коррозийная стойкость, высокая прочность и трещиностойкость, стойкость к термоудару. Материал легко поддается механической обработке. Эти свойства определили его промышленное применение при изготовлении труб для циркуляции жидкого свинца [2–4], защитных покрытий на оболочках из Zircaloy-сплавов [5–7], электродов для электролиза HCl при получении Cl2 [8], электрических контактов [9].
Синтез МАХ-фазы Ti3SiC2 проводится, как правило, из элементов методом горячего изостатического прессования (HIP) [10–12], спеканием в разряде плазмы (SPS) [13–15], методом самораспространяющегося высокотемпературного синтеза (СВС) [16–19], комбинацией методов СВС + HIP [20, 21], методом реакционного спекания (RS) [22, 23] и механического сплавления [24, 25], химическим осаждением из паровой фазы (CVD) [26, 27], магнетронным напылением (MS) [28] и дуговой плавкой (AR) [29].
Несмотря на многообразие способов синтеза, все они предполагают использование бескислородных соединений в качестве исходных компонентов. Известна работа [30], где для получения Ti3SiC2 использовали восстановление TiO2 смесью SiC и Si. Было показано, что использование комбинированного восстановителя позволяет получать тройную фазу Ti3SiC2 путем одновременных карбо- и силикотермических процессов по суммарной реакции
Цель настоящей работы – исследование возможности получения МАХ-фазы Ti3SiC2 методом СВС с восстановительной стадией с использованием оксида титана, магния в качестве восстановителя, кремния и сажи.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В экспериментах использовали следующие порошки: Mg с содержанием основного вещества 98.5–99.5% и размером частиц меньше 250 мкм; TiO2 технический, марка 1, анатаз, ТУ 1715-347-00545484–94; Si кристаллический марка КР 00, размолотый, размер частиц менее 10 мкм, удельная поверхность более 6.5 м2/г; перхлорат магния безводный Mg(ClO4)2, МРТУ 6-09-3856-67; хлорид натрия NaCl квалификации “Х. Ч.”, ГОСТ 4233-77; сажа марки П804-Т с Sуд = 12 м2/г. Для выделения МАХ-фазы из полупродукта, содержащего MgO, использовали разбавленную соляную кислоту (1 : 3).
Смешение шихты проводили в барабане валковой шаровой мельницы объемом 2 л в течение 2 ч при соотношении массы шихты и стальных нержавеющих шаров 1 : 3. Для синтеза использовали смесь с насыпной плотностью (ρ = 0.63 ± ± 0.05 г/см3). Шихту массой 250 г засыпали в графитовую лодочку. Синтез проводили в реакторе СВС-8 в среде аргона при давлении p = 4 МПа. Горение инициировали с торца шихтовой засыпки вольфрамовой спиралью. Сгоревший материал размалывали в щековой дробилке и в барабане валковой шаровой мельницы при соотношении массы полупродукта к массе шаров 1 : 5 в течение 3 ч. Далее полупродукт подвергали химическому выщелачиванию в разбавленной соляной кислоте по реакции
(2)
${\text{MgO}} + 2{\text{HCl}} = {\text{MgC}}{{{\text{l}}}_{2}} + {{{\text{H}}}_{{\text{2}}}}{\text{O}}.$Для увеличения температуры горения в шихту вводили окислитель – перхлорат магния. При этом перхлорат магния, взаимодействуя с магнием, дает добавочное тепло:
(3)
${\text{Mg}}{{\left( {{\text{Cl}}{{{\text{O}}}_{{\text{4}}}}} \right)}_{2}} + 8{\text{Mg}} = 8{\text{MgO}} + {\text{MgC}}{{{\text{l}}}_{2}} + Q.$Адиабатическая температура горения для реакции (3) составляет Тад = 3771 К.
Состав продуктов синтеза после выщелачивания исследовали методом рентгенофазового анализа (РФА) на дифрактометре ДРОН 3М. Регистрация дифрактограмм проводилась в режиме пошагового сканирования на излучении CuKα в интервале углов 2θ = 8°–65° с шагом съемки 0.02° и экспозицией 5 с в точке. При расшифровке рентгенограмм использовали базу данных ICDD PDF-2. Количественный РФА проводили методом Ритвельда в программном пакете PDWin6.0. В расчетах уточнялись профильные параметры линий, фон, параметры ячеек и содержание фаз. Взвешенный фактор Rwp составлял 6–8%.
Все указанные в статье содержания фаз приведены в мас. %. Распределение размера частиц исследовали на анализаторе Fritch particle sized. Микроструктуру и морфологию частиц порошков изучали на сканирующем электронном микроскопе LEO-1450 с рентгеновским анализатором IN-CA ENERGY 350 (EDS).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Синтез МАХ-фазы Ti3SiC2 в режиме горения осуществлялся по суммарной реакции
(4)
$3{\text{Ti}}{{{\text{O}}}_{2}} + 6{\text{Mg}} + {\text{Si}} + 2{\text{C}} = {\text{T}}{{{\text{i}}}_{{\text{3}}}}{\text{Si}}{{{\text{C}}}_{2}} + 6{\text{MgO}}.$Адиабатическая температура горения данной шихты составляет 2750 K. После химического выщелачивания продукта горения, полученного из смеси, молярный состав которой отвечает реакции (4), порошок состоял из 53%Ti3SiC2, 7% (TiSi2 + + Ti5Si3) и 40% TiC (рис. 1а).
Рис. 1.
Зависимость фазового состава продуктов синтеза от содержания дополнительного количества Mg в шихте (а) и микрофотография порошка при 15%-ном избытке Mg (б).
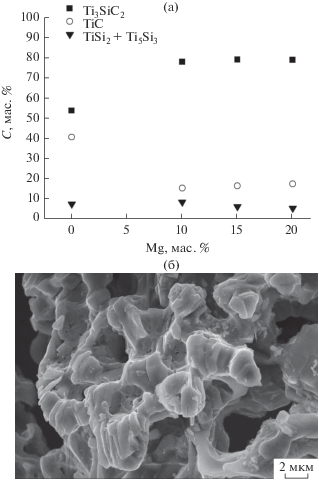
Для уменьшения температуры горения в шихту уравнения (4) вводили от 10 до 20% избытка Mg. Избыток магния рассчитывался относительно стехиометрического содержания в уравнении (4), при этом соотношение остальных компонентов оставалось постоянным. РФА показал, что минимальное количество TiC в продукте синтеза получено при 10% избыточного содержания Mg в шихте и составляет 16% (рис. 1а).
Максимальное содержание фазы Ti3SiC2 78.0% приходится на состав с 15%-ным избытком магния (рис. 1а). Микрофотография продукта (рис. 1б) показывает, что порошок состоит из пластинчатых агломератов.
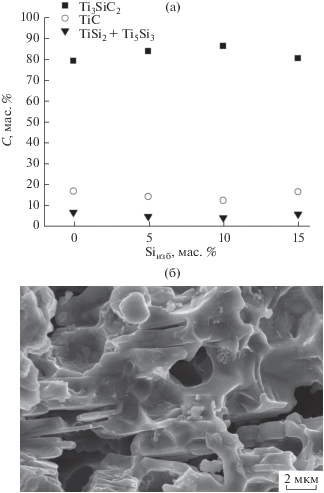
Для состава с 15%-ным избытком магния в шихте проводились исследования влияния избытка кремния в шихте на продукт синтеза. Избыток кремния в шихте менялся от 5 до 15%. РФА показал, что содержание карбида титана и силицидов титана проходит через минимум при Siизб = 10% (рис. 2а), при этом концентрация фазы Ti3SiC2 увеличивается до 85.0%. Продукт также характеризуется пластинчатой формой частиц (рис. 2б).
Рис. 2.
Зависимость фазового состава продуктов синтеза от содержания дополнительного количества Si в шихте (а) и микрофотография порошка при 10%-ном избытке Si и 15%-ном избытка Mg в шихте (б).
Анализ распределения частиц по размерам показал, что для состава шихты с 15%-ным избытком магния и 10%-ным избытком кремния порошок является полидисперсным, с размером частиц меньше 50 мкм. Около 50% частиц относятся к фракции от 12 до 25 мкм, причем доля частиц меньше 12 мкм составляет 35%.
В связи с тем, что избыток кремния понижает температуру горения, для состава, обеспечивающего максимальный выход фазы Ti3SiC2 (Siизб = 10%), в шихту вводили от 0 до 4% высокоэнергетической добавки Mg(ClO4)2 согласно реакции (3). РФА показал, что при увеличении содержания указанной добавки в шихте от 0 до 4% концентрация карбида титана в продукте синтеза увеличивается почти в 2.5 раза. В данном случае оптимальной для получения продукта с минимальным содержанием TiC является добавка 1% Mg(ClO4)2.
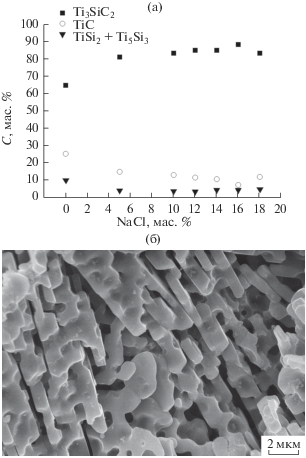
Следующим шагом, направленным на увеличение выхода Ti3SiC2, было введение в шихту, содержащую 15% избытка магния, 10% избытка кремния и 2% Mg(ClO4)2, добавки хлорида натрия. Содержание хлорида натрия в шихте менялось от 0 до 18% (рис. 3а). При содержании 16% NaCl в шихте концентрация фазы Ti3SiC2 в продукте достигает 87.9%, содержание фазы TiC – 7.5%, а силицидов титана – 4.6% (рис. 3а). Пластинчатая морфология частиц порошка (рис. 3б) типична для МАХ-фаз. При 18% NaCl наблюдается уменьшение содержания Ti3SiC2 и увеличение TiC (рис. 3а), что связано, видимо, с уменьшением температуры горения.
Рис. 3.
Зависимость фазового состава продуктов синтеза от содержания NaCl (а) и микрофотография порошка, полученного из шихты, содержащей 16% NaCl и 0.9% Mg(ClO4)2 (б).
Для проверки этого предположения в шихту с 15%-ным избытком магния и 10%-ным избытком кремния добавляли подогревающую добавку Mg(ClO4)2. Содержание Mg(ClO4)2 в шихте менялось от 0.8 до 3.1%, при этом добавка NaCl в шихте была постоянной и составляла 18%.
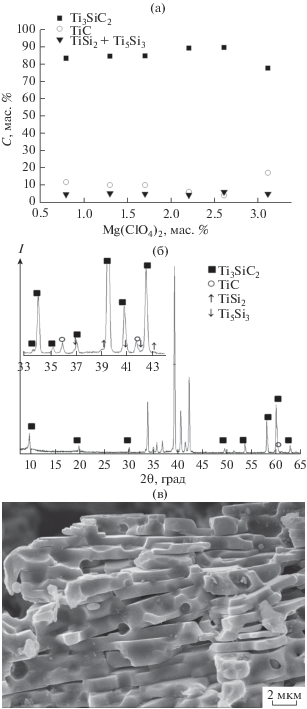
При увеличении количества Mg(ClO4)2 в шихте от 0.8 до 2.6% происходит увеличение содержания Ti3SiC2 от 82.9 до 89.1%, а количество TiC уменьшается от 12 до 4.4% (рис. 4а). Содержание силицидов титана в исследуемом диапазоне меняется незначительно. На рис. 4б приведена дифрактограмма порошка с минимальным содержанием карбида титана, равным 4.4%, а на рис. 4в его микрофотография.
Рис. 4.
Зависимость фазового состава продукта синтеза от содержания Mg(ClO4)2 в шихте (а), дифрактограмма (б) и микрофотография (в) порошка, полученного из смеси, содержащей 15% избытка магния, 10% избытка кремния, 2.6% Mg(ClO4)2 и 18% NaCl.
Порошок является полидисперсным, с размером частиц менее 50 мкм. Анализ распределения частиц показал увеличение доли фракции менее 12 мкм, которая составляет 45%. Это вызвано добавкой NaCl, которая при температуре горения образует жидкую среду, препятствующую укрупнению мелких частиц.
Микроструктура продукта показывает, что в случае синтеза Ti3SiC2 из смеси, содержащей добавки NaCl и Mg(ClO4)2 (рис. 3б, рис. 4в), образуются характерные для МАХ-фаз пластинчатые структуры, толщина которых превышает толщину слоев в материале, синтезированном из смесей с избытком Mg (рис. 1б) и Si (рис. 2б).
ЗАКЛЮЧЕНИЕ
Результаты исследований показали возможность получения материала, содержащего более 90% Ti3SiC2, методом СВС с восстановительной стадией при использовании в качестве исходного сырья TiO2. Установлено, что на выход продукта с максимальным содержанием Ti3SiC2 оказывают влияние избыток Mg и Si, а также добавки NaCl и Mg(ClO4)2. Определен оптимальный состав смеси для получения материала с минимальным количеством карбидной и силицидных фаз титана. Морфология частиц синтезированного вещества имеет выраженную ламинатную структуру с толщиной слоев 130–770 нм, характерную для МАХ-фаз.
Список литературы
Jeitschko W., Nowotny H., Benesovsky F. Die Kristallstruktur von Ti3SiC2 – ein neuer Komplexcarbid-Typ// Monatsh. Chem. 1967. V. 98. № 2. P. 329–337.
Barnes L.A., Dietz Rago N.L., Leibowitz L. Corrosion of Ternary Carbides by Molten Lead // J. Nucl. Mater. 2008. V. 373. № 1–3. P. 424–428. https://doi.org/10.1016/j.jnucmat.2007.04.054
Utili M., AgostiniM., Coccoluto G., Lorenzini E. Ti3SiC2 as a Candidate Material for Lead Cooled Fast Reactor // Nucl. Eng. Des. 2011. V. 241. № 5. P. 1295–1300. https://doi.org/10.1016/j.nucengdes.2010.07.038
Heinzel A., Muller G., Weisenburger A. Compatibility of Ti3SiC2 with Liquid Pb and PbBi Containing Oxygen // J. Nucl. Mater. 2009. V. 392. № 2. P. 255–258. https://doi.org/10.1016/j.jnucmat.2009.03.004
Nappe J., Grosseau P., Audubert F., Guilhot B., Beauvy M., Benabdesselam M., Monnet I. Damages Induced by Heavy Ions in Titanium Silicon Carbide: Effects of Nuclear and Electronic Interactions at Room Temperature // J. Nucl. Mater. 2009. V. 385. № 2. P. 304–307. https://doi.org/10.1016/j.jnucmat.2008.12.018
Le Flem M., Liu X., Doriot S., Cozzika T. Irradiation damage in Ti3(Si,Al)C2: a TEM investigation // Int. J. Appl. Ceram. Technol. 2010. V. 7. № 6. P. 766–775. https://doi.org/10.1111/j.1744-7402.2010.02523.x
Whittle K.R., Blackford M.G., Aughterson R.D., Moricca S., Lumpkin G.R., Riley D.P., Zaluzec N.J. Radiation Tolerance of Mn + 1AXn Phases, Ti3AlC2 and Ti3SiC2 // Acta Mater. 2010. V. 58. № 13. P. 4362–4368. https://doi.org/10.1016/j.actamat.2010.04.029
Jovic V.D., Barsoum M.W. Electrolytic Cell and Electrodes for Use in Electrochemical Processes // Patent US 2006. 7,001,494.
Tuller H.L., Spears M.A., Mlcak R. Stable Electrical Contact for Silicon Carbide Devices: Patent US 2003. 6,544,674.
Barsoum M.W., El-Raghy T. Synthesis and Characterization of a Remarkable Ceramic Ti3SiC2// J. Am. Ceram. Soc. 1996. V. 79. № 7. P. 1953–1956. https://doi.org/10.1111/j.1151-2916.1996.tb08018.x
Luo Y.-M., Pan W., Li S., Chen J. Synthesis and Mechanical Properties of in-situ Hot Pressed Ti3SiC2 Polycrystals // Ceram. Int. 2002. V. 28. № 2. P. 227–230. https://doi.org/10.1016/S0272-8842(01)00083-9
Zhang Z.F., Sun Z.M., Hashimoto H., Abe T. Effects of Sintering Temperature and Si Content on the Purity of Ti3SiC2 Synthesized from Ti/Si/TiC Powders // J. Alloys Comp. 2003. V. 352. № 1–2. P. 283–289. https://doi.org/10.1016/S0925-8388(02)01171-4
Zhang Z.F., Sun Z.M., Hashimoto H. Rapid Synthesis of Ternary Carbide Ti3SiC2 through Pulse-Discharge Sintering Technique from Ti/Si/TiC Powders // Metall. Mater. Trans. A. 2002. V. 33. № 11. P. 3321–3328. https://doi.org/10.1007/s11661-002-0320-1
Zhang Z.F., Sun Z.M., Hashimoto H., Abe T. A New Synthesis Reaction of Ti3SiC2 through Pulse Discharge Sintering Ti/SiC/TiC Powder // Scr. Mater. 2001. V. 45. № 12. P. 1461–1467. https://doi.org/10.1016/S1359-6462(01)01184-8
Gao N.F., Li J.T., Zhang D., Miyamoto Y. Rapid Synthesis of Dense Ti3SiC2 by Spark Plasma Sintering // J. Eur. Ceram. Soc. 2002. V. 22. № 13. P. 2365–2370. https://doi.org/10.1016/S0955-2219(02)00021-3
Vadchenko S.G., Sytschev A.E., Kovalev D.Yu., Shukin A.S., Belikova A.F. SHS of MAX Compounds in the Ti–Si–C System: Influence of Mechanical Activation // Int. J. Self-Propag. High-Temp. Synth. 2014. V. 23. № 3. P. 141–144. https://doi.org/10.3103/S106138621403011X
Pampuch R., Lis J., Stobierski L., Tymkiewicz M. Solid Combustion Synthesis of Ti3SiC2 // J. Eur. Ceram. Soc. 1989. V. 5. № 5. P. 283–287. https://doi.org/10.1016/0955-2219(89)90022-8
Meng F., Liang B., Wang M. Investigation of Formation Mechanism of Ti3SiC2 by Self-Propagating High-Temperature Synthesis // Int. J. Refract. Met. Hard Mater. 2013. V. 41. P. 152–161. https://doi.org/10.1016/j.ijrmhm.2013.03.005
Riley D.P., Kisi E.H., Phelan D. SHS of Ti3SiC2: Ignition Temperature Depression by Mechanical Activation // J. Eur. Ceram. Soc. 2006. V. 26. № 6. P. 1051–1058. https://doi.org/10.1016/j.jeurceramsoc.2004.11.021
Lis J., Miyamoto Y., Pampuch R., Tanihata K. Ti3SiC2-Based Materials Prepared by HIP-SHS Techniques // Mater. Lett. 1995. V. 22. № 3–4. P. 163–168. https://doi.org/10.1016/0167-577X(94)00246-0
Gao F., Miyamoto Y., Zhang D. Dense Ti3SiC2 Prepared by Reactive HIP//J. Mater. Sci. 1999. V. 34. № 18. P. 4385–4392. https://doi.org/10.1023/A:1004664500254
Racault C., Langlais F., Naslain R. Solid-State Synthesis and Characterization of the Ternary Phase Ti3SiC2 // J. Mater. Sci. 1994. V. 29. № 13. P. 3384–3392. https://doi.org/10.1007/BF00352037
Sato F., Li J.F., Watanabe R. Reaction Synthesis of Ti3SiC2 from Mixture of Elemental Powders // Mater. Trans. JIM. 2000. V. 4. № 5. P. 605–608. https://doi.org/10.2320/matertrans1989.41.605
Li J.F., Matsuki T., Watanabe R. Combustion Reaction during Mechanical Alloying Synthesis of Ti3SiC2 Ceramics from 3Ti/Si/2C Powder Mixture // J. Am. Ceram. Soc. 2005. V. 88. № 5. P. 1318–1320. https://doi.org/10.1111/j.1551-2916.2005.00179.x
Li S.B., Zhai H.X., Zhou Y., Zhang Z.L. Synthesis of Ti3SiC2 Powders by Mechanically Activated Sintering of Elemental Powders of Ti, Si and C // Mater. Sci. Eng. A. 2005. V. 407. № 1–2. P. 315–321. https://doi.org/10.1016/j.msea.2005.07.043
Nickle J.J., Schweitzer K.K., Luxenberg P. Gasphasenabscheidung in Systeme Ti–C–Si // J. Less-Common Met. 1972. V. 26. № 3. P. 335–353. https://doi.org/10.1016/0022-5088(72)90083-5
Goto T., Hirai T. Chemically Vapor Deposited Ti3SiC2//Mater. Res. Bull. 1987. V. 22. № 9. P. 1195–1201. https://doi.org/10.1016/0025-5408(87)90128-0
Emmerlich J., Hogberg H., Sasvari S., Persson P.O.A., Hultman L., Palmquist J.P., Jansson U., Molina-Aldareguia J.M., Czigany Z. Growth of Ti3SiC2 Thin Films by Elemental Target Magnetron Sputtering // J. Appl. Phys. 2004. V. 96. № 9. P. 4817–4823. https://doi.org/10.1063/1.1790571
Arunajatesan S., Carim A.H. Synthesis of Titanium Silicon Carbide // J. Am. Ceram. Soc. 1995. V. 78. № 3. P. 667–672. https://doi.org/10.1111/j.1151-2916.1995.tb08230.x
Istomina E.I., Istomin P.V., Nadutkin A.V. Preparation of Ti3SiC2 through Reduction of Titanium Dioxide with Silicon Carbide // Inorg. Mater. 2016. V. 52. № 2. P. 134–140. https://doi.org/10.1134/S0020168516020059
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы


