Неорганические материалы, 2020, T. 56, № 2, стр. 208-213
Новые минералоподобные Gd- и B-содержащие соединения для нейтрон-захватной терапии
Л. С. Алексеева 1, *, Д. А. Пушкова 1, А. П. Горшков 1, Д. О. Савиных 1
1 Национальный исследовательский Нижегородский государственный университет им. Н.И. Лобачевского
603950 Нижний Новгород, пр. Гагарина, 23, Россия
* E-mail: golovkina_lyudmila@mail.ru
Поступила в редакцию 27.12.2018
После доработки 20.08.2019
Принята к публикации 17.09.2019
Аннотация
Методом соосаждения проведен синтез новых Gd- и B-содержащих соединений со структурами граната вида Y3 – xGdxAl2(AlO4)3 – 0.01x(BO4)0.01x и перовскита вида Y1 – xGdx(AlO3)1 – 0.01x(BO3)0.01x, где x = 0.2–1.0. Полученные соединения исследованы методами РФА и ИК-спектрометрии. Выявлено образование непрерывного ряда твердых растворов с ожидаемой структурой граната. Добиться формирования соединений со структурой перовскита не удалось. Исследование цитотоксичности полученных соединений со структурой граната показало, что они не оказывают какого-либо значительного влияния на жизнеспособность клеток крови экспериментальных животных.
ВВЕДЕНИЕ
Нейтрон-захватная терапия (НЗТ) – нетрадиционная лучевая терапия, которая объединяет низкоэнергетическое нейтронное облучение с присутствием поглощающего нейтроны вещества в раковых клетках [1, 2]. Два изотопа представляют большой интерес из-за их большого сечения захвата нейтронов: B-10 и Gd-157. В случае В-10 нерадиоактивный изотоп захватывает нейтроны и распадается на альфа-частицы и ядро лития, вызывающие необратимое повреждение клетки, в которой они находились [3]. В настоящее время, несмотря на клиническое применение B-содержащих препаратов и их эффективную и безопасную B-НЗТ [5–10], они демонстрируют низкую избирательность, и несколько исследовательских групп прилагают большие усилия для разработки новых более избирательных агентов доставки бора [11, 12].
Использование гадолиния в качестве агента для НЗТ становится все более привлекательным из-за его большого сечения захвата нейтронов (255 000 бн для Gd-157), что примерно в 65 раз больше по сравнению с сечением захвата нейтронов бором-10 [12]. В результате захвата нейтрона изотопом Gd-157 образуется возбужденный атом гадолиния-158 (158Gd*), который генерирует сложный переход внутри оболочки с большой длиной свободного пробега в тканях, электроны внутренней конверсии и, наконец, оже-электроны вместе с характерным рентгеновским излучением.
Хотя идея Gd-НЗТ была впервые сформулирована в 1980-х гг. [13, 14], остается проблема отсутствия подходящих Gd-содержащих агентов. Преимуществом является то, что несколько соединений на основе Gd обычно используются в клинической диагностике как контрастные агенты для МРТ, что делает их “идеальными” терапевтическими агентами, способными объединить НЗТ и МРТ-диагностику для улучшения персонализированного лечения пациента [15].
Принимая во внимание различные механизмы действия агентов в B- и Gd-НЗТ, довольно логично исследовать возможное преимущество объединения обоих методов.
Рассматриваются две возможные стратегии: одновременное использование двух агентов НЗТ, один из которых содержит B-10, а другой Gd-157; разработка одного агента НЗТ, содержащего как B-10, так и Gd-157. Однако в первом случае поглощение и распределение внутри опухоли могут быть различными для этих соединений. А использование соединений, содержащих одновременно B и Gd, может быть полезным для увеличения дозы облучения опухоли.
Для реализации выбранных подходов использовали кристаллический материал на основе природных минералов граната и перовскита.
Гранаты представляют собой группу минералов с общей формулой ${\text{B}}_{3}^{{2 + }}$${\text{R}}_{2}^{{3 + }}$(XO4)3. Структура граната устойчива в весьма широком диапазоне катионных замещений во всех кристаллографических позициях. Позиция катиона B2+ может быть занята катионами Mg, Fe, Mn, Ca, актиноидов и РЗЭ, позиция катиона R3+ – катионами Al, Fe, Cr, Ga, позиция X – катионами Al, Fe, Ga, Si [16–18].
Перовскиты относятся к классу сложных оксидов с общей химической формулой ABX3. Важной характеристикой перовскитов является их способность к многочисленным изоморфным замещениям как в A-, так в В-позициях. В структуре перовскита может аккумулироваться большое количество разных типов элементов в различной валентности, что приводит к возможности химического дизайна данных материалов. Позиция A может быть занята катионами щелочных, щелочноземельных и редкоземельных металлов; позиция B – катионами Cu, Co, Cr, Ni, Mn, Al, Fe, Ru, Ti, Nb, Ta, X – анионами H, OH, O, F, Cl [19–21].
Целью настоящей работы являлось получение соединений, содержащих в своем составе одновременно Gd и B, со структурами граната и перовскита и изучение их биосовместимости.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Образцы соединений со структурами граната вида Y3 – xGdxAl2(AlO4)3 – 0.01x(BO4)0.01x (x = 0.2–1.0) и перовскита вида Y1 – xGdx(AlO3)1 – 0.01x(BO3)0.01x (x = 0.2–1.0) синтезировали в виде поликристаллических порошков методом соосаждения (золь–гель-процесс). Водные растворы исходных реагентов: нитраты солей (Al(NO3)3 · 9H2O, Y(NO3)3 · 6H2O, Gd(NO3)3 · 6H2O), борную кислоту H3BO3 смешивали с гидроксидом аммония NH4OH (5%-ный водный раствор). Получали гель, который нагревали при температуре 90°С в течение суток для удаления воды. Сухой остаток последовательно нагревали при температурах 300°С в течение 3 ч, 700, 900, 1000, 1100°С в течение 8 ч на каждой стадии.
Фазообразование изучали методом рентгенофазового анализа. Для записи дифрактограмм использовали установку Shimadzu LabX XRD-6000: CuKα-излучение, λ = 1.54078 Å.
ИК-спектры поглощения образцов в виде тонких пленок на подложке KBr записывали в диапазоне 1300–400 см–1 на Фурье-спектрофотометре DIGILAB FTS 7000.
Размер частиц определяли на растровом электронном микроскопе JEOL JSM-6495 с EDS-микроанализатором Oxford Instruments INCA 350. Анализ проводили при комнатной температуре.
Исследование цитотоксичности синтезированных частиц проводили методом проточной цитометрии с использованием цельной крови мышей линии C57BL/6 в возрасте 5–6 нед. Для этого кровь гепаринизировали, а затем инкубировали с полученными составами для НЗТ в разных разведениях (37°С, 60 мин). От эритроцитов избавлялись с помощью лизирующего буфера RBC Lysis Buffer (Cat#420301, Biolegend, США), клетки разводили в буфере для окрашивания (2% BSA в фосфатно-солевом буфере) и инкубировали в растворе, содержащем йодид пропидия (1 мкг/мл, 37°С, 5 мин). Анализ клеточной суспензии проводили с помощью проточного цитометра Cytoflex S (Beckman Coulter, США), детекцию флуоресценции йодида пропидия проводили с использованием светофильтра 690/50 нм.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
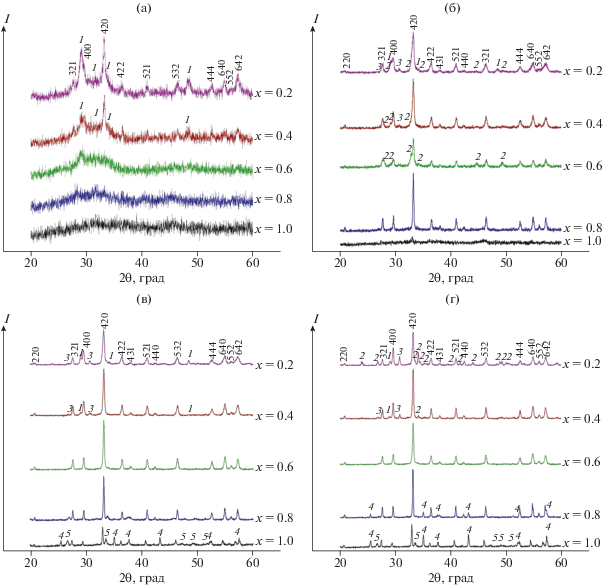
В ходе эксперимента не удалось получить соединения со структурой перовскита ряда Y1 – xGdx(AlO3)1 – 0.01x(BO3)0.01x (x = 0.2–1.0). После отжига при 700°C (рис. 1а) наблюдалось формирование фазы, изоструктурной фазе граната состава Y3Al5O12 (ICDD DataBase № 08-0178), и фазы, изоструктурной фазе оксида иттрия Y2O3 (ICDD DataBase № 05-0574), для x = 0.2 и 0.4. Остальные образцы были рентгеноаморфными. Увеличение температуры отжига до 900°C привело к увеличению кристалличности фазы граната (кроме образца с х = 1, где только начиналось ее формирование) (рис. 1б). Кроме того, наблюдались рефлексы примесных фаз: оксида иттрия Y2O3 (х = 0.2), сложного иттрий-алюминиевого оксида Y4Al2O9 (ICDD DataBase № 14-0475) (для х = 0.2 и 0.4) и гексагональной модификации перовскита YAlO3 (ICDD DataBase № 16-0219) (для х = 0.2, 0.4 и 0.6). Увеличение температуры отжига до 1000°C привело к исчезновению фазы перовскита (рис. 1в). Образец с х = 1 представлял собой фазу, изоструктурную фазе граната Y3Al5O12, с примесью Al2O3 (ICDD DataBase № 11-0661) и бората гадолиния GdBO3 (ICDD DataBase № 74-1932). Увеличение температуры отжига до 1100°C не привело к существенному изменению фазовых составов образцов с х = 0.4, 0.6 и 1 (рис. 1г). В образце с х = 0.8 наблюдалось появление примеси Al2O3, а в образце с х = 0.2 происходило образование орторомбической модификации перовскита YAlO3 (ICDD DataBase № 70-1677). Следует отметить, что дифракционные максимумы фазы граната при увеличении x смещаются в сторону меньших углов, что, по-видимому, связано с включением гадолиния в кристаллическую решетку граната.
Рис. 1.
Дифрактограммы соединений ряда Y1 – xGdx(AlO3)1 – 0.01x(BO3)0.01x (x = 0.2–1.0) после отжига при 700 (а), 900 (б), 1000 (в) и 1100°C (г): 1 – Y2O3, 2 – YAlO3, 3 – Y4Al2O9, 4 – Al2O3, 5 – GdBO3.
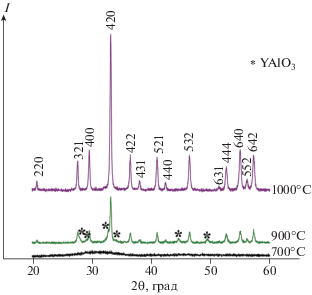
Полученные образцы граната ряда Y3 – xGdxAl2(AlO4)3 – 0.01x(BO4)0.01x (x = 0.2–1.0) представляли собой поликристаллические порошки белого цвета. По данным РФА (рис. 2), они являлись однофазными и кристаллизовались в ожидаемой структуре граната (пр. гр. Ia3d, ICDD DataBase № 79-1891). Установлено, что образование однофазного продукта происходит при 1000°C (рис. 3), однако уже при 900°C наблюдаются соответствующие пики совместно с пиками перовскита YAlO3 (ICDD DataBase № 74-1334).
Рис. 3.
Дифрактограммы соединения Y2.4Gd0.6Al2(AlO4)2.994(BO4)0.006 после нагревания при разных температурах.
На рис. 4 представлены ИК-спектры изучаемых образцов. Полосы поглощения 430 и 460 см–1 отнесены к валентным колебаниям тетраэдра [AlO4], а 720 и 790 см–1 – к валентным колебаниям октаэдра [AlO6]. Полосы поглощения 510, 570 и 690 см–1 связаны с колебаниями связи Y–O. Полосы поглощения 980, 1040 и 1080 см–1 соответствуют колебаниям связи B–O в тетраэдрах [BO4].
Из анализа данных РФА и ИК-спектрометрии следует, что бор занимает позицию Х в кристаллической решеткe граната и образует тетраэдры [BO4].
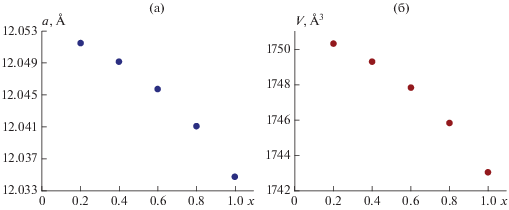
Графики, иллюстрирующие изменение параметра a и объема V элементарной ячейки исследуемых соединений, приведены на рис. 5. Установлено, что с увеличением содержания гадолиния и бора наблюдается уменьшение параметра a и объема V элементарной ячейки, что свидетельствует о существовании непрерывного ряда твердых растворов состава Y3 – xGdxAl2(AlO4)3 – 0.01x(BO4)0.01x при х = = 0.2–1.0.
Рис. 5.
Зависимости параметра a (а) и объема V (б) элементарной ячейки от состава соединений ряда Y3 –xGdxAl2(AlO4)3 – 0.01x(BO4)0.01x.
Частицы исследуемых соединений со структурой граната представляли собой легкоразушаемые агломераты (рис. 6). Минимальный размер частиц был примерно одинаковым для всех соединений и составил ~316–334 нм. Максимальный размер частиц составил 33–39 мкм.
Рис. 6.
Микрофотографии порошков соединений ряда Y3 – xGdxAl2(AlO4)3 – 0.01x(BO4)0.01x с х = 0.2 (а), 0.4 (б), 0.6 (в), 0.8 (г), 1.0 (д).

Поскольку процедура НЗТ подразумевает взаимодействие терапевтических агентов с кровью пациентов, на начальном этапе исследования изучили цитотоксический эффект полученных соединений в отношении клеток крови: нейтрофилов, лимфоцитов и моноцитов. Процент мертвых нейтрофилов составил 9.90–17.73% (10.13% – в контрольном опыте), лимфоцитов – 0.51–2.18% (0.51% – в контрольном опыте), моноцитов – 0.31–2.86% (2.86% – в контрольном опыте). Полученные результаты о биосовместимости исследуемых соединений свидетельствуют о том, что полученные частицы не оказывают какого-либо значительного влияния на жизнеспособность клеток крови экспериментальных животных в диапазоне концентраций от 0.0001 до 1 мг/мл. И даже после инкубации в самой большой концентрации (1 мг/мл) не наблюдалось каких-либо изменений в степени окрашивания клеток йодидом пропидия.
ЗАКЛЮЧЕНИЕ
Получены новые Gd- и B-содержащие соединения со структурой граната вида Y3 – xGdxAl2(AlO4)3 – 0.01x(BO4)0.01x (x = 0.2–1.0). Установлено, что образование однофазного продукта происходит при 1000°С. Методом ИК-спектрометрии установлено, что бор входит в позицию X кристаллической решетки граната и образует тетраэдры [BO4]. Непрерывное изменение параметров элементарных ячеек свидетельствует о существовании непрерывного ряда твердых растворов состава Y3 – xGdxAl2(AlO4)3 – 0.01x(BO4)0.01x при х = 0.2–1.0. Полученные соединения для НЗТ не являются токсичными в отношении клеток крови – жизнеспособность клеток после взаимодействия с ними была сопоставима с контрольными значениями.
Список литературы
Hawthorne M.F., Lee M. A Critical Assessment of Boron Target Compounds for Boron Neutron Capture Therapy // J. Neurooncol. 2003. V. 62. I. 1–2. P. 33. https://doi.org/10.1023/A:1023253309343
Hosmane N.S., Maguire J.A., Zhu Y., Takagaki M. Principles of Neutron Capture Therapy // Boron and Gadolinium Neutron Capture Therapy for Cancer Treatment. Singapore: World Scientific Publishing Company, 2012. P. 35. https://doi.org/10.1142/9789814338684_0003
Barth R.F., Coderre J.A., Vicente M.G.H., Blue T.E. Boron Neutron Capture Therapy of Cancer: Current Status and Future Prospects // Clin. Cancer Res. 2005. V. 11. № 11. P. 3987. https://doi.org/10.1158/1078-0432.CCR-05-0035
Kageji T., Nagahiro S., Mizobuchi Y. et al. Boron Neutron Capture Therapy (BNCT) for Newly Diagnosed Glioblastoma: Comparison of Clinical Results Obtained with BNCT and Conventional Treatment // J. Med. Invest. 2014. V. 61. № 3–4. P. 254. https://doi.org/10.2152/jmi.61.254
van Rij C.M., Wilhelm A.J., Sauerwein W.A., van Loenen A.C. Boron Neutron Capture Therapy for Glioblastoma Multiforme // Pharm. World Sci. 2005. V. 27. № 2. P. 92. https://doi.org/10.2217/fon.12.118
Liu Y.W., Chang C.T., Yeh L.Y. et al. BNCT Treatment Planning for Superficial and Deep-Seated Tumors: Experience from Clinical Trial of Recurrent Head and Neck Cancer at THOR // Appl. Radiat. Isot. 2015. V. 106. P. 121. https://doi.org/10.1016/j.apradiso.2015.08.002
Aihara T., Morita N., Kamitani N. et al. BNCT for Advanced or Recurrent Head and Neck Cancer // Appl. Radiat. Isot. 2014. V. 88. P. 12. https://doi.org/10.1016/j.apradiso.2014.04.007
Menéndez P.R., Roth B.M., Pereira M.D. et al. BNCT for Skin Melanoma in Extremities: Updated Argentine Clinical Results // Appl. Radiat. Isot. 2009. V. 67. P. S50. https://doi.org/10.1016/j.apradiso.2009.03.020
Zonta A., Prati U., Roveda L. et al. Clinical Lessons from the First Applications of BNCT on Unresectable Liver Metastases // J. Phys: Conf. Ser. 2006. V. 41. P. 484. https://doi.org/10.1088/1742-6596/41/1/054
Barth R.F., Vicente M.G., Harling O.K. et al. Current Status of Boron Neutron Capture Therapy of High Grade Gliomas and Recurrent Head and Neck Cancer // Radiat. Oncol. 2012. V. 7. P. 146. https://doi.org/10.1186/1748-717X-7-146
Luderer M.J., de la Puente P., Azab A.K. Advancements in Tumor Targeting Strategies for Boron Neutron Capture Therapy // Pharm. Res. 2015. V. 32. № 9. P. 2824. https://doi.org/10.1007/s11095-015-1718-y
Salt C., Lennox A.J., Takagaki M. et al. Boron and Gadolinium Neutron Capture Therapy // Russ. Chem. Bull., Int. Ed. 2004. V. 53. P. 1871. https://doi.org/10.1007/s11172-005-0045-6}
Brugger R.M., Shih J.A. Evaluation of Gadolinium-157 as a Neutron Capture Therapy Agent // Strahlenther. Onkol. 1989. V. 165. № 2–3. P. 153.
De Stasio G., Casalbore P., Pallini R. et al. Gadolinium in Human Glioblastoma Cells for Gadolinium Neutron Capture Therapy // Cancer Res. 2001. V. 61. № 10. P. 4272.
Shih J.L.A., Brugger R.M. Gadolinium as a Neutron Capture Therapy Agent // Med. Phys. 1992. V. 19. № 3. P. 733. doi.org/https://doi.org/10.1118/1.596817
Golovkina L.S., Orlova A.I., Nokhrin A.V. et al. Ceramics Based on Yttrium Aluminum Garnet Containing Nd and Sm Obtained by Spark Plasma Sintering // Ad. Ceram. Sci. Eng. (ACSE). 2013. V. 2. № 4. P. 161–165.
Potanina E., Golovkina L., Orlova A. et al. Lanthanide (Nd, Gd) Compounds with Garnet and Monazite Structures. Powders Synthesis by “Wet” Chemistry to Sintering Ceramics by Spark Plasma Sintering // J. Nucl. Mater. 2016. V. 473. P. 93. https://doi.org/10.1016/j.jnucmat.2016.02.014
Лаверов Н.П., Величкин В.И., Омельяненко Б.И. и др. Изменение окружающей среды и климата: природные и связанные с ними техногенные катастрофы. Т. 5: Изоляция отработавших ядерных материалов: геолого-геохимические основы. М.: ИГЕМ РАН, 2008. 256 с.
Pena M.A., Fierro J.L.G. Chemical Structures and Performance of Perovskite Oxides // Chem. Rev. 2001. V. 101. P. 1981–2018. https://doi.org/10.1021/cr980129f
Davies R.A., Islam M.S., Chadwick A.V., Rush G.E. Cation Dopant Sites in the CaZrO3 Proton Conductor: a Combined EXAFS and Computer Simulation Study // Solid State Ionics. 2000. V. 130. № 2. P. 115. https://doi.org/10.1016/S0167-2738(00)00573-7
Davies R.A., Islam M.S., Gale J.D. Dopant and Proton Incorporation in Perovskite-Type Zirconates // Solid State Ionics. 1999. V. 126. № 4. P. 323. https://doi.org/10.1016/S0167-2738(99)00244-1
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы




