Неорганические материалы, 2020, T. 56, № 2, стр. 214-220
О совместимости катодного материала LiCoPO4 с литийпроводящим твердым электролитом Li1.5Al0.5Ge1.5(PO4)3
Г. Б. Куншина 1, *, И. В. Бочарова 1, В. И. Иваненко 1
1 Институт химии и технологии редких элементов и минерального сырья им. И.В. Тананаева – обособленное подразделение ФИЦ “Кольский научный центр Российской академии наук”
184209 Мурманская обл., Апатиты, Академгородок, 26а, Россия
* E-mail: kunshina@chemy.kolasc.net.ru
Поступила в редакцию 10.12.2018
После доработки 24.07.2019
Принята к публикации 05.09.2019
Аннотация
Впервые изучена устойчивость электродного материала LiCoPO4 в контакте с литийпроводящим твердым электролитом со структурой NASICON состава Li1.5Al0.5Ge1.5(PO4)3 (LAGP) с широким окном электрохимической стабильности. Установлена оптимальная температура, при которой не происходит взаимодействия исходных компонентов композита и сохраняется их химическая и термическая стабильность. Совместным спеканием механической смеси синтезированных однофазных порошков LiCoPO4 и LAGP субмикронных размеров при 750°C получен устойчивый двухфазный композит LiCoPO4/LAGP, проводимость которого выше на 3 порядка проводимости двойного фосфата лития-кобальта при комнатной температуре. Композиты на основе LiCoPO4 и ионного проводника LAGP можно рассматривать в качестве перспективных катодных материалов для полностью твердотельных литий-ионных аккумуляторов.
ВВЕДЕНИЕ
В последние годы большое внимание уделяется исследованию нового класса катодных материалов для литий-ионных аккумуляторов (ЛИА) – ортофосфатов лития и переходных металлов общей формулы LiMPO4 (M = Fe, Mn, Co или Ni) со структурой оливина [1]. Фосфат лития-кобальта LiCoPO4 вызывает повышенный интерес из-за его большой теоретической емкости (167 мАч/г) и высокого окислительно-восстановительного потенциала (4.8 В относительно Li+/Li). В этой связи LiCoPO4 рассматривают в качестве перспективного 5-вольтового электродного материала для ЛИА большой мощности [2]. Существенным недостатком LiCoPO4 является низкая электронная и, главным образом, ионная проводимость (на уровне 10–8–10–10 См/см), что приводит к неудовлетворительной циклируемости при высоких скоростях заряда–разряда [3, 4]. Модификацию катодных материалов осуществляют методом гетерогенного допирования [5] или путем получения двухфазных композиций с использованием высокопроводящих твердых электролитов для повышения ионного переноса [6]. В этом качестве представляют интерес твердые электролиты со структурой NASICON, которые не разлагаются при высоком потенциале и могут применяться в твердотельных ячейках с LiCoPO4. Они обладают свойствами, необходимыми для изготовления полностью твердотельных аккумуляторов: высокой ионной проводимостью при комнатной температуре, термической и химической устойчивостью, стабильностью на воздухе [7, 8]. Использование твердых электролитов вместо органических легковоспламеняющихся жидких электролитов позволит повысить надежность, электрохимическую стабильность, циклируемость и плотность энергии полностью твердотельных перезаряжаемых ЛИА. Понимание эволюции интерфейса при совместном спекании твердых литийпроводящих электролитов и активных электродных материалов имеет решающее значение для разработки полностью твердотельных ЛИА [9].
Сложность при изготовлении полностью твердотельных ЛИА заключается в формировании стабильного ионпроводящего интерфейса между твердым электролитом и электродным материалом. Температурная обработка в виде спекания, горячего прессования или плазменно-искрового спекания, которая используется для улучшения контакта на границе раздела, может вызвать нежелательные химические реакции между электродом и электролитом с образованием непроводящих фаз [10]. Таким образом, химическая стабильность, или химическая совместимость, твердого электролита с электродными материалами является чрезвычайно важной характеристикой.
Оксидные катодные материалы (LiCoO2, LiMn2O4, LiMn0.5Ni0.5O2) деградируют в контакте с твердым электролитом состава Li1.3Al0.3Ti1.7(PO4)3 (LATP) со структурой NASICON, образуя электрохимически неактивные примесные фазы, блокирующие ионный перенос. Гораздо стабильнее в контакте с LATP фосфатные электродные материалы (LiFePO4, LiCoPO4, LiMn0.5Fe0.5PO4 и Li3V2(PO4)3) [11, 12]. Для формирования улучшенного электрического контакта LiCoPO4 с LATP авторы [13] применили процесс плазменно-искрового спекания (SPS). По результатам рентгенофазового анализа, LiCoPO4 не разрушается в контакте с LATP в процессе SPS. Нами разработан способ получения композитного материала на основе LiCoPO4, модифицированного твердым электролитом LATP. Способ заключается в пропитке порошков LiCoPO4 насыщенным раствором-прекурсором LATP с последующей сушкой и спеканием при 700°C с образованием двухфазного композита [14]. Ионная проводимость композита LiCoPO4/LATP значительно выше по сравнению с проводимостью исходного фосфата лития-кобальта.
Твердый электролит Li1.5Al0.5Ge1.5(PO4)3(LAGP) по сравнению с изоструктурным LATP обладает широким окном электрохимической стабильности (до 6 В относительно Li+/Li) и низкой температурой спекания керамики (~850°C) [15, 16]. В недавно опубликованной работе [16] изучена химическая и фазовая стабильность LAGP с 3 типами катодных материалов (LiNi0.8Co0.15Al0.05O2, LiNi0.5Mn1.5O4 и Li3V2(PO4)3) в температурном интервале 500–700°C. Как и следовало ожидать, оксидные катодные материалы неустойчивы в контакте с LAGP. Данных об устойчивости твердого электролита LAGP в контакте с фосфатными электродными материалами в литературе приводится немного [17–20] и нет сведений о композитах состава LiCoPO4/LAGP. Авторами [17] изучено влияние состава композитных электродов LiFePO4/LAGP и Li3V2PO4/LAGP на электрохимические характеристики полностью твердотельных элементов LiFePO4/LAGP/Li3V2PO4. Здесь частицы твердого электролита LAGP размещались в матрице активных материалов обоих электродов (LiFePO4 и Li3V2(PO4)3), при этом оптимальное содержание электролита составляло 60% LAGP [18].
Цель настоящей работы заключалась в исследовании устойчивости двойного фосфата лития-кобальта LiCoPO4 в контакте с твердым электролитом LAGP, возможности получения модифицированных электродных материалов на основе LiCoPO4 с высокой ионной проводимостью для использования в полностью твердотельных ЛИА.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Однофазные порошки LAGP (не содержащие непроводящих примесей GeP2O7 и GeO2) получали из жидкофазного прекурсора [21, 22]. В качестве водорастворимого германийсодержащего компонента готовили германощавелевую кислоту H2[Ge(C2O4)3] растворением GeO2 гексагональной модификации (ОСТ 48-21-72) в концентрированном растворе H2C2O4. О существовании комплексного иона [Gе(С2О4)3]2–, в котором германий октаэдрически окружен тремя оксалатными группами, сообщают авторы [23]. К полученному устойчивому раствору германощавелевой кислоты H2[Ge(C2O4)3] добавляли в соответствии со стехиометрией водные растворы LiNO3 ∙ 3H2O, Al(NO3)3 ∙ 9H2O и (NH4)2HPO4. Далее раствор (плотностью 1.15 г/см3, содержащий 38–40 г/л в пересчете на LAGP) нагревали в муфельной печи МИМП-3П с программным управлением со скоростью 10°С/мин. В ходе выпаривания сиропообразный раствор разлагался при температуре 300°С с образованием вспененной массы, что обусловлено разложением нитратов и оксалатов. В ИК-спектре прекурсора LAGP после выпаривания при 280–300°C отсутствовали полосы поглощения при 1736 и 1401 см–1, которые относятся к валентным колебаниям оксалат-иона, что может свидетельствовать о разложении оксалатного комплекса германия с образованием оксида германия в реакционно-активном состоянии. Последующее твердофазное взаимодействие протекало с образованием целевого продукта LAGP при температуре 650°С в одну стадию без промежуточных соединений. Таким образом, способ подготовки исходной шихты с переводом всех исходных компонентов в раствор и формированием объединенного истинного раствора существенно влияет на механизм последующего твердофазного взаимодействия. Преимущество синтеза германофосфата лития-алюминия заключается в том, что после разложения оксалатного комплекса GeO2 образуется в активном аморфном состоянии.
Однофазные порошки LiCoPO4 стехиометрического состава были получены золь–гель-методом из водных растворов [24]. В гидратированном прекурсоре состава CoHPO4 ∙ aq протоны гидрофосфат-иона обладают повышенной подвижностью и способны к замещению на ионы лития с образованием LiCoPO4 ∙ aq. При термической обработке гидратированного фосфата кобальта-лития происходят дегидратация и образование аморфного порошка при температуре 200–300°С, далее при температуре 505–535°С завершается кристаллизация LiCoPO4.
Химический состав LAGP и композитов анализировали методом атомно-эмиссионной спектрометрии с индуктивно связанной плазмой на спектрометре ICPE-9000 (Shimadzu, Япония). Пробы для анализа готовили разложением в смеси кислот (HNO3, HF, H2SO4). Близкие значения химического состава для LAGP из разных партий свидетельствуют о том, что процедура синтеза дает воспроизводимые результаты (табл. 1).
Таблица 1.
Химический состав Li1.5Al0.5Ge1.5(PO4)3
| Образец | Содержание, мас. % | |||
|---|---|---|---|---|
| Li | Al | Ge | P | |
| Li1.5Al0.5Ge1.5(PO4)3 (теор.) | 2.49 | 3.23 | 26.07 | 22.24 |
| 1 | 2.70 | 2.85 | 24.70 | 22.40 |
| 2 | 2.80 | 2.90 | 25.50 | 21.90 |
| 3 | 2.70 | 2.60 | 25.50 | 22.40 |
| 4 | 2.75 | 2.90 | 25.10 | 21.70 |
Фазовый состав порошков LAGP и модифицированных электродных материалов определяли с использованием рентгеновского дифрактометра XRD-6000 Shimadzu (СuKα-излучение, графитовый монохроматор). Съемку проводили в диапазоне углов 2θ 10°–80° со скоростью вращения гониометра 2 град/мин. При расшифровке рентгенограмм использовали базу данных ICDD PDF-2.
Проводимость твердого электролита LAGP и композитов LiCoPO4/LAGP изучали методом импедансной спектроскопии. Импеданс Z(ω) определяют как общее сопротивление ячейки протеканию переменного тока на заданной частоте и представляют в виде комплексного числа, что графически изображается на векторной плоскости в координатах Z', Z" в виде годографа или спектра импеданса [25]. Дисперсию комплексного импеданса образцов исследовали в диапазоне частот переменного тока 102–2 × 106 Гц с амплитудой переменного сигнала 50 мВ. Измерения проводили по двухэлектродной схеме импедансметром Z-2000 (Elins, Россия) в ячейке зажимной конструкции.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
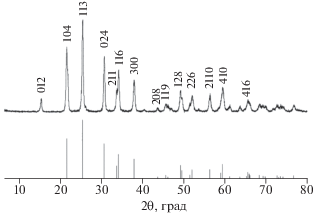
Рентгенограмма синтезированного порошка LAGP после спекания при температуре 650°С представлена на рис. 1. Идентификацию Al-замещенных образцов выполняли в соответствии с рефлексами LiGe2(PO4)3 (ICDD 80-1924), т.к. частичное замещение в структуре LiGe2(PO4)3 катионов Ge4+ на Al3+ с близкими ионными радиусами приводит к образованию твердых растворов Li1 + xAlxGe2 – x(PO4)3 в интервале 0.1 < x < 0.6 и не изменяет фазового состава получаемых материалов [22]. Синтез LAGP из жидкофазного прекурсора обеспечивал получение однофазного продукта, не содержащего примесных фаз.
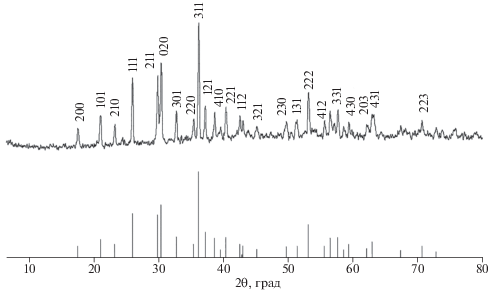
На рис. 2 представлена рентгенограмма синтезированного золь–гель-методом однофазного порошка LiCoPO4 (ICDD 89-6192) после термообработки при температуре 800°C.
Композитные образцы получали в виде механической смеси порошков LiCoPO4 и твердого электролита LAGP разного состава (25, 50 и 60% LAGP). К навеске порошка LiCoPO4 добавляли рассчитанную навеску LAGP, тщательно измельчали в агатовой ступке до получения однородной смеси, прессовали таблетку усилием 100 МПа и помещали ее в муфельную печь МИМП-3П. Деформация таблеток после спекания не наблюдалась.
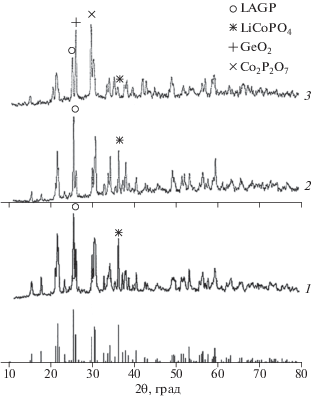
На рис. 3 представлены дифрактограммы механической смеси LiCoPO4 + LAGP до и после термической обработки в интервале 750–800°C. По данным РФА, после нагревания при 750°C с изотермической выдержкой в течение 2 ч смеси LiCoPO4 + LAGP (в соотношении 1 : 1) в виде прессованной таблетки на воздухе на рентгенограмме 2 (рис. 3) не было обнаружено никаких дополнительных пиков, помимо рефлексов исходных LiCoPO4 и LAGP. Эти результаты указывают на то, что оба соединения сохраняют кристаллическую структуру и фазовый состав без изменений после температурной обработки при 750°C. Дальнейшее повышение температуры спекания композита до 800°C с изотермической выдержкой в течение 2 ч показало, что начинается взаимодействие между компонентами с образованием новых фаз (тесный контакт в прессованной таблетке композита способствует взаимодействию компонентов). На рентгенограмме 3 смеси после спекания при 800°C (рис. 3) происходит изменение соотношения между интенсивностями дифракционных пиков по сравнению с рентгенограммой 2. В результате на рентгенограмме 3 кроме LAGP четко идентифицируются новые фазы: пирофосфат кобальта Co2P2O7 (ICDD 84-2126) и GeO2 (ICDD 85-1515). При 2θ = 29.8° появляется рефлекс с максимальной интенсивностью, который соответствует Co2P2O7. Значительно возрастает интенсивность рефлекса при 2θ = 26.2°, который соответствует GeO2. При этом практически исчезает пик в интервале 2θ = 36.2°, относящийся к LiCoPO4, что свидетельствует о разложении соединения. Таким образом, установлено, что при нагревании на воздухе выше 750°C химическая и термическая стабильность исходных компонентов смеси не сохраняется, происходит их взаимодействие с образованием непроводящих фаз.
Рис. 3.
Дифрактограммы механической смеси LiCoPO4 + + LAGP (1 : 1) до (1) и после нагревания на воздухе при 750 (2), 800°C (3) в течение 2 ч (символами обозначены рефлексы с максимальной (100%) интенсивностью).
Измерения проводимости LAGP и композитов были выполнены в экранированной ячейке зажимной конструкции на таблетках диаметром 10–12 и толщиной 1–2 мм, на торцы которых после спекания графитовые электроды в виде тонкого слоя наносили грифелем карандаша. Теоретическая плотность композитов была рассчитана как линейная комбинация 2 фаз по формуле:
где ρ1 и ρ2 – теоретические плотности фаз, составляющих композит, N1 и N2 – массовые доли фаз.В табл. 2 представлены значения проводимости LAGP и композитов разного состава, которые рассчитывали по формуле:
где h – высота таблетки, S – площадь контакта, R – сопротивление таблетки, определенное по годографу импеданса.Таблица 2.
Характеристики композитов LiCoPO4/LAGP при 20°С
| Состав | Условия спекания | Плотность, г/см3 | h, см | S, см2 | R, Ом | σ, См/см | ||
|---|---|---|---|---|---|---|---|---|
| t,oC | τ, ч | ρрасч | ρизмер | |||||
| 25% LAGP | 750 | 2 | 3.67 | 2.73 (74%) | 0.172 | 0.998 | 350 000 | 4.8 × 10–7 |
| 50% LAGP | 700 | 2 | 3.59 | 2.35 (65%) | 0.160 | 1.123 | 40 000 | 3.5 × 10–6 |
| 50% LAGP | 750 | 2 | 3.59 | 2.92 (81%) | 0.151 | 0.955 | 10 000 | 1.6 × 10–5 |
| 60% LAGP | 750 | 2 | 3.55 | 2.7 (76%) | 0.155 | 0.994 | 6100 | 2.6 × 10–5 |
| 60% LAGP | 750 | 10 | 3.55 | 2.86 (81%) | 0.160 | 0.936 | 6000 | 2.8 × 10–5 |
| LAGP | 900 | 6 | 3.41 | 3.03 (89%) | 0.161 | 0.826 | 1300 | 1.5 × 10–4 |
| LiCoPO4 | 800 | 1 | 3.76 | 2.64 (70%) | 0.215 | 1.075 | ‒ | 10–8–10–10* |
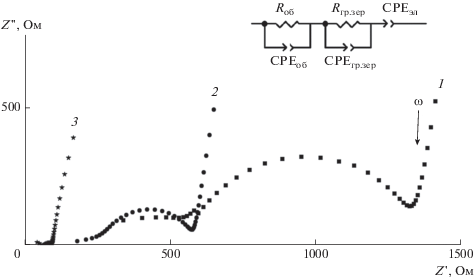
На рис. 4 показаны годографы импеданса (комплексного сопротивления переменному току) LAGP, измеренные в интервале 25–92°С. Зависимость Z" = f(Z') для LAGP при комнатной температуре представляет собой две последовательные полуокружности на высоких и средних частотах, которые приписывают сопротивлению зерен (Rоб) и зернограничному сопротивлению (Rгр. зер) соответственно, и прямую линию в низкочастотной области спектра. Спектр импеданса может быть смоделирован эквивалентной схемой, состоящей из двух последовательно соединенных (R, СРЕ) контуров, один из которых связан с объемом зерен (Rоб, СРЕоб), а другой – с границей зерен (Rгр. зер, СРЕгр. зер). Суммарный диаметр указанных полуокружностей соответствует общему сопротивлению образца. При повышении температуры измерения годографы смещаются к началу координат, при этом суммарный диаметр двух полуокружностей значительно уменьшается, что свидетельствует о повышении проводимости образца. Так, с ростом температуры от 25 до 92°C удельная ионная проводимость увеличивается с 1.5 × 10–4 до 2 × 10–3 См/см.
Рис. 4.
Годографы импеданса LAGP при различной температуре: 1 – 25, 2 – 42, 3 – 92°C; на вставке – эквивалентная электрическая схема.
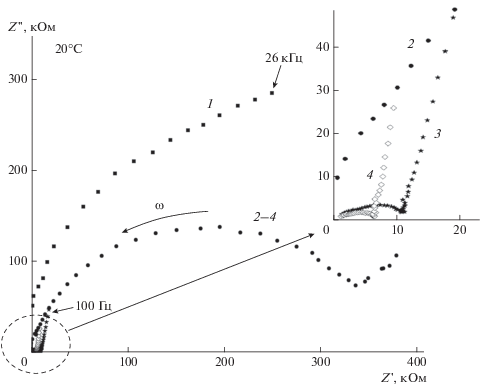
На рис. 5 показаны годографы импеданса исходного LiCoPO4 (1) и композитов LiCoPO4/LAGP разного состава (2–4), полученных спеканием в одинаковых условиях (при 750°С в течение 2 ч). В соответствии со спектром электрохимического импеданса композиты LiCoPO4/LATP характеризуются повышенной ионной проводимостью в сравнении с исходным LiCoPO4. По мере увеличения содержания LAGP в композитах общая проводимость повышается на 2–3 порядка и составляет для композита оптимального состава (60% LAGP) 2.6 × × 10–5 См/см (табл. 2).
Рис. 5.
Годографы импеданса исходного LiCoPO4 (1) и композитов LiCoPO4/LATP после спекания при 750°С с различным содержанием LAGP (2 – 25%, 3 – 50%, 4 – 60%); на вставке – зависимость комплексного сопротивления композитов LiCoPO4/LAGP в высокочастотном диапазоне.
Таким образом, композиты на основе LiCoPO4 и ионного проводника LAGP можно рассматривать в качестве перспективных катодных материалов для полностью твердотельных ЛИА. Окончательное заключение о принципиальной возможности использования композитов LiCoPO4/LAGP в ЛИА можно сделать после проведения циклирования материалов на испытательных стендах.
ЗАКЛЮЧЕНИЕ
Изучена устойчивость катодного материала LiCoPO4 при нагревании в контакте с твердым электролитом LAGP с высокой проводимостью по иону Li+. Установлена оптимальная температура (750°C), при которой не происходит взаимодействия исходных компонентов и сохраняется их химическая и термическая стабильность.
Показано, что совместным спеканием механической смеси исходных порошков при температуре 750°C можно получать композитные электродные материалы, ионная проводимость которых (при содержании ионного проводника LAGP 60%) повышается до 2.6 × 10–5 См/см.
Список литературы
Кулова Т.Л., Скундин А.М. Высоковольтовые материалы положительных электродов литий-ионных аккумуляторов (Обзор) // Электрохимия. 2016. Т. 52. № 6. С. 563–588.
Prabu M., Selvasekarapandian S., Kulkarni A.R. et al. Ionic Transport Properties of LiCoPO4 Cathode Material // Solid State Sci. 2011. V. 13. P. 1714–1718.
Harada R., Aso K., Hayashi A., Tatsumisago M. Preparation of Composites with LiCoPO4 Electrode and LiTi2(PO4)3 Electrolyte for Bulk-type All-solid-state Lithium Batteries // Electrochemistry. 2015. V. 83. № 10. P. 898–901.
Allen J.L., Thompson T., Sakamoto J. et al. Transport Properties of LiCoPO4 and Fe-substituted LiCoPO4 // J. Power Sources. 2014. V. 254. P. 204–208.
Svitan’ko A., Scopets V., Novikova S., Yaroslavtsev A. The Effect of Composite Formation with Oxides on the Ion Conductivity of NASICON-Type LiTi2(PO4)3 and Olivine-Type LiFePO4 // Solid State Ionics. 2015. V. 271. P. 42–47.
Svitan’ko A.I., Novikova S.A., Kulova T.L., Skundin A.M., Yaroslavtsev A.B. An Improvement in the Ionic Conductivity and Electrochemical Characteristics of LiFePO4 by Heterogeneous Doping with NASICON-Type Phosphate // Mendeleev Commun. 2015. V. 25. P. 207–208.
Ren Y., Chen K., Chen R. et al. Oxide Electrolytes for Lithium Batteries // J. Am. Ceram. Soc. 2015. V. 98. P. 3603–3623.
Jian Z., Hu Y.-S., Ji X., Chen W. NASICON-Structured Materials for Energy Storage // Adv. Mater. 2017. V. 29. № 20. P. 1601925.
Deiner L.J., Howell T.G., Koenig G.M., Rottmayer M.A. Interfacial Reaction During Co-Sintering of Lithium Manganese Nickel Oxide and Lithium Aluminum Germanium Phosphate // Int. J. Appl. Ceram. Technol. 2019. V. 16. P. 1659–1667.
Nagata K., Nanno T. All Solid Battery with Phosphate Compounds Made through Sintering Process // J. Power Sources. 2007. V. 174. P. 832–837.
Gellert M., Dashjav E., Grüner D. et al. Compatibility Study of Oxide and Olivine Cathode Materials with Lithium Aluminum Titanium Phosphate // Ionics. 2018. V. 24. № 4. P. 1001–1006. https://doi.org/10.1007/s11581-017-2276-6
Yu S., Mertens A., Tempel H., Schierholz R., Kungl H., Eichel R.-A. Monolithic All-Phosphate Solid-State Lithium-Ion Battery with Improved Interfacial Compatibility // ACS Appl. Mater. Interfaces. 2018. V. 10. P. 22264–22277.
Okumura T., Takeuchi T., Kobayashi H. Application of LiCoPO4 Positive Electrode Material in All-Solid-State Lithium-Ion Battery // Electrochemistry. 2014. V. 82. № 10. P. 906–908.
Куншина Г.Б., Иваненко В.И., Громов О.Г., Локшин Э.П. Получение электродного материала, модифицированного литийпроводящим твердым электролитом // Журн. неорган. химии. 2014. Т. 59. № 10. С. 1415–1419.
Feng J.K., Lu L., Lai M.O. Lithium Storage Capability of Lithium Ion Conductor Li1.5Al0.5Ge1.5(PO4)3 // J. Alloys Compd. 2010. V. 501. P. 255–258.
Liu Y., Chen J., Gao J. Preparation and Chemical Compatibility of Lithium Aluminum Germanium Phosphate Solid Electrolyte // Solid State Ionics. 2018. V. 318. P. 27–34.
Delaizir G., Viallet V., Aboulaich A. et al. The Stone Age Revisited: Building a Monolithic Inorganic Lithium-Ion Battery // Adv. Funct. Mater. 2012. V. 22. P. 2140–2147.
Aboulaich A., Bouchet R., Delaizir G. et al. A New Approach to Develop Safe All-Inorganic Monolithic Li-Ion Batteries // Adv. Energy Mater. 2011. V. 1. P. 179–183.
Kubanska A., Castro L., Tortet L. et al. Effect of Composite Electrode Thickness on the Electrochemical Performances of All-Solid-State Li-ion Batteries // J. Electroceram. 2017. V. 38. № 2–4. P. 189–196.
Robinson J.P., Kichambare P.D., Deiner J.L. et al. High Temperature Electrode-Electrolyte Interface Formation between LiMn1.5Ni0.5O4 and Li1.4Al0.4Ge1.6(PO4)3 // J. Am. Ceram. Soc. 2018. V. 101. № 3. P. 1087–1094.
Куншина Г.Б., Бочарова И.В., Локшин Э.П. Синтез и исследование проводимости твердого электролита Li1.5Al0.5Ge1.5(PO4)3 // Неорган. материалы. 2016. Т. 52. № 3. С. 320–326.
Kunshina G.B., Bocharova I.V., Ivanenko V.I. Preparation of the Li1.5Al0.5Ge1.5(PO4)3 Solid Electrolyte with High Ionic Conductivity // Inorg. Mater: Appl. Res. 2017. V. 8. № 2. P. 238–244.
Тананаев И.В., Авдуевская К.А. Исследование взаимодействия в системе GeO2–H2C2O4–H2O при 25°С // ЖНХ. 1958. Т. 3. № 9. С. 2172–2177.
Иваненко В.И., Аксенова С.В., Локшин Э.П. и др. Синтез монофазных наноразмерных порошков двойных фосфатов переходных металлов // Тр. Кольского науч. центра РАН. 2015. № 31. С. 354–358.
Гнеденков С.В., Синебрюхов С.Л. Импедансная спектроскопия в исследовании процессов переноса заряда // Вестн. ДВО РАН. 2006. № 5. С. 6–16.
Rissouli K., Benkhouja K., Ramos-Barrado J.R., Julien C. Electrical Conductivity in Lithium Orthophosphates // Mater. Sci. Eng. B. 2003. V. 98. № 3. P. 185–189.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы