Неорганические материалы, 2020, T. 56, № 2, стр. 165-172
Структурные преобразования TiO2 при механоактивации и последующем отжиге
Ю. В. Кузьмич 1, Л. Г. Герасимова 1, *, Е. С. Щукина 1
1 Институт химии и технологии редких элементов и минерального сырья им. И.В. Тананаева – обособленное подразделение ФИЦ “Кольский научный центр Российской академии наук”
184209 Мурманской обл., Апатиты, Академгородок, 26а, Россия
* E-mail: gerasimova@chemy.kolasc.net.ru
Поступила в редакцию 11.03.2019
После доработки 13.09.2019
Принята к публикации 17.09.2019
Аннотация
Показано, что метастабильная структура диоксида титана анатазной модификации является благоприятной основой для направленного воздействия на нее с формированием новых оксидных фаз с наноразмерными частицами и, соответственно, новым набором свойств. Механоактивация и последующий отжиг активированных порошков позволяют осуществить цепочку фазовых преобразований (анатаз–брукит–рутил) и тем самым упорядочить структуру диоксида титана. Трансформация оксидных титановых фаз изучена с использованием рентгеновского дифракционного анализа. По уширению дифракционных рефлексов методом аппроксимации с применением функции псевдо-Фойгта найдены размер кристаллитов (ОКР) и микродеформации (ε). После механоактивации размер частиц составляет в среднем 20 нм, а после термообработки увеличивается почти в два раза. Аналогичная зависимость характерна и для величин микронапряжений. Поровая система частиц представлена мезопорами. Наличие петли гистерезиса на изотерме сорбции–десорбции азота свидетельствует о пластинчатой морфологии частиц диоксида титана. Результаты исследований использованы для разработки инновационной технологии специальной марки диоксида титана, предназначенной для получения термостойких клеев с диэлектрическими свойствами и высокими показателями по устойчивости к разрыву и сдвигу.
ВВЕДЕНИЕ
Неорганические соединения с М–О-связями интересны как с научной, так и практической точек зрения. Свойства таких соединений в значительной степени определяются их структурой и ее стабильностью. В частности, четырехзарядный диоксид титана существует в виде трех структурных разновидностей: стабильного рутила и метастабильных анатаза и брукита [1–3]. Основой структур этих модификаций являются октаэдры TiO6, которые расположены таким образом, что каждый ион кислорода принадлежит трем октаэдрам. Однако на один октаэдр в рутиле приходится 2 общих ребра, в анатазе – 4, в бруките – 8. Этот факт влияет на прочность связи кислорода с титаном в кристаллической решетке. Рутил практически не обладает свойствами фотокатализатора, но является диэлектриком и устойчив к атмосферным воздействиям и повышенной температуре. Благодаря такому сочетанию свойств рутил используется в качестве базового пигмента при изготовлении косметики, специальных лакокрасочных материалов для ответственных покрытий, эксплуатируемых в экстремальных условиях, в том числе Арктики, и вводится в состав терморегулируемых клеев и герметиков, используемых в аэрокосмической отрасли [2].
Термодинамическая устойчивость кристаллитов диоксида титана определяется размером частиц. Так, при размере частиц менее 14 нм анатаз более устойчив, чем рутил [4, 5]. Если нанокристаллический диоксид титана нагревать, то рост кристаллов приводит к изменению фазовой стабильности и, в конечном счете, превращению анатаза и брукита в рутил. Однако до сих пор отсутствуют достоверные данные о том, какова последовательность превращений в ходе трансформации фаз: брукит в анатаз или наоборот [6]. Эффективное использование нанокристаллических частиц требует изучения размера кристаллитов, который определяется по размеру областей когерентного рассеяния (ОКР) [7–10].
Как правило, свойства TiO2 формируются в процессе синтеза. Многие из известных методов синтеза (золь–гель, сонохимические и микроволновые, гидротермальные, гидрохимические) сопряжены с определенными трудностями в их реализации, поскольку основаны на процессах, протекающих в жидкофазном режиме с образованием значительного количества стоков, требующих затрат на их утилизацию. Способы, основанные на твердофазных процессах, протекающих при высокоэнергетическом воздействии на систему, позволяют устранить названные недостатки [11].
Целью настоящей работы является изучение твердофазных реакций в процессе механоактивации (МА) и термолиза метастабильных оксотитановых фаз, а также их структурных и морфологических характеристик.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Метастабильное состояние любой системы, в частности системы анатаз–рутил, – благоприятная основа для направленного воздействия на нее для формирования новых фаз с заданным размером частиц и, соответственно, новым набором свойств. В качестве эффективных факторов воздействия выбрана комбинация из двух последовательных методов обработки: МА и отжига порошков.
В результате высокоэнергетического воздействия достигается уменьшение размера частиц до нанометрового масштаба c одновременным ростом микродеформаций кристаллической решетки. При последующем отжиге удается упорядочить активированную механическим воздействием структуру частиц порошка.
Исходным объектом исследования служил порошок диоксида титана анатазной модификации, который получали из двойной титановой соли (NH4)2TiO(SO4)2 ∙ H2O [12]. Соль прокаливали в электрической муфельной печи при температуре 700°С в течение 4 ч. Скорость нагревания до заданной температуры – 10°С/мин. Полученный порошок помещали в футерованные титаном барабаны шаровой планетарной мельницы Pulverisette-7 объемом 45 мл. Измельчающие элементы – титановые шары диаметром 10 мм. Скорость вращения рабочих сосудов 750 об./мин. Массовое отношение шары : порошок = 10 : 1. Продолжительность обработки 2 ч. При проведении экспериментов по измельчению диоксида титана в указанных условиях отмечено налипание плотного слоя продукта на стенки барабанов мельницы. Для устранения этого недостатка измельчение проводили в присутствии ПАВ – олеиновой кислоты, количество которой варьировали в пределах от 1 до 4 мас. %. По окончании измельчения активированный порошок подвергали отжигу при 850°С в течение 3 ч.
Исходные, механоактивированные и прокаленные образцы изучались с помощью химических и физико-химических методов. В частности, фазовый состав устанавливали с помощью дифрактометра Shimadzu XRD 6000. Съемку рентгенограмм проводили в условиях пошагового сканирования с шагом 0.1° в пределах от 6° до 110°. Несмотря на доступность сбора данных методом рентгеновской дифрактометрии, существует значительная трудность при расшифровке получаемой информации. В данной работе использовалось программное обеспечение, разработанное на основе метода Rietveld [13–15], которое позволяет с достаточной степенью точности, путем подгонки профиля рефлексов дифрактограмм, идентифицировать фазы и осуществить оценку размеров ОКР, микронапряжений (ε) и проследить ход трансформации фаз нанокристаллических частиц TiO2. Микроструктурные характеристики исследованы с использованием “дубль-Фойгт”-методологии, в которой профили дифракции как ОКР, так и на микроискажениях обобщенно описываются функциями Фойгта. Для разделения вкладов в уширение пиков от ОКР использовали функцию Лоренца, от микронапряжений – функцию Гаусса.
В результате проведенных вычислений для каждого рефлекса дифрактограммы рассчитаны уширения, амплитуды и углы. Полученные данные были использованы для расчета размера наночастиц, который совпадает в данном случае с ОКР [16]. В работе [14] подробно описан расчет размера кристаллитов и микродеформаций. Так, уширение находили по выражению β*(2θ) = = β(2θ)cosθ/λ. Учитывая факт, что экспериментальное уширение представляет собой суперпозицию двух уширений – размерного βs и деформационного βd, можно путем построения зависимости приведенного уширения от вектора рассеяния (s = = 2sinθ/λ) и экстраполяции уширения на нулевое значение вектора рассеяния определить размер кристаллита D = 1/β*(2θ = 0). Микродеформацию ε устанавливали по наклону зависимости приведенного уширения βd(2θ) = 4εtgθ, ε = Δd/d, где Δd – изменение межплоскостного расстояния. Удельную поверхность и объем пор определяли на приборе TriStar 3020 Micromeritics (США) по показателям сорбции–десорбции азота.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
По результатам рентгеновского дифракционного анализа (рис. 1, 2) удалось установить характер изменения фазового состава диоксида титана при его МА и последующем отжиге полученного порошка.
Рис. 1.
Дифрактограммы исходного анатаза (1) и образцов после его МА при скорости 750 об./мин и продолжительности 2 ч с добавкой 1 (2), 2.5 (3), 4 мас. % ПАВ (4).
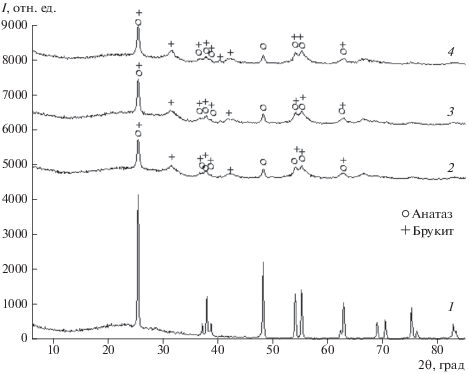
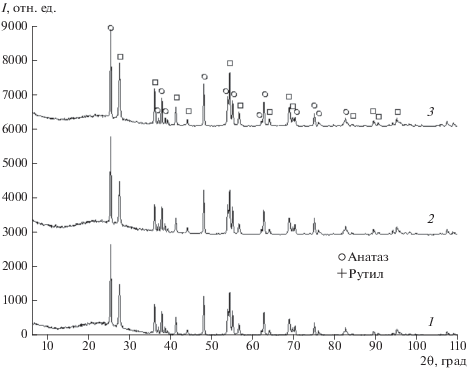
Рис. 2.
Дифрактограммы образцов с добавкой 1 (1), 2.5 (2), 4 мас. % ПАВ (3) после МА и отжига при 850°С в течение 3 ч.
Влияние механического воздействия на частицы анатаза с заданной добавкой ПАВ (1–4 мас. %) проявляется в снижении интенсивности рефлексов на дифрактограммах, а также в появлении нового рефлекса, характерного для фазы брукита. Из-за существенной величины уширения рефлексов и их углового смещения идентификация фаз оказалась затруднительной. В частности, рефлексы анатаза 101 и брукита 120, 111 перекрываются, поэтому фазу брукита идентифицировали по другим рефлексам, например 002.
Отжиг порошков после МА при 850°С приводит к повышению кристалличности порошков с параллельным преобразованием нестабильной фазы брукита в анатаз и рутил.
Количественный анализ уширения рефлексов показал, что в зависимости от условий проведения МА размер частиц различных фаз диоксида титана изменяется в соответствии с изменением показателя микронапряжения. Оценка размера ОКР была проведена с использованием метода Вильямсона–Холла [17, 18] с разделением размерных и деформационных уширений. Расчеты, сделанные для построения зависимостей приведенного уширения от величины вектора рассеяния, позволили оценить изменение ОКР и микродеформационные подвижки. Зависимости приведенного уширения от величины вектора рассеяния представлены на рис. 3 и 4. Результаты расчета размера ОКР и величины микронапряжений приведены в табл. 1. Уравнение линии позволяет рассчитать размер ОКР при экстраполяции на нулевое значение вектора рассеяния: ОКР = 1/β*(2θ). По тангенсу угла наклона линии (в данном случае tg(θ) = 0.0002) рассчитана микродеформация: βd(2θ) = 4ε tg θ [19].
Рис. 3.
Зависимость приведенного уширения от величины вектора рассеяния анатаза до МА (линия тренда построена по расчетным данным).
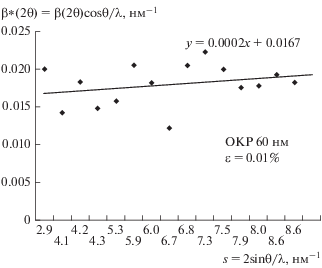
Рис. 4.
Зависимости приведенного уширения от величины вектора рассеяния анатаза (а) и рутила (б): 750 об./мин, 2 ч, с добавкой 4 мас. % ПАВ; последующий отжиг при 850°С в течение 3 ч.
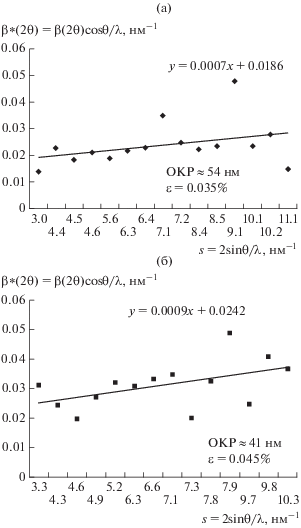
Таблица 1.
ОКР и микронапряжения исследуемых образцов с добавкой 1, 2.5 и 4 мас. % ПАВ
| Образец | ОКР, нм | ε, % | ОКР, нм | ε, % | ОКР, нм | ε, % |
|---|---|---|---|---|---|---|
| 1 | 2.5 | 4 | ||||
| Без отжига | ||||||
| Анатаз | 27 | 0.30 | 25 | 0.22 | 21 | 0.24 |
| Брукит | 21 | 1.14 | 21 | 0.58 | 14 | 0.52 |
| Отжиг при 850оС, 3 ч | ||||||
| Анатаз | 51 | 0.01 | 56 | 0.02 | 54 | 0.035 |
| Рутил | 33 | 0.03 | 37 | 0.015 | 41 | 0.045 |
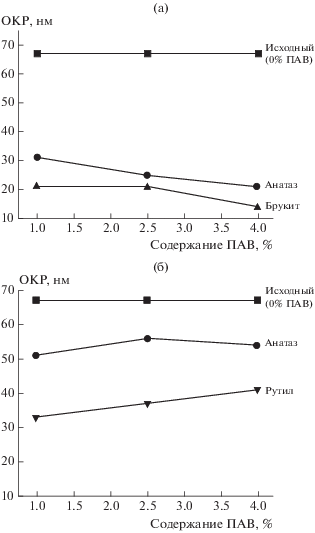
Отмечено, что после МА величина микронапряжения достаточно высокая: для анатаза ε ~ ~ 0.24–0.30%, для брукита ε ~ 0.52–1.14% (табл. 1). В образце после МА идентифицированы три фазовые модификации диоксида титана. У всех трех модификаций ОКР существенно больше (30–60 нм) по сравнению с ОКР МА-образца. Отжиг образцов диоксида титана приводит к снижению величины микронапряжений в кристаллитах. Зависимость размера ОКР от количества добавки ПАВ приведена на рис. 5.
Рис. 5.
Зависимости ОКР фаз диоксида титана после МА при скорости 750 об./мин от содержания ПАВ: а – без отжига активированных порошков, б – с отжигом порошков при температуре 850°С.
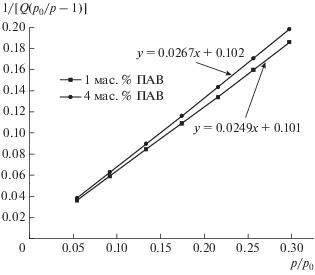
Для определения удельной поверхности образцов и объема пор использовали метод БЭТ [20, 21]. Изучаемые объекты содержат весь спектр нанопор: микропоры (<2 нм), мезопоры (2–50 нм) и макропоры (>50 нм) [22]. Фактические измерения были проведены в области, характерной для мезо- и макропор. Изотермы адсорбции–десорбции азота для образцов диоксида титана (рис. 6), построенные с использованием метода БЭТ, позволяют охарактеризовать их по классификации IUPAC [22] как тип IVa в области значений р/р0 от 0.1 до 0.95, при р/р0 > 0.95 изотермы относятся к типу II. Для описания изотерм используют линейное уравнение [22]
Рис. 6.
Изотермы адсорбции–десорбции образцов диоксида титана после МА: 750 об./мин, 2 ч; отжиг при 850°С, 3 ч (пунктирная линия при добавке ПАВ 1 мас. %, сплошная – 4 мас. %).
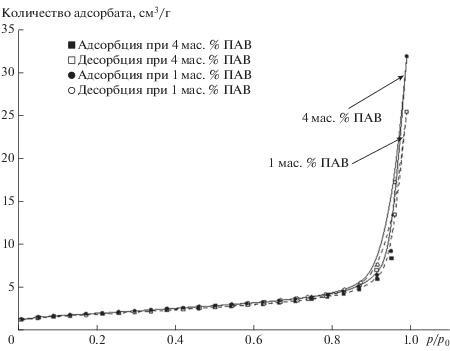
У обоих образцов в начале изотермы (рис. 6) отсутствует выраженное “колено” (точка В), что объясняется наличием многослойной адсорбции, маскирующей начальный однослойный процесс. Характерное отличие от традиционных изотерм [23] – линейность графика – соблюдается в интервале р/р0 от 0.05 до 0.55. В области относительных давлений выше диапазона линейности изотерма приобретает резкую крутизну, что является признаком узкого распределения мезопор по размеру.
Петля гистерезиса на изотермах обоих образцов относится к типу Н3. Петли подобного типа [22] отличаются следующими особенностями: ветвь адсорбции напоминает изотерму типа II; нижний предел ветви десорбции находится в кавитационно-индуцированном интервале значений относительного давления, что характерно для пластинчатых частиц с мезо- и макропорами. Характер петли гистерезиса позволяет утверждать, что исследуемые частицы диоксида титана после МА имеют пластинчатую структуру, что подтверждает данные, полученные нами ранее [24].
Резкий рост изотермы в области петли гистерезиса (0.8 < р/р0 < 1.0) объясняется большой внешней поверхностью и наличием значительной мезопористости, началом поровой конденсации в крупных порах. Если отсутствует влияние стенок пор и краевых эффектов (мезопоры, близкие к размеру 50 нм, и макропоры) на частицы адсорбата (азот), то сорбция происходит по типу многослойного покрытия площади. На это также указывает отсутствие плато после верхнего края петли гистерезиса, поры заполняются без образования полусферического мениска, продолжается многослойная конденсация, как на беспористой поверхности.
При всех прочих равных параметрах процесса МА количество введенного ПАВ оказывает следующее влияние на сорбционную емкость продукта: при добавке 1 мас. % удельная адсорбция при р/р0 = 1 достигает 25.5 см3/г, а при 4 мас. % – 31.9 см3/г.
График БЭТ линеен в диапазоне относительных давлений от 0.05 до 0.30 (рис. 7). Это позволяет утверждать, что в данном случае расчет удельной поверхности образцов после МА проведен с достаточной достоверностью (табл. 2).
Таблица 2.
Результаты исследования методом БЭТ образцов после МА и отжига
| ПАВ, мас. % | 1 | 2.5 | 4 |
| Удельная площадь поверхности (одноточечный метод) при р/р0 = 0.297, м2/г | 6.5414 | 7.5971 | 6.975 |
| Удельная площадь поверхности (многоточечный метод) при р/р0 = 0.05–0.3, м2/г | 6.6317 | 7.7233 | 7.0925 |
| Средняя ширина пор адсорбции, нм | 7.84 | 7.71 | 8.06 |
| Общий объем адсорбирующих пор с диаметром менее 39–41 нм при р/р0 = 0.297 (одноточечный метод), см3/г | 0.013 | 0.015 | 0.014 |
В табл. 3 приведены показатели образца рутила, полученного по методике, разработанной с учетом полученных результатов. Свойства рутила определялись в соответствии с ТУ 2321-001-04694196-2016 для диоксида титана марки ТРК.
Таблица 3.
Физико-технические свойства диоксида титана
| Образец | Опытный образeц | ТУ 2321-001-04694196-2016 |
|---|---|---|
| Массовая доля диоксида титана, % | 96.9 | Не менее 96% |
| Массовая доля рутильной формы, % | 95 | Не менее 95% |
| Массовая доля веществ, растворимых в воде, % | 0.28 | Не более 0.3% |
| Массовая доля летучих веществ, % | 0.45 | Не более 0.5% |
| рН водной суспензии | 6.8 | 6.5–7.5 |
| Остаток на сите с сеткой 0045, % | 0.09 | Не более 0.1 |
| Масляное число, мл/100 г | 29 | 25–35 |
| Удельная поверхность, м2/г | 6.86 | 6.5–7.5 |
| Общий объем пор, см3/г | 0.0155 | 0.015–0.017 |
Опытный образец использовали для получения клеев специального назначения. Получены положительные результаты по регламентируемым показателям: устойчивость к разрыву и сдвигу. Технология защищена патентом на изобретение [25].
ЗАКЛЮЧЕНИЕ
Показано, что метастабильное состояние структуры диоксида титана анатазной модификации является благоприятной основой для направленного воздействия на нее с целью формирования новых оксидных фаз с заданным размером частиц и новым набором свойств.
Выбранная авторами комбинация такого воздействия на твердофазную систему – МА с помощью планетарной мельницы (скорость вращения барабана 750 об./мин в течение 1 ч) и отжиг активированных порошков (температура 850°С, 3 ч) – позволила установить механизм фазовых переходов.
Показано, что в ходе МА анатаза происходит диспергирование его частиц до нанометрических размеров с одновременным ростом микродеформаций кристаллической решетки. При отжиге удается упорядочить структуру порошка, активированную механическим воздействием.
Трансформация оксидных титановых фаз изучена с использованием результатов рентгеновского дифракционного анализа. После МА в образцах идентифицированы две фазы – анатаз и брукит. После отжига порошки состоят преимущественно из рутила, брукит отсутствует, количество анатаза не превышает 5–10%. По уширению дифракционных рефлексов методом аппроксимации с применением функции псевдо-Фойгта найдены размеры кристаллитов (ОКР) и величины микродеформаций (ε). После МА и отжига величина ОКР частиц в среднем составляет 40 нм, без отжига – 20 нм. Такая же зависимость характерна и для величины микронапряжения. С увеличением расхода ПАВ размер частиц уменьшается.
При изучении поверхностных свойств титановых фаз методом БЭТ установлено, что после МА в присутствии ПАВ адсорбция азота описывается изотермой типа IVa в области значений р/р0 от 0.1 до 0.95, при р/р0 > 0.95 изотермы относятся к типу II. Петля гистерезиса изотерм образцов относится к типу Н3, что характерно для частиц с пластинчатой морфологией. Пористая система частиц представлена мезопорами с диаметром 20–50 нм.
Результаты исследований использованы для разработки инновационной технологии специальной марки диоксида титана, предназначенной для получения термостойких клеев с диэлектрическими свойствами и высокими регламентируемыми показателями по устойчивости к разрыву и сдвигу.
Список литературы
Guoma P.I., Mills M.J. Anatase-to-Rutile Transformation in Titania Powders // J. Am. Ceram. Soc. 2001. V. 84. № 3. P. 619–622. https://doi.org/10.1111/j.1151-2916.2001.tb00709
Salari M., Rezaee M., Mousavikoie S.M., Marashi P., Aboutalebi H. Effect of Milling Time on Mechanochemical Synthesis of TiO2 Nanoparticles // Int. J. Modern Phys. B. 2008. V. 22. № 18, 19. P. 2955–2961. https://doi.org/10.1142/S0217979208047808
Muscat J., Swamy V., Harrison N.M. First-Principles Calculations of the Phase Stability of TiO2 // Phys. Rev. B. 2002. V. 65. 224112. P. 224112-1–224112-15. https://doi.org/10.1103/PhysRevB.65.224112
Zhang H., Banfield J.F. Thermodynamic Analysis of Phase Stability of Nanocrystalline Titania // J. Mater. Chem. 1998. V. 8. № 9. P. 2073–2076. https://doi.org/10.1039/A802619J
Lu H.M., Zhang W.X., Jiang Q. Phase Stability of Nanoanatase // Adv. Eng. Mater. 2003. V. 5. № 11. P. 787–788. https://doi.org/10.1002/adem.200300359
Zhang H., Banfield J.F. Understanding Polymorphic Phase Transformation Behavior During Growth of Nanocrystalline Aggregates: Insights from TiO2 // J. Phys. Chem. B. 2000. V. 104. № 15. P. 3481–3487. https://doi.org/10.1021/jp000499j
Cheng P., Zheng M., Jin Y., Huang Q., Gu M. Preparation and Characterization of Silica-Doped Titania Photocatalyst Through Sol–Gel Method // Mater. Lett. 2003. V. 57. № 20. P. 2989–2994. https://doi.org/10.1016/S0167-577X(02)01409-X
Li Y., White T.J., Lim S.H. Low-Temperature Synthesis and Microstructural Control of Titania Nano-Particles // J. Solid State Chem. 2004. V. 177. № 4–5. P. 1372–1381. https://doi.org/10.1016/j.jssc.2003.11.016
Li G.L., Wang G.H. Synthesis of Nanometer-Sized TiO2 Particles by a Microemulsion Method // Nanostruct. Mater. 1999. V. 11. № 5. P. 663–668. https://doi.org/10.1016/s0965-9773(99)00354-2
Tavangarian F., Emadi R. Mechanochemical Synthesis of Single Phase Nanocrystalline Forsterite Powder // Int. J. Modern Phys. B. 2010. V. 24. № 3. P. 343–350. https://doi.org/10.1142/S0217979210053987
Raiender G., Giri P.K. Strain Induced Phase Formation, Microstructural Evolution and Bandgap Narrowing in Strained TiO2 Nanocrystals Grown by Ball Milling // J. Alloys Comp. 2016. V. 676. P. 591–600. https://doi.org/10.1016/j.jallcom.2016.03.154
Герасимова Л.Г., Маслова М.В., Щукина Е.С. Технология сфенового концентрата с получением титановых солей // Хим. технология. 2008. № 6. С. 241–244.
Rietveld H. A Profile Refinement Method for Nuclear and Magnetic Structures // J. Appl. Crystallogr. 1969. V. 2. № 2. P. 65–71.
Кожевникова Н.С., Курлов А.С., Урицкая А.А., Ремпель А.А. Дифракционный анализ размера нанокристаллических частиц сульфидов свинца и кадмия, полученных методом химического осаждения из водных растворов // Журн. структурной химии. 2004. Т. 45. № 7. С. 156–161.
Курлов А.С., Гусев А.И. Определение размера частиц, микронапряжений и степени негомогенности в наноструктурированных веществах методом рентгеновской дифракции // Физика и химия стекла. 2007. Т. 33. № 3. С. 383–392.
Валеева А.А., Петровых К.А., Шретнер Х., Ремпель А.А. Влияние состава монооксида титана на размер наночастиц при фрагментации // Неорган. материалы. 2015. Т. 51. № 11. С. 1221–1227.
Williamson G.K., Hall W.H. X-ray Line Broadening from Fild Aluminium and Wolfram // Acta Metall. 1953. V. 1. № 1. P. 22–31.
Mingming Wei, Li Zhang, Yongqiang Xiong, Jinhua Li, Ping’an Peng Nanopore Structure Characterization for Organic-Rich Shale Using the Non-Local-Density Functional Theory by a Combination of N2 and CO2 Adsorption // Microporous Mesoporous Mater. 2016. V. 227. P. 88–94. https://doi.org/10.1016/j.micromeso.2016.02.050
Курлов А.С., Гусев А.И. Размер частиц нанокристаллических порошков как функция параметров механического размола // Письма в ЖТФ. 2007. Вып. 19. Т. 33. С. 46–54.
Lowell S., Shields J.E., Thomas M.A., Thommes M. Characterization of Porous Solids and Powders: Surface Area, Pore Size and Density. Dordrecht: Kluwer, 2004. 350 p.
Brunauer S., Emmett P.H., Teller E. Adsorption of Gases in Multimolecular Layers // J. Am. Chem. Soc. 1938. V. 60. № 2. P. 309–319.
Thommes M., Kaneko K., Neimark A.V., Olivier J.P., Rodriguez-Reinoso F., Rouquerol J., Sing K.S.W. Physisorption of Gases, with Special Reference to the Evaluation of Surface Area and Pore Size Distribution (IUPAC Technical Report) // Pure Appl. Chem. 2015. V. 87. № 9–10. P. 1051–1069. https://doi.org/10.1515/pac-2014-1117
Вячеславов А.С., Ефремова М. Определение площади поверхности и пористости материалов методом сорбции газов (Методическая разработка). М.: Изд-во МГУ, 2011. 65 с.
Кузьмич Ю.В., Герасимова Л.Г. Влияние мелющей среды на ход фазовой трансформации анатаза в рутил // Всерос. науч. конф. с международным участием, посвященная 60-летию ИХТРЭМС ФИЦ КНЦ РАН, Исследования и разработки в области химии и технологии функциональных материалов: Тр. КНЦ РАН. Ч. 1. Апатиты, 2018. С. 315–318.
Герасимова Л.Г., Кузьмич Ю.В., Николаев А.И., Щукина Е.С., Киселев Ю.Г. Способ получения диоксида титана: Патент 2613509 РФ. Б.И. 2017. № 8.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы