Неорганические материалы, 2020, T. 56, № 4, стр. 378-384
Модифицированные мезопористые материалы МСМ-48 и их сорбционная способность по отношению к ионам цветных металлов
Т. Д. Батуева 1, *, Н. Б. Кондрашова 1, М. Г. Щербань 2
1 Институт технической химии Уральского отделения Российской академии наук – филиал Пермского федерального исследовательского центра УрО Российской академии наук
614013 Пермь, ул. Королева, 3, Россия
2 Пермский государственный национальный исследовательский университет
614990 Пермь, ул. Букирева, 15, Россия
* E-mail: tdbatueva@mail.ru
Поступила в редакцию 07.09.2018
После доработки 19.11.2019
Принята к публикации 19.11.2019
Аннотация
Синтезированы сорбенты на основе кремнеземов со структурой пор MCM-48, модифицированные гидразидными и амидными группами на основе фракций трет-карбоновых кислот Versatic. Определены текстурно-структурные свойства исследуемых кремнеземов. Изучена кинетика сорбции Cu(II), Ni(II), Co(II) из водных растворов полученными реагентами, определена зависимость сорбционной способности реагентов от способа модификации кремнеземной основы и концентрации модификатора при совместной сорбции металлов. Показана возможность разделения исследуемых цветных металлов полученными реагентами.
ВВЕДЕНИЕ
Мезопористые кремнеземы представляют несомненный интерес для ученых, занимающихся поисковыми исследованиями в области материаловедения. Это обусловлено тем, что данные материалы благодаря значительной площади поверхности (>1000 м2/г) и упорядоченной структуре мезопор обладают значительными преимуществами в каталитических и сорбционных процессах по сравнению с другими кремнеземами. Мезопористые кремнеземные материалы могут найти применение при очистке сточных вод, очистке воздуха внутри помещений, как наноструктурные “хозяин-гость”-соединения и сорбенты, обладающие способностью группового извлечения ионов металлов, а также их выделения из растворов сложного состава.
В течение последних лет изучено множество мезопористых кремнеземов (SBA-15, SBA-16, MCM-41, MCM-48 и т.д.) с широким диапазоном геометрии пор (гексагональной, кубической и т.д.) и установлено, что химическое модифицирование их поверхности способствует значительному улучшению сорбционных характеристик [1–3].
Использование для модифицирования поверхности аморфного диоксида кремния с высокими текстурными характеристиками гидразидов и амидов, полученных из фракций трет-карбоновых кислот Versatic, позволит проводить концентрирование микрокомпонентов из больших объемов растворов на относительно небольшой массе сорбента и не использовать при этом органические растворители.
Целью данной работы является изучение влияния модификации поверхности мезопористого диоксида кремния MCM-48 гидразидными и амидными функциональными группами на их текстурно-структурные характеристики, форму и размер частиц, а также сорбционные свойства по отношению к соединениям никеля(II), кобальта(II), меди(II).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Кремнеземную основу сорбентов со структурой пор MCM-48 получали методом темплатного синтеза в гидротермальных условиях при температуре выдержки 120°С в течение 2 суток [4]. В качестве источника кремния использовали тетраэтоксисилан (TEOS), в качестве структурообразующего агента – бромид цетилтриметиламмония (CTAB). Компоненты синтеза брали в следующих соотношениях: 1TEOS : 0.44 СTAB : 0.4NaOH : 100H2O.
Модификацию поверхности мезопористых кремнеземов проводили двумя способами: методом пропитки (ПP) диоксида кремния со структурой MCM-48 (образцы ПP-ДМГД, ПP-ДБА), а также в процессе гидротермального синтеза (ГС) кремнезeмной основы (образцы ГС-ДМГД, ГС-ДБА), где ДМГД и ДБА – N',N'-диметилгидразиды и N',N'-дибутиламиды соответственно – на основе фракций трет-карбоновых кислот CH3R1R2CC(O)ОH Versatic (R1 и R2 – алкильные радикалы, сумма атомов углерода равна 10).
Получение сорбентов ПP-ДМГД и ПP-ДБА осуществлялось при кипячении с обратным холодильником смеси кремнеземной основы (MCM-48) и модифицирующего агента – диметилгидразида либо дибутиламида – в различных мольных соотношениях в среде неполярного растворителя (гексана) в течение 4 ч.
Синтез сорбентов ГС-ДМГД и ГС-ДБА проводили по следующей схеме. Растворяли темплат (CTAB) в водном растворе NaOH при перемешивании на магнитной мешалке, затем добавляли источник диоксида кремния – TEOS. После образования золя SiO2 вводили модифицирующий агент – диметилгидразид либо дибутиламид. Смесь выдерживали в гидротермальных условиях при температуре 120°С в течение 48 ч. Темплат удаляли экстракцией этиловым спиртом, затем образцы сушили при температуре 80°С.
Структуру модифицированных кремнеземных сорбентов исследовали методом ИК-спектроскопии на ИК-Фурье-спектрометре IFS – 66/S (Bruker, Германия) в области 150–4000 см–1 при комнатной температуре; число сканирований 100, разрешающая способность 2 см–1.
Текстурные показатели сорбентов (удельную поверхность, объем и диаметр пор, распределение пор по размерам) определяли низкотемпературной сорбцией азота (при t = –196°С) на приборе ASAP 2020 (Micromeritics, США) после дегазации исследуемого материала в вакууме при температуре 90°С в течение 3 ч.
Сорбционные свойства полученных реагентов исследовали следующим образом. К 100 мл раствора с определенным значением рН, содержащего только ионы меди(II) или совместно ионы Cu(II), Ni(II), Co(II), вносили 0.2 г модифицированного кремнезема. Через 20 мин в водной фазе определяли остаточное содержание ионов металлов на атомно-абсорбционном спектрометре SOLAAR iCE 3500 с пламенной атомизацией (Thermo Ficher Scientific, США). Титры стандартных растворов сульфатов меди(II), никеля(II), кобальта(II) устанавливали также на атомно-абсорбционном спектрометре SOLAAR iCE 3500. Для создания необходимого рН добавляли хлороводородную кислоту или аммиак соответствующей концентрации.
Величину статической сорбционной емкости по металлу (ЕМ, моль/г), степень извлечения (Е, %), коэффициент распределения (D, л/г) и коэффициент разделения β рассчитывали по следующим формулам с погрешностью не более 5%:
где С0 – концентрация металла в исходном растворе, моль/л; Ср– остаточная равновесная концентрация извлекаемого металла в растворе, моль/л; V – объем раствора, л; m – масса навески сорбента, г.Термодинамические характеристики адсорбционных равновесий – предельную адсорбцию сорбента (Γ∞, моль/г) и константу адсорбционного равновесия (К) – рассчитывали путем линеаризации изотермы Ленгмюра [5]:
(5)
$\Gamma = {{\Gamma }_{\infty }}{{KC} \mathord{\left/ {\vphantom {{KC} {{\text{(}}1 + KC{\text{)}},}}} \right. \kern-0em} {{\text{(}}1 + KC{\text{)}},}}$(6)
${C \mathord{\left/ {\vphantom {C \Gamma }} \right. \kern-0em} \Gamma } = {{\text{1}} \mathord{\left/ {\vphantom {{\text{1}} {{\text{(}}K{{\Gamma }_{\infty }}{\text{)}}}}} \right. \kern-0em} {{\text{(}}K{{\Gamma }_{\infty }}{\text{)}}}}{\text{ + }}{C \mathord{\left/ {\vphantom {C {{{\Gamma }_{\infty }}}}} \right. \kern-0em} {{{\Gamma }_{\infty }}}},$Морфологию поверхности сорбентов исследовали с помощью сканирующего электронного микроскопа FEI Quanta 650FEA. Поверхность образцов сканировалась при увеличении в 1500 раз.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Исследование структуры кремнеземной основы методом РФА в малоугловой области 2θ = = 1.4°–10° продемонстрировало наличие на рентгенограмме диоксида кремния малоугловых рефлексов 211, 220, 420, 332 и др., что подтверждает кубическую организацию пор (MCM-48) полученного материала. Методом РФА установлено, что модификация кремнезема MCM-48 гидразидными и амидными группами приводит к разупорядочению пористой структуры.
По результатам исследований, проведенных методом ИК-спектроскопии, можно предположить, что в процессе модификации кремнеземной основы, скорее всего, происходит взаимодействие кремнеземной матрицы с модифицирующими объектами с образованием, как минимум, водородных связей и ассоциатов. На это указывают снижение интенсивности полосы 3900–2900 см–1 и появление полос 3252, 1523, 1469–1488 см–1, соответствующих деформационным и валентным колебаниям NH-, CN-, C=N-групп.
Исследование текстурных характеристик кремнеземной основы MCM-48 показало, что изотермы сорбции образца имеют форму, характерную для организованных мезопористых структур (IV тип в соответствии с классификацией IUPAC) – изотермы с четко выраженной областью капиллярной конденсации азота. Адсорбционная и десорбционная ветви практически совпадают, что свидетельствует о высокой степени упорядоченности структуры сорбента.
Исследования текстурно-структурных свойств сорбентов, проведенные методами низкотемпературной сорбции азота, продемонстрировали, что образцы представляют собой мезопористый материал с достаточно развитой удельной поверхностью (до 1420 м2/г). Модифицирование приводит к уменьшению удельной поверхности сорбентов и снижению степени их дисперсности.
Из данных СЭМ (рис. 1) следует, что диоксид кремния со структурой пор MCM-48 имеет сферическую форму частиц размером 100–500 нм (рис. 1а). Частицы кремнеземного сорбента, модифицированного диметилгидразидом (ПР-ДМГД), имеют форму многогранников с несколько бóльшим размером частиц (рис. 1б). В образце диоксида кремния, модифицированного дибутиламидом (ПР-ДБА), можно наблюдать агломераты частиц различной формы и размеров (рис. 1в).
Из данных термогравиметрического (ТГМ) анализа были определены значения энергии активации, характеризующие прочность связи носителя с функциональными группами сорбента (табл. 1). Увеличение диаметра зерен сорбента и, как следствие, снижение удельной поверхности незначительно снижают сорбируемость металлов, а также скорость сорбционного процесса. Рост температуры активирует десорбционный процесс, что согласуется с данными [5].
Таблица 1.
Значения энергий активации образцов ГС-ДМГД, ПР-ДМГД, ПР-ДБА, ГС-ДБА
| Сорбент | ГС-ДМГД | ПР-ДМГД | ПР-ДБА | ГС-ДБА |
|---|---|---|---|---|
| Ea, Дж/моль | 34.8 | 63.3 | 58.2 | 55.6 |
| t, °С | 120–215 | 130–225 | 100–200 | 103–200 |
Учитывая высокое содержание функциональных групп (13–22 ммоль/г) [6] в составе модифицированных образцов, способных образовывать с ионом-комплексообразователем шестичленные хелатные циклы, можно сделать вывод о перспективности использования этих материалов в качестве эффективных сорбентов для концентрирования, разделения и извлечения ионов цветных металлов из сложных смесей.
Так как синтезированные образцы планируется использовать в качестве сорбентов для очистки сточных вод, исследована адсорбционная способность полученных сорбентов по отношению к ионам никеля(II), кобальта(II), меди(II).
Количество извлекаемого металла зависит от условий адсорбции: кислотности среды и времени контакта сорбента с раствором, поэтому прежде всего изучали зависимость величины адсорбции от этих факторов.
Пористая структура материала может в значительной степени влиять на кинетику адсорбции. При адсорбции на пористых материалах появляется стадия переноса вещества внутри пор, для которой характерен, главным образом, диффузионный механизм. Часто эта стадия определяет время установления адсорбционного равновесия. Механизм адсорбции в адсорбентах, размеры пор которых соизмеримы с размерами адсорбируемых молекул, существенно отличается от механизма адсорбции на крупнопористых адсорбентах. Адсорбция в микро- и мезопорах не сопровождается образованием адсорбционных слоев, а происходит путем объемного заполнения адсорбционного пространства [7].
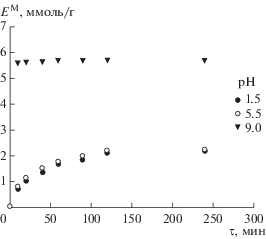
На рис. 2 приведены кинетические зависимости извлечения ионов кобальта модифицированными сорбентами. Адсорбция в щелочной среде протекала практически мгновенно, что позволило предположить химический характер адсорбции. Зависимости адсорбции от времени при рН 1.1 и 1.5 линеаризовались в координатах F = f(τ1/2) с коэффициентами корреляции соответственно 0.996 и 0.998, что указывает на то, что лимитирующей стадией процесса адсорбции является внутренняя диффузия [8]. С переходом рН от 1.5 до 5.5 константа скорости возрастает с 0.098 до 0.104 ммоль/(г мин0.5).
Исследования показали, что медь извлекается сорбентом MCM-48 только в щелочной среде. Максимальная степень предельной адсорбции достигается в течение нескольких минут. Адсорбция кобальта и никеля достигает предельных значений в кислой и нейтральной средах в течение 60 мин, а в щелочной среде в течение 20 мин.
Применение метода атомно-абсорбционной спектроскопии для контроля содержания ионов металлов в равновесных растворах в процессе сорбции позволило изучить сорбцию ионов переходных металлов при совместном присутствии и учесть их взаимное влияние на процесс сорбции.
Поскольку полученные сорбенты предполагается использовать также для решения производственных задач, была исследована сорбционная способность металлов на кремнеземных сорбентах ПР-ДМГД, где соотношение ДМГД : SiO2 = 0.05, 0.1, 0.2 и 0.4. Результаты исследований приведены в табл. 2. Видно, что наилучшие показатели емкости сорбентов по металлам наблюдаются в образцах при соотношении ДМГД : SiO2 = 0.1–0.2. Сравнительная оценка сорбционной емкости сорбентов ПР-ДМГД (табл. 2) с немодифицированным SiO2 показывает, что модифицирование поверхности МСМ-48 N',N'-диметилгидразидом кислот Versatic делает возможным отделение кобальта от никеля и меди при их совместном присутствии в интервале рН 0.8–4.
Таблица 2.
Сорбционная емкость сорбентов ПР-ДМГД при различных соотношениях SiO2/ДМГД
| Металл | EМ, ммоль/г | ||
|---|---|---|---|
| SiO2 : ДМГД = 1 : 0.05(992)*/1 : 0.1(555)*/1 : 0.2(214)* | |||
| рН 0.8 | рН 4.1 | рН 10.3 | |
| Сo | 0.28/0.3/0.43 | 0.41/0.38/0.45 | 3.99/3.92/4.07 |
| Ni | 0/0/0 | 0.01/0/0 | 2.57/2.61/2.65 |
| Cu | 0 /0/0 | 0/0.09/0.07 | 3.53/3.56/3.71 |
Способ модификации поверхности мезопористых кремнеземов также существенно влияет на степень извлечения металлов. На примере образцов ПР-ДМГД, ПР-ДБА, ГС-ДМГД, ГС-ДБА и немодифицированного диоксида кремния (MCM-48) изучена зависимость сорбционной емкости различных сорбентов (табл. 3, 4; рис. 3) по отношению к ионам меди(II), никеля(II), кобальта(II) при их совместном присутствии в зависимости от рН среды. Определено, что наибольшей сорбционной способностью обладают кремнеземные сорбенты ПР-ДМГД.
Таблица 3.
Зависимость сорбционной емкости образцов МСМ-48, ПР-ДМГД, ПР-ДБА по отношению к ионам меди(II), никеля(II), кобальта(II) от рН среды (mсорб = 0.02 г, Vколб = 10 мл)
| рН | ЕМ ,ммоль/г | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Cu | Ni | Co | |||||||
| МСМ-48 | ПР-ДМГД | ПР-ДБА | МСМ-48 | ПР-ДМГД | ПР-ДБА | МСМ-48 | ПР-ДМГД | ПР-ДБА | |
| 1.03 | 0 | 1.41 | 0.20 | 0.39 | 1.25 | 1.85 | 0.50 | 6.42 | 6.93 |
| 4.58 | 0 | 1.77 | 2.26 | 0.30 | 1.40 | 2.09 | 0.40 | 6.37 | 6.92 |
| 8.20 | 3.10 | 3.98 | 3.84 | 1.85 | 3.37 | 3.62 | 1.70 | 8.09 | 8.24 |
Таблица 4.
Зависимость сорбционной емкости образов МСМ-48, ГС-ДМГД, ГС-ДБА по отношению к ионам меди(II), никеля(II), кобальта(II) от рН среды (mсорб = 0.200 г, Vколб = 100 мл)
| рН | ЕМ, ммоль/г | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Cu | Ni | Co | |||||||
| МСМ-48 | ГС-ДМГД | ГС-ДБА | МСМ-48 | ГС-ДМГД | ГС-ДБА | МСМ-48 | ГС-ДМГД | ГС-ДБА | |
| 5.20 | 0 | 0.45 | 2.60 | 0.3 | 0 | 2.12 | 0.40 | 4.90 | 6.69 |
| 1.07 | 0 | 0.30 | 1.34 | 0.39 | 0.12 | 0.87 | 0.50 | 5.30 | 6.35 |
| 8.10 | 3.10 | 3.51 | 3.92 | 1.85 | 1.73 | 3.22 | 1.70 | 6.63 | 7.90 |
Рис. 3.
Влияние рН раствора и способа синтеза на извлечение (R) модифицированных силикатных материалов: а – ГС-ДМГД, б – ПP-ДМГД, в – ГС-ДБА, г – ПP-ДБА (mсорб = 0.200 г, Vколб = 100 мл, СМ(исх) = 0.1 моль/л).
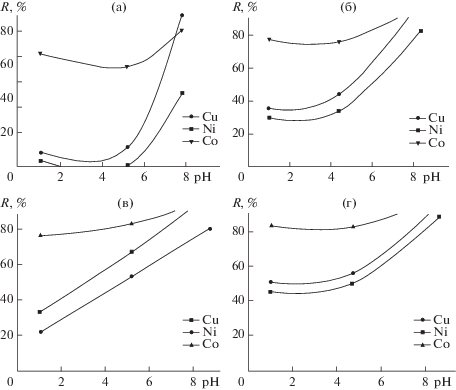
Полученные данные позволяют говорить о возможности извлечения с высокой эффективностью из растворов всех трех цветных металлов. Все три образца – МСМ-48, ПР-ДМГД, ПР-ДБА – извлекают ионы никеля(II), кобальта(II), меди(II) из растворов при переходе от слабокислых к сильнощелочным растворам. Качественные закономерности адсорбции ионов металлов от рН среды для ГС-ДМГД и ГС-ДБА одинаковы. Максимальное извлечение происходит в нейтрально-щелочных средах.
Метод ПР увеличивает сорбционную способность модифицированного материала в большей степени, чем метод ГС. Из данных, представленных на рис. 3, следует, что из трех металлов при совместном присутствии в наибольшей степени извлекается кобальт(II), который может быть выделен из раствора, содержащего все три иона. При этом интервал рН его извлечения становится шире по сравнению с сорбентами, модифицированными в процессе ГС, и составляет 1.5–6.0.
С целью использования сорбентов для высокотемпературной сорбции изучено влияние температуры на сорбцию металлов полученными модифицированными кремнеземами. Температурную зависимость степени извлечения от рН изучали при 20-минутном контакте сорбента с исследуемым раствором, основываясь на данных о кинетике сорбционного процесса, полученных ранее.
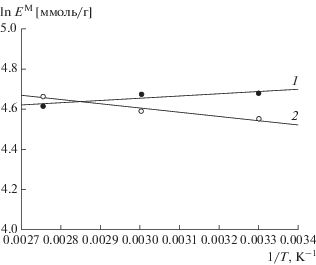
В общем случае с ростом температуры в области низких и средних значений рН сорбционная емкость уменьшается, что свидетельствует о протекании физической адсорбции. На рис. 4 приведена зависимость ln EМ – 1/T для МСМ-48 и ПР-ДМГД. Видно, что на исходном сорбенте в области высоких значений рН адсорбция протекает за счет физического взаимодействия. Ситуация меняется, когда возможно образование комплексных соединений ионов цветных металлов с ДМГД-группами. Изменяется знак тангенса угла наклона зависимости ln EМ – 1/T (рис. 4), т.е. с ростом температуры адсорбция возрастает. Это возможно в том случае, если на поверхности протекает химическая реакция [5].
ЗАКЛЮЧЕНИЕ
В работе изучено влияние способа модифицирования поверхности мезопористого диоксида кремния гидразидными и амидными группами на его структурные и адсорбционные свойства. Показано, что присутствие модификатора приводит к уменьшению удельной поверхности сорбентов. Определено, что метод пропитки увеличивает сорбционную способность в большей степени, чем метод гидротермального синтеза кремнеземов модифицированными гидразидными группами. Установлено, что процесс адсорбции при рН 1.5 и 5.5 лимитируется стадией внутренней диффузии. При рН 8 ионы меди и кобальта химически адсорбируются поверхностью модифицированного МСМ-48.
Проведенное комплексное исследование позволило выбрать оптимальные условия взаимодействия ионов металлов (меди(II), никеля(II), кобальта(II)) с функциональными группами синтезированных хелатообразующих сорбентов. Изучение адсорбции катионов цветных металлов показало, что в зависимости от рН среды возможно как совместное извлечение, так и разделение катионов.
Образцы МСМ-48, ПР-ДМГД, ПР-ДБА сорбируют ионы никеля(II), кобальта(II), меди(II) из растворов при переходе от слабокислых к щелочным растворам.
Наибольшее извлечение (80–90%) всех трех цветных металлов достигается в нейтральной и щелочной средах сорбентом, модифицированным амидными группами методом гидротермального синтеза. В наибольшей степени извлекается кобальт(II) (EМ = 4–5.3 ммоль/г). В интервале рН 1.5–6.0 кобальт может быть отделен от раствора, содержащего все три иона.
Список литературы
Балакаин В.М., Драницина Н.В., Холманская Ю.Б. и др. Новые азотфосфорсодержащие амфолиты на полиакрилатной матрице и исследование сорбции ими меди, цинка и железа из сернокислых растворов // ЖПХ. 1981. Т. 54. № 4. С. 781–785.
Николаев А.В., Фокин А.В., Коломиец А.Ф. и др. Сорбция меди и цветных металлов серу-, азот,-серуазотсодержащими сорбентами // Изв. СО АН СССР. Сер. хим. наук. 1977. Т. 4. № 9. С. 34–40.
Оскотская Э.П., Басаргин H.H., Игнатов Д.Е. и др. Предварительное групповое концентрирование меди, кобальта и никеля полимерным хелатным сорбентом в анализе природных вод // Зав. лаборатория. Диагностика материалов. 1999. Т. 65. № 3. С. 10–14.
Kondrashova N., Saenko E., Lebedeva I., Valtsifer V., Strelnikov V. Effect of Organic-Silane Additives on Textural–Structural Properties of Mesoporous Silicate Materials // Microporous Mesoporous Mater. 2012. V. 153. P. 275–281. https://doi.org/10.1016/j.micromeso.2011.12.017
Фролов Ю.Г. Курс коллоидной химии: поверхностные явления и дисперсные системы. М.: Химия, 1988. 464 с.
Батуева Т.Д., Кондрашова Н.Б., Кузьмичева Н.Д. и др. Физико-химические свойства мезопористых кремнеземов, модифицированных гидразидными и амидными функциональными группами // ЖПХ. 2017. Т. 90. Вып. 11. С. 1437–1443. https://doi.org/10.1134/S1070427217110039
Тагер А.А. Физикохимия полимеров. М.: Научный мир, 2007. 573 с.
Алосманов Р.М. Исследование кинетики сорбции ионов свинца и цинка фосфорсодержащим катионом // МГУ. Сер. 2. Химия. 2011. Т. 52. № 2. С. 145–148.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы