Неорганические материалы, 2021, T. 57, № 4, стр. 437-441
Сорбция из растворов катионов серебра фосфатотитановыми сорбентами
Р. И. Корнейков *
Институт химии и технологии редких элементов и минерального сырья им. И.В. Тананаева – обособленное подразделение ФИЦ “Кольский научный центр Российской академии наук”
184209 Мурманская обл., Апатиты, Академгородок, 26а, Россия
* E-mail: korneikov@ksc.ru
Поступила в редакцию 26.08.2020
После доработки 19.11.2020
Принята к публикации 20.11.2020
Аннотация
Исследована возможность использования сорбентов на основе гидрофосфатов оксотитана(IV) для очистки высокосолевых жидких радиоактивных отходов от радиоизотопов серебра. Изучена сорбционная активность ионитов по отношению к катионам серебра во времени и определены равновесные значения рН эффективного применения фосфатотитановых сорбентов. Установлено, что материалы на основе гидрофосфатов оксотитана(IV) обладают повышенным сродством к катионам серебра и способны обеспечивать глубокую очистку жидких радиоактивных отходов от радионуклидов.
ВВЕДЕНИЕ
При эксплуатации реакторов атомных электростанций в большом объеме образуются высокосолевые многокомпонентные жидкие радиоактивные отходы (ЖРО) [1]. Вследствие сложного химического состава переработка таких технологических отходов ограничена, что приводит к их накоплению. Вместе с основными долгоживущими радионуклидами цезия, стронция и кобальта [1–3] в ЖРО могут присутствовать и другие радионуклиды с меньшим периодом полураспада, но все же привносящие вклад в общую удельную активность, в частности радионуклиды серебра 110Ag, которые являются продуктом коррозии, как и радионуклиды кобальта, хрома, марганца и т.д. [4–6]. Исследования по извлечению 110Ag в основном приобрели интерес после техногенных катастроф на Чернобыльской и Фукусимской атомных электростанциях [4]. Для выделения радиоизотопов серебра из растворов предложены электрохимические методы, процессы осаждения или их комбинации [7]. Однако наиболее перспективны с технологической точки зрения (эффективность, простота организации процесса и т.д.) сорбционные методы [6, 8, 9].
Среди сорбционных материалов для извлечения из растворов радионуклидов серебра могут быть интересны неорганические соединения на основе аморфных гидрофосфатов оксотитана(IV) с мольным соотношением фосфора к титану ≤1. Такие материалы обладают высокими сорбционными характеристиками, устойчивостью в агрессивных средах и способны обеспечивать надежную иммобилизацию радионуклидов в течение длительного времени [10–12]. Анализ литературы показал, что исследования по извлечению из растворов катионов серебра титанофосфатными сорбентами отсутствуют. Цель работы заключалась в исследовании возможности применения сорбентов на основе оксогидрофосфатов титана(IV) и поиск условий их эффективного применения при извлечении из растворов катионов серебра.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Получение сорбционного фосфатотитанового материала осуществляли согласно разработанному подходу [13] – осаждением из раствора высокогидратированного прекурсора оксогидроксида титана(IV) с последующим внедрением функциональных групп в состав образца обработкой ортофосфорной кислотой. Последующая сушка при 20°С приводила к образованию целевого продукта. Состав ионитов определяли следующим образом: содержание Р(V) – фотоколориметрически с молибдатом аммония (фотоэлектроколориметр Leki-1107); Ti(IV) – атомно-абсорбционным и фотоколориметрическим (с пероксидом водорода) методами; H2O, OH–- и ${\text{HPO}}_{4}^{{2 - }}$˗групп – сопоставлением результатов химического, дифференциального-термического (ДТА) и термогравиметрического (ТГА) методов анализа.
Для ДТА твердых фаз использовали низкочастотный термографический регистратор НТР-70 с программным нагревательным устройством ПРТ-1000М (эталоном выступал прокаленный оксид алюминия). ТГА проводили с помощью тензорных весов ВТ-1000. Температуру измеряли платина-платинородиевыми термопарами в комплекте с потенциометром ПП-63. Скорость нагрева составляла 10°С/мин. Удельную поверхность воздушно-сухого исходного сорбента, средний диаметр и объем пор определяли методом термической десорбции азота на электронном измерителе удельной поверхности TriStar II 3020 фирмы Micrometritics. Распределение по размерам частиц определяли методом лазерной дифракции на анализаторе SALD-201 фирмы Shimadzu.
Исходное и остаточное содержание катионов металлов в растворах, а также в отработанных сорбционных материалах при их вскрытии определяли атомно-абсорбционным методом (прибор AAS-30 фирмы Karl Zeiss). При химическом анализе использовали масс-спектрометрическую систему с индуктивно-связанной плазмой (ИСП-МС) с динамической реакционной системой ELAN 9000 DRC-e фирмы Perkin Elmer. Сорбционный процесс на фосфатотитановых матрицах осуществляли в статических условиях при различных равновесных значениях рН. Равновесные значения рН контролировали рН-метром Анион 7000. Индикаторным электродом служил селективный по отношению к протонам электрод марки ЭСЛ-43-07, вспомогательным – хлорсеребряный электрод Ag/AgCl марки ЭВЛ-1М3. Коэффициенты распределения (Kd) рассчитывали по уравнению Kd = Аα/(100 – А), где А – процентное содержание сорбированного катиона металла, α – отношение объема жидкой фазы к массе сорбента.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Сопоставлением результатов химического анализа, а также ДТА и ТГА был определен состав полученного сорбционного материала (мас. %): TiO2 – 34.01, P2O5 – 30.25, Н2О – 35.74. Данному химическому составу соответствует соединение TiOНPO4 ⋅ 4.16 Н2О. Сорбент подвергали размолу и ситованию через сито с размером ячеи 0.05 мм. Удельная поверхность образца Sуд составила 13.89 м2/г, средний диаметр d и объем V пор ‒ 19.41 нм и 0.06 см3/г соответственно. Диапазон среднего размера частиц сорбента составлял от 7 до 20 мкм.
В работе изучены процессы сорбционного извлечения катионов серебра из растворов сорбентом состава TiOНРО4 ⋅ 4.16Н2О при различных значения рН. Выбор исходной концентрации катионов серебра в растворе обусловлен остаточной концентрацией ионов серебра в щелочной области – при рН 11 согласно [14].
Поскольку титанофосфатная матрица содержит в функциональных группах в качестве активного центра катионы водорода, при контакте с раствором, содержащем катионы металлов, происходит его подкисление (рН исходного раствора равно 6) вследствие замещения протонов гидрофосфатных групп на катионы металлов. Корректировку и поддерживание равновесного значения рН растворов осуществляли гидроксидом натрия. Сорбционное извлечение микроколичеств катионов серебра осуществляли из высокосолевых растворов.
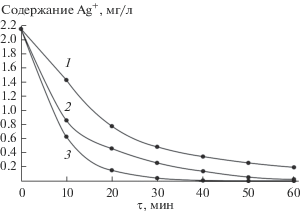
На атомных электростанциях общее солесодержание технологических растворов может доходить до нескольких десятков г/л. Основным макрокомпонентом ЖРО является натрий в виде нитратной соли. Поэтому в работе проведено исследование сорбционного извлечения катионов Ag+ в присутствии катионов Na+ в существенно превосходящих количествах по отношению к серебру. На рис. 1 представлены результаты исследований процесса замещения катионов серебра на ионы водорода функциональных групп сорбента во времени в зависимости от равновесного значения рН раствора при отношении жидкой и твердой фаз (Ж : Т), равном 100.
Как видно из рис. 1 , наиболее эффективно катионы серебра извлекаются при равновесном значении рН, равном 11, по сравнению с равновесными значениями рН 2 и 7. За 30 мин репульпирования сорбировалось свыше 97%. Связано это с отсутствием конкуренции со стороны ионов водорода и натрия в этой области значений рН. Также, возможно, это связано и с усилением подвижности ионов водорода функциональных групп сорбента. В табл. 1 представлены результаты исследований по извлечению катионов серебра и рассчитанные по экспериментальным данным значения коэффициентов распределения. Репульпирование осуществляли в течение 1 ч при Ж : Т = 100.
Таблица 1.
Извлечение катионов Ag+ (Ж : Т = 100) из раствора состава (г/л): Ag+ – 2.13 × 10–3; NaNO3 – 35
| рН сорбции | Остаточное содержание Ag+, мг/л | Извлечение, % | Кd, мг/л |
|---|---|---|---|
| 2 | 0.167 | 92.2 | 1175 |
| 7 | 0.027 | 98.7 | 8178 |
| 11 | 0.0029 | 99.9 | 77 139 |
Видно, что фосфатотитановый сорбент эффективно извлекает катионы Ag+ из высокосолевого раствора. О сродстве сорбента к Ag+ свидетельствуют высокие значения коэффициентов распределения.
Поскольку в ЖРО могут присутствовать меньшие количества по отношению к натрию, но существенно превосходящие по отношению к серебру катионов калия [1], в работе исследована возможность извлечения катионов серебра из модельных растворов при совместном присутствии катионов Na+ и К+ (табл. 2). Репульпирование осуществляли в течение 1 ч при Ж : Т = 100.
Таблица 2.
Извлечение катионов Ag+ (Ж : Т = 100) из раствора состава (г/л): Ag+ – 2.23 × 10–3, NaNO3 – 27.4, КNO3 – 9.3 (общее солесодержание 36.7)
| рН сорбции | Остаточное содержание Ag+, мг/л | Извлечение, % | Кd, мг/л |
|---|---|---|---|
| 2 | 0.178 | 92.0 | 1153 |
| 7 | 0.058 | 97.4 | 3745 |
| 11 | 0.0051 | 99.8 | 43 625 |
В присутствии высокого содержания катионов щелочных металлов фосфатотитановый сорбент эффективно извлекает катионы серебра, о чем свидетельствуют данные табл. 2. Наиболее эффективно серебро извлекается из растворов, как и в вышеописанном эксперименте, в щелочной области.
Поскольку после упаривания ЖРО т. н. кубовые остатки (КО) могут содержать значительно бóльшие концентрации солей (100–150 г/л) [1], в работе проведены исследования по сорбционному извлечению катионов серебра из модельных растворов с близким к КО содержанием макрокомпонентов (табл. 3). Репульпирование осуществляли в течение 1 ч при Ж : Т = 100.
Таблица 3.
Извлечение катионов Ag+ (Ж : Т = 100) из раствора состава (г/л): Ag+ – 1.896 × 10–3, NaNO3 – 93.4, КNO3 – 31.7 (общее солесодержание 125.1)
| рН сорбции | Остаточное содержание Ag+, мг/л | Извлечение, % | Кd, мг/л |
|---|---|---|---|
| 2 | 0.193 | 89.8 | 882 |
| 7 | 0.083 | 95.6 | 2184 |
| 11 | 0.0056 | 99.6 | 33 757 |
Видно, что, несмотря на существенное увеличение содержания катионов щелочных металлов в растворе, сорбционная активность фосфатотитановой матрицы в отношении катионов серебра остается высокой, о чем свидетельствуют значения степеней извлечения и коэффициентов распределения (табл. 3).
Для подтверждения предположения об усилении подвижности протонов функциональных групп в зависимости от равновесного значения рН сорбции, в результате чего происходит более эффективное извлечение катионов Ag+, был определен состав отработанных образцов сорбента. Перед анализом состава насыщенные катионами металлов образцы промывались на фильтре дистиллированной водой и сушились при 20°С. В табл. 4 представлены результаты химического анализа ионитов, апробированных в растворе с общим солесодержанием 125.1 г/л. Видно, что при увеличении равновесного значения рН сорбции изменяется соотношение катионов щелочных металлов в отработанном сорбционном материале. В кислой области сорбируются преимущественно более крупные, обладающие большим ионным радиусом, катионы калия, т.к. в растворе ионы водорода конкурируют с катионами металлов. При этом заполнение функциональных групп сорбента осуществляется только на 60%. Однако при увеличении равновесного значении рН повышается извлечение менее крупных катионов натрия, что может свидетельствовать об усилении подвижности протонов функциональных групп сорбентов при повышении равновесного значения рН сорбции. Заполнение ионогенных групп осуществляется практически на 100%.
Таблица 4.
Химический состав образцов сорбента после сорбции катионов серебра из раствора с общим солесодержанием 125.1 г/л при различном равновесном значении рН
| рН сорбции | Состав отработанного сорбента, мас. % | Заполнение емкости сорбента, мол. % | ||||
|---|---|---|---|---|---|---|
| Na2O | К2O | TiO2 | Р2О5 | Н2О | ||
| 2 | 3.06 | 6.52 | 34.71 | 30.35 | 25.36 | >60 |
| 7 | 8.61 | 7.62 | 33.53 | 30.29 | 19.95 | ~100 |
| 11 | 9.46 | 6.30 | 34.95 | 31.56 | 17.73 | ~100 |
Таким образом, экспериментально установлено высокое сродство фосфатотитановых ионитов состава TiOHPO4 ⋅ nH2O по отношению к катионам серебра на фоне многократно превосходящего содержания катионов металлов, в частности натрия и калия.
ЗАКЛЮЧЕНИЕ
Показана эффективность применения титанофосфатных сорбционных материалов при извлечении из растворов микроколичеств катионов серебра на фоне значительно превосходящих по содержанию катионов натрия и калия. Изучена сорбционная активность ионообменных материалов по отношению к катионам серебра во времени. Установлено, что сорбенты на основе гидрофосфатов оксотитана(IV) обладают повышенным сродством к катионам серебра.
Определены равновесные значения рН, при которых катионы Ag+ максимально полно извлекаются из высокосолевых растворов. Установлено, при рН 11 происходит эффективная сорбция Ag+ фосфатотитановыми сорбентами, о чем свидетельствуют высокие значения степеней извлечения и коэффициентов распределения.
Экспериментально подтверждено предположение, что при повышении щелочности происходит усиление подвижности ионов водорода функциональных групп сорбента, обеспечивающее глубокую очистку растворов от катионов серебра.
Сорбенты на основе гидрофосфатов оксотитана могут рассматриваться как перспективные материалы для глубокой очистки высокосолевых ЖРО от радионуклидов серебра.
Список литературы
Рябчиков Б.Е. Очистка жидких радиоактивных отходов. М.: ДеЛи принт, 2008. 516 с.
Abdel-Karima A.M., Zaki A.A., Elwana W., El-Naggar M.R., Gouda M.M. Experimental and Modeling Investigations of Cesium and Strontium Adsorption onto Clay of Radioactive Waste Disposal // Appl. Clay Sci. 2016. № 132–133. P. 391–401. https://doi.org/10.1016/j.clay.2016.07.005
Mansy M.S., Hassana R.S., Selim Y.T., Kenawy S.H. Evaluation of Synthetic Aluminum Silicate Modified by Magnesia for the Removal of 137Cs, 60Co and 152 + 154Eu from Low-Level Radioactive Waste // Appl. Radiat. Isot. 2017. № 130. P. 198–205. https://doi.org/10.1016/j.apradiso.2017.09.042
Lepage H., Evrard O., Onda Yu., Patin J., Chartin C., Lefèvre I., Bonté P., Ayrault S. Environmental Mobility of 110 mAg: Lessons Learnt from Fukushima Accident (Japan) and Potential Use for Tracking the Dispersion of Contamination within Coastal Catchments // J. Environ. Radioactiv. 2014. № 130. P. 44–55. https://doi.org/10.1016/j.jenvrad.2013.12.011
Hirschberg G., Baradlai P., Varga K., Myburg G., Schunk J., Tilky P., Stoddart P. Accumulation of Radioactive Corrosion Products on Steel Surfaces of VVER Type Nuclear Reactors. I. 110mAg // J. Nucl. Mater. 1999. № 265. P. 273–284.
Marton G., Szanya T., Hanak L., Simon G., Hideg J., Makai J., Schunk J. Purification of Nuclear Power Plant Decontamination Solutions by Preparative Scale Reactive Adsorption // Chem. Eng. Sci. 1996. V. 51. № 11. P. 2655–2660.
Штромер Ф., Семпере-Бельда Л. Способ и установка для извлечения радиоактивных нуклидов из отработанных смоляных материалов: Патент РФ № 2 666 415, опубл. 07.09.2018. Б.И. № 25.
Johnson B.E., Santschi P.H., Addleman R.S., Douglas M., Davidson J., Fryxell G.E., Schwantes J.M. Optimization and Evaluation of Mixed-Bed Chemisorbents for Extracting Fission and Activation Products from Marine and Fresh Waters // Anal. Chim. Acta. 2011. № 708. P. 52–60.https://doi.org/10.1016/j.aca.2011.08.017
Ремез В.П. Способ переработки жидких радиоактивных отходов, содержащих, в том числе, изотопы трития: Патент РФ № 2706019, опубл. 13.11.2019. Б. И. № 32.
Корнейков Р.И., Иваненко В.И. Извлечение катионов цезия и стронция из растворов ионитами на основе фосфатов титана(IV) // Неорган. материалы. 2020. Т. 56. № 5. С. 528–532 https://doi.org/10.31857/S0002337X20050085
Корнейков Р.И., Аксенова С.В., Иваненко В.И., Локшин Э.П. Устойчивость оксогидрофосфатов титана(IV) в водных средах // Неорган. материалы. 2018. Т. 54. № 7. С. 727–732. https://doi.org/10.7868/S0002337X18070126
Иваненко В.И., Корнейков Р.И., Локшин Э.П. Иммобилизация катионов металлов титанофосфатными сорбентами // Радиохимия. 2016. Т. 58. № 2. С. 140–146.
Иваненко В.И., Локшин Э.П., Аксенова С.В., Корнейков Р.И., Калинников В.Т. Термодинамика гетерогенного катионного замещения на гидрофосфате титанила // Журн. неорган. химии. 2008. Т. 53. № 4. С. 557–563.
Краткий справочник по химии / Под ред. Куриленко О.Д. Киев: Наук. думка, 1965. 835 с.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы