Неорганические материалы, 2022, T. 58, № 12, стр. 1320-1330
Синтез Bi2Ge3O9
Т. В. Бермешев 1, *, В. П. Жереб 1, 2, М. П. Бундин 1, А. С. Ясинский 1, О. В. Юшкова 1, Д. С. Ворошилов 1, А. Н. Залога 1, А. А. Ковалева 1, О. В. Якивьюк 1, А. С. Самойло 1, Е. В. Мазурова 3
1 Сибирский федеральный университет
660041 Красноярск, пр. Свободный, 79, Россия
2 Сибирский университет науки и технологий им. академика М.Ф. Решетнева
660037 Красноярск, пр. им. газеты “Красноярский рабочий”, 31, Россия
3 Институт химии и химической технологии СО Российской академии наук
660036 Красноярск,
Академгородок, 50, стр. 24, Россия
* E-mail: irbis_btv@mail.ru
Поступила в редакцию 05.05.2022
После доработки 27.07.2022
Принята к публикации 29.07.2022
- EDN: GTDEFE
- DOI: 10.31857/S0002337X22120028
Аннотация
Исследованы условия получения соединения Bi2Ge3O9 при ускоренной кристаллизации стехиометрического расплава. Показана возможность ускоренного получения соединения Bi2Ge3O9 из предварительно синтезированного аморфного материала (стекла) с помощью термической обработки в твердом состоянии. Отжиг при температуре 670°С и выше в течение короткого времени (30 мин) способствует переходу аморфного материала в стабильный Bi2Ge3O9 на 98–99 мас. % с незначительным содержанием в образце двух примесных фаз: метастабильной ή-Bi2GeO5 и стабильной Bi4Ge3O12. Повышение температуры отжига до 950°С, а также увеличение времени выдержки до 360 мин приводит к полному переходу стекла в Bi2Ge3O9.
ВВЕДЕНИЕ
Германат висмута Bi2Ge3O9 с кристаллической структурой бенитоита (КСБ) впервые получен в 1979 г. [1]. К настоящему времени исследованы оптические, абсорбционные, фото- и термолюминесцентные свойства его монокристаллов [1–4], тонких пленок [5] и керамики [6]. Предпринимались также попытки улучшения свойств Bi2Ge3O9 с помощью легирования Eu [7] и Nd [8]. Микроволновые диэлектрические свойства керамики состава Bi2Ge3O9 исследованы в [9].
Германат висмута с КСБ представляет интерес как материал для рентгеновских спектрометров и фотоакустических дефлекторных устройств [1], для генерации стимулированного излучения [8], а также в качестве перспективного материала керамических подложек для миниатюрных и высокопроизводительных пассивных компонентов в системах СВЧ-связи [9].
Однако в последние годы опубликовано мало работ, посвященных исследованию свойств Bi2Ge3O9.
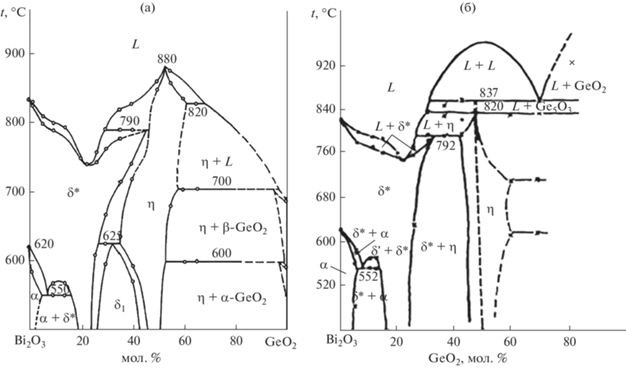
Как известно, система Bi2O3–GeO2 представлена одной диаграммой стабильного равновесия (рис. 1) и двумя диаграммами метастабильного равновесия (рис. 2) [10]. По результатам исследований температурных и концентрационных зависимостей структурно-чувствительных свойств расплава, в основном вязкости, область жидкого состояния на фазовой диаграмме системы Bi2O3–GeO2 была разделена на 3 температурные зоны: A, B и С, охлаждение расплава от которых, т.е. температура начала охлаждения (tнач.охл) расплава, по-разному влияет на состояние образующихся кристаллических фаз (рис. 1). Существование температурных зон и влияние условий охлаждения расплава на фазовый состав образующихся кристаллических фаз экспериментально подтверждено в [11].
Рис. 1.
Границы температурных зон (1) в области расплава на фазовой диаграмме (2) стабильного равновесия системы Bi2O3–GeO2 [10].
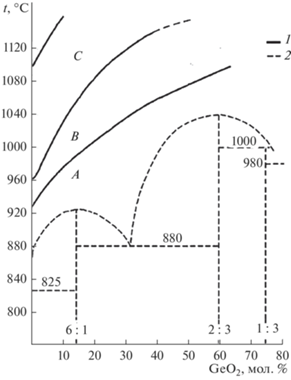
Рис. 2.
Фазовые диаграммы метастабильного равновесия системы Bi2O3–GeO2, построенные по результатам охлаждения расплавов от температур, лежащих в зоне В (а) и в зоне С (б) [10].
Инконгруэнтный характер плавления и кристаллизации Bi2Ge3O9, а также высокое содержание оксида германия в сплаве вносят некоторые сложности в получение данного соединения из расплава. К настоящему времени известно, что его можно получать в виде монокристаллов методом Чохральского [1, 2, 8] и Бриджмена [7], керамики – с помощью твердофазного синтеза (в т.ч. методом частичного сплавления, когда температура синтеза находится выше либо около температуры плавления чистого Bi2O3) [6, 9] и отжига из стекла [12], а также в виде тонких пленок методом дискретного испарения в вакууме [5].
Однако все вышеперечисленные способы при всех своих достоинствах довольно трудоемки и очень длительны. Для выращивания же монокристаллов гораздо удобнее использовать заранее синтезированное поликристаллическое соединение, т.к. предварительный синтез в расплаве существенно ограничен из-за риска образования метастабильных фаз, ухудшающих свойства получаемых монокристаллов [13, 14]. Поэтому поиск более простых и эффективных способов синтеза поликристаллического германата висмута с КСБ является важной научно-технической задачей.
В работе [15] наглядно показано, что образование метастабильных фаз в системе Bi2O3–GeO2 происходит благодаря переходу расплава в метастабильное состояние в результате его термической обработки, во время которой, по-видимому, сохраняется структура высокотемпературного расплава с полимеризацией его структурных составляющих и микрогетерогенность. Монотонное (без термических градиентов, вибрационных и ударных воздействий) охлаждение метастабильного расплава от температур, лежащих в зоне С, способствует сохранению полимерной структуры, переохлаждению и кристаллизации метастабильных фаз. Нарушение же данного состояния, например, посредством вибрационных нагрузок [16] или термическим “ударом” (метод литья) [17] инициирует образование и рост зародышей стабильных фаз.
Таким образом, целью данной работы было исследование возможных условий получения соединения Bi2Ge3O9 при ускоренной кристаллизации стехиометрического расплава.
ЭКПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В данной работе для всех видов синтеза использовали оксид висмута (III) в α-модификации квалификации “ос. ч.” и оксид германия квалификации “ч. д. а.”.
Исходные реагенты в стехиометрическом соотношении (25 мол. % Bi2O3 : 75 мол. % GeO2) помещали в платиновый тигель объемом 32 см3 и нагревали в электрической печи сопротивления LMV 02/12 на воздухе до температуры зоны С (1200°С) со скоростью ~20°С/мин, затем выдерживали в изотермических условиях 1 ч. Далее расплав либо выливался на подогретую платиновую подложку (вариант 1), либо закаливался между двумя массивными медными пластинами с целью получения стекла, которое затем подвергалось отжигу (вариант 2).
Вариант 1. После сплавления и выдержки в зоне С (1200°С, 1 ч) расплав выливали из тигля на подогретую платиновую пластину. Температуры подогрева составляли 450 и 920°С. Нагрев платиновой пластины, на которую осуществлялось литье, проводился на массивном шамотном кирпиче, предотвращающем быстрое остывание пластины при извлечении ее из печи непосредственно перед началом процесса литья. Температура разогрева пластины должна была обеспечивать предотвращение стеклования расплава при его охлаждении.
Вариант 2. После сплавления и выдержки в зоне С расплав выливали из тигля и охлаждали между двумя массивными медными пластинами для получения полностью аморфного материала. Полученные стекла подвергали термическому анализу, по результатам которого выбирали температуру отжига для обеспечения полного перехода материала в стабильное состояние со структурой Bi2Ge3O9.
Термический анализ проводили на приборе синхронного термического анализа STA 449 C Jupiter (NETZSCH, Германия): нагрев до 970°С и охлаждение до 250°С со скоростью 10 К/мин в динамической воздушной атмосфере, скорость продувки – 15 мл/мин. Поверхность образцов изучали с помощью стереоскопа Stemi 2000 (Carl Zeiss). Исследование микроструктуры выполняли с использованием оптического микроскопа Carl Zeiss Axio Observer A1m на микрошлифах, полученных после шлифовки, полировки и химического травления. Растровую электронную микроскопию (РЭМ) и локальный рентгеноспектральный анализ (ЛРСА) проводили на HITACHI TM-3000 и HITACHI TM-4000. Рентгенофазовый анализа (РФА) порошка проводили на дифрактометре Shimadzu XRD 6000 (CuKα-излучение).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Благодаря высокому содержанию оксида германия в расплаве (75 мол. %), являющегося хорошим стеклообразующим компонентом, расплав даже при охлаждении на воздухе будет затвердевать с образованием стекла. Подогрев подложки, на которую осуществляется литье, до 450°С (рис. 3а) будет приводить лишь к частичной кристаллизации в той области, где охлаждаемый расплав контактировал с подложкой (рис. 3б).
Рис. 3.
Макрофотографии образца, полученного литьем расплава на платиновую подложку, подогретую до 450°С: вид сверху (а), вид снизу – в месте контакта расплава с Pt-подложкой (б).

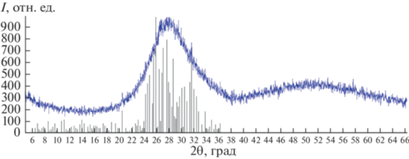
Рентгенофазовый анализ показывает, что бóльшая часть затвердевшего материала при охлаждении становится стеклом, но также присутствуют и некоторые характерные рефлексы, указывающие на некоторое количество одной или нескольких кристаллических фаз (рис. 4). Однако точно идентифицировать их не представляется возможным.
Анализ микроструктуры образцов, полученных литьем на подогретую до 450°С платиновую подложку, показывает, что данные кристаллы имеют форму многогранников и обладают ультрамелкодисперсной субструктурой (рис. 5), трудноразличимой даже при максимальном увеличении оптического микроскопа (×1000, рис. 5в). При этом данная субструктура будет неоднородной – внутри многогранников мы видим хорошо различимые центральные области темно-серого цвета, окруженные по периферии более светлыми скоплениями кристаллов (рис. 5г). Подобная структура не похожа ни на одну известную нам структуру соединений системы Bi2O3–GeO2.
Рис. 5.
Микроструктура образца, закаленного от 1200°С на платиновую подложку (подогретую до 450°С), в месте контакта расплава с подложкой при обычном свете (а–в), при поляризованном освещении (г).

Также следует отметить и возможную частичную кристаллизацию стекла за пределами рассмотренных выше крупных многогранных кристаллов. Обычно при химическом травлении подобных материалов кристаллические участки хорошо вытравливаются, а аморфные нет (остаются просто светлым/белым фоном). В данном же случае (рис. 5а, нижняя часть фотографии) мы видим, что, помимо крупных многогранников, хорошо вытравливаются и некоторые участки окружающего их стекла. Эти участки выглядят как однородные вытянутые зерна. По-видимому, из-за высокой температуры разогрева подложки, на которую осуществлялось литье расплава, происходит частичная кристаллизация еще одной фазы, которая тонким слоем присутствует в зоне контакта Pt/расплав.
При повышении температуры подогрева подложки до 920°С удается избежать стеклообразования. Однако образец, полученный таким способом, даже при визуальном осмотре будет неоднородным. На макрофотографии закристаллизовавшегося расплава хорошо видны как светло-серые, так и серые участки (рис. 6), каждый из которых отличается своей текстурой.
Микроструктура такого образца представляет собой сложную мелкодисперсную смесь из светлых и темных участков, схожую с дендритной структурой (рис. 7а). При относительно небольших увеличениях (×100) дендритный характер хорошо различим, хоть и имеет некоторые особенности: оси дендритов первого порядка образуют правильные геометрические фигуры в виде многоугольников, зачастую пересекающихся друг с другом практически под прямыми углами. Многоугольники также образуют некое подобие “каскада”, что характерно для кристаллизации металлического висмута.
При изучении микроструктуры при больших увеличениях (×500 и выше) хорошо заметно, что оси первого порядка так же неоднородны, как и окружающее их пространство, и тоже состоят из чередующихся темных и светлых участков.
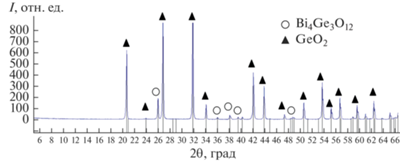
Результаты рентгенофазового анализа (рис. 8) показывают наличие в образце двух фаз: Bi4Ge3O12 с кристаллической структурой эвлитина и α-GeO2. Как показано в работе [15], охлаждение расплава в тигле после его термической обработки приводит к кристаллизации согласно диаграмме метастабильного равновесия (рис. 2). Нарушение же взаимодействия расплава с материалом тигля, а также образовавшейся во время термической обработки в зоне С (рис. 1) полимерной структуры расплава, например в процессе литья, приводит к кристаллизации согласно диаграмме стабильного равновесия [17–19]. Однако в данном случае для состава 75 мол. % GeO2 была получена смесь из Bi4Ge3O12, стехиометрический состав которого 60 мол. % GeO2 (диаграмма стабильного равновесия), и α-GeO2 (диаграмма метастабильного равновесия). Подобный факт можно объяснить инконгруэнтным характером плавления и кристаллизации расплава состава, отвечающего соединению со структурой бенитоита (Bi2Ge3O9). При ускоренном охлаждении на подогретую до высоких температур платиновую подложку будет исключаться образование стекла и метастабильной фазы ή-Bi2GeO5, однако благодаря инконгруэнтному характеру плавления и неравновесной кристаллизации будет образовываться крайне неоднородная по химическому составу мелкодисперсная дендритная структура, состоящая из смеси Bi4Ge3O12 и α-GeO2.
Подобные предположения подтверждаются результатами РЭМ (рис. 9а), где при очень большом увеличении (×5000) также хорошо виден дендритный характер строения материала. Исследование темных и светлых участков структуры при помощи ЛРСА (табл. 1, рис. 9б) также показывает крайне неоднородный химический состав как при сравнении светлых и темных участков, так и внутри них. При этом в темных участках содержание германия втрое превышает содержание висмута, в то время как в светлых участках концентрации Bi и Ge близки друг к другу.
Рис. 9.
РЭМ-изображение (а) и результаты ЛРСА (б) образца, закаленного от 1200°С на платиновую подложку, подогретую до 920°С.

Таблица 1.
Результаты ЛРСА образца, закаленного от 1200°С на платиновую подложку, подогретую до 920°С
| Элемент | C, ат. % | |||
|---|---|---|---|---|
| светлые участки | темные участки | |||
| среднее значение | диапазон значений | среднее значение | диапазон значений | |
| Bi | 19.2 ± 2.3 | 15.8–22.4 | 9.0 ± 3.3 | 4.2–13.3 |
| Ge | 24.0 ± 2.2 | 20.0–27.0 | 31.6 ± 2.5 | 28.6–35.6 |
| O | 56.8 ± 1.3 | 54.9–59.3 | 59.4 ± 1.5 | 57.4–61.4 |
Учитывая невозможность получения Bi2Ge3O9 при выбранных условиях синтеза из расплава методом литья, предприняли попытку более подробного изучения возможности получения данного соединения из аморфного состояния (стекла).
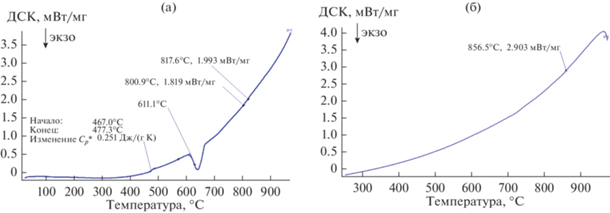
Термический анализ стекол, закаленных из расплава от 1200°С, показал (рис. 10), что в интервале 467–477°С происходит стеклование образца с его последующей кристаллизацией при 611°С. Согласно диаграммам метастабильного равновесия (рис. 2), в данном случае должна образовываться метастабильная фаза ή-Bi2GeO5, которая при дальнейшем нагреве будет претерпевать распад около 800°С. По-видимому, небольшие экзотермические эффекты при 801 и 818°С соответствуют данному распаду. Наличие же двойного эффекта фазового перехода, как и незначительного эндотермического эффекта, заметного при охлаждении около 857°С, объясняется кинетическими процессами, протекающими в материале при съемке ДСК-кривой. Даже при довольно высоких температурах, превышающих температуру распада метастабильной фазы, в материале некоторое время еще могут оставаться локальные области, содержащие аморфные составляющие. Разумеется, со временем они также будут кристаллизоваться и претерпевать распад, однако это может быть растянуто во времени и давать дополнительные эффекты на ДСК-кривых. В нашем случае (рис. 10) съемка велась в режиме непрерывного нагрева и охлаждения, без изотермической выдержки, что и могло привести к появлению подобных эффектов. При повторном нагреве и охлаждении никаких фазовых превращений в материале не наблюдалось, что говорит о необратимости рассмотренных выше процессов.
Рис. 10.
Результаты термического анализа стекол, закаленных из расплава от 1200°С: скорость нагрева (а) и охлаждения (б) 10 К/мин.
На основе результатов термического анализа были выбраны различные режимы отжигов образцов, где варьировались температура отжига, время выдержки, а также дисперсность материала (кусковой образец/порошок). Фазовый состав образцов, закаленных из расплава, после проведения отжигов по различным режимам приведен в табл. 2.
Таблица 2.
Фазовый состав стекла состава 1 : 3 (Bi2O3 : GeO2) после отжига при различных температурах и временах, а также в зависимости от вида образца
| Режим | Температура отжига, °С |
Время отжига, мин | Вид образца | Фазовый состав |
|---|---|---|---|---|
| 1 | 670 | 40 | Порошок | Bi2Ge3O9 и Bi2GeO5 + Bi4Ge3O12 (<2 мас. %) |
| 2 | 670 | 180 | Порошок | Bi2Ge3O9 и Bi2GeO5 + Bi4Ge3O12 (<1 мас. %) |
| 3 | 940 | 30 | Кусковой | Bi2Ge3O9 и Bi2GeO5 + Bi4Ge3O12 (<1 мас. %) |
| 4 | 970 | 30 | Кусковой | Bi2Ge3O9 и Bi2GeO5 + Bi4Ge3O12 (~2 мас. %) |
| 6 | 950 | 40 | Порошок | Bi2Ge3O9 и Bi4Ge3O12 (<1 мас. %) |
| 7 | 950 | 180 | Порошок | Bi2Ge3O9 и Bi4Ge3O12 (<1 мас. %) |
| 8 | 950 | 360 | Порошок | Bi2Ge3O9 |
Как видно из табл. 2, при довольно низкой температуре (670°С) и непродолжительной выдержке (40 мин) стекло на 98 мас. % переходит в Bi2Ge3O9. При этом в образце содержится всего 2 мас. % примесных фаз: метастабильного ή-Bi2GeO5 и стабильного Bi4Ge3O12. Столь малое содержание ή-Bi2GeO5 в условиях короткого отжига при температуре, лежащей сразу за пиком кристаллизации, говорит о слабой устойчивости данного соединения в области 75 мол. % GeO2. Уже после 40 мин отжига происходит практически полный его распад по всему объему образца. На этот процесс также будет существенно влиять и размер частиц отжигаемого материала.
Таким образом, присутствие едва различимых экзотермических пиков около 801 и 818°С с крайне небольшим выделением энергии объясняется тем, что бóльшая часть соединения ή-Bi2GeO5 к этому моменту уже распалась и при данных температурах происходит распад последних оставшихся в образце его объемов. Также эти процессы могут быть связаны и с возможными небольшими остатками аморфной составляющей. В пользу этой версии говорит и факт наличия метастабильной фазы ή-Bi2GeO5 в образце после кратковременных отжигов до очень высоких температур, намного превышающих температуру распада данного соединения (табл. 2, режимы 3, 4). Однако такое явление наблюдается только в кусковых образцах – предварительно перетертый (порошковый) материал уже не содержит метастабильной фазы (табл. 2, режимы 6, 7).
Для образцов, полученных по режимам 3, 4 (табл. 2, рис. 11), характерна неоднородная микроструктура. Основной объем состоит все же из однородных зерен, имеющих сложную многогранную форму с несплошной границей раздела в виде “точек”, которые при детальном рассмотрении с помощью РЭМ (рис. 12) оказываются микропорами. По микроструктуре эти образцы схожи с образцами Bi2Ge3O9, полученными в работе [9] твердофазным синтезом. В отдельных участках микроструктуры хорошо заметны области со строением, схожим с дендритным (рис. 11б), в которых, по-видимому, и содержатся примесные фазы.
Рис. 11.
Микроструктура стекол состава 1 : 3 (Bi2O3 : GeO2), отожженных в течение 30 мин при температуре 940 (а), 970°С (б).

Рис. 12.
РЭМ-изображения стекла состава 1 : 3 (Bi2O3 : GeO2), отожженного в течение 30 мин при температуре 940°С (×2000): а – общий вид, б – картирование по распределению Bi и Ge.

Мы считаем, что данные области неполного превращения – следствие микрогетерогенности, возникающей в расплаве при высоких температурах. В недавней работе [20] в области составов 1 : 1 мол. % системы Bi2O3–SiO2 было обнаружено и подробно рассмотрено макрорасслаивание, которое удалось сохранить до комнатных температур закалкой расплава от 1100–1180°С. При более низких температурах начала охлаждения (1040°С и ниже) расслаивание зафиксировать не удавалось. Данное расслаивание является следствием полимеризации (поликонденсации) тетраэдров [SiO4] и связанного с ней процесса формирования элементов [Bi2O2] в расплаве. Макрорасслаиванию, которое проявляется при повышении температуры, предшествует микрогетерогенность расплава при более низких температурах, которая не приводит к разделению расплава на слои.
Аналогичные процессы полимеризации протекают и в германатной системе, однако макрорасслаивания в ней на настоящий момент зафиксировать не удалось. Мы предполагаем, что закалка от температуры 1200°С, хоть и не приводит к макрорасслаиванию, однако может способствовать микрогетерогенности и, как следствие, – концентрационной неоднородности в закаленном стекле. При последующем отжиге в областях с пониженной концентрацией оксида германия могут образовываться другие, ближайшие, соединения, на формирование которых потребуется меньше оксида германия, например Bi4Ge3O12. При этом следует учесть и промежуточное образование метастабильной фазы ή-Bi2GeO5. Сам факт ее наличия в материале после отжига, пусть и в виде примеси (0.5 мас. % по данным РФА), говорит о сложном характере превращений, протекающих в твердом состоянии во время отжига стекол данного состава.
Все вышеперечисленные факты не совсем согласуются со схемой, предложенной в работе [12]. Согласно ей, формирование стабильного Bi2Ge3O9 из аморфного материала стехиометрического состава при температуре 900°С происходит за 48 ч и идет в два этапа. Сначала из стекла образуется смесь из Bi4Ge3O12 и аморфного оксида германия (1), а затем ее компоненты начинают взаимодействовать между собой с образованием Bi2Ge3O9 (2):
(1)
$\begin{gathered} 2\left( {{\text{B}}{{{\text{i}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}}{\kern 1pt} \cdot {\kern 1pt} {\text{3Ge}}{{{\text{O}}}_{2}}} \right)\left( {{\text{стекло}}} \right) \to \\ \to \,\,{\text{B}}{{{\text{i}}}_{{\text{4}}}}{\text{G}}{{{\text{e}}}_{{\text{3}}}}{{{\text{О}}}_{{12}}} + 3{\text{Ge}}{{{\text{O}}}_{2}}\left( {{\text{стекло}}} \right), \\ \end{gathered} $(2)
${\text{B}}{{{\text{i}}}_{{\text{4}}}}{\text{G}}{{{\text{e}}}_{{\text{3}}}}{{{\text{О}}}_{{12}}} + 3{\text{Ge}}{{{\text{O}}}_{{\text{2}}}}{\text{(стекло}}){\text{ }} \to {\text{B}}{{{\text{i}}}_{{\text{2}}}}{\text{G}}{{{\text{e}}}_{{\text{3}}}}{{{\text{O}}}_{{\text{9}}}}.$Однако в работе [13] не приведены результаты микроструктуры образцов после отжига, не учитывается возможная неоднородность стекла и совершенно не берется в расчет промежуточное метастабильное фазообразование.
При сравнении двух образцов, отожженных при температурах 930, 970°С в кусковом виде (табл. 2, режимы 3 и 4), с образцами, отожженными при температурах 670, 950°С в порошкообразном состоянии (табл. 2, режимы 1, 6), не выявлено заметного влияния степени дисперсности на скорость и полноту протекания реакции. После 30–40 мин выдержки образцы показывают примерно одинаковый процент образования Bi2Ge3O9 – 98–99 мас. %. Это говорит о том, что фазовые переходы, протекающие в стекле при отжиге, носят объемный, а не поверхностный характер.
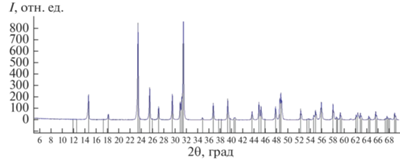
Увеличение же продолжительности отжига до 6 ч (табл. 2, режим 8) и предварительное измельчение стекла перед термической обработкой приводят к получению чистого германата висмута со структурой бенитоита (рис. 13).
ЗАКЛЮЧЕНИЕ
Показана возможность ускоренного получения соединения Bi2Ge3O9 из предварительно синтезированного аморфного материала (стекла) с помощью термической обработки в твердом состоянии. Отжиг при температурах 670°С и выше в течение рекордно короткого времени (30 мин) способствует переходу аморфного материала в стабильный Bi2Ge3O9 на 98–99 мас. %, по данным рентгенофазового анализа, с незначительным содержанием в образце двух примесных фаз: метастабильной ή-Bi2GeO5 и стабильной Bi4Ge3O12.
Метастабильная фаза Bi2GeO5 присутствует в отожженных кусковых и порошкообразных образцах при низких температурах отжига (670°С) и только в кусковых образцах при высоких температурах (940–970°С).
Показано, что повышение температуры отжига до 950°С, а также увеличение времени выдержки до 360 мин приводит к полному переходу стекла в Bi2Ge3O9.
Полученные результаты могут быть использованы для синтеза поликристаллического Bi2Ge3O9 в качестве исходной шихты для выращивания монокристаллов, что имеет важное научное и практическое значение.
Список литературы
Grabmaier B.C., Hanssuhl S., Klufers P. Crystal Growth, Structure and Physical Properties of Bi2Ge3O9 // Z. Kristallogr. 1979. V. 149. № 341. P. 261–267. https://doi.org/10.1524/zkri.1979.149.3-4.261
Zaldo C., Contreras L., Arizmendi L., Dieguez E. Optical Properties of Bi2Ge3O9 Single Crystals X-Ray Irradiation Effects // Phys. Status Solidi. 1989. V. 114. № 1. P. 397–405. https://doi.org/10.1002/pssa.2211140142
Timmermans C.W.M., Boen O., Blasse G. The Luminescence of Bi2Ge3O9 // Solid State Commun. 1982. V. 42. № 7. P. 505–507. https://doi.org/10.1016/0038-1098(82)90630-5
Timmermans C.W.M., Blasse G. The Luminescence of Some Oxidic Bismuth and Lead Compounds // J. Solid State Chem. 1984. V. 52. № 3. P. 222–232. https://doi.org/10.1016/0022-4596(84)90005-7
Бордун О.М., Кухарский И.И., Антонюк В.Г. Люминесценция тонких пленок германата висмута со структурой эвлитина и бенитоита // Журн. прикл. спектроскопии. 2005. Т. 72. № 3. С. 377–380.
Bordun O.M., Kukharskii I.I., Gaidai S.I. Thermally Stimulated Luminescence of Bismuth Germanate Ceramics with The Benitoite, Eulitine, and Sillenite Structures // J. Appl. Spectrosc. 2008. V. 75. № 3. P. 379–384.
Sekita M. Emission and Excitation Spectra of Bi2Ge3O9 : Eu3+ // J. Lumin. 1981. V. 22. № 4. P. 335–347. https://doi.org/10.1016/0022-2313(81)90011-9
Каминский А.А., Саркисов С.Э., Майер А.А., Ломонов В.А., Асафов Д.В., Заказной П.Н. Выращивание и спектрально-люминесцентные свойства гексагональных кристаллов Bi2Ge3О9–Nd3+ // Изв. АН СССР. Неорган. материалы. 1983. Т. 19. № 7. С. 1148–1157.
Xing-Hua Ma, Sang-Hyo Kweon, Sahn Nahm, Chong-Yun Kang, Seok-Jin Yoon, Young-Sik Kim. Synthesis and Microwave Dielectric Properties of Bi2Ge3O9 Ceramics for Application as Advanced Ceramic Substrate // J. Eur. Ceram. Soc. 2017. V. 37. P. 605–610. https://doi.org/10.1016/j.jeurceramsoc.2016.08.037
Жереб В.П. Метастабильные состояния в оксидных висмутсодержащих системах. М.: МАКС Пресс, 2003. 162 с.
Corsmit G., Van Driel M.A., Elsenaar R.J. et al. Thermal Analysis of Bismuth Germanate Compounds // J. Cryst. Growth. 1986. V. 75. P. 551–560.
Dimesso L., Gnappi G., Montenero A., Fabeni P., Pazzi G.P. The Crystallization Behaviour of Bismuth Germanate Glasses // J. Macromol. Sci. 1991. V. 26. P. 4215–4219. https://doi.org/10.1007/BF00553513
Жереб В.П., Скориков В.М. Влияние метастабильных фаз на совершенство монокристаллов стабильных соединений с оксидом висмута. // Неорган. материалы. 2003. Т. 39. № 11. С. 1365–1372.
Новоселов И.И., Макаров И.В., Федотов В.А., Иванникова Н.В., Шубин Ю.В. Синтез оксидной висмут-германиевой шихты для выращивания монокристаллов // Неорган. материалы. 2013. Т. 49. № 4. С. 429–433. https://doi.org/10.7868/S0002337X13030135
Жереб В.П., Бермешев Т.В., Каргин Ю.Ф., Мазурова Е.В., Денисов В.М. Фазовый состав и микроструктура продуктов кристаллизации расплава Bi2O3⋅GeO2 при различных условиях охлаждения // Неорган. материалы. 2019. Т. 55. № 7. С. 782–797. https://doi.org/10.1134/S0002337X19060162
Майер А.А., Фомченков Л.П., Горащенко Н.Г., Грачева Н.А. Исследование высокотемпературного синтеза соединений висмута со структурой силленита // Тр. МХТИ им. Д.И. Менделеева. 1973. Т. 76. С. 85–89.
Bermeshev T.V., Zhereb V.P., Yasinskiy A.S., Mazurova E.V., Bundin M.P., Samoilo A.S., Bespalov V.M., Merdak N.V., Yushkova O.V., Yuryev P.O., Bezrukikh A.I. Casting Synthesis of Bi12SiO20 // Mendeleev Commun. 2021. V. 31. P. 721–722. https://doi.org/10.1016/j.mencom.2021.09.043
Жереб В.П., Бермешев Т.В. Способ получения германата висмута Bi4Ge3O12 методом литья: Патент № 2753671. Опубликовано: 19.08.2021, БИ № 23.
Жереб В.П., Бермешев Т.В. Способ получения германата висмута Bi12GeO20 методом литья: Патент № 2753672. Опубликовано: 19.08.2021. БИ № 23.
Жереб В.П., Бермешев Т.В., Тас-Оол Р.Н., Мазурова Е.В., Метелица С.И. Расслаивание в системе Bi2O3–SiO2. Влияние условий охлаждения расплава на фазовый состав и микроструктуру продуктов затвердевания // Изв. АН. Сер. хим. 2021. № 8. С. 1462–1470.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы