Неорганические материалы, 2022, T. 58, № 2, стр. 162-167
Влияние высокомолекулярного источника углерода на электрохимические свойства композиционных материалов Li4Ti5O12/С
И. А. Стенина 1, *, А. Н. Соболев 1, Т. Л. Кулова 2, А. Б. Ярославцев 1
1 Институт общей и неорганической химии им. Н.С. Курнакова Российской академии наук
119991 Москва, Ленинский пр., 31, Россия
2 Институт физической химии и электрохимии им. А.Н. Фрумкина Российской академии наук
119071 Москва, Ленинский пр., 31 корп. 4, Россия
* E-mail: irina_stenina@mail.ru
Поступила в редакцию 02.10.2021
После доработки 04.11.2021
Принята к публикации 08.11.2021
- EDN: LJFVSG
- DOI: 10.31857/S0002337X22020129
Аннотация
С использованием в качестве источника углерода высокомолекулярных соединений (полистирола, полиэтиленгликоля или поливинилиденфторида) золь–гель-методом синтезированы анодные материалы на основе титаната лития (Li4Ti5O12/C). Полученные композиты охарактеризованы методами РФА, СЭМ, КР-спектроскопии, проведено их электрохимическое тестирование. Модификация приводит к формированию высокопроводящего углеродного покрытия на поверхности частиц титаната лития и улучшению электрохимических свойств полученных материалов. При высоких плотностях тока наибольшими значениями обратимой разрядной емкости характеризуются материалы, полученные с использованием 5 мас. % полистирола или полиэтиленгликоля (при 3200 мА/г 75 и 70 мАч/г соответственно).
ВВЕДЕНИЕ
В последние годы в связи с негативным влиянием традиционных энергосистем на изменение климата все острее встает необходимость полного перехода к возобновляемым экологичным источникам энергии. Для этого необходимо решение проблем не только преобразования энергии, но и ее хранения. Одним из наиболее часто используемых типов аккумуляторов в настоящее время являются литий-ионные аккумуляторы (ЛИА) [1–3]. Однако требования к их мощности, плотности энергии, сроку работы и безопасности продолжают расти [4–6]. Ввиду этого активно ведется поиск новых материалов для ЛИА и методов улучшения существующих [7–9].
Емкость ЛИА определяется используемыми электродными материалами [10–12]. Наиболее распространенным анодным материалом в современных ЛИА является графит. При интеркаляции и деинтеркаляции ионов лития графит претерпевает объемное расширение и усадку, в результате чего происходит потеря электрического контакта между частицами. Одной из перспективных альтернатив графиту является титанат лития Li4Ti5O12 [13–15]. Среди его преимуществ стоит отметить сравнительно высокую теоретическую электрохимическую емкость (175 мАч/г), крайне низкую степень расширения решетки при внедрении ионов лития (0.2–0.3%) и высокую степень безопасности [16–18]. К основным недостаткам титаната лития следует отнести низкие величины его электронной (<10–13 См/см) и ионной (<10–6 См/см) проводимости [19–21] и образование пассивирующей пленки SEI (Solid Electrolyte Interphase) в ходе циклирования, что приводит к потере емкости [22–24].
Нанесение углеродных покрытий [25–32] и проводящих полимеров, таких как полианилин [33, 34], полипиррол [35, 36], политиофен и его производные [37, 38], часто используется для повышения стабильности электродных материалов, в т. ч. титаната лития, и улучшения проводимости, емкостных характеристик и мощности ЛИА на их основе. В работах [39, 40] показано, что использование непроводящих полимеров для покрытия частиц Li4Ti5O12 также может быть эффективным для предотвращения газовыделения во время работы аккумулятора и уменьшения деградации электрохимической ячейки. Предложенный метод позволяет получать тонкие и однородные пленки из различных полимеров [39]. Использование данного подхода с последующим пиролизом в инертной или восстановительной атмосфере может быть эффективным и для получения высококачественного углеродного покрытия.
В качестве источника углерода были использованы различные органические вещества, в т. ч. полимеры [7, 25, 41, 42]. Так, использование полистирола позволило значительно улучшить электрохимические характеристики LiFePO4, в т. ч. в расширенном диапазоне температур [43]. Нанесение полиэтиленгликоля с последующей карбонизацией повысило разрядную емкость кремниевого анода и его стабильность в ходе продолжительного циклирования, в т. ч. при повышенных скоростях заряда/разряда [44]. В то же время количество исследований по применению различных полимеров в качестве источника углерода для создания композитов с титанатом лития сравнительно невелико.
Целью данной работы являлись синтез и исследование электрохимических свойств анодных материалов на основе титаната лития с углеродным покрытием, полученным из высокомолекулярных соединений (полистирола, поливинилиденфторида и полиэтиленгликоля).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для синтеза Li4Ti5O12/C (далее по тексту LTO/C) в качестве источника углерода использовали полиэтиленгликоль (PEG, Sigma-Aldrich), полистирол (PS, Sigma-Aldrich) или поливинилиденфторид (PVDF, Sigma-Aldrich). Количество добавляемого полимера составляло 5 и 10% от массы прекурсора титаната лития. Для получения последнего использовали разработанную ранее методику [45]: стехиометрические количества Ti(C4H9O)4 (99%, AlfaAesar) и Li2CO3 (≥99.0% Fluka) растворяли в смеси этанола и азотной кислоты и к полученной смеси при перемешивании добавляли раствор лимонной кислоты (99%, Sigma-Aldrich) в минимальном количестве воды. Далее реакционную массу подвергали термообработке на воздухе при 95 и 400°С в течение 24 и 5 ч соответственно, а затем гомогенизировали перетиранием в агатовой ступке. К полученному прекурсору титаната лития добавляли раствор полимера (PEG в воде, PS в диметилсульфоксиде, PVDF в N-метил-2-пирролидиноне), проводили ультразвуковую обработку и сушили при 80°C. После этого материалы отжигали при 800°C в течение 5 ч в токе аргона. В качестве образца сравнения синтезировали композит LTO/C, в котором источником углерода служила (5 мас. %) сахароза (Sucr). В обозначениях композитов использованы аббревиатура добавленного прекурсора углерода и его количество (в мас. %), например: LTO/С-5PS, Li4Ti5O12/С-10PEG. Также был получен образец титаната лития отжигом его прекурсора при 800°C на воздухе.
Рентгенофазовый анализ (РФА) образцов проводили на дифрактометре Rigaku D/MAX 2200 (излучение CuKα). Для обработки рентгенограмм использовали пакет программ Rigaku Data Processing. Для определения размера частиц на основании уширения линий рентгенограмм (области когерентного рассеяния (ОКР)) использовали формулу Шеррера. Содержание углерода в полученных композитах определяли методом CHN-анализа на элементном анализаторе EuroVektor EA3000. Анализ микроструктуры полученных композитов проводили с помощью сканирующего электронного микроскопа (СЭМ) Carl Zeiss NVision 40. Исследования методом спектроскопии комбинационного рассеяния (КР) проводили на приборе LabRAM 300 HORIBA Jobin Yvon с возбуждением линией 632.8 нм He–Ne-лазера (мощность излучения 1 мВт).
Электрохимические характеристики анодных материалов из полученных композитов исследовали с помощью трехэлектродных герметичных электрохимических ячеек с литиевыми рабочим электродом и электродом сравнения. Рабочие электроды были изготовлены по стандартной намазной технологии. В качестве токоотвода и сепаратора использовали сетку из нержавеющей стали и нетканый полипропилен (НПО “Уфим”) соответственно. Активную массу готовили смешением порошка нанокомпозита, сажи (Timcal) и раствора поливинилиденфторида (Sigma-Aldrich) в N-метилпирролидиноне (Sigma-Aldrich) в соотношении 88 : 10 : 2, прессовали под давлением 0.1 ГПа с последующей сушкой при 120°С под вакуумом. Количество активного вещества на электроде составляло около 8–10 мг/см2. Электрохимические ячейки собирали в перчаточном боксе в атмосфере сухого аргона. В качестве электролита выступал 1 М раствор LiPF6 в смеси этиленкарбоната, диэтилкарбоната и диметилкарбоната (1 : 1 : 1) (все компоненты электролита имели квалификацию extra dry, Sigma-Aldrich). Ячейки циклировали в гальваностатическом режиме в интервале потенциалов 1–3 В с помощью зарядно-разрядного стенда ЗРУ 50 мА‑10 В (ООО “НТЦ Бустер”), диапазон плотностей тока 20–3200 мА/г.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На рентгенограммах композитов Li4Ti5O12/C, полученных с использованием в качестве прекурсора углерода сахарозы, PS, PEG, а также 5 мас. % PVDF, присутствуют только рефлексы титаната лития (PDF-2, карточка № 72‑0426) (рис. 1). По данным РФА можно заключить, что полученное углеродное покрытие является рентгеноаморфным. Следует отметить, что увеличение количества используемого в синтезе PVDF до 10 мас. % привело к образованию значительных количеств рутила, что свидетельствует о нарушении стехиометрии за счет фторирования поверхности титаната лития. Причиной этого, вероятно, является выход из прекурсора части лития с образованием его фторида на поверхности частиц.
Рис. 1.
Рентгенограммы полученных композитов: LTO/С-5Sucr (1), LTO/С‑5PEG (2), LTO/С-10PEG (3), LTO/С-5PS (4), LTO/С-10PS (5), LTO/С‑5PVDF (6) и LTO/С-10PVDF (7).
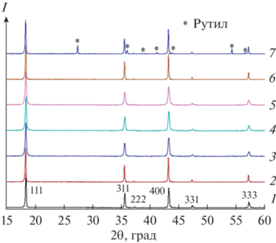
Таблица 1.
Размер частиц (ОКР) и содержание углерода в полученных композитах LTO/С
| Образец | Содержание углерода, % | Размер частиц ±5, нм |
|---|---|---|
| Li4Ti5O12 | – | 130 |
| LTO/С-5Sucr | 2.4 | 50 |
| LTO/С-5PVDF | 0.7 | 85 |
| LTO/С-5PEG | 1.9 | 48 |
| LTO/С-10PEG | 2.2 | 46 |
| LTO/С-5PS | 1.7 | 46 |
| LTO/С-10PS | 1.9 | 41 |
Анализ уширения рефлексов рентгенограмм в совокупности с данными СЭМ полученных материалов (рис. 2) показывает, что использование как низко- (сахароза), так и высокомолекулярных соединений в качестве источника углерода при синтезе композитов LTO/С препятствует росту частиц титаната лития (табл. 1). При этом наибольший размер ОКР наблюдается для образца LTO/С-5PVDF. Его отличие заключается в том, что, по данным CNH‑анализа, содержание углеродного покрытия в нем оказывается заметно ниже (табл. 1) за счет удаления части углерода в виде фторидов в ходе высокотемпературной карбонизации. Это, видимо, свидетельствует о том, что в существенной мере эффект уменьшения размера частиц определяется формирующимся углеродным покрытием. Можно также отметить некоторую корреляцию между содержанием углерода и размером ОКР в полученных композитах.
Согласно данным СЭМ, образец Li4Ti5O12 представляет собой поликристаллическую массу, состоящую из частиц различного размера (от 30 до 500 нм) и с ярко выраженными ступенями роста (рис. 2а). Использование высокомолекулярных соединений в качестве источника углерода в ходе синтеза композитов LTO/С не приводит к значимому изменению морфологии частиц титаната лития (рис. 2б–2в). Можно отметить лишь некоторое уменьшение размера частиц Li4Ti5O12. При этом средний размер частиц, полученный с помощью этого метода, заметно больше, чем рассчитанный на основании уширения рефлексов. Таким образом, наблюдаемые на микрофотографиях частицы представляют собой агломераты.
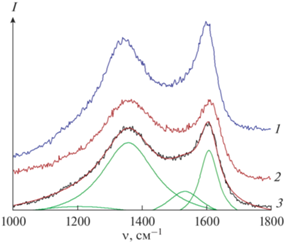
Данные электронной микроскопии не позволяют наблюдать непосредственно углеродное покрытие, имеющее малую толщину. В то же время о качестве его формирования дают сведения данные КР-спектроскопии [30]. Во всех материалах образуются хорошо сформированные графитоподобные структуры, представленные двумя явно выраженными полосами с максимумами при 1355 и 1610 см–1 (рис. 3), которые обычно называют D- и G-линиями. Разложение спектров (рис. 3) показывает наличие еще пары менее интенсивных линий, принадлежащих аморфным формам углерода [30, 46].
Рис. 3.
КР-спектры некоторых полученных композитов: LTO/С-5PVDF (1), LTO/С-10PS (2), LTO/С-10PEG (3).
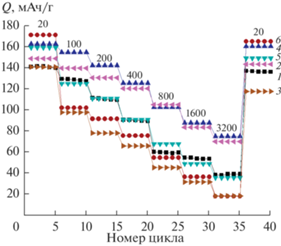
Результаты электрохимического тестирования материалов представлены на рис. 4. Наилучшими характеристиками обладают образцы LTO/C-5PS и LTO/C-5PEG. Разрядная емкость этих материалов при плотности тока 20 мА/г достигла 162 мАч/г. В пересчете на активный материал она составляет 165 мАч/г. В случае использования PVDF для нанесения покрытия, несмотря на наибольшую начальную разрядную емкость, она резко снижается при повышении плотности тока. Емкость остальных образцов оказывается заметно меньше, что обусловлено понижением содержания электрохимически активного материала за счет повышения содержания углерода или других примесных фаз, как, например, в случае материала, полученного с использованием 10 мас. % PVDF. Как отмечалось выше, в образцах, содержащих PVDF, по данным РФА, отмечалось наличие диоксида титана, а ранее было показано, что на поверхности таких образцов формируется и заметная доля рентгеноаморфных фторидов [47]. Немаловажно также и то, что емкость лучших из полученных материалов даже при плотности тока 3200 мА/г сохранилась на уровне 70–75 мАч/г. Это означает, что образец можно зарядить или разрядить за 3 мин более чем на 50%. Кроме того, сохранение высоких значений разрядной емкости при возвращении плотности тока к низким значениям (20 мА/г) свидетельствует о низкой деградации полученных материалов в ходе циклирования.
ЗАКЛЮЧЕНИЕ
Золь–гель-методом синтезированы композиционные анодные материалы Li4Ti5O12/C с углеродным покрытием, полученным с использованием сахарозы или различных полимерных материалов. Использование высокомолекулярных соединений в качестве источника углерода приводит к получению титаната лития с меньшим размером первичных частиц. Образцы, полученные с добавлением к прекурсору 5% полистирола или полиэтиленгликоля, показывают высокую емкость, до 162 мАч/г, при плотности тока 20 мА/г и могут быть заряжены или разряжены за 3 мин более чем на 50%.
Список литературы
Zubi G., Dufo-López R., Carvalho M., Pasaoglu G. The Lithium-Ion Battery: State of the Art and Future Perspectives // Renew. Sust. Energy Rev. 2018. V. 89. P. 292–308.
Xie W., Liu X., He R., Li Y., Gao X., Li X., Peng Z., Feng S., Feng X., Yang S. Challenges and Opportunities toward Fast-Charging of Lithium-Ion Batteries // J. Energy Storage. V. 32. Art. 101837.
Kang Y., Deng C., Chen Y., Liu X., Liang Z., Li T., Hu Q., Zhao Y. Binder-Free Electrodes and Their Application for Li-Ion Batteries // Nanoscale Res. Lett. 2020. V. 15. Art. 112.
Dong H., Xiao X., Jin C., Wang X., Tang P., Wang C., Yin Y., Wang D., Yang S., Wu C. High Lithium-Ion Conductivity Polymer Film to Suppress Dendrites in Li Metal Batteries // J. Power Sources. 2019. V. 423. P. 72–79.
Chen X., Li H., Yan Z., Cheng F., Chen J. Structure Design and Mechanism Analysis of Silicon Anode for Lithium-Ion Batteries // Sci. China Mater. 2019. V. 62. P. 1515–1536.
Chen Y., Kang Y., Zhao Y., Wang L., Liu J., Li Y., Liang Z., He X., Li X., Tavajohi N., Li B. A Review of Lithium-Ion Battery Safety Concerns: The Issues, Strategies, and Testing Standards // J. Energy Chem. 2021. V. 59. P. 83–99.
Zuo D., Tian G., Li X., Chen D., Shu K. Recent Progress in Surface Coating of Cathode Materials for Lithium Ion Secondary Batteries // J. Alloys Compd. 2017. V. 706. P. 24–40.
Aravindan V., Lee Y.-S., Madhavi S. Research Progress on Negative Electrodes for Practical Li-Ion Batteries: Beyond Carbonaceous Anodes // Adv. Energy Mater. 2015. Art. 1402225.
Zhao B., Ran R., Liu M., Shao Z.A. A Comprehensive Review of Li4Ti5O12-Based Electrodes for Lithium-Ion Batteries: The Latest Advancements and Future Perspectives // Mater. Sci. Eng. 2015. V. R98. P. 1–71.
Goodenough J.B., Park K.-S. The Li-Ion Rechargeable Battery: A Perspective // J. Am. Chem. Soc. 2013. V. 135. P. 1167–1173.
Li M., Feng M., Luo D., Chen Z. Fast Charging Li-Ion Batteries for a New Era of Electric Vehicles // Cell Rep. Phys. Sci. 2020. V. 1. Art. 100212.
Stenina I.A., Yaroslavtsev A.B. Nanomaterials for Lithium-Ion Batteries and Hydrogen Energy // Pure Appl. Chem. 2017. V.89. P. 1185–1194.
Sandhya C.P., Bibin J., Gouri C. Lithium Titanate as Anode Material for Lithium-Ion Cells: a Review // Ionics. 2014. V. 20. P. 601–620.
Yi T.-F., Yang S.-Y., Xie Y. Recent Advances of Li4Ti5O12 as a Promising Next Generation Anode Material for High Power Lithium-Ion Batteries // J. Mater. Chem. A. 2015. V. 3. P. 5750–5777.
Chauque S., Oliva F.Y., Visintin A., Barraco D., Leiva E.P.M., Cámara O.R. Lithium Titanate as Anode Material for Lithium Ion Batteries: Synthesis, Posttreatment and Its Electrochemical Response // J. Electroanal. Chem. 2017. V. 799. P. 142–155.
Shu J. Electrochemical Behavior and Stability of Li4Ti5O12 in a Broad Voltage Window // J. Solid State Electrochem. 2009. V. 13. P. 1535–1539.
Han C., He Y.-B., Wang S., Wang C., Du H., Qin X. Large Polarization of Li4Ti5O12 Lithiated to 0 V at Large Charge/Discharge Rates // ACS Appl. Mater. Interfaces. 2016. V. 8. P. 18788–18796.
Liu J., Wei X., Meng F. Lithium Titanate-Based Lithium-Ion Batteries // Advanced Battery Materials / Ed. Sun C. Beverly: Scrivener, 2019. P. 87–157.
Yi T.F., Jiang L.J., Shu J., Yue C.-B., Zhu R.-S., Qiao H.-B. Recent Development and Application of Li4Ti5O12 as Anode Material of Lithium Ion Battery // J. Phys. Chem. Solids. 2010. V. 71. P. 1236–1242.
Zhao B., Ran R., Liu M., Shao Z.A. A Comprehensive Review of Li4Ti5O12-Based Electrodes for Lithium-Ion Batteries: The Latest Advancements and Future Perspectives // Mater. Sci. Eng. 2015. V. R98. P. 1–71.
Kulova T.L., Kreshchenova Y.M., Kuz’mina A.A., Skundin A.M., Stenina I.A., Yaroslavtsev A.B. New High-Capacity Anode Materials Based on Gallium-Doped Lithium Titanate // Mendeleev Commun. 2016. V. 26. P. 238–239.
He Y.-B., Liu M., Huang Z.-D., Zhang B., Yu Y., Li B., Kang F., Kim J.-K. Effect of Solid Electrolyte Interface (SEI) Film on Cyclic Performance of Li4Ti5O12 Anodes for Li Ion Batteries // J. Power Sources. 2013. V. 239. P. 269–276.
Han C., He Y.-B., Liu M., Li B., Yang Q.-H., Wong C.-P., Kangad F. A Review of Gassing Behavior in Li4Ti5O12-Based Lithium Ion Batteries // J. Mater. Chem. A. 2017. V. 5. P. 6368–6381.
Li X., Xu J., Huang P., Yang W., Wang Z., Wang M., Huang Y., Zhou Y., Qu M., Yu Z., Lin Y. In-situ Carbon Coating to Enhance the Rate Capability of the Li4Ti5O12 Anode Material and Suppress the Electrolyte Reduction Decomposition on the Electrode // Electrochim. Acta. 2016. V. 190. P. 69–75.
Yaroslavtsev A.B., Stenina I.A. Carbon Coating of Electrode Materials for Lithium-Ion Batteries // Surf. Innov. 2021. V. 9. P. 92–110.
Nisar U., Muralidharan N., Essehli R., Amin R., Belharouak I. Valuation of Surface Coatings in High-Energy Density Lithium-Ion Battery Cathode Materials // Energy Storage Mater. 2021. V. 38. P. 309–328.
Novikova S., Yaroslavtsev S., Rusakov V., Kulova T., Skundin A., Yaroslavtsev A. LiFe1 –x${\text{M}}_{x}^{{{\text{II}}}}$PO4/C (MII = = Co, Ni, Mg) as Cathode Materials for Lithium-Ion Batteries // Electrochim. Acta. 2014. V. 122. P. 180–186.
Eftekhari A. LiFePO4/C Nanocomposites for Lithium-Ion Batteries // J. Power Sources. 2017. V. 3431. P. 395–411.
Sun X., Hegde M., Wang J., Zhang Y., Liao J., Radovanovic P.V., Cui B. Structural Analysis and Electrochemical Studies of Carbon Coated Li4Ti5O12 Particles Used as Anode for Lithium Ion Battery // ECS Trans. 2014. V. 58. P. 79–88.
Stenina I.A., Sobolev A.N., Kuz’mina A.A., Kulova T.L., Skundin A.M., Tabachkova N.Y., Yaroslavtsev A.B. Electrochemical Properties of Li4Ti5O12/C and Li4Ti5O12/C/Ag Nanomaterials // Inorg. Mater. 2017. V. 53. P. 1039–1045.
Li R., Lin C., Wang N., Luo L., Chen Y., Li J., Guo Z. Advanced Composites of Complex Ti-Based Oxides as Anode Materials for Lithium-Ion Batteries // Adv. Compos. Hybrid Mater. 2018. V. 1. P. 440–459.
Li D., Zhang X., Miao X., Liu Y., Chen S., Chen Y., Wang W., Zhang Y. Solid-State Synthesized Li4Ti5O12 for Ultrafast Lithium Ion Storage Enabled by Carbon-Coating Induced Particle Size Tailoring // J. Alloys Compd. 2019. V. 797. P. 1258–1267.
Shen W., Wang Y., Yan J., Wu H., Guo S. Enhanced Electrochemical Performance of Lithium Iron(II) Phosphate Modified Cooperatively via Chemically Reduced Graphene Oxide and Polyaniline // Electrochim. Acta. 2015. V. 173. P. 310–315.
Luo Y., Guo R., Li T., Li F., Liu Z., Zheng M., Wang B., Yang Z., Luo H., Wan Y. Application of Polyaniline for Li-Ion Batteries, Lithium-Sulfur Batteries, and Supercapacitors // ChemSusChem. 2019. V. 12. P. 1591–1611.
Huang Y.-H., Goodenough J.B. High-Rate LiFePO4 Lithium Rechargeable Battery Promoted by Electrochemically Active Polymers // Chem. Mater. 2008. V. 20. P. 7237–7241.
Vicente N., Haro M., Cíntora-Juárez D., Pérez-Vicente C., Tirado J. L., Ahmad S., Garcia-Belmonte G. LiFePO4 Particle Conductive Composite Strategies for Improving Cathode Rate Capability // Electrochim. Acta. 2015. V. 163. P. 323–329.
Dong Xu, Peifeng Wang, Rui Yang. Conducting Polythiophene-Wrapped Li4Ti5O12 Spinel Anode Material for Ultralong Cycle-Life Li-Ion Batteries // Ceram. Int. 2017. V. 43. P. 4712–4715.
Wang X., Shen L., Li H., Wang J., Dou H., Zhang X. PEDOT Coated Li4Ti5O12 Nanorods: Soft Chemistry Approach Synthesis and Their Lithium Storage Properties // Electrochim. Acta. 2014. V. 129. P. 283–289.
Daigle J.-C., Asakawa Y., Beaupré M., Arnold A.A., Laul D., Trudeau M., Zaghib K. A Versatile Method for Grafting Polymers onto Li4Ti5O12 Particles Applicable to Lithium-Ion Batteries // J. Power Sources. 2019. V. 421. P. 116–123.
Desalegn Assresahegn B., Bélanger D. Multifunctional Carbon for Electrochemical Double-Layer Capacitors // Adv. Funct. Mater. 2015. V. 25. P. 6775–6785.
Xin Y.-M., Xu H.-Y., Ruan J.-H., Li D.-C., Wang A.-G., Sun D.-S. A Review on Application of LiFePO4 Based Composites as Electrode Materials for Lithium Ion Batteries // Int. J. Electrochem. Sci. 2021. V. 16. Art. 210655.
Sun J., Ren X., Li Z., Wang L., Liang G. Synthesis and Electrochemical Performance of LiFePO4/C Composite Based on Xylitol-Polyvinyl Alcohol Complex Carbon Sources // Ionics. 2019. V. 25. P. 1567–1575.
Zhou Y., Gu C.D., Zhou J.P., Cheng L.J., Liu W.L., Qiao Y.Q., Wang X.L., Tu J.P. Effect of Carbon Coating on Low Temperature Electrochemical Performance of LiFePO4/C by Using Polystyrene Sphere as Carbon Source // Electrochim. Acta. 2011. V. 56. P. 5054–5059.
Kim M.K., Shin W.H., Jeong H.M. Protective Carbon-Coated Silicon Nanoparticles with Graphene Buffer Layers for High Performance Anodes in Lithium-Ion Batteries // Appl. Surf. Sci. 2019. V. 467–468. P. 926–931.
Stenina I.A., Sobolev A.N., Yaroslavtsev S.A., Rusakov V.S., Kulova T.L., Skundin A.M., Yaroslavtsev A.B. Influence of Iron Doping on Structure and Electrochemical Properties of Li4Ti5O12 // Electrochim. Acta. 2016. V. 219. P. 524–530.
Baddour-Hadjean R., Pereira-Ramos J.-P. Raman Microspectometry Applied to the Study of Electrode Materials for Lithium Batteries // Chem. Rev. 2010. V. 110. P. 1278–1319.
Stenina I.A., Kulova T.L., Skundin A.M., Yaroslavtsev A.B. Effects of Carbon Coating from Sucrose and PVDF on Electrochemical Performance of Li4Ti5O12/C Composites in Different Potential Ranges // J. Solid State Electrochem. 2018. V. 22. P. 2631–2639.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы